Шта су алкални земљопољски метали? Група 2 коначно има смисла
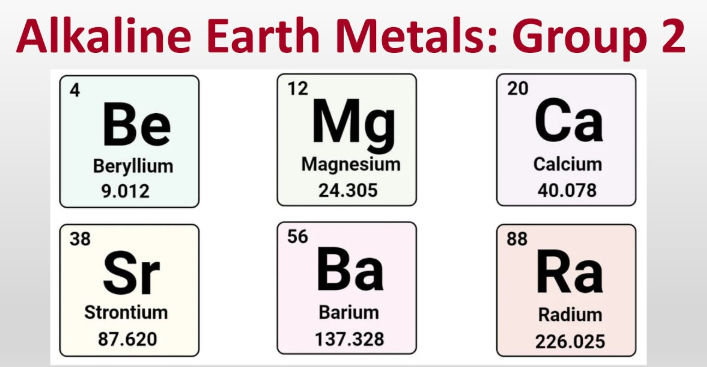
Шта су алкални земљопољски метали?
Ако сте тражили шта су алкални земљопољски метали , овде је директни одговор: они су шест елемената у Група 2 периодичног система. Тако брзо дефиниција алкалних метала земље је почетна тачка, али име такође говори много о томе како се ова породица понаша.
Који су алкални метали у једној реченици
Алкални метали су берилијум, магнезијум, калцијум, стронцијум, баријум и радијум, шест металних елемената у групи 2 који обично формирају +2 јоне.
- Берилијум (Be)
- Магнезијум (Мг)
- Калцијум (Ca)
- Stroncijum (Sr)
- Баријум (Ба)
- Радијум (Ra)
Зашто име алкални метали има смисла
За почетнике, дефиниција алкалне земље постаје много лакше када поделите фразу на три дела.
Алкални значи да су њихови оксиди и хидроксиди базични, а не кисели. Земља је историјска реч. Рани хемичари су га користили за топлотно стабилне, минералне супстанце које се нису лако топиле или растворавале у води, што је објашњено Британика . Метали значи да су сами елементи метални, обично сјајни и добри у губитку електрона у реакцијама.
То вам даје основне алкални метали значења без потребе да прво научите напредну хемију. То је такође користан кратак опис алкалних метала земље : група метала из групе 2 са заједничком хемијом, заједничком позицијом у периодичном табели и великом улогом у стварном свету. Магнезијум се налази у легурама и биологији. Калцијум је важан за кости, љуске и грађевинске материјале. Баријум, стронцијум и радијум се појављују у специјализованијим контекстима.
Овај чланак намерно почиње једноставно. Чиста листа је лако запамтити, али породица заиста кличе када видите где се ти елементи налазе и зашто им то место даје тако слично понашање.
Где група 2 седи на периодичном табели
Име породице постаје много лакше запамтити када га заиста можете препознати. Ако се питате где се на периодичном табели налазе алкални метали , погледајте другу колону са леве стране. Та вертикална колона је група 2 на периодичној табели , који се налази одмах поред алкалних метала у групи 1. А група 2 периодичне табеле у сваком случају, у овом погледу се види иста права линија: берилијум на врху, а затим магнезијум, калцијум, стронцијум, баријум и радијум који се крећу доле кроз периоде.
У алкални метали периодичне табеле тхеатричка карта, ове шест елемената припадају S-блоку. Њихова заједничка локација је важна јер одражава заједнички електронски образац. Као ЛибреТекст објашњава, елементи групе 2 имају ns 2валентна конфигурација, што значи да носе два електрона из спољне љуске.
Где се на периодичном табели налазе алкални метали
Визуелно, образац је једноставан. У елементи групе 2 периодичног табела формирају једну колону породице у периодима од 2 до 7. Многи дијаграми у учионици истичу алкални метали у периодичном табели распореди са истом бојом јер се породице елемената читају вертикално, а не хоризонтално. Претрага за периодични систем алкални метали земље стварно траже ту једну колону.
| Елемент | Симбол | Позиција групе 2 | Типични јон | Познато једињење |
|---|---|---|---|---|
| Берилијум | Be | Период 2, врх групе 2 | Be2+ | БиО |
| Магнезијум | Mg | Период 3 | Mg2+ | MgO |
| Калцијум | Ca | Период 4 | Ca2+ | КаКО 3 |
| Стронцијум | Sr | Период 5 | Sr2+ | SrCO 3 |
| Баријум | BA | Период 6 | BA 2+ | Басо 4 |
| Радијум | РА | Период 7, дно групе 2 | РА 2+ | РаCl 2 |
Зашто се елементи из групе 2 формирају плус два јона
Ови два спољашња електрона управљају хемијом. Атоми групе 2 имају тенденцију да губе оба електрона јер им то даје стабилнији распоред електрона. Резултат је +2 јон , као што је Mg 2+или Ка 2+- Да ли је то истина? Зато ове метале обично чине једињења као што су оксиди, хлориди, карбонати и сулфати. Узорак у формулама одмах видите: MgO, CaCl 2, ЦАЦО 3, БаСО 4.
Како брзо препознати породицу алкалних метала
Брз трик за идентификацију је да тражите три трага одједном: другу колону, металне елементе и уобичајени +2 наплата. У поређењу са суседним алкалним металима, који имају један валентни електрон и обично формирају +1 јоне, елементи групе 2 имају један додатни спољни електрон и генерално су мање реактивни. Ипак, очигледно је да припадају једној породици. Занимљиво је да сваки део изразује тај образац мало другачије, посебно од берилија на врху до радија на дну.
Познајте шест алкалних земљених метала
Список је користан, али сам по себи није веома запамћен. Група 2 почиње да се осећа стварније када сваки члан има јасан идентитет. Неки се појављују у костима или морској води. Неке боје ватромет. Један је углавном историјски упозоравајући знак. Заједно, они и даље припадају истој породици, али сваки има своју индивидуалност.
| Елемент | Симбол | Често појављивање | Изгледна имовина | Реална релевантност |
|---|---|---|---|---|
| Берилијум | Be | Налази се у минералима као што је берил | Веома лага и крута за метал | Користи се у специјализованим ваздухопловним и рентгенским апликацијама; прашина је опасна ако се удуши |
| Магнезијум | Mg | Присутно у морској води и минералима | Мала густина и сјајан бели пламен приликом горивања | Важан у лажима са малом тежином, додацима и биологији |
| Калцијум | Ca | Уобичајено у варовљу, костима, љушкама и креди | Биолошки познати јони групе 2 | Кључ у скелетима, цементу, гипсу и многим природним минералима |
| Стронцијум | Sr | Углавном се налази у целеститу и стронтианиту | Соле у пламену стварају живо црвену боју | Користи се у ватроверку, факелама, сјајним материјалима и неким стоматолошким производима |
| Баријум | BA | Обично повезана са баритом | Тешки, алкални метали од земље | Баријум сулфат је важан у бушење и медицинске сликање; растворљиве баријумске једињења захтевају опрез |
| Радијум | РА | У трагама се налази у руди урана | Силна радиоактивност доминира у његовој хемијској причи | Углавном историјска или строго контролисана научна релевантност данас |
Берилијум и магнезијум на врху групе 2
The елемент берилијум седи на врху породице и већ намеће да група 2 није савршено униформан. Обично је повезан са минералом берилом, истом породицом минерала која укључује смарагд и аквамарин. Берилијум се истиче због тога што је необично лаган и круг. То га чини корисним у деловима високих перформанси где је мала маса важна. Истовремено, берилијум је материјал који захтева пажњу у индустријским окружењима, јер фина прашина може бити штетна ако се удуши. Зато се сећају и на његове перформансе и на опрезност у управљању.
Магнезијум је много познатији. У хемијски симбол магнезијума је Mg, и један је од најпознатијих метала из ове групе јер се налази у морској води, у обичним минералима и живим системима. То је веома лаган метал, и када гори, изводи интензивно бело светло. Зато се магнезијум дуго повезује са факелама и сјајним материјалима. Међутим, у свакодневном животу, већина људи се суочава с тим у нежним облицима као што су дијеталне улоге, антиацидни једињења или лажи које се користе за смањење масе.
Калцијум и стронцијум у свакодневним материјалима
Калцијум је најпознатији члан групе 2 за многе читаоце. Појављује се у варовници, креди, љушкама и костима, тако да је хемија скоро одмах повезана са геологијом и биологијом. Калцијум карбонат је познато једињење овде. То помаже да се објасни зашто једна и иста породица може бити важна у пећинама, камену и скелетима. Сам калцијум је реактивни метал, али су једињења калцијума свуда, због чега се овај елемент често осећа више као познат него као егзотичан.
Стонцијум је лакше запамтити када га прикључите боји. У симбол за стронцијум је Sr, и стронцијум налази се углавном у минералима селеститу и стронтианиту. Краљевско друштво за хемију описује га као меки сребрни метал који гори у ваздуху и реагује са водом. Његове соли су познате по томе што стварају сјајне црвене боје у ватроверцима и факелама. У истом извору се такође наводи да се користи у материјалима који сјају у мраку и у хексахидрату стронциовог хлорида у пастама за зубе за осетљиве зубе. То чини стронцијум одличним примером како елемент може бити хемијски реактиван, али се углавном налази кроз једињења.
Баријум и радијум у напредним или специјализованим контекстима
The баријумски елемент често се сећају тежеће. Обично се повезује са баритом, а једно од најпознатијих једињења је баријум сулфат. То једињење је важно јер је веома нерастворљиво, што помаже да се објасни зашто се баријум може појавити у практичним окружењима као што су бушилице и медицинска сликања, док се други растворљиви једињења барија третирају пажљивије због забринутости за токсичност. Баријум подсећа читаоце да је користан облик елемента из групе 2 често једињење, а не сам сјајни метал.
Радијум се налази на дну породице, али се не мијеша тихо. На периодичан табела радијума ра означује тачку где радиоактивност постаје дефинишућа особина. Радијум се природно јавља само у малим количинама, обично повезан са рудама урана. Историјски гледано, постао је познат по светлећим бојевима и раним медицинским експериментима. Данас је опасност ради радијеактивности, а не од обичног понашања метала, тако да се са њим руководи под строгом контролом. У једноставним речима, радијум и даље припада групи 2, али се о њему разговара са нуклеарном сигурношћу у виду колико и хемије.
Поставите ове шест поред себе и породица престаје да изгледа као гола листа имена. Величина, реактивност, заједничка једињења, па чак и начин на који се сваки елемент појављује у животној промјени док се крећете надоле. То мења образац је где група 2 постаје посебно корисна, јер ред од берилија до радијума почиње да открива трендове уместо тривија.
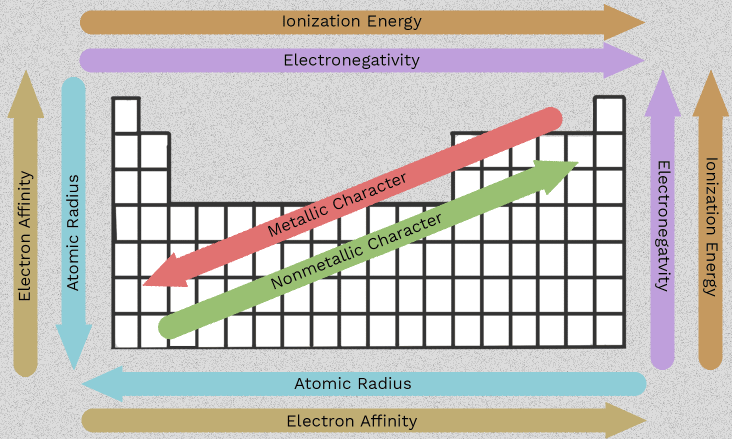
Свойства и трендови Алкални земљопољски метали
То мења поредак од берилија на радијум је оно што прави Групу 2 корисно. Уместо да запамтите шест изолованих чињеница, можете следити неколико узорака који се понављају широм колоне. Најважнији својства метала алкалних земљишта сви расту из једне заједничке особине: сваки атом има два спољашња електрона која имају тенденцију да изгубе.
Када видите како се величина, електронски штит и ионизацијска енергија померају према групи, породица постаје много лакше предвиђати. Ови карактеристике алкалних метала нису само чињенице из испита. Они објашњавају зашто неки елементи реагују брже, зашто се неке једињењења боље растворају од других и зашто је за неколико трендова потребно пажљиво израчунавање, а не једноставне стреле.
Сподељена својства алкалних метала земље
Већина чланова групе 2 су сребрни метали који обично формирају М 2+иони и чине углавном јонске једињења. Поводе се као редукторске агенсе јер губе електроне. У поређењу са металима из групе 1, они су генерално мање реактивни, али су и даље хемијски довољно активни да формирају многе уобичајене оксиде, хлориде, карбонате и сулфате.
Једноставан начин да се организује хемијска својства алкалних метала је да се одвоји оно што остаје константно од онога што се мења. Оно што остаје константно је обично +2 оксидационо стање. Оно што се мења је колико лако сваки елемент даје два електрона. То је место где трендови почињу да имају значај.
Тенденције доње групе 2 и шта они значе
Подаци прикупљени од стране ЛибреТекстса и објашњења трендова из Сачувајте моје испите показују исти укупни образац. Атомски радијус се повећава са 112 pm за Бе на 253 pm за Ба, док прва енергија јонизације пада са 900 на 503 кЈ / мол. На једноставном енглеском језику, спољни електрони седе даље од језгра и заштићени су више унутрашњим љускама, тако да их је лакше уклонити.
| Тренд | Спуштање у групу 2 | Хемијски разлог | Шта ово значи у пракси |
|---|---|---|---|
| Атомски радијус | Повећања | Сваки елемент има додатну електронску љуску и више штитене | Веће атоме мање чврсто држе спољне електроне |
| Прва и друга енергија јонизације | Укупно смањење | Извански електрони су удаљенији од језгра, тако да је привлачност слабија | Формирање М 2+јони постају лакши |
| Реактивност | Укупна пораст | Ниже енергије јонизације олакшавају губитак електрона | Теже чланове реакције снажније са киселина, кисеоника, а често и воде |
| Точка топљења | Уопштено се смањује, али не равномерно | Већи метални јони ослабљавају метално везивање, иако је и структура важна | Користимо овде реч "општа", јер Mg и Ca не одговарају савршено уредној линији |
| Gustina | Нередовно | Маса, атомска величина и метална паковања се мењају заједно | Не можете третирати густину као један обичан тренд на опадању |
| Растворљивост у хидроксиду | Повећања | Баланс енергије решетке и хидратације се помера доле у групи | Теже хидроксиде стварају више алкалних раствора |
| Растворљивост сулфата | Смање | Хидратацијска енергија пада док катион постаје већи | Соједишта као што је BaSO 4постају веома нерастворљиви |
Тешкост и понашање топљења су два тренда која студенти често превише поједностављају. Тешкост се не креће у правој линији јер се и маса и запремина мењају, а атоми метала се не пакују на исти начин у сваком кристалу. Такође је потребно бринути о тајаним местима. Они углавном имају тенденцију ка опадању јер већи јони ослабе металну ретицу, али Mg има необично ниску тачку топљења од 650 C, док се Ca повећава на 842 C пре него што вредности поново падне. Тако да је један од најбезбеднијих карактеристике алкалних метала земље је ово: широк образац је реалан, али физички детаљи нису савршено глатки.
Растворљивост има исту упозоравајућу ознаку. Не постоји једно правило које покрива све соли групе 2. Хидроксиди постају растворљивији доле у групи, док сулфати постају мање растворљиви. Ако неко каже "растворљивост се повећава до групе 2", важно питање је, "Које једињења?"
Зашто алкални метали реагишу на начин на који то раде
Па, су алкални метали реактивни да ли је то истина? Да, и општи одговор је да постају реактивнији док се крећете надоле. Разлог је иста прича о електронима коју видимо горе. Нижа прва и друга ионизацијска енергија значи да атоми могу лакше изгубити два електрона и достићи заједнички М 2+шта је брже.
То утиче на стварне реакције. У доњем делу групе, реакције са разређеним киселинама постају брже, реакције са кисеоником постају снажније, а теже чланове се лакше оксидишу. Save My Exams примећује да је баријум довољно реактиван да се може чувати под нафтом, што је практичан знак колико далеко тренд реактивности може да иде.
- Атомски радијус се повећава у групи 2.
- Енергија јонисације се смањује доле у групи 2.
- Реактивност се повећава јер губитак два електрона постаје лакши.
- Точка топљења и густина показују нерегуларности, па избегавајте апсолутна правила.
- Хидроксиди и сулфати показују супротне трендове растворљивости.
Ови обрасци чине породицу предвидљивом, али не и савршено јединственом. Веома близу врха групе, берилијум већ почиње да превазилази правила, а магнезијум додаје још један свакодневни изузетак који је важан више него што многи почетници очекују.
Алкални и алкалноземни метали
Широки трендови олакшавају учење групе 2, али породица престаје да има смисла ако се сваки члан третира као идентичан. Највећи знак упозорења је берилијум. Магнезијум додаје практичнији свакодневни изузетак. И када људи упоређују алкални и алкалноземни метали , слична имена могу крити неке веома различите хемије.
Зашто се берилијум не понаша као типичан метал групе 2
БЈЈУС описује берилијум као јасан изметник у групи 2. Необично мала величина, висока јонизациона енергија и јака сила поларизације дају му понашање које је мање типично за породицу. У једноставном језику, Бити 2+јако привлачи оближње електронске облаке, тако да су берилијумска једињења често ковалентнија од јонских једињења које формирају тежи чланови. Исто извор такође примећује да берилијум има већу тачку топљења и кључања од осталих чланова групе и да не реагује са водом као његови другови.
Магнезијум није тако необичан као берилијум, али ипак може изгледати мање реактивно него што ученици очекују. Либре Текстс примећује да веома чист магнезијум само благо реагује са хладном водом, а реакција убрзо успорава јер скоро нерастворљив магнезијум хидроксид формира препреку на површини. На дну породице, радијум се обично дискутује одвојено јер његова радиоактивност доминира практичном употребом и дискусијама о безбедности.
Како се алкални метали разликују од алкалних метала
Једноставно алкални против алкални у реченицама, метали групе 1 губе један спољни електрон, док метали групе 2 губе два. Та једина разлика обликује својства алкалних и алкалноземних метала више него скоро било шта друго.
| Особност | Алкални метали, група 1 | Алкални земљопољски метали, група 2 |
|---|---|---|
| Валентни електрони | 1 | 2 |
| Типични јон | M + | M 2+ |
| Реакција са хладном водом | Често је снажан или чак насилан, формирајући хидроксид и водоник | Мање једноставан: Бе не реагује са водом, Мг реагује благо, Ка, Ср и Ба реагују са све већим снагом |
| Заједничка хемија кисеоника | Може формирати оксиде, пероксиде или супероксиде | Обично формирају моноксиде; већина ових оксида даје хидроксиде са водом, али БеО је изузетак |
Важни изузеци које ученици често пропуштају
- Не реагују сви метали из групе 2 са водом на исти начин.
- Берилијум једињења су ковалентнија од остатка породице.
- Не мешајте алкални и алкални земљишта као иста група само зато што су имена слична.
- The својства алкалних метала и алкалних земљених метала најбоље се уче као обрасци са изузецима, а не као крути слогани.
То је такође најбољи начин да се разуме хемијска својства алкалних метала и алкалних земљених метала - Да ли је то истина? Електронски обрасци вам дају правило, али стварне супстанце додају текстуру. И та текстура постаје још јача када погледате где се елементи групе 2 заправо јављају: ретко као чисти метали, а много чешће унутар минерала, стене, морске воде, костију и индустријских једињења.
Како се у природи појављују алкални земљопољски метали
Ако замислите алкални метали као светли, чисти узор који седи у камену, природа ради другачије. Елементи из 2. групе су довољно реактивни да се обично појављују као јони унутар минерала, соли, стене, морске воде, костију и љустица, а не као слободни метали. Да ли неко тражи алкални земљопољски метали или стандарднији термин, природни образац је исти: ова породица снажно воли једињења.
Тај образац долази директно из хемијска својства алкалних метала - Да ли је то истина? Они имају тенденцију да изгубе два спољашња електрона и формирају стабилни М 2+јони. Када се то деси, кисеоник, карбонат, сулфат и халоидни јони их лако закључавају у чврсте једињења која могу да се задржавају у геологији и биологији.
Зашто се у природи не налазе алкални земљопољски метали
Британика i ТоугтКо оба описују групу 2 као реактивну, што објашњава зашто се ови елементи ретко налазе некомбинирани. У ваздуху, многи од њих брзо формирају оксидни слој. У природном окружењу, они се још више стабилизују као карбонати, сулфати, силикати, флуориди или хлориди. Зато се калцијум налази у варовници и љушћицама, магнезијум у минералима и морској води, а стронцијум или баријум у рудничким лежиштима. Радијум је још ређа, и налази се само у траговима у уранијумским рудама.
Обични минерали и једињења групе 2
| Елемент | Заједнички природни извор | Познато једињење | Зашто је то важно? |
|---|---|---|---|
| Берилијум | Берил | БиО | Берил је комерцијални извор овог елемента, док је бериллијум оксид важно једињење у специјализованим материјалима |
| Магнезијум | Магнезит, доломит, морска вода | МГЦО 3или Mg ((OH) 2 | Показао је зашто се магнезијум често налази у минералима, морској води и лековима него у чистој форми метала |
| Калцијум | Варовник, креда, мермер, гипс, кости, љуске | КаКО 3 | Везује геологију, грађевинске материјале и скелете у једно веома уобичајено једињење |
| Стронцијум | Селестит, стронцијанит | СРСО 4или СРЦО 3 | Ови минерали су главни природни извори стронционих једињења |
| Баријум | Барит, утерит | Басо 4 | Барит је кључна руда, а баријум сулфат је једно од најпознатијих баријумских једињења |
| Радијум | Трага у пичбленду и другим рудама урана | РаCl 2 | Његова реткост и радиоактивност чине радијумске једињењења историјски важним, али ретким |
ЕБСЦО напомиње да се калцијум и магнезијум такође налазе у морској води са око 0,4 г/л и 1,3 г/л, респективно. То помаже да се објасни зашто ово алкална земља породица се повезује не само са рудама, већ и са тврдом водом, морским системима и живим ткивом.
Како се ови метали изоловају од њихових једињења
Пошто се метали из групе 2 обично налазе унутар једињења, екстракција почиње рудама, сланом или минералним лежиштима. Заједничка индустријска идеја је једноставна: прво преобразите материјал у више радног оксида или халида, а затим користите електролизу или хемијску редукцију да бисте ослободили метал. Британска књига описује рану изоловање магнезијума, калцијума, стронцијума и барија електролизом, док ЕБСЦО напомиње да се модерна производња и даље обично ослања на растворене хлориде, редукцију оксида или сродне путеве у зависности од елемента. Берилијум је користан подсетник да породица није савршено јединствена, јер се може произвести редуковањем берилијум флуорида.
Дакле, у свакодневном животу, људи обично упознају групу 2 кроз варовник, гипс, магнезијум из морске воде, барит или биолошки калцијум, а не кроз узорке сирових метала. Тај детаљ је важан, јер је стварна важност ових елемената везана много више за њихове једињења и облике него за саме метале.
Алкални земљопољски метали Примери у свакодневном животу
Друга група постаје много памтаванија када прикључите сваки елемент нечему стварном. Кости, антациди, гипс, ватромет, течности за бушење и стари светловити цифри су сви корисни примере алкалних метала - Да ли је то истина? Ако сте се икада питали да ли је магнезијум метал или неметал? ili је Ка метал , оба одговора су једноставна: магнезијум и калцијум су метали. Међутим, у обичном животу, људи се обично суочавају са овим супстанцама као саставцима, а не као голим металним узорцима.
Свакодневна употреба магнезијума и калцијума
- Магнезијум : Магнезијум је један од најважнијих биолошких алкални елементи земље . Информативни лист о магнезијуму за НИХ наводи да је кофактор у више од 300 ензимских система и подржава функцију мишића и нерва, производњу енергије и структуру костију. Магнезијумски једињења се такође појављују у неким антиацидима и лаксативама, док се магнезијумски метал цени у лагима са масом која се смањује.
- Калцијум : Калцијум су једињења која доминирају свакодневном животом. Калцијум помаже у структури костију и зуба, а једињења као што су калцијум карбонат и калцијум сулфат су кључна у варовљу, цементу, гипсу и гипсома. То чини калцијум једном од најјачих веза између хемије, биологије и грађевинарства.
Специјализоване апликације стронцијума и барија
- Стронцијум : Стронцијумске соли су најпознатије по томе што производе длакоцрвене боје у ватроверцима и сигналним факелама. Чак и читаоци који се не сећају потпуне листе групе 2 често се сећају стронцијума када му се додаје боја.
- Баријум : Баријумски једињења су важна у индустрији и медицини. У Профил барија НЛМ описује главне употребе у бушилишту кал, боје, пластике, цигле и стакла. Такође се примећује важна медицинска контрастност: високо нерастворљив баријум сулфат се користи као радиоопачан материјал у неким рентгенским испитивањима јер га тело генерално не апсорбује.
- Радијум : Радијум је углавном историјски или строго контролисан научни случај. У Страница за НРЦ радијум описује његову прошлу употребу у светлећим бојама и раној терапији рака. Већина тих употреба је замењена, иако још увек постоје неке регулисане употребе, као што су одређене индустријске апликације за радиографију.
Зашто је облик и тип једињења важни у стварној употреби
У групи 2, облик који људи користе је често једињење, а не чист метал.
Та једна идеја очисти много конфузије. Магнезијум у храни или лековима није исто што и спаљивање магниевне траке. Калцијум у костима није исто што и реактивни калцијум метал. Баријум је најоштрији пример зашто је облик важан: нерастворљив баријум сулфат може бити користан у снимању, док растворљивије баријумске једињењења захтевају много већу опрезу. Радијум још више доводи до тога, јер његова радиоактивност, а не само његово место међу металима, контролише како се са њим руководи.
Дакле, вредност групе 2 уопште није апстрактна. Ови елементи помажу да се објасни како једна и иста породица може бити важна у исхрани, материјалима, медицини, индустријској обради и безбедносним правилима. Кратка листа стварних коришћа често је све што је потребно да би се већи образац заглавио.
Кључне информације о елементима из 2. групе
До овог тренутка, група алкалних метала треба да се осећа мање као листа за памћење и више као образац можете прочитати директно са група 2 у периодичном табели колона. Ако још неко пита, шта су алкални земљопољски метали , кратак одговор остаје једноставан: берилијум, магнезијум, калцијум, стронцијум, баријум и радијум. Пунији дефиниција алкалних метала још је кориснији: шест металних елемената у групи 2 који обично губе два спољашња електрона и формирају М 2+јони.
Кључне чињенице о алкалним земљеним металима
- Помештај је важан: ове шест елементи групе 2 седи у другој колони са леве стране, у секцији групе 2 у s-блоку.
- Чланови породице су фиксирани: Би, Мг, Ца, Ср, Ба и Ра чине цео скуп.
- Заједничка хемија објашњава сличност породице: њихових 2валентни образац чини +2 јона заједничким исходом, кључну тачку која је резмирана од стране ЛибреТекста.
- Главни трендови опадања су предвидљиви: атомски радиус се повећава, енергија јонизације генерално опада, а реактивност обично расте док се крећете доле у групи.
- Изузеци су важни: берилијум се понаша ковалентније од других, магнезијум може изгледати мање реактивно због свог површинског слоја, а радијум се углавном разматра кроз радиоактивност.
- Реални живот обично значи једињења, а не чисте метале: људи сусрећу калцијум карбонат, магнезијум оксид и баријум сулфат много чешће него елементарни Ка, Мг или Ба.
The алкална периодична табела колумна је најлакше запамтити као шест метала повезаних једним правилом: обично постају 2+ јона, али сваки члан изражава то правило мало другачије.
Од хемије групе 2 до инжењерских металних делова
То је хемија која се простире далеко изван уџбеника. ЛибреТекстс напомиње да се елементарни магнезијум производи у великом обиму и користи у лажима са мањом тежином за оквире авиона и делове моторних аутомобила. Шири водич за легуре показује зашто је то важно: инжењери прилагођавају састав и обраду како би уравнотежили тежину, чврстоћу, отпорност на корозију и обраду у стварним компонентама.
За читаоце који се крећу са група 2 у периодичном табели поглед на производњу, Шаои Метал Технологија нуди практичан пример те везе. Његове странице за аутомобилске материјале и обраду описују производњу металних делова од прототипа до масовне производње, где понашање материјала и контрола процеса морају да раде заједно. То чини алкална периодична табела више од табеле у учионици. То је такође део логике која се налази иза избора метала и легова за инжењерске делове који морају бити лагани, поуздани и производљиви.
Често постављене питања о алкалним земљеним металима
1. у вези са Који су шест алкалних метала?
Шест алкалних метала су берилијум, магнезијум, калцијум, стронцијум, баријум и радијум. Они заузимају групу 2 периодичног табела и групују се заједно јер обично губе два спољашња електрона, што доводи до заједничког 2+ јонског обрасца у многим једињењима.
2. Уколико је потребно. Како се алкални метали разликују од алкалних метала?
Алкални метали припадају групи 1 и обично формирају 1+ јона јер имају један спољашњи електрон. Алкални земљопољски метали су у групи 2, обично формирају 2+ јона, и имају тенденцију да буду мање реактивни у целини. То један додатни валентни електрон мења колико су јако повезани, како реагују са водом, и које врсте соли и оксида обично чине.
3. Уколико је потребно. Зашто се у природи не налазе алкални метали?
Ови метали су довољно реактивни да обично не остају у чистом елементарном облику дуго у природним условима. Уместо тога, они се комбинују са киселином, карбонатом, сулфатом, хлоридом или силикатним јонима и постају део минерала, стене, морске воде, љуска и костију. Због тога људи обично наилазе на групу 2 кроз једињења, а не у примероцима сирових метала.
4. Уколико је потребно. Да ли се сви алкални метали земљопољске врсте реагују са водом?
Не, и ово је један од најкориснијих изузека који треба запамтити. Берилијум је у великој мери отпоран на воду, магнезијум се бавно реагује у хладној води јер површински слој ограничава реакцију, а калцијум, стронцијум и баријум лакше реагују. Уопштено, реактивност воде постаје јача док се крећете до групе 2.
5. Појам Зашто су алкални земљопољски метали важни у индустрији и производњи?
Њихова важност долази и од њихових једињења и њихове улоге у избору легура. Магнезијум је вредан тамо где је нижа тежина важна, калцијумске једињењења су централна ствар за цемент и гипс, а баријумске једињењења су изабране за специјализоване индустријске и медицинске употребе. У стварној производњи, разумевање понашања метала помаже у вођењу обраде, стабилности процеса и квалитета делова, због чега добављачи као што је Шаои Метал Технологија истичу сертификовану аутомобилну обраду, контролу процеса и подршку од прототипа делова до масовне производње.
 Мале партије, високи стандарди. Наша услуга брзе прототипирања чини валидацију бржем и лакшим
Мале партије, високи стандарди. Наша услуга брзе прототипирања чини валидацију бржем и лакшим 
