アルカリ土類金属とは何か?第2族がようやく理解できる
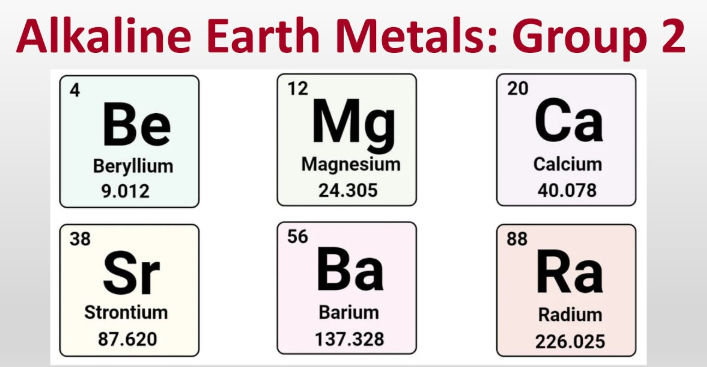
アルカリ土類金属とは何ですか?
あなたが検索したのは アルカリ土類金属とは何ですか というキーワードでしたら、ここに直接的な答えがあります:それらは周期表の 第2族 に属する6つの元素です。このアルカリ土類金属の簡潔な 定義 は出発点にすぎませんが、その名称自体が、この元素族の振る舞いについて多くの情報を伝えています。
一文でアルカリ土類金属を説明すると
アルカリ土類金属とは、ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、ラジウムの6つの金属元素であり、第2族に属し、通常+2価のイオンを形成します。
- ベリリウム (Be)
- マグネシウム (Mg)
- カルシウム (Ca)
- ストロンチウム(Sr)
- バリウム (Ba)
- ラジウム (Ra)
なぜ「アルカリ土類金属」という名称が妥当なのか
初心者にとって、 アルカリ土類金属の定義 という語を3つの部分に分けて考えると、はるかに理解しやすくなります。
アルカリ性 これは、これらの元素の酸化物および水酸化物が酸性ではなく、塩基性であることを意味します。 地球 「土類(earth)」という語は歴史的な用語です。初期の化学者は、熱に対して安定で、鉱物に似た性質を持ち、水に溶けにくく、また容易に融解しない物質を指してこの語を用いていました。この点については、「 ブリタニカ . 金属 」が、これらの元素自体が金属的である——つまり通常は光沢があり、反応において電子を失いやすい——ことを意味します。
これにより、基本的な理解が得られます。 アルカリ土類金属の意味 高度な化学の知識を事前に必要とせずに理解できます。また、これはアルカリ土類金属の簡潔な説明としても役立ちます。 アルカリ土類金属の説明:周期表の第2族に属する金属元素の一群であり、共通の化学的性質、周期表上における共通の位置、および現実世界における重要な役割を特徴としています。マグネシウムは合金や生物学に登場します。カルシウムは骨・貝殻・建築材料において重要です。バリウム、ストロンチウム、ラジウムはより専門的な分野で見られます。 この記事は意図的にシンプルな内容から始めています。すっきりとした一覧表は暗記しやすいですが、これらの元素が周期表のどこに位置し、なぜその位置が類似した性質をもたらすのかを実際に確認することで、この元素族の本質がより深く理解できるようになります。
第2族(Group 2)の周期表上での位置
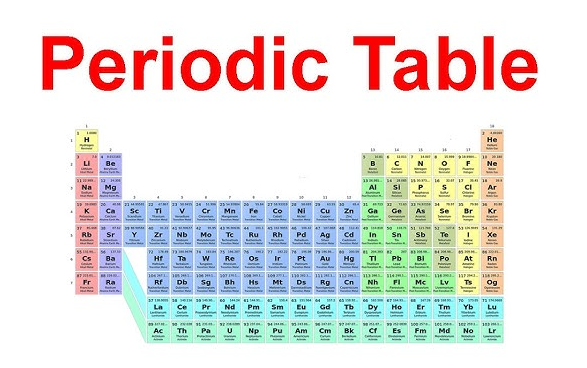
元素族の名称は、実際にその位置を確認できれば、はるかに覚えやすくなります。
もし「アルカリ土類金属は周期表のどこにあるのか?」と疑問に思われているなら、 アルカリ土類金属は周期表のどこに存在するか? 左端から2番目の縦列をご覧ください。この縦列が 周期表における第2族(Group 2)です 、アルカリ金属が属する第1族の直ぐ隣に位置する。 第2族の周期表 図では、毎回同じ直線が示され、上からベリリウム、次にマグネシウム、カルシウム、ストロンチウム、バリウム、ラジウムと、周期を下方向に順に並ぶ。
において アルカリ土類金属の周期表 図において、これらの6つの元素はsブロックに属している。共通の位置関係は重要であり、それは共通の電子配置を反映している。 LibreTexts 説明するように、第2族元素はns 2価電子配置を持ち、すなわち最外殻に2個の電子を有する。
アルカリ土類金属が周期表上でどこに位置するか
視覚的には、このパターンは単純である。第2族の 周期表の第2族元素 第2周期から第7周期にわたって、1つの族(縦列)を形成します。多くの教室用周期表の図では、 周期表におけるアルカリ土類金属 元素族は縦方向(列方向)に読み取られるため、横方向(行方向)ではなく、同じ色で強調表示されています。「周期表 アルカリ土類金属」に関する検索は、 周期表 アルカリ土類金属 実際にはこの1つの縦列(列)を指しています。
| 元素 | シンボル | 第2族の位置 | 典型的なイオン | 身近な化合物 |
|---|---|---|---|---|
| ベリリウム | Be | 第2周期、第2族の最上位 | Be2+ | BeO |
| マグネシウム | Mg | 第3周期 | Mg2+ | ロープ |
| カルシウム | Ca | 第4周期 | Ca2+ | カコ 3 |
| ストロンチウム | Sr | 第5周期 | Sr2+ | SrCO 3 |
| バリウム | BA | 第6周期 | BA 2+ | BaSO 4 |
| ラジウム | RA | 第7周期、2族の最下部 | RA 2+ | RaCl 2 |
2族元素が+2価イオンを形成する理由
この2つの外側の電子が化学反応を支配します。第2族の原子は、より安定した電子配置を得るために、通常、この2つの電子を失います。その結果として生じるのは +2価のイオン (例:Mg 2+やCa) 2+です。そのため、これらの金属は酸化物、塩化物、炭酸塩、硫酸塩などの化合物をよく形成します。化学式におけるパターンはすぐにわかります:MgO、CaCl 2₂、CaCO 3₃、BaSO 4.
アルカリ土類金属族を素早く識別する方法
素早い識別のコツは、以下の3つの手がかりを同時に確認することです:周期表の第2列に位置する、金属元素である、そして通常+2の電荷を帯びる。隣接するアルカリ金属(1つの価電子を持ち、通常+1イオンを形成する)と比較すると、第2族元素は外側に1つ多い価電子を持ち、一般に反応性はやや低いです。とはいえ、明らかに共通の族に属しています。興味深いのは、各元素がこのパターンをわずかに異なる形で示す点であり、特に最上位のベリリウムから最下位のラジウムまでその違いが顕著です。
6種類のアルカリ土類金属に出会う
リストは便利ですが、それだけではあまり記憶に残りません。グループ2の各メンバーが明確な個性を持つようになると、より現実味を帯びてきます。一部は骨や海水に存在し、一部は花火の色を付けます。また、ある元素は主に歴史的な警告標識として知られています。これらはまとめて同じ族(グループ)に属していますが、それぞれ独自の「性格」を持っています。
| 元素 | シンボル | 一般的な発生 | 際立った性質 | 実走行における関連性 |
|---|---|---|---|---|
| ベリリウム | Be | ベリルなどの鉱物に含まれる | 金属としては非常に軽量で剛性が高い | 特殊な航空宇宙機器およびX線関連用途に使用されるが、粉塵を吸入すると危険 |
| マグネシウム | Mg | 海水および鉱物中に存在 | 低密度で、燃焼時に明るい白色の炎を出す | 軽量合金、栄養補助食品、生物学において重要 |
| カルシウム | Ca | 石灰岩、骨、貝殻、チョークなどに多く含まれる | 生物学的に身近な第2族イオン | 骨格、セメント、プラスター、および多くの天然鉱物の主要成分 |
| ストロンチウム | Sr | 主にセレスタイトおよびストロンチアナイト中に産出 | 塩類は炎中で鮮やかな赤色を呈する | 花火、信号弾、発光材料、および一部の歯科用製品に使用 |
| バリウム | BA | 通常、バリウム鉱(バリテ)と関連して産出 | 密度が高く重いアルカリ土類金属 | 硫酸バリウムは掘削および医療用画像診断において重要であるが、水溶性バリウム化合物は取り扱いに注意を要する |
| ラジウム | RA | ウラン鉱石中に微量に存在 | 強い放射能がその化学的性質を支配している | 今日では、主に歴史的または厳密に管理された科学的な意義を持つ |
第2族の最上位にあるベリリウムおよびマグネシウム
ランハイ社製の 元素ベリリウム この元素は第2族の最上位に位置し、すでに第2族が完全に均一でないことを示唆しています。ベリリウムは、エメラルドやアクアマリンを含む鉱物ベリルと密接に関連しています。ベリリウムは異常に軽量かつ剛性が高いという特徴から、質量が重要な高機能部品に有用です。一方で、産業現場では細かい粉塵が吸入された場合に有害となるため、取り扱いには十分な注意が必要な材料でもあります。そのため、ベリリウムはその優れた性能と、取り扱い上の注意の両方において記憶されています。
マグネシウムははるかに身近に感じられます。この マグネシウムの化学記号 マグネシウム(Mg)は、このグループで最もよく知られた金属の一つであり、海水、一般的な鉱物、および生物系に存在するためです。これは非常に軽量な金属であり、燃焼すると強烈な白色光を発します。そのため、マグネシウムは長年にわたり、照明弾や高輝度で燃える材料と関連づけられてきました。しかし日常生活においては、人々がマグネシウムに触れる機会は、主に栄養素としての役割、制酸剤成分、あるいは質量低減が重要な場面で用いられる軽量合金など、より穏やかな形態であることが多いです。
日常的な素材におけるカルシウムとストロンチウム
カルシウムは、多くの読者にとって最も馴染み深い第2族元素です。石灰岩、チョーク、貝殻、骨などに存在するため、化学を地質学および生物学とほぼ即座に結びつけることができます。ここでよく知られた化合物は炭酸カルシウムです。これにより、同じ族の元素が鍾乳洞の形成、建築用石材、そして骨格といった多様な場面で重要となる理由が説明されます。カルシウム金属自体は反応性が高い一方で、カルシウム化合物はいたるところに存在するため、この元素はしばしば「異質」ではなく「身近」と感じられるのです。
ストロンチウムは、色と関連付けると覚えやすくなります。この元素の 記号はSrであり、 主にセレスタイトおよびストロンチアナイトという鉱物中に存在します。英国王立化学会(RSC)によると、ストロンチウムは空気中で燃え、水と反応する柔らかく銀白色の金属です。その塩類は花火や信号炎で鮮やかな赤色を発生させることで知られています。同資料では、また、蛍光材料や知覚過敏用歯磨き粉に配合されるストロンチウム塩化物六水和物(SrCl₂・6H₂O)への応用も挙げています。これにより、ストロンチウムは、化学的に反応性が高くても、実際にはほとんどが化合物の形で私たちの身近に存在するという、元素の典型例と言えるでしょう。 ストロンチウム ストロンチウムは、色と関連付けると覚えやすくなります。この元素の記号はSrであり、主にセレスタイトおよびストロンチアナイトという鉱物中に存在します。英国王立化学会(RSC)によると、ストロンチウムは空気中で燃え、水と反応する柔らかく銀白色の金属です。その塩類は花火や信号炎で鮮やかな赤色を発生させることで知られています。同資料では、また、蛍光材料や知覚過敏用歯磨き粉に配合されるストロンチウム塩化物六水和物(SrCl₂・6H₂O)への応用も挙げています。これにより、ストロンチウムは、化学的に反応性が高くても、実際にはほとんどが化合物の形で私たちの身近に存在するという、元素の典型例と言えるでしょう。
高度または専門的な文脈におけるバリウムおよびラジウム
ランハイ社製の バリウム元素 重さによって思い出されることが多い。これは一般的にバリウムを含む鉱物であるバリテと関連付けられており、その最も身近な化合物の一つは硫酸バリウムである。この化合物が重要である理由は、極めて不溶性である点にある。これにより、バリウムはドリル流体や医療用画像診断といった実用的な場面で使用される一方、他の可溶性バリウム化合物は毒性に関する懸念から、より慎重に取り扱われる必要があることが説明できる。バリウムは読者に、第2族元素の有用な形態は、光沢のある金属そのものではなく、しばしばその化合物であることを思い起こさせる。
ラジウムはこの族の最下位に位置するが、静かに溶け込むことはない。それは、 ラジウム周期表 視点を変えると、Ra(ラジウム)は放射能がその特徴となる分岐点を示します。ラジウムは天然にはごく微量しか存在せず、通常はウラン鉱石に伴って産出されます。歴史的には、発光塗料や初期の医療実験で有名になりました。今日では、その危険性は通常の金属としての性質ではなく、放射能に起因するため、厳格な管理のもとで取り扱われます。簡潔に言えば、ラジウムは依然として第2族に属しますが、化学的観点だけでなく、核安全の観点からも議論されることが多くなっています。
この6つの元素を並べてみると、第2族は単なる元素名の羅列ではなく、ひとつの「族」としてのまとまりが見えてきます。原子サイズ、反応性、代表的な化合物、さらには各元素が日常生活や自然界にどのように現れるかまで、下に向かうにつれて変化していきます。こうした変化のパターンこそが、第2族の学習において特に有用な点であり、ベリリウムからラジウムに至る順序を追うことで、単なる雑多な知識ではなく、明確な傾向性が浮かび上がってくるのです。
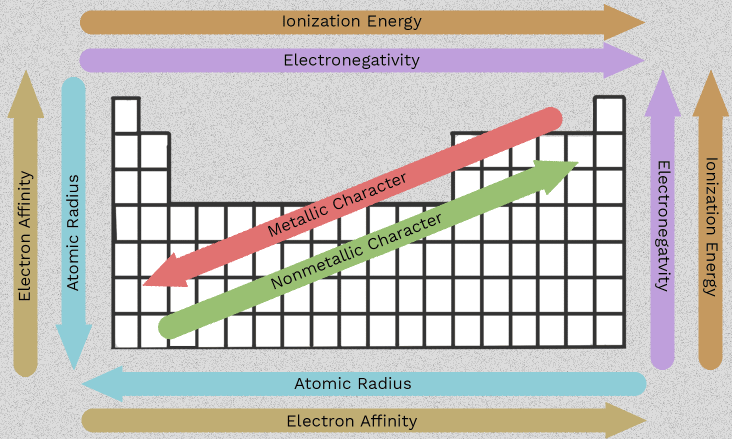
アルカリ土類金属の性質および第2族の周期的傾向
ベリリウムからラジウムへと変化する順序こそが、第2族元素を有用なものにしている。6つの孤立した事実を暗記する代わりに、この族全体にわたって繰り返される数個のパターンに従えばよい。 アルカリ土類金属の性質 すべてが一つの共通する特徴から生じる:各原子は外側に2個の電子を持ち、それらを失いやすい。
原子サイズ、電子遮蔽、およびイオン化エネルギーが族内で下方へとどのように変化するかを理解すれば、この族の性質を予測することがずっと容易になる。これらの アルカリ土類金属の特徴 は単なる試験対策用の知識ではない。これらは、なぜ一部の元素がより速く反応するのか、なぜ一部の化合物が他のものよりもよく溶解するのか、またなぜいくつかの傾向については単純な矢印ではなく、慎重な表現が必要なのかを説明する。
アルカリ土類金属の共通する性質
第2族のほとんどの元素は銀白色の金属であり、通常M 2+イオンを形成し、主にイオン性化合物を作ります。電子を失うため、還元剤として振る舞います。第1族金属と比較すると、一般に反応性はやや低いですが、それでも十分に化学的に活性であり、多くの一般的な酸化物、塩化物、炭酸塩、硫酸塩を形成します。
化学的性質を整理する簡単な方法は、 アルカリ土類金属の化学的性質を 一定であるものと変化するものに分けることです。一定なのは、通常+2の酸化数です。変化するのは、各元素がその2つの電子を放出する容易さです。ここから傾向(トレンド)が重要になってきます。
第2族を下方向へ進む際の傾向とその意味
LibreTexts が収集したデータおよび「Save My Exams」による傾向の解説は、 Save My Exams 同じ全体的なパターンを示しています。原子半径はBeで112 pmからBaで253 pmへと増加し、第一イオン化エネルギーは900 kJ/molから503 kJ/molへと低下します。平易な言葉で言えば、最外殻電子は原子核からより遠くに位置し、内側の電子殻によってより強く遮蔽されるため、取り除きやすくなります。
| 傾向 | 第2族を下方向へ進む方向 | 化学的な理由 | これが実際に意味すること |
|---|---|---|---|
| 原子半径 | 増加する | 各元素は電子殻を1つ追加し、遮蔽効果も大きくなる | 原子が大きくなると、外側の電子をより弱く保持する |
| 第1および第2イオン化エネルギー | 全体的に減少する | 外側の電子は原子核からより遠く離れているため、引力が弱くなる | Mを形成する 2+イオンになることが容易になる |
| 反応性 | 全体的に増加する | イオン化エネルギーが低くなると、電子の喪失が容易になる | 原子量の大きい元素は、酸や酸素、そしてしばしば水ともより活発に反応する |
| 溶解点 | 一般に減少するが、滑らかには減少しない | 大きな金属イオンは金属結合を弱めるが、結晶構造もまた重要である | 「一般に」という語をここでは用いる。これはMgおよびCaが完全に整然とした直線上に並ばないためである |
| 密度 | 不規則 | 質量、原子サイズ、金属の充填密度はすべて同時に変化する | 密度を単純な下方傾向として扱うことはできない |
| 水酸化物の溶解度 | 増加する | 格子エネルギーと水和エネルギーのバランスが族内で下方へとシフトする | 原子量の大きい水酸化物ほど、より強いアルカリ性の溶液を生成する |
| 硫酸塩の溶解度 | 減少する | カチオンのサイズが大きくなるにつれて、水和エネルギーは低下する | BaSOなどの化合物 4非常に不溶性になる |
密度および融点の挙動は、学生がしばしば単純化しすぎてしまう2つの傾向である。密度は直線的に変化しない。これは、質量と体積の両方が変化していること、および金属原子がすべての結晶中で同じように配列されていないためである。融点についても注意が必要である。一般に、イオンのサイズが大きくなることで金属格子が弱まるため、融点は下方へ向かって低下する傾向があるが、Mgは異常に低い融点650°Cを示し、Caでは842°Cまで上昇した後、再び値が低下していく。したがって、最も確実な アルカリ土類金属の特徴の一つ は次の通りである:広範な傾向は確かに存在するが、物理的な詳細は完全に滑らかではない。
溶解度についても同様の注意が必要である。第2族の塩すべてを網羅する単一の法則は存在しない。水酸化物は族の下方に向かってより可溶になり、硫酸塩は逆に不溶性が増す。誰かが「第2族では溶解度が下方に向かって増加する」と述べた場合、重要な問いは「どの化合物についてですか?」である。
アルカリ土類金属がそのように反応する理由
したがって、 アルカリ土類金属は反応性がありますか ?はい。一般的な答えは、周期表で下に進むにつれて反応性が高まることです。その理由は、上記で述べた電子に関する同じ説明に基づいています。第1および第2イオン化エネルギーが低くなると、原子は2つの電子をより容易に失うことができ、共通のM 2+状態に達するのが速くなります。
これは実際の反応に影響を与えます。族を下に進むにつれて、希薄酸との反応は速くなり、酸素との反応はより激しくなり、より重い元素は酸化されやすくなります。「Save My Exams」のノートによると、バリウムは十分に反応性が高いため、油中で保存されるほどであり、これは反応性の傾向がどこまで及ぶかを示す実用的な証拠です。
- 原子半径は第2族で下に進むにつれて増加します。
- イオン化エネルギーは第2族で下に進むにつれて減少します。
- 2つの電子を失いやすくなるため、反応性が高まります。
- 融点および密度は不規則な傾向を示すため、絶対的な法則は避けましょう。
- 水酸化物および硫酸塩は、相反する溶解度の傾向を示します。
こうしたパターンにより、第2族元素は予測可能ではあるが、完全に均一ではない。グループの最上部近くでは、ベリリウムですでに規則が緩められており、マグネシウムはさらに日常的に遭遇するもう一つの例外を加えるが、その重要性は多くの初心者が予想するよりも大きい。
アルカリ金属およびアルカリ土類金属
広範な傾向により、第2族は学びやすくなっているが、すべての構成元素を同一と見なすと、この族としての整合性が失われる。最も大きな警告サインはベリリウムである。マグネシウムは、より実用的で日常的な例外を追加する。そして人々が アルカリ金属およびアルカリ土類金属 を比較する際、似た名称が非常に異なる化学的性質を隠している可能性がある。
なぜベリリウムが典型的な第2族金属のように振る舞わないのか
BYJU'S は、ベリリウムを第2族における明確な異常値として記述している。その異常に小さい原子サイズ、高いイオン化エネルギー、および強い分極化能が、この元素に第2族の他の元素とは異なる特徴的な挙動をもたらしている。平易な言葉で言えば、Be 2+ベリリウムは近接する電子雲を強く引き寄せるため、ベリリウム化合物は、より重い族元素が形成するイオン性の強い化合物よりも、しばしば共有結合性が高くなります。同資料では、ベリリウムの融点および沸点がこの族の他の元素よりも高いこと、また水とはその仲間と異なり反応しないことも指摘しています。
マグネシウムはベリリウムほど特異ではありませんが、それでも学生が予想するよりも反応性が低いように見えることがあります。LibreTextsでは、非常に清浄なマグネシウムは冷水と僅かにしか反応せず、反応はすぐに遅くなると記されています。これは、ほとんど不溶性の水酸化マグネシウムが表面に被膜を形成し、反応を阻害するためです。族の最下位にあるラジウムは、その放射能が実用および安全上の議論を支配するため、通常は別途取り扱われます。
アルカリ土類金属とアルカリ金属の違い
単純に アルカリ対アルカリ土類 いえば、第1族の金属は外殻電子を1個失うのに対し、第2族の金属は2個の外殻電子を失います。このわずかな違いが、アルカリ金属およびアルカリ土類金属の性質を、ほぼ他のいかなる要因よりも大きく規定します。 アルカリ金属およびアルカリ土類金属の性質 ほぼ他のいかなる要因よりも大きく規定します。
| 特長 | アルカリ金属、第1族 | アルカリ土類金属、第2族 |
|---|---|---|
| 価電子 | 1 | 2 |
| 典型的なイオン | M + | M 2+ |
| 冷水との反応 | しばしば激しく、あるいは甚至に爆発的に起こり、水酸化物と水素を生成する | 反応性は一様ではなく、ベリリウム(Be)は水と反応せず、マグネシウム(Mg)は穏やかに反応し、カルシウム(Ca)、ストロンチウム(Sr)、バリウム(Ba)は順次激しく反応する |
| 共通の酸素化学 | 酸化物、過酸化物、または超酸化物を形成できる | 一般に一酸化物を形成する。これらの酸化物の多くは水と反応して水酸化物を与えるが、BeOは例外である |
学生が見落としがちな重要な例外
- 第2族のすべての金属が同じように水と反応するわけではない。
- ベリリウム化合物は、この族の他の元素の化合物よりも共有結合性が強い。
- 混同しないでください アルカリ金属とアルカリ土類金属を 名称が似ているからといって、同じ族であると誤解しないでください。
- ランハイ社製の アルカリ金属およびアルカリ土類金属の性質 は、硬直した標語ではなく、例外を伴う傾向として学ぶのが最も効果的です。
それはまた、 アルカリ金属およびアルカリ土類金属の化学的性質を理解するための最良の方法でもあります 。電子配置が法則を示しますが、実在する物質はそれに「質感」を加えます。そして、第2族元素が実際にどこに存在するかを観察すると、その「質感」はさらに明確になります:純金属として存在することは稀であり、むしろ鉱物、岩石、海水、骨、工業用化合物の中に遥かに多く含まれています。
アルカリ土類金属の自然界における存在形態
もし、 アルカリ土類金属 を、岩石の中に輝く純粋な試料として思い浮かべるなら、自然界はまったく異なる仕組みで働いています。第2族元素は反応性が高いため、通常は自由な金属としてではなく、鉱物・塩類・岩石・海水・骨・貝殻などの中にイオンの形で存在します。誰かが「 アルカリ土類金属 」と検索しようが、より標準的な用語である「アルカリ土類金属」で検索しようが、自然における出現パターンは同じです:この元素族は、明確に化合物を好むのです。
このパターンは、 アルカリ土類金属の化学的性質 から直接生じます。これらの元素は、外側の電子を2個失い、安定したM 2+²⁺
なぜアルカリ土類金属は自然界で遊離状態(単体)として見つからないのか
ブリタニカ および ThoughtCo どちらも第2族元素を反応性が高いと記述しており、これがこれらの元素が単体で存在することが極めて稀である理由を説明しています。空気中では、多くの元素が急速に酸化被膜を形成します。自然環境下では、それらはさらに炭酸塩、硫酸塩、ケイ酸塩、フッ化物、または塩化物として安定化されます。そのため、カルシウムは石灰岩や貝殻に、マグネシウムは鉱物や海水に、ストロンチウムやバリウムは鉱床にそれぞれ存在します。ラジウムはさらに希少で、ウラン鉱石中に僅かに含まれるのみです。
第2族の代表的な鉱物および化合物
| 元素 | 一般的な天然由来源 | 身近な化合物 | その化合物が重要な理由 |
|---|---|---|---|
| ベリリウム | ベリル | BeO | ベリルはこの元素の商業的供給源であり、ベリリウム酸化物は特殊材料において重要な化合物です |
| マグネシウム | マグネサイト、ドロマイト、海水 | MgCO₃ 3または Mg(OH)₂ 2 | マグネシウムが純金属よりもむしろ鉱物、海水、医薬品などにおいてより頻繁に見られる理由を示しています |
| カルシウム | 石灰岩、チョーク(白亜)、大理石、石膏、骨、貝殻 | カコ 3 | 地質学、建築材料、および骨格を一つの非常に一般的な化合物で結びつける |
| ストロンチウム | セレスタイト、ストロンチアナイト | SrSO₄ 4または SrCO₃ 3 | これらの鉱物は、ストロンチウム化合物の主な天然資源である |
| バリウム | バリテ、ウィザライト | BaSO 4 | バリテは主要な鉱石であり、硫酸バリウムは最もよく知られたバリウム化合物の一つである |
| ラジウム | ピッチブレンドおよびその他のウラン鉱石に微量含まれる | RaCl 2 | その希少性と放射能により、ラジウム化合物は歴史的には重要であったが、実際には稀なものである |
EBSCO カルシウムおよびマグネシウムが、それぞれ約0.4 g/Lおよび1.3 g/Lの濃度で海水にも存在することに注目する。これにより、この アルカリ土類金属 族が鉱石だけでなく、硬水、海洋系、および生体組織とも関係している理由が説明される。
これらの金属をその化合物から分離する方法
第2族金属は通常、化合物中に閉じ込められているため、抽出は鉱石、塩水、または鉱物堆積物から始まる。一般的な工業的アプローチは単純なものである:まず、原料をより取り扱いやすい酸化物またはハライドに変換し、その後、電解または化学還元によって金属を遊離させる。『ブリタニカ百科事典』(Britannica)では、マグネシウム、カルシウム、ストロンチウム、バリウムの初期の分離が電解法によって行われたと記述しており、EBSCOは現代の製造においても、元素に応じて溶融塩化物を用いた電解、酸化物の還元、あるいはそれらに関連する手法が依然として広く採用されていると指摘している。ベリリウムは、この族が完全に均質でないことを示す有用な例であり、ベリリウムフッ化物の還元によって製造可能である。
つまり、日常生活において人々が第2族元素に触れるのは、石灰岩、石膏、海水由来のマグネシウム、重晶石、または生物由来のカルシウムなどの形でであり、純金属の試料としてではない。この点は重要である。なぜなら、これらの元素の実社会における重要性は、むしろその化合物や存在形態に大きく依存しており、単体の金属そのものよりもはるかに大きいからである。
日常生活中のアルカリ土類金属の例
各元素を現実の具体物(例:骨、制酸剤、石膏、花火、掘削液、かつての発光文字盤など)と結びつけることで、第2族元素ははるかに記憶に残りやすくなる。 アルカリ土類金属の例 もし皆さんがこれまでに疑問に思ったことがあれば マグネシウムは金属か非金属か または caは金属か ——両方の問いに対する答えはシンプルである:マグネシウムもカルシウムも金属である。しかし、日常生活では、これらは通常、単体の金属ではなく、化合物の形で人々に知られている。
マグネシウムおよびカルシウムの化合物の日常的な用途
- マグネシウム :マグネシウムは、最も生物学的に重要な元素の一つである アルカリ土類元素 。この NIH マグネシウム事実情報シート マグネシウムは300種類以上の酵素系の補因子であり、筋肉および神経機能、エネルギー産生、骨構造をサポートすることに言及しています。また、マグネシウム化合物は一部の制酸剤および下剤にも含まれており、マグネシウム金属は質量低減が重要な軽量合金においても高く評価されています。
- カルシウム カルシウム化合物は日常生活で広く使われています。カルシウムは骨や歯の構造形成に寄与し、炭酸カルシウムや硫酸カルシウムなどの化合物は石灰岩、セメント、プラスター(石膏)、乾式壁材(ドライウォール)の中心的成分です。これにより、カルシウムは化学・生物学・建設工学の間で最も明確な関連性を持つ元素の一つとなっています。
ストロンチウムおよびバリウムの特殊用途
- ストロンチウム ストロンチウム塩は花火や信号用フレアにおける鮮やかな赤色発色に最もよく知られています。グループ2元素の一覧を完全には思い出せない読者でも、色と結びつけることでストロンチウムを思い出すことが多いでしょう。
- バリウム バリウム化合物は産業および医療分野で重要です。その NLM バリウムプロフィール ドリル・マッド、塗料、プラスチック、レンガ、ガラスなどの主要な用途を説明しています。また、重要な医療上の対比として、水に極めて難溶性の硫酸バリウムが、体内で一般に吸収されないため、一部のX線検査において放射不透過性造影剤として使用されていることが述べられています。
- ラジウム :ラジウムは、主に歴史的あるいは厳格に管理された科学的な事例に属します。この 米国原子力規制委員会(NRC)のラジウム関連ページ では、過去に発光塗料や初期の癌治療への応用が行われていたことについて記述されています。これらの用途のほとんどはすでに置き換えられていますが、特定の産業用放射線検査など、現在でも規制下で限定的に使用されるケースが残っています。
実際の使用において、形態および化合物の種類が重要となる理由
第2族元素の場合、実際に使用されるのは純金属ではなく、しばしばその化合物です。
その単一の考え方が、多くの混乱を解消します。食品や医薬品に含まれるマグネシウムは、燃焼するマグネシウムリボンとは同じものではありません。骨に存在するカルシウムは、反応性の高い金属カルシウムとは同じではありません。バリウムは「形態が重要である」ことを示す最も明確な例です:不溶性の硫酸バリウムは画像診断において有用ですが、より可溶性のバリウム化合物は、はるかに厳重な取り扱いが求められます。ラジウムはさらにこの点を推し進めます。なぜなら、その取り扱いを決定づけるのは、単に金属元素としての位置ではなく、むしろその放射能だからです。
したがって、第2族元素の価値はまったく抽象的ではありません。これらの元素は、同一の族が栄養学、材料科学、医療、工業プロセス、そして安全規則といった多様な分野でいかに重要であるかを説明する手助けとなります。実際の用途を簡潔に列挙するだけでも、全体的なパターンを定着させるには十分です。
第2族元素に関する主要な要点
この時点で、 アルカリ土類金属族 は、暗記すべき単なるリストというよりも、周期表の 第2族の縦列 から直接読み取れるパターンのように感じられるはずです。もし誰かがまだ「 アルカリ土類金属とは何ですか 、簡潔な答えはシンプルです:ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、ラジウムです。より包括的な アルカリ土類金属の定義 はさらに有用です:通常、最外殻の電子を2個失い、M 2+イオンを形成する、sブロックの第2族に属する6つの金属元素です。
アルカリ土類金属に関する主な要点
- 位置が重要です: この6つの 第2族元素 は、左から2番目の列、つまりsブロックの第2族セクションに位置しています。
- 族の構成員は固定されています: Be、Mg、Ca、Sr、Ba、Raがこの族全体を構成します。
- 共有される化学的性質が、族内の類似性を説明しています: ns電子配置 2価電子配置により+2イオンが一般的な生成物となり、これはLibreTextsによって要約された核心的な要点です。
- 主な下方への傾向は予測可能です: 原子半径は増加し、イオン化エネルギーは一般に減少し、反応性は通常、族を下るにつれて高まります。
- 例外も重要です: ベリリウムは他の元素と比べてより共有結合的性質を示し、マグネシウムは表面被膜のためにやや反応性が低く見える場合があり、ラジウムについては主にその放射能を通じて議論されます。
- 実際の応用では、純金属ではなく化合物が用いられることがほとんどです: 人々がカルシウム、マグネシウム、バリウムの元素形態よりも、はるかに頻繁に炭酸カルシウム、酸化マグネシウム、硫酸バリウムに触れる。
ランハイ社製の アルカリ土類金属の周期表 この族は、6つの金属が1つのルール(通常+2価のイオンになる)で結ばれていると覚えるのが最も簡単ですが、各元素はそのルールをわずかに異なる形で示します。
第2族元素の化学から、設計された金属部品へ
このような化学的性質は教科書の範囲をはるかに超えています。LibreTextsでは、元素状態のマグネシウムが大規模に生産され、航空機のフレームや自動車エンジン部品向けの軽量合金に使用されていると指摘しています。より包括的な合金ガイドでは、それがなぜ重要であるかが示されています:エンジニアは実際の部品において、重量、強度、耐食性、切削性のバランスを取るために、組成および加工条件を調整します。
「 第2族の縦列 」の視点から製造現場へと進む読者にとって、 シャオイ金属技術 その関係性を実践的に示す例を提供しています。自動車用材料および機械加工に関するページでは、試作から量産に至るまでの金属部品の製造工程について説明しており、ここで材料の挙動と工程制御が相互に連携して機能する必要があります。このため、 アルカリ土類金属の周期表 は単なる教室用の図表ではありません。また、軽量性・信頼性・製造可能性を兼ね備えたエンジニアリング部品向けに金属および合金を選定する際の論理的根拠の一部でもあります。
アルカリ土類金属に関するよくあるご質問(FAQ)
1. アルカリ土類金属にはどのような元素がありますか?
アルカリ土類金属は、ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、ラジウムの6種類です。これらは周期表の第2族に属し、一般に最外殻電子を2個失う傾向があるため、多くの化合物において共通の2+イオンを形成します。
2. アルカリ土類金属とアルカリ金属の違いは何ですか?
アルカリ金属は第1族に属し、最外殻電子が1個であるため、通常+1価のイオンを形成します。アルカリ土類金属は第2族に属し、通常+2価のイオンを形成し、全体としてアルカリ金属よりも反応性が低い傾向があります。この1個の余分な価電子が、結合の強さ、水との反応性、および生成される塩や酸化物の種類を決定します。
3. なぜアルカリ土類金属は自然界で遊離状態(単体)では見つからないのですか?
これらの金属は十分に反応性が高いため、自然環境下では純粋な単体の形で長期間安定して存在しません。代わりに、酸素、炭酸イオン、硫酸イオン、塩化物イオン、またはケイ酸塩イオンなどと結合し、鉱物、岩石、海水、貝殻、骨などの構成成分となります。そのため、人々が第2族元素に触れる機会は、通常、単体の金属ではなく、その化合物を通じて生じます。
4. すべてのアルカリ土類金属は水と反応しますか?
いいえ。これは覚えておくと非常に役立つ例外の一つです。ベリリウムは水に対してほとんど反応せず、マグネシウムは表面に生成される被膜によって反応が制限されるため、冷水ではゆっくりと反応します。一方、カルシウム、ストロンチウム、バリウムはより容易に反応します。一般に、第2族元素では、周期表の上から下へ進むにつれて水との反応性が強くなります。
5. アルカリ土類金属は、産業および製造業においてなぜ重要なのでしょうか?
その重要性は、それらの化合物および合金選定における役割の両方に由来します。マグネシウムは軽量性が求められる場面で価値があり、カルシウム化合物はセメントやプラスターの製造において中心的な役割を果たし、バリウム化合物は特殊な産業用途および医療用途に選ばれます。実際の生産現場では、金属の挙動を理解することが、機械加工の最適化、工程の安定性確保、部品品質の向上に不可欠です。そのため、シャオイ・メタル・テクノロジー(Shaoyi Metal Technology)などのサプライヤーは、自動車部品向けの認証済み機械加工、工程管理、試作部品から量産までを支援するサービスを強調しています。
 少量のバッチ、高い基準。私たちの迅速なプロトタイピングサービスにより、検証がより速く簡単になります——
少量のバッチ、高い基準。私たちの迅速なプロトタイピングサービスにより、検証がより速く簡単になります——
