Jakie są metale w układzie okresowym? Liczba, którą większość stron pomija
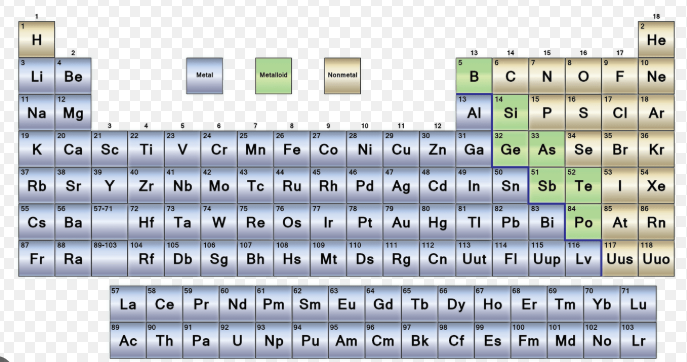
Jakie są metale w układzie okresowym pierwiastków?
Jeśli szukali Państwo odpowiedzi na pytanie, jakie są metale w układzie okresowym pierwiastków, to krótka odpowiedź jest prostsza, niż wydaje się na pierwszy rzut oka. Metale to pierwiastki, które zwykle zachowują się w charakterystyczny dla metali sposób, np. przewodzą prąd elektryczny, odbijają światło, gięją się bez pękania oraz tracą elektrony w reakcjach.
Bezpośrednia odpowiedź na pytanie: jakie są metale w układzie okresowym?
Metale to pierwiastki w układzie okresowym, które zazwyczaj wykazują właściwości metaliczne. Większość z nich dobrze przewodzi ciepło i prąd elektryczny, często ma połysk, jest zwykle kowalna i ciągliwa oraz ma tendencję do tworzenia jonów dodatnich poprzez utratę elektronów. Większość znanych pierwiastków stanowią metale, choć dokładna liczba może nieznacznie się różnić w zależności od klasyfikacji pierwiastków pogranicznych.
Prościej mówiąc, czytelnicy zadający pytanie, jakie są pierwiastki metaliczne w układzie okresowym pytają o dużą grupę obejmującą znane przykłady, takie jak sód, glin, żelazo, miedź, srebro i złoto. W podstawowej chemii układ okresowy jest często wprowadzany jako trzy szerokie kategorie: metale, niemetale i metaloidy.
Dlaczego większość pierwiastków jest klasyfikowana jako metale
Większość pierwiastków zalicza się do kategorii metali ze względu na zachowanie ich elektronów walencyjnych. Metale zwykle łatwiej tracą elektrony niż niemetale, co wyjaśnia, dlaczego tworzą one jony dodatnie oraz dlaczego wiele z nich dobrze przewodzi ciepło i prąd elektryczny. Britannica zauważa, że około trzech czwartych znanych pierwiastków chemicznych to metale, a LibreTexts opisuje metale jako pierwiastki, które zwykle tworzą jony dodatnie poprzez utratę elektronów.
- Większość pierwiastków w układzie okresowym to metale.
- Kluczowe cechy obejmują przewodnictwo, połysk, kowalność i ciągliwość.
- Metale zwykle tracą elektrony podczas reakcji chemicznych.
- Wzór rozmieszczenia metali i niemetali w układzie okresowym staje się łatwiejszy do odczytania, gdy zauważymy również graniczną grupę metaloidów.
- Dokładna liczba metali nie jest zawsze przedstawiana w ten sam sposób na każdej tabeli.
Ostatni szczegół ma większe znaczenie, niż się wydaje, ponieważ klasyfikacja zaczyna się od właściwości, ale układ układu okresowego pokazuje, gdzie zwykle znajdują się metale, niemetale i metaloidy.
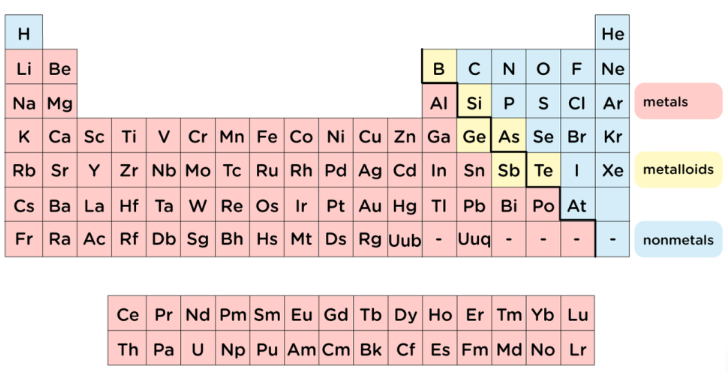
Gdzie znajdują się metale w układzie okresowym?
Szybkie spojrzenie na kolorową tabelę ujawnia podstawowy wzór. Jeśli pytacie, gdzie znajdują się metale w układzie okresowym, należy spojrzeć na lewą stronę oraz szeroki środek tabeli. Sód znajduje się daleko po lewej stronie , żelazo zajmuje środek, a metale takie jak glin i złoto pokazują, że pierwiastki metaliczne rozciągają się na dużą część tabeli. Nawet dwie rzędy zwykle umieszczane poniżej głównej części tabeli – lantanowce i aktynowce – są również metalami.
Gdzie znajdują się metale w układzie okresowym
Studenci, którzy pytają, gdzie znajdują się metale w układzie okresowym pierwiastków, mogą posłużyć się linią zygzakową (schodkową) jako wytyczną. Elementy po lewej stronie tej linii są zazwyczaj metalami. Elementy po prawej stronie to głównie niemetale. Elementy znajdujące się wzdłuż granicy to metaloidy. Podsumowanie układu z ThoughtCo umieszcza większość metali po lewej stronie układu okresowego pierwiastków, podczas gdy ChemistryTalk opisuje niemetale jako skupiające się po prawej stronie oraz metaloidy jako leżące wzdłuż granicy zygzakowej.
Zatem gdzie w praktyce znajdują się metale w układzie okresowym pierwiastków? Przede wszystkim po lewej stronie linii schodkowej oraz w jego środkowej części. Odpowiada to również na pytanie, gdzie w większości podręczników znajdują się metale w układzie okresowym pierwiastków. Jednym z znanych wyjątków jest wodór. Pojawia się w górnym lewym rogu, ale jest niemetalem.
| Obszar tabeli | Typowa klasyfikacja | Przykłady |
|---|---|---|
| Strona lewa i środek | Przeważnie metale | Sód, glin, żelazo, złoto |
| Granica w kształcie zygzaka | Przeważnie metaloidy | Krzem, arsen, tellur |
| Górny prawy róg | Przeważnie niemetale | Tlen, azot, chlor |
Prosta, kolorowo zakodowana tablica okresowa znacznie ułatwia zapamiętanie tego wzorca już przy pierwszym spojrzeniu.
Jak zmienia się charakter metaliczny w okresach i grupach
Położenie nie jest przypadkowe – odzwierciedla zachowanie elektronów. LibreTexts wyjaśnia, że charakter metaliczny ogólnie wzrasta w miarę przesuwania się w dół grupy oraz w lewo w obrębie okresu. W dół grupy atomy stają się większe, a energia jonizacji maleje, więc elektrony walencyjne łatwiej jest usunąć. W obrębie okresu, od lewej do prawej strony, atomy silniej wiążą elektrony, dlatego charakter metaliczny maleje.
Ten trend pomaga wyjaśnić, dlaczego sód jest bardziej metaliczny niż pierwiastki położone dalej w prawo w tym samym okresie oraz dlaczego w lewym dolnym rogu układu znajduje się najbardziej reaktywnych metali. Żelazo, glin i złoto są wszystkie metalami, ale ich położenie sugeruje, że nie wszystkie metale zachowują się w ten sam sposób. Mapa jest wyraźna. Liczba jednak staje się trudniejsza do ustalenia, ponieważ przypadki brzegowe nie mieszczą się w dokładnie ten sam sposób we wszystkich tabelach.
Metale, niemetale i metaloidy w układzie okresowym
Ten wzór obejmujący lewą i środkową część układu ułatwia rozpoznawanie metali, ale ich zliczanie jest mniej jednoznaczne, niż sugerują wiele stron internetowych. Królewskie Towarzystwo Naukowe stwierdza, że ponad dwie trzecie wszystkich pierwiastków stanowią metale w warunkach otoczenia. Niemniej jednak różne źródła nie zawsze podają tę samą dokładną liczbę, ponieważ odpowiedź zależy od tego, jak traktowane są pierwiastki brzegowe w tabeli metali, niemetali i metaloidów.
Dlaczego źródła różnią się w ocenie liczby metali
Niezgodności wynikają zazwyczaj z reguł klasyfikacji, a nie z błędów w liczeniu. Ta sama recenzja Royal Society wskazuje na ważny szczegół: układ okresowy zawiera pierwiastki, ale etykiety takie jak „metal” i „niemetal” opisują sposób, w jaki te pierwiastki zachowują się w swojej postaci pierwiastkowej w warunkach normalnych. W pobliżu „schodów”, to zachowanie nie jest zawsze wyraźnie rozgraniczone. Recenzja podkreśla również, że niektóre części bloku p, zwłaszcza wokół grup 14 i 15, mogą leżeć na granicy między metalami a niemetalem. Zatem choć schemat klasowy układu okresowego z podziałem na metale niemetale i metaloidy jest przydatny, upraszcza on bardziej skomplikowaną rzeczywistość.
Jeśli strona podaje jedną dokładną liczbę metali bez określenia przyjętych reguł klasyfikacji, estetyka może przeważać nad dokładnością.
W jaki sposób reguły klasyfikacji wpływają na całkowitą liczbę
Konserwatywna liczba zaczyna się od wyraźnie metalicznych rodzin. Szeroka liczba może obejmować także metaliczne elementy bloku p, traktując jednak elementy położone przy „schodach” z większą ostrożnością. IUPAC prowadzi aktualizację układu okresowego i zauważa, że nawet pytania strukturalne, takie jak umiejscowienie grupy 3, były przedmiotem debat. Ta debata nie zaciera ogólnego obrazu, lecz przypomina czytelnikom, że klasyfikacja naukowa obejmuje zarówno konwencję, jak i obserwację. W praktyce największym problemem zliczania jest zwykle obszar brzegowy, gdzie oznaczenie jako metalu, niemetalu lub metaloidu może się różnić w zależności od wykresu.
| Kategoria | Typowe traktowanie | Dlaczego to ważne? |
|---|---|---|
| Wyraźnie metaliczne rodziny | Prawie zawsze zaliczane do metali | Obejmuje główne bloki metaliczne i budzi niewiele sporów |
| Metaliczne elementy bloku p | Zwykle zaliczane do metali | Nadal metaliczne, ale bliżej granicy schodkowej |
| Obszar brzegowy | Mogą być oznaczane jako metaloidy lub elementy pośrednie | To miejsce, w którym porównania metaloidów, metali i niemetali prowadzą do różnych wyników |
Przydatną odpowiedzią nie jest więc po prostu liczba. Jest to przegląd rodzin pierwiastków z podziałem na poszczególne rodziny, który pokazuje, które grupy są zawsze klasyfikowane jako metale, a które znajdują się wystarczająco blisko granicy, by powodować zamieszanie.
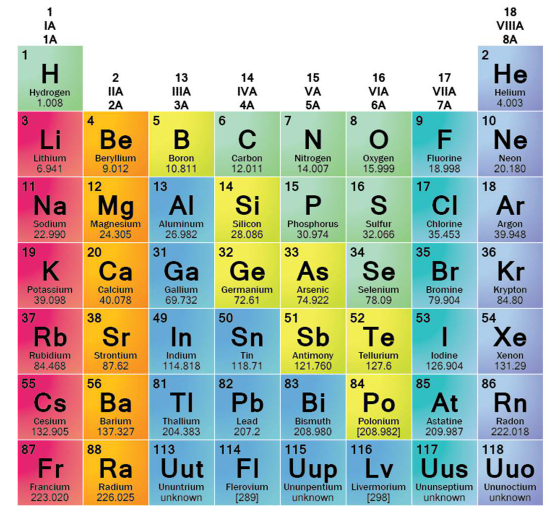
Rodziny układu okresowego pierwiastków
Przegląd rodzinami znacznie ułatwia zrozumienie strony metalicznej układu okresowego. W chemii rodzina pierwiastków w układzie okresowym obejmuje pierwiastki o podobnej budowie zewnętrznego powłoki elektronowej oraz – w konsekwencji – podobnym zachowaniu chemicznym. Dlatego klasyfikacja metali jest bardziej użyteczna niż prosta mapa „lewa strona kontra prawa strona”. Krótkie podsumowanie z serwisu ThoughtCo, wraz z klasyfikacją metali stosowaną przez Los Alamos , zapewnia czytelnikom praktyczny sposób porządkowania głównych rodzin pierwiastków metalicznych.
Rodziny metali w układzie okresowym
Sześć rodzin, które większość czytelników powinna znać, to metale alkaliczne, metale ziem alkalicznych, metale przejściowe, metale po przejściowe, lantanowce i aktynowce. Jeśli widziałeś/-aś inne nazwy grup w układzie okresowym, jest to normalne. Współczesne układy okresowe numerują kolumny od 1 do 18, ale nazwy rodzin koncentrują się na wspólnych cechach chemicznych; niektóre rodziny obejmują więcej niż jedną kolumnę lub nawet oddzielne wiersze umieszczone poniżej głównej części tabeli.
| Rodzina metali | Gdzie występuje | Cechy do zapamiętania |
|---|---|---|
| Metale alkaliczne | Grupa 1, z wyłączeniem wodoru | Jeden elektron walencyjny, miękkie, błyszczące, wysoce reaktywne, zwykle tworzą jony o ładunku +1 |
| Metale ziem alkalicznych | Grupa 2 | Dwa elektrony walencyjne, twardsze i gęstsze niż metale alkaliczne, zwykle tworzą jony o ładunku +2 |
| Metale przejściowe | Grupy 3–12, blok d-centralny | Twarde, gęste, przewodzące, często o wysokich temperaturach topnienia, występujące w kilku stopniach utlenienia |
| Metale poprzeczne | bloki p, po prawej stronie bloku przejściowego | Miększe metale, które przewodzą gorzej niż metale przejściowe |
| Lantanowce | Elementy o numerach atomowych 57–71, pierwszy oddzielny wiersz | Bardzo podobne właściwości chemiczne, część bloku f |
| Aktynowce | Elementy o numerach atomowych 89–103, drugi oddzielny wiersz | metale bloku f, wszystkie radioaktywne |
Co czyni każdą grupę metali inną
Zacznij od skrajnej lewej strony. Metale alkaliczne z układu okresowego są najłatwiejsze do zidentyfikowania, ponieważ posiadają jeden elektron walencyjny i reagują gwałtownie, zwłaszcza z wodą. Metale grupy 2 nadal ulegają reakcji, ale ich dwa zewnętrzne elektrony czynią je mniej reaktywnymi i ogólnie twardszymi niż metale grupy 1. W środkowej części układu okresowego znajdują się metale przejściowe, obejmujące szeroki centralny blok, znany z tworzenia twardych ciał metalicznych, dobrej przewodności oraz szerokiego zakresu stopni utlenienia.
Przesuń się nieco dalej w prawo, a wzór staje się łagodniejszy. Metale poprzeczne pozostają metalami, ale zwykle są miększe i gorszymi przewodnikami niż metale przejściowe. Dwie rzędy umieszczone poniżej tabeli wprowadzają jeszcze większą subtelność. Lantanowce charakteryzują się bardzo podobną chemią, podczas gdy aktynowce wyróżniają się promieniotwórczością. Niektóre źródła opisują oba te rzędy nawet jako specjalne metale przejściowe, co pokazuje, dlaczego nazwy grup w układzie okresowym mogą być pomocne, ale nie mogą zastąpić rzeczywistego zachowania chemicznego.
- Grupa 1 oznacza metale miękkie i wysoce reaktywne.
- Grupa 2 oznacza metale reaktywne, ale zwykle twardsze niż te z Grupy 1.
- Grupy 3–12 oznaczają centralny blok zawierający wiele klasycznych metali.
- Metale poprzeczne oznaczają miększe metale znajdujące się w pobliżu regionu „schodów”.
- Lantanowce i aktynowce oznaczają dwa rzędy bloku f umieszczone poniżej głównej części tabeli.
Te etykiety rodzin czynią tabelę bardziej uporządkowaną, ale głębszym testem metalu nie jest jego nazwa rodziny samodzielnie. Przewodnictwo elektryczne, połysk, kowalność oraz utrata elektronów wyjaśniają, dlaczego wszystkie te grupy znajdują się w pierwszej kolejności po stronie metali.
Jakie są właściwości metali?
Etykiety rodzin ułatwiają przeglądanie układu okresowego, ale chemicy identyfikują metal na podstawie jego zachowania, a nie wyłącznie na podstawie nazwy. Gdy uczniowie pytają, jakie są właściwości metali, odpowiedź zaczyna się od wzorca wspólnych cech fizycznych i chemicznych. W LibreTexts opisie wiązania metalicznego atomy metalu są przyciągane przez chmurę ruchomych, zdelokalizowanych elektronów. Ten prosty model pomaga wyjaśnić właściwości metaliczne metali oraz dlaczego tak wiele różnych rodzin metali nadal wykazuje rozpoznawalny zestaw zachowań.
Wspólne właściwości większości metali
Jeśli porównać właściwości metali i niemetali, metale zwykle wyróżniają się w kilku wyraźnych aspektach.
- Przewodność elektryczna: Swobodne elektrony pozwalają metalom dobrze przewodzić prąd elektryczny. Przykładem klasycznym jest drut miedziany.
- Przewodność cieplna: Te same elektrony wspomagają przewodzenie ciepła, dlatego metale takie jak miedź i aluminium są przydatne tam, gdzie istotna jest wymiana ciepła.
- Połysk: LibreTexts wyjaśnia, że elektrony w metalach mogą pochłaniać energię, a następnie ponownie emitować światło, nadając metalom ich błyszczącą powierzchnię. Wyraźnie widać to na przykładzie złota, srebra i miedzi.
- Kowalność: Metale można kовать lub walcować w arkusze zamiast tego, aby się kruszyły. Łatwymi przykładami są folia aluminiowa i cienka złota folia.
- Kruczość: Metale można wydłużać w druty. Miedź ponownie stanowi powszechnie znany przykład.
- Tworzenie jonów dodatnich: Wiele metali traci elektrony podczas reakcji chemicznych. Sód tworzy jon Na⁺, magnez – Mg²⁺, a glin – Al³⁺.
| Nieruchomości | Element reprezentatywny | Co to pokazuje |
|---|---|---|
| Przewodnictwo elektryczne | Miedź | Przydatny do okablowania i obwodów |
| Przewodność cieplna | Aluminium | Skutecznie przekazuje ciepło |
| Blask | Srebro | Powierzchnia odbijająca, polerowana |
| Ciągliwość | Złoto | Może być formowany w bardzo cienkie arkusze |
| PLASTYCZNOŚĆ | Miedź | Może być wyciągany w długie druty |
Przykłady pokazujące, że metale nie są wszystkie takie same
Te cechy to silne tendencje, a nie doskonała lista kontrolna. W źródle LibreTexts zauważono, że rtęć jest cieczą w temperaturze pokojowej, mimo że metale zwykle są stanu stałego. To samo źródło wskazuje, że sód i potas są na tyle miękkie, że można je kroić nożem, co czyni je bardzo różnymi od twardych metali, takich jak żelazo. Przewodność również się różni: srebro i miedź są szczególnie dobrymi przewodnikami, podczas gdy niektóre metale osiągają znacznie gorsze wyniki. Również reaktywność różni się w dużym stopniu: złoto zachowuje swój wygląd lepiej niż wiele innych metali, ponieważ znacznie skuteczniej opiera się korozji niż metale takie jak żelazo.
Dlatego cechy metali najlepiej traktować jako zbiór wskazówek. Same błyszczenie nie wystarcza. Samą przewodność również nie można uznać za wystarczającą. Chemicy analizują całą strukturę: sposób, w jaki dany pierwiastek przewodzi prąd, ulega odkształceniu oraz jak zachowuje się w reakcjach podczas utraty elektronów. Patrząc na to w ten sposób, kolejne praktyczne pytanie staje się znacznie łatwiejsze do odpowiedzi: które konkretne pierwiastki należą do kategorii metali przy porządkowaniu ich według rodzin?
Lista metali według rodziny układu okresowego
Czytelnicy, którzy chcą praktycznej listy metali zwykle nie potrzebują ściany nazw pierwiastków. Potrzebują struktury. Grupowanie pierwiastków metalicznych według rodziny ułatwia badanie, porównywanie i zapamiętywanie tej struktury. Poniższa główna tabela opiera się na ogólnych klasyfikacjach metali stosowanych przez Notatkami naukowymi i ThoughtCo, przy jednoczesnym zaznaczeniu tych nielicznych przypadków, w których źródła chemiczne czasem różnią się w podejściu. Jest to najbardziej przejrzysta metoda odpowiedzi na pytanie, które pierwiastki są metalami w układzie okresowym, bez pozorowania, że każda etykieta graniczna jest powszechnie ustalona.
Lista pierwiastków metalicznych według grupy rodzinnej
| Rodzina | Pierwiastki w danej grupie | Uwaga klasyfikacyjna |
|---|---|---|
| Metale alkaliczne | Lit, sód, potas, rubid, cez, frans | Wodór znajduje się w grupie 1, ale w normalnych warunkach jest zazwyczaj traktowany jako niemetal. |
| Metale ziem alkalicznych | Beryl, magnez, wapń, stront, bar, rad | Są one jednoznacznie klasyfikowane jako metale. |
| Metale przejściowe | Skand, tytan, wanad, chrom, mangan, żelazo, kobalt, nikiel, miedź, cynk, itr, cyrkon, niob, molibden, technet, ruten, rod, pallad, srebro, kadm, hafn, tantal, wolfram, ren, osm, iryd, platyna, złoto, rtęć, rutherford, dubn, seaborg, bohrium, hassium, meitner, darmstadtium, roentgenium, kopernik | Większość szkolnych układów okresowych umieszcza Zn, Cd i Hg w tej grupie, choć niektóre dyskusje chemiczne traktują je nieco inaczej. |
| Metale po przejściu lub metale zasadotwórcze | Aluminium, gal, ind, cyna, tal, ołów, bizmut, polon, nihonium, flerowium, moskowium, livermorium | Notatki naukowe dotyczące metali podstawowych zaznaczają, że skład tej grupy różni się najbardziej w zależności od źródła. Polon jest często do niej zaliczany, ale jego przynależność bywa kwestionowana. Livermorium jest często traktowane jako metal możliwy do uzyskania lub przewidywany. |
| Lantanowce | Lantan, cer, prazeodym, neodym, promet, samar, europ, gadolin, terb, dysproz, holm, erp, tul, iterb, lutec | Są to pierwszy oddzielny wiersz poniżej głównej tabeli i mają charakter metaliczny. |
| Aktynowce | Aktyn, tor, protaktyn, uran, neptun, pluton, ameryk, kur, berkeli, kaliforn, einstein, fermi, mendelew, nobel, lawrens | Są to drugi oddzielny wiersz poniżej głównej tabeli i mają charakter metaliczny, choć wiele z nich jest znanych głównie ze swojej radioaktywności, a nie typowego zachowania metali w codziennym użytkowaniu. |
Jak czytać główną listę bez pomyłek
Jeśli potrzebujesz szybkiej listy metali do pracy domowej lub powtórki użyj najpierw kolumny „rodzina”, a dopiero potem kolumny „uwagi”. Kolumna „rodzina” wskazuje, gdzie dany pierwiastek znajduje się w układzie okresowym. Kolumna „uwagi” wyjaśnia, gdzie granice klasyfikacji stają się niejasne. Ma to największe znaczenie w pobliżu „schodów” oraz wśród najcięższych pierwiastków bloku p.
Gdy nauczyciele proszą uczniów o wypisanie metali , zazwyczaj mają na myśli stabilne jądro tych rodzin, a nie dyskusję na temat każdego przypadku brzegowego. Jeśli chcesz podać tylko najbardziej znane nazwy metali , rozpocznij od najlepiej znanych członków każdej grupy i rozszerzaj listę stopniowo.
- Metale alkaliczne: sód, potas
- Metale ziem alkalicznych: magnez, wapń
- Metale przejściowe: żelazo, miedź, srebro, złoto
- Metale po przejściowe: glin, cyna, ołów
- Lantanowce: lantan, neodym
- Aktynowce: uran, pluton
To są kilka przykładów metali które większość czytelników już zna. Stanowią również dobre punkty odniesienia pamięciowe, gdy pełna tabela wydaje się zbyt „przepiętniona”. W notatkach do nauki warto pamiętać, że typowe nazwy metali często pochodzą z grup przejściowych i po-przejściowych, podczas gdy lantanowce i aktynowce łatwiej zapamiętać jako serie.
Jeszcze jedno ostrzeżenie zapewnia wiarygodność tej wyczerpującej listy: nie każda tabela wyznacza takie same granice dla pierwiastków takich jak polon czy najcięższe sztuczne pierwiastki bloku p. Dlatego przydatne źródło informacji robi więcej niż tylko wymienia nazwy pierwiastków — pokazuje także, gdzie granice stają się rozmyte, ponieważ etykietę „metal” najłatwiej zaakceptować, gdy można ją jednoznacznie odróżnić od metaloidu lub niemetalu.
Przewodnik po układzie okresowym: metale kontra niemetale
Długa główna lista jest przydatna, ale większość czytelników potrzebuje szybszego sposobu klasyfikacji danego pierwiastka w jednym rzucie oka. Dobrą wiadomością jest to, że układ okresowy dostarcza wyraźnego wrażenia wizualnego. Jeszcze lepszą wiadomością jest to, że chemia oferuje dodatkowy test potwierdzający, gdy sama układówka nie wystarcza.
Jak oddzielić metale od metaloidów i niemetali
Wizualna mapa z serwisu Science Notes wyraźnie przedstawia podstawowy wzór: metale znajdują się głównie po lewej stronie i w centrum, natomiast niemetale skupiają się po prawej stronie. Między nimi znajduje się znany schodkowy kształt granicy. Jeśli zadajesz pytanie, gdzie na układzie okresowym znajdują się metaloidy, zwykle leżą one wzdłuż tej zygzakowatej granicy. Przewodnik chemiczny UMD korzysta z tego samego wzoru do szybkiej identyfikacji.
Jednak pytanie o podział pierwiastków na metale i niemetale w układzie okresowym nie rozstrzyga się wyłącznie na podstawie ich położenia. Najlepszym sposobem oddzielenia metali od niemetali na schematach układu okresowego jest także uwzględnienie ich właściwości chemicznych i fizycznych. Metale zwykle dobrze przewodzą ciepło i prąd elektryczny oraz często tracą elektrony, tworząc kationy. Niemetale w układzie okresowym mają tendencję do przyjmowania lub udostępniania elektronów, a wiele z nich słabo przewodzi prąd. Metaloidy w układzie okresowym znajdują się w strefie przejściowej i często wykazują właściwości pośrednie oraz zachowanie półprzewodnikowe.
- Znajdź linię schodową na tabeli.
- Spójrz najpierw w lewą lub środkową część tabeli. Większość tam znajdujących się pierwiastków to metale.
- Spójrz w prawy górny róg tabeli. Większość tam znajdujących się pierwiastków to niemetale.
- Sprawdź samą granicę. Pierwiastki leżące bezpośrednio na niej są zazwyczaj metaloidami.
- W razie potrzeby sprawdź zachowanie pierwiastka. Dobrze przewodzący materiał sugeruje metal, słabo przewodzący – niemetal, natomiast zachowanie pośrednie lub półprzewodnikowe wskazuje na metaloid.
- Zwróć uwagę na wyjątki. Wodór znajduje się po lewej stronie, ale zwykle jest niemetalem. Jeśli zadasz pytanie, czy krzem jest metalem, niemetalem czy metaloidem, to krzem jest zazwyczaj klasyfikowany jako metaloid. Jego rolę jako półprzewodnika podkreśla przewodnik po metaloidach firmy MISUMI.
Schodkowa linia jest jedynie wskazówką, a nie gwarancją. Elementy pograniczne mogą być oznaczone różnie w zależności od danej tabeli oraz zastosowanych zasad klasyfikacji.
Proste środki wspomagające pamięć do szybszej identyfikacji
- Po lewej i w centrum – myśl o metalach.
- W prawym górnym rogu – myśl o niemetalach.
- Na schodkowej linii – myśl o metaloidach.
- Pamiętaj o wskazówce zachowania: przewodzenie, opór lub półprzewodnictwo.
Ten szybki schemat znacznie ułatwia odczytywanie na diagramach układu okresowego, które pierwiastki są metalami, a które niemetalem – zwłaszcza w sytuacjach stresu. Wskazuje on również na coś ważniejszego niż sama pamięciowa nauka, ponieważ różnica między przewodzącym metalem a półprzewodzącym metaloidem decyduje o wyborze rzeczywistych materiałów w elektronice i przemyśle.

Dlaczego metale w układzie okresowym mają znaczenie w przemyśle
Wzór schodowy robi więcej niż tylko pomaga uczniom sortować elementy. W projektowaniu i produkcji pytanie „czym jest metal?” szybko przekształca się w praktyczną decyzję dotyczącą właściwości użytkowych. Wiedza na temat położenia metali w układzie okresowym daje inżynierom pierwsze wskazówki dotyczące przewodności elektrycznej, wytrzymałości, plastyczności oraz przewodzenia ciepła, ale rzeczywista produkcja idzie dalej niż etykiety stosowane w klasie.
Dlaczego klasyfikacja metali ma znaczenie w rzeczywistej produkcji
Metaliczny pierwiastek chemiczny często stanowi punkt wyjścia, a nie końcowy etap. AJProTech opisuje dobór materiału jako równowagę między obciążeniami, środowiskiem, masą, możliwością produkcji, dostępnością, kosztem oraz zgodnością z przepisami. Dlatego różne typy metali rozwiązują różne problemy. TIRapid wyraźnie ilustruje ten wzór: miedź jest ceniona ze względu na przewodnictwo elektryczne i cieplne, aluminium – ze względu na niską gęstość i odporność na korozję, stal – ze względu na wytrzymałość i opłacalność, a tytan – ze względu na wysoką wytrzymałość właściwą w wymagających warunkach eksploatacyjnych. W praktyce wiele gotowych części wykonuje się z stopów, a nie z czystych pierwiastków metalicznych, ponieważ zadanie zwykle wymaga lepszego balansu właściwości.
- Transport: Aluminium i magnez pomagają zmniejszyć masę, podczas gdy stal pozostaje powszechnym wyborem dla elementów konstrukcyjnych ze względu na połączenie wytrzymałości z realnymi kosztami.
- Elektronika: Miedź jest preferowanym materiałem tam, gdzie istotne są przepływ prądu i przewodzenie ciepła.
- Surowe środowiska: Stal nierdzewna, tytan oraz materiały oparte na niklu są przydatne w przypadku, gdy kluczowe stają się odporność na korozję lub stabilność w wysokich temperaturach.
- Planowanie produkcji: Obrobialność ma również znaczenie. Materiał, który wydaje się idealny na papierze, może nadal zwiększać zużycie narzędzi, czas realizacji czy wymagania dotyczące kontroli jakości.
Gdzie można zapoznać się z precyzyjną obróbką metali
Pierwiastek metaliczny w układzie okresowym staje się użytecznym materiałem dopiero wtedy, gdy proces produkcyjny jest dostosowany do jego właściwości. Aluminium umożliwia szybką obróbkę i lekkie konstrukcje, podczas gdy bardziej wytrzymałe stopy stalowe lub tytanu mogą wymagać ścislejszej kontroli procesu. Dlatego inżynierowie zwracają uwagę nie tylko na skład chemiczny, ale także na wymiary graniczne, obróbkę powierzchni, walidację oraz powtarzalność.
Jako praktyczny przykład Shaoyi Metal Technology przedstawia przepływ pracy związany z obróbką elementów samochodowych, łączący szybkie prototypowanie, produkcję małoseryjną i masową z systemem zarządzania jakością IATF 16949 oraz statystyczną kontrolą procesu (SPC). W takim ujęciu układ okresowy przestaje być jedynie tabelą do nauki na pamięć i staje się przewodnikiem przy wyborze materiałów, które można skutecznie obrobić, zweryfikować i zaufać im w rzeczywistych komponentach.
- Wykorzystaj skład chemiczny, aby zawęzić wybór.
- Korzystaj z kryteriów inżynierskich przy wyborze ostatecznego materiału.
- Wykorzystaj kontrolę procesu, aby przekształcić odpowiedni metal w niezawodny element.
To właśnie prawdziwa wartość poznawania metali znajdujących się w układzie okresowym: nie tylko ich nazewnictwo, ale także zrozumienie, jak klasyfikacja metali wpływa na elementy, którymi ludzie jeżdżą, przewodzą prąd, chłodzą i budują codziennie.
Najczęstsze pytania dotyczące metali w układzie okresowym
1. Ile metali znajduje się w układzie okresowym?
Nie istnieje jedna, uznawana przez wszystkie źródła, ostateczna liczba. Większość pierwiastków to metale, jednak dokładna liczba może się zmieniać w zależności od tego, jak dana tabela traktuje przypadki pograniczne – zwłaszcza w obszarze tzw. „schodów” oraz wśród niektórych cięższych pierwiastków bloku p. Dokładna odpowiedź rozróżnia wyraźnie rodziny pierwiastków metalicznych od tych, które czasem są klasyfikowane inaczej, zamiast wymuszać jedno uproszczone podsumowanie.
2. Gdzie znajdują się metale w układzie okresowym?
Metale znajdują się głównie po lewej stronie i w centrum układu okresowego. Dwie oddzielne rzędy u dołu – lantanowce i aktynowce – są również metalami. Szybkim sposobem odczytania układu jest linia schodowa: większość pierwiastków po lewej stronie to metale, większość po prawej to niemetale, a obszar graniczny zawiera wiele metaloidów. Wodor jest typowym wyjątkiem wizualnym, ponieważ znajduje się po lewej stronie, ale zwykle klasyfikowany jest jako niemetal.
3. Jakie są główne rodziny metali w układzie okresowym?
Główne rodziny metali to metale alkaliczne, metale ziem alkalicznych, metale przejściowe, metale poprzeczne, lantanowce oraz aktynowce. Każda z tych rodzin charakteryzuje się własnymi cechami. Metale alkaliczne są bardzo reaktywne, metale ziem alkalicznych są mniej reaktywne, ale nadal aktywne, metale przejściowe obejmują wiele znanych metali stosowanych w budownictwie i inżynierii, metale poprzeczne są zazwyczaj miększe, natomiast lantanowce i aktynowce tworzą dwa rzędy metali umieszczone poniżej głównej części układu okresowego.
4. Jakie właściwości sprawiają, że dany pierwiastek jest metalem?
Chemicy zazwyczaj identyfikują metal na podstawie zestawu cech, a nie pojedynczej cechy. Metale zwykle dobrze przewodzą ciepło i prąd elektryczny, odbijają światło, uginają się bez pęknięcia, rozciągają się w druty oraz mają tendencję do oddawania elektronów w reakcjach chemicznych. Niemniej jednak nie wszystkie metale zachowują się w ten sam sposób. Niektóre są miękkie, inne wykazują dużą odporność na korozję, a jeden znany przykład – rtęć – jest cieczą w temperaturze pokojowej.
5. Dlaczego ma znaczenie, czy dany pierwiastek jest metalem, w procesach produkcyjnych?
Klasyfikacja metali pomaga powiązać chemię z rzeczywistymi decyzjami dotyczącymi materiałów. Gdy inżynierowie wiedzą, że dany materiał jest metalem, mogą zacząć rozważać jego przewodność elektryczną, wytrzymałość, odporność na korozję, masę oraz obrabialność. Ma to znaczenie w elektronice, elementach stosowanych w transporcie oraz komponentach przemysłowych. W praktyce przekształcenie metalicznego pierwiastka lub stopu w użyteczny detal zależy również od kontroli procesu oraz precyzyjnej obróbki skrawaniem. Na przykład firma Shaoyi Metal Technology stosuje obróbkę skrawaniem certyfikowaną zgodnie ze standardem IATF 16949 oraz kontrolę jakości opartą na statystycznej kontroli procesu (SPC), aby wspierać przejście od etapu prototypowania do produkcji gotowych części metalowych.
 Małe partie, wysokie standardy. Nasza usługa szybkiego prototypowania sprawia, że weryfikacja jest szybsza i łatwiejsza —
Małe partie, wysokie standardy. Nasza usługa szybkiego prototypowania sprawia, że weryfikacja jest szybsza i łatwiejsza —
