Czym są metale ziem alkalicznych? Grupa 2 wreszcie nabiera sensu
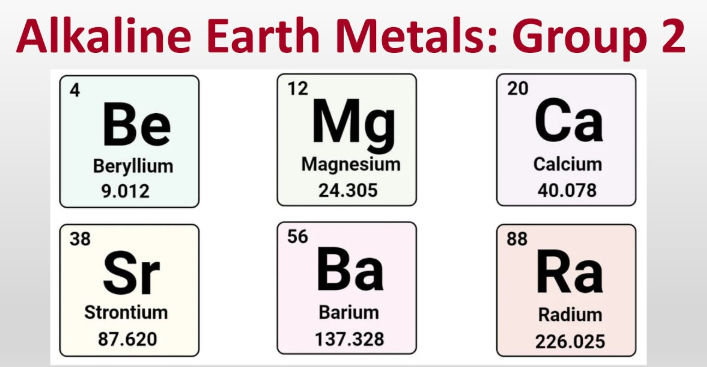
Czym są metale ziem alkalicznych?
Jeśli wyszukiwałeś czym są metale ziem alkalicznych , oto bezpośrednia odpowiedź: są to sześć pierwiastków w Grupa 2 grupie 2 definicja metali ziem alkalicznych stanowi punkt wyjścia, ale nazwa mówi także wiele o tym, jak zachowuje się ta rodzina pierwiastków.
Jak brzmi definicja metali ziem alkalicznych w jednym zdaniu?
Metalami ziem alkalicznych są beryl, magnez, wapń, stront, bar i rad – sześć pierwiastków metalicznych z grupy 2, które zwykle tworzą jony o ładunku +2.
- Beryll (Be)
- Magnez (Mg)
- Wapń (Ca)
- Stront (Sr)
- Bar (Ba)
- Rad (Ra)
Dlaczego nazwa metale ziem alkalicznych jest uzasadniona
Dla początkujących definicja metali ziem alkalicznych staje się znacznie łatwiejsza, gdy podzieli się to wyrażenie na trzy części.
Alkaliczny oznacza, że ich tlenki i wodorotlenki są zasadowe, a nie kwasowe. Ziemi jest terminem historycznym. Wcześni chemicy używali go do opisu substancji odpornych na ciepło, przypominających minerały, które nie topią się ani nie rozpuszczają łatwo w wodzie – punkt wyjaśniony przez Britannica . Metali oznacza, że same pierwiastki są metaliczne, zwykle błyszczące i dobrze oddają elektrony w reakcjach.
To daje podstawową definicję metali ziem alkalicznych bez konieczności najpierw poznanie zaawansowanej chemii. Jest to również przydatne krótkie opisanie metali ziem alkalicznych : rodziny metali grupy 2 o wspólnej chemii, wspólnym położeniu w układzie okresowym oraz istotnej roli w świecie rzeczywistym. Magnez występuje w stopach i biologii. Wapń odgrywa kluczową rolę w kościach, skorupkach i materiałach budowlanych. Bar, stront i rad występują w bardziej specjalistycznych zastosowaniach.
Ten artykuł zaczyna się celowo od podstaw. Prosta lista jest łatwa do zapamiętania, ale prawdziwe zrozumienie tej rodziny pojawia się dopiero wtedy, gdy zobaczy się, gdzie te pierwiastki się znajdują, oraz dlaczego ich położenie nadaje im tak podobne właściwości.
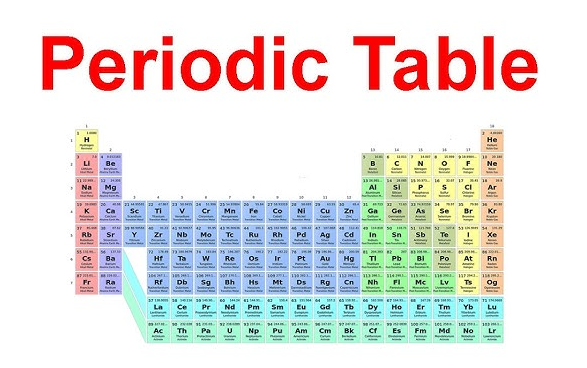
Położenie grupy 2 w układzie okresowym
Nazwa rodziny staje się znacznie łatwiejsza do zapamiętania, gdy można ją faktycznie zlokalizować. Jeśli zastanawiasz się gdzie znajdują się metale ziem alkalicznych w układzie okresowym , spojrzyj na drugą kolumnę od lewej strony. Ta pionowa kolumna to grupa 2 w układzie okresowym , położona bezpośrednio obok metali alkalicznych z grupy 1. A grupa 2 układu okresowego widok pokazuje tę samą prostą linię za każdym razem: beryl na górze, następnie magnez, wapń, stront, bar i rad w kolejności od góry do dołu przez okresy.
W tunelu układ okresowy metali ziem alkalicznych na wykresie te sześć pierwiastków należy do bloku s. Ich wspólne położenie ma znaczenie, ponieważ odzwierciedla wspólny wzór rozmieszczenia elektronów. Jak LibreTexts wyjaśnia, pierwiastki grupy 2 mają konfigurację walencyjną ns 2, co oznacza, że posiadają dwa elektrony na zewnętrznej powłoce.
Gdzie znajdują się metale ziem alkalicznych w układzie okresowym
Wizualnie wzór jest prosty. pierwiastki grupy 2 układu okresowego tworzą jedną rodzinę w kolumnie obejmującej okresy od 2 do 7. Wiele diagramów szkolnych podkreśla tę metale ziem alkalicznych w układzie okresowym układy z tym samym kolorem, ponieważ rodziny pierwiastków odczytuje się pionowo, a nie poziomo. Wyszukiwania frazy układ okresowy metali ziem alkalicznych właściwie dotyczą właśnie tej jednej kolumny.
| Element | Symbol | Pozycja grupy 2 | Typowy jon | Znany związek chemiczny |
|---|---|---|---|---|
| Beryllium | Be | Okres 2, górna część grupy 2 | Be2+ | BeO |
| Magnez | Mg | Okres 3 | Mg2+ | Mgo |
| Wapń | Ca | Okres 4 | Ca2+ | Caco 3 |
| Strychn | Sr | Okres 5 | Sr2+ | SrCO 3 |
| Barium | Ba | Okres 6 | Ba 2+ | BaSO 4 |
| Rad | RA | Okres 7, dolna część grupy 2 | RA 2+ | RaCl 2 |
Dlaczego pierwiastki grupy 2 tworzą jony o ładunku +2
Te dwa zewnętrzne elektrony decydują o chemii pierwiastków. Atomy grupy 2 mają tendencję do utraty obu elektronów, ponieważ nadaje to im bardziej stabilną konfigurację elektronową. Wynikiem jest +2 jon , takie jak Mg 2+ lub Ca 2+. Dlatego też metale te tworzą zwykle związki takie jak tlenki, chlorki, węglany i siarczany. Wzorzec ten można od razu zauważyć we wzorach chemicznych: MgO, CaCl 2, CaCO 3, BaSO 4.
Jak szybko rozpoznać rodzinę metali ziem alkalicznych
Szybka metoda identyfikacji polega na jednoczesnym poszukiwaniu trzech cech: położenia w drugiej kolumnie układu okresowego, charakteru metalicznego oraz typowego ładunku +2. W porównaniu z sąsiadującymi metalami alkalicznymi, które mają jeden elektron walencyjny i zwykle tworzą jony o ładunku +1, pierwiastki grupy 2 posiadają jeden dodatkowy elektron na zewnętrznej powłoce i są ogólnie mniej reaktywne. Niemniej jednak wyraźnie należą do wspólnej rodziny. Ciekawym aspektem jest to, że każdy jej członek wykazuje ten wzorzec w nieco inny sposób – szczególnie od berylu na szczycie do radu na dole.
Zapoznaj się z sześcioma metalami ziem alkalicznych
Lista jest przydatna, ale sama w sobie nie jest zbyt zapadająca w pamięć. Grupa 2 zaczyna wydawać się bardziej rzeczywista, gdy każdy jej członek ma wyraźną tożsamość. Niektóre występują w kościach lub wodzie morskiej. Niektóre nadają kolor ogniom strzelającym. Jedna z nich stanowi głównie historyczny znak ostrzegawczy. Razem nadal należą do tej samej rodziny, ale każda z nich ma własną osobowość.
| Element | Symbol | Powszechne występowanie | Wyróżniająca się właściwość | Reprezentatywność w warunkach rzeczywistych |
|---|---|---|---|---|
| Beryllium | Be | Występuje w minerałach takich jak beryl | Bardzo lekki i sztywny dla metalu | Stosowany w specjalistycznych zastosowaniach lotniczych i rentgenowskich; pył jest szkodliwy przy wdychaniu |
| Magnez | Mg | Występuje w wodzie morskiej i minerałach | Niska gęstość oraz jasnobiała płomień podczas spalania | Ma znaczenie w lekkich stopach, suplementach oraz biologii |
| Wapń | Ca | Występuje powszechnie w wapieniu, kościach, muszlach i kredzie | Biologicznie znany jon grupy 2 | Kluczowy składnik szkieletów, cementu, gipsu oraz wielu minerałów naturalnych |
| Strychn | Sr | Występuje głównie w celestycie i stracjanie | Sole wywołują intensywnie czerwone zabarwienie płomienia | Stosowany w fajerwerkach, sygnałach oświetleniowych, materiałach świecących oraz niektórych produktach stomatologicznych |
| Barium | Ba | Zwykle występuje w stowarzyszeniu z barytom | Gęzki, ciężki metal ziem alkalicznych | Siarczan baru ma znaczenie w wiertnictwie i obrazowaniu medycznym; rozpuszczalne związki baru wymagają ostrożności |
| Rad | RA | Występuje w śladowych ilościach w rudach uranu | Silna radioaktywność dominuje jego historią chemiczną | Obecnie głównie historyczne lub ściśle kontrolowane znaczenie naukowe |
Beryl i magnez u góry grupy 2
The pierwiastek beryl znajduje się na szczycie rodziny i już sugeruje, że grupa 2 nie jest w pełni jednorodna. Często kojarzony jest z minerałem berylu, który należy do tej samej rodziny minerałów co szmaragd i akwamaryn. Beryl wyróżnia się tym, że jest niezwykle lekki i sztywny. Daje to możliwość jego zastosowania w elementach wysokiej wydajności, gdzie ma znaczenie niewielka masa. Jednocześnie beryl to materiał wymagający ostrożności w środowisku przemysłowym, ponieważ drobny pył może być szkodliwy przy wdychaniu. Dlatego zapamiętany jest zarówno ze względu na swoje właściwości użytkowe, jak i konieczność zachowania ostrożności podczas obsługi.
Magnez wydaje się znacznie bardziej znajomy. symbol chemiczny magnezu to magnez (Mg) i jest jednym z najlepiej znanych metali w tej grupie, ponieważ występuje w wodzie morskiej, powszechnych minerałach oraz układach żywych. Jest bardzo lekkim metalem, a podczas spalania wydziela intensywne białe światło. Dlatego też magnez od dawna kojarzony jest z sygnalizacyjnymi rakietami i materiałami intensywnie palącymi. W życiu codziennym większość ludzi spotyka go jednak w łagodniejszych formach, takich jak jego rola w diecie, związki stosowane jako leki przeciwwzdorowe lub lekkie stopy wykorzystywane tam, gdzie istotne jest zmniejszenie masy.
Wapń i stront w materiałach codziennego użytku
Wapń jest najbardziej rozpoznawalnym pierwiastkiem grupy 2 dla wielu czytelników. Występuje w wapieniu, kredzie, muszelkach i kościach, łącząc w ten sposób chemię niemal natychmiast z geologią i biologią. Związekem znanym w tym kontekście jest węglan wapnia. Pomaga on wyjaśnić, dlaczego ten sam rodzaj pierwiastków odgrywa ważną rolę zarówno w tworzeniu jaskiń, jak i w kamieniach budowlanych czy szkielecie. Sam metaliczny wapń jest reaktywny, ale związki wapnia są powszechne, co sprawia, że ten pierwiastek wydaje się bardziej znajomy niż egzotyczny.
Stront jest łatwiejszy do zapamiętania, gdy powiąże się go z kolorem. symbolem strontu jest Sr, a strychn występuje głównie w minerałach celestynie i strontianicie. Królewskie Towarzystwo Chemii opisuje go jako miękki, srebrzysty metal, który płonie w powietrzu i reaguje z wodą. Jego sole są znane z wywoływania intensywnie czerwonego koloru w fajerwerkach i sygnałach oświetleniowych. To samo źródło wspomina również o zastosowaniach w materiałach świecących w ciemności oraz w chlorku strontu heksahydracie stosowanym w pastach do zębów przeznaczonych dla osób z nadwrażliwymi zębami. Dzięki temu stront stanowi doskonały przykład pierwiastka, który – choć chemicznie aktywny – występuje najczęściej w postaci związków.
Bar i rad w zaawansowanych lub specjalistycznych kontekstach
The pierwiastek bar jest często kojarzony z ciężkością. Często kojarzony jest z baritem, a jednym z jego najbardziej znanych związków jest siarczan baru. Ten związek ma znaczenie, ponieważ jest bardzo mało rozpuszczalny, co wyjaśnia, dlaczego bar może występować w praktycznych zastosowaniach, takich jak płyny wiertnicze czy obrazowanie medyczne, podczas gdy inne rozpuszczalne związki baru są stosowane z większą ostrożnością ze względu na ich toksyczność. Bar przypomina czytelnikom, że użyteczną formą pierwiastka grupy 2 jest często związek chemiczny, a nie sam błyszczący metal.
Rad, znajduje się u podstawy rodziny, ale nie pozostaje bezgłośnie w tle. Na okresowym radu widok, Ra oznacza punkt, w którym promieniotwórczość staje się cechą definiującą. Rad występuje w naturze jedynie w śladowych ilościach, zwykle w połączeniu z rudami uranu. Historycznie słynął z farb luminiscencyjnych oraz wczesnych eksperymentów medycznych. Dziś jego zagrożenie wynika z promieniotwórczości, a nie z typowego zachowania metalu, dlatego jest on obsługiwany w ścisłych warunkach kontrolnych. Prostym językiem mówiąc, rad nadal należy do grupy 2, ale omawiany jest przede wszystkim pod kątem bezpieczeństwa jądrowego, równie ważnego jak aspekty chemiczne.
Umieszczenie tych sześciu obok siebie sprawia, że rodzina przestaje wyglądać jak pusta lista nazw. Wielkość atomów, reaktywność, typowe związki chemiczne oraz nawet sposób, w jaki każdy z tych pierwiastków pojawia się w życiu codziennym, zmieniają się przy przesuwaniu się w dół grupy. To właśnie ta zmienność tworzy charakterystyczny wzór, dzięki któremu grupa 2 staje się szczególnie użyteczna – porządek od berylu do radu zaczyna ujawniać prawidłowości zamiast przypadkowych faktów.
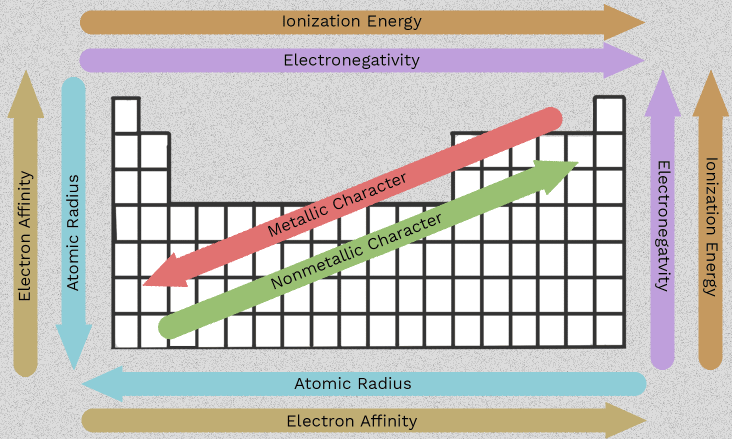
Właściwości metali ziem alkalicznych i trendy grupy 2
To właśnie zmieniające się uporządkowanie od berylu do radu czyni grupę 2 użyteczną. Zamiast zapamiętywać sześć izolowanych faktów, można śledzić garstkę wzorów powtarzających się w całej kolumnie. Najważniejsze właściwości metali ziem alkalicznych wynikają z jednej wspólnej cechy: każdy atom ma dwa elektrony walencyjne, które tendencja do utraty.
Gdy zrozumie się, jak rozmiar atomu, ekranowanie elektronowe oraz energia jonizacji zmieniają się w dół grupy, cała rodzina staje się znacznie łatwiejsza do przewidywania. Te charakterystyczne cechy metali ziem alkalicznych to nie tylko fakty wymagane na egzaminach. Wyjaśniają one, dlaczego niektóre pierwiastki reagują szybciej, dlaczego niektóre związki lepiej rozpuszczają się niż inne oraz dlaczego niektóre trendy wymagają starannej sformułowania zamiast prostych strzałek.
Wspólne właściwości metali ziem alkalicznych
Większość członków grupy 2 to srebrzyste metale, które zwykle tworzą kationy M 2+jony i tworzą głównie związki jonowe. Zachowują się jako reduktory, ponieważ tracą elektrony. W porównaniu z metalami grupy 1 są ogólnie mniej reaktywne, ale nadal wystarczająco aktywne chemicznie, aby tworzyć wiele powszechnych tlenków, chlorków, węglanów i siarczanów.
Prosty sposób uporządkowania właściwości chemicznych metali ziem alkalicznych polega na oddzieleniu tego, co pozostaje stałe, od tego, co się zmienia. Stałą wartością jest zwykle stopień utlenienia +2. To, co się zmienia, to łatwość, z jaką każdy z pierwiastków oddaje te dwa elektrony. To właśnie w tym miejscu zaczynają mieć znaczenie trendy.
Trendy w dół grupy 2 oraz ich znaczenie
Dane zebrane przez LibreTexts oraz wyjaśnienia trendów z Save My Exams wykazują ten sam ogólny wzór. Promień atomowy rośnie od 112 pm dla Be do 253 pm dla Ba, podczas gdy pierwsza energia jonizacji maleje od 900 do 503 kJ/mol. W prostym języku: elektrony walencyjne znajdują się coraz dalej od jądra i są osłonięte przez coraz więcej wewnętrznych powłok, więc łatwiej je usunąć.
| Tendencja | Kierunek w dół grupy 2 | Powód chemiczny | Co to oznacza w praktyce |
|---|---|---|---|
| Promień atomowy | Zwiększa | Każdy pierwiastek ma dodatkową powłokę elektronową oraz większą ekranizację | Większe atomy słabiej utrzymują elektrony zewnętrzne |
| Pierwsza i druga energia jonizacji | Ogólnie maleje | Elektrony zewnętrzne znajdują się dalej od jądra, więc przyciąganie jest słabsze | Tworzenie jonów M 2+staje się łatwiejsze |
| Reaktywność | Ogólnie rośnie | Niższe energie jonizacji ułatwiają utratę elektronów | Cięższe pierwiastki reagują bardziej gwałtownie z kwasami, tlenem i często z wodą |
| Temperatura topnienia | Ogólnie maleje, ale nie w sposób gładki | Większe jony metalu osłabiają wiązanie metaliczne, choć struktura również ma znaczenie | Użyj słowa „ogólnie”, ponieważ Mg i Ca nie wpisują się doskonale w prostą zależność |
| Gęstość | Nieregularny | Masa, rozmiar atomowy oraz upakowanie metalu zmieniają się równocześnie | Nie można traktować gęstości jako jednej prostej tendencji malejącej |
| Rozpuszczalność wodorotlenków | Zwiększa | Równowaga między energią siatki a energią hydratacji przesuwa się w dół grupy | Cięższe wodorotlenki tworzą bardziej alkaliczne roztwory |
| Rozpuszczalność siarczanów | Zmniejsza | Energia hydratacji maleje w miarę wzrostu rozmiaru kationu | Związki takie jak BaSO 4stają się bardzo mało rozpuszczalne |
Gęstość i zachowanie podczas topnienia to dwie tendencje, które uczniowie często nadmiernie upraszczają. Gęstość nie zmienia się w sposób liniowy, ponieważ zarówno masa, jak i objętość ulegają zmianie, a atomy metalu nie układają się w ten sam sposób w każdej sieci krystalicznej. Temperatury topnienia również wymagają ostrożności. Ogólnie maleją one w dół grupy, ponieważ większe jony osłabiają sieć metaliczną, ale magnez ma nietypowo niską temperaturę topnienia wynoszącą 650 °C, podczas gdy wapń osiąga wartość 842 °C, zanim wartości te ponownie spadają. Jedną z najbezpieczniejszych cech metali ziem alkalicznych jest więc następująca: ogólna tendencja jest rzeczywista, ale szczegóły fizyczne nie są idealnie gładkie.
Rozpuszczalność nosi tę samą ostrzegawczą etykietę. Nie istnieje jedna reguła obejmująca wszystkie sole grupy 2. Wodorotlenki stają się bardziej rozpuszczalne w dół grupy, podczas gdy siarczany stają się mniej rozpuszczalne. Jeśli ktoś stwierdza: „rozpuszczalność rośnie w dół grupy 2”, kluczowym pytaniem jest: „o które związki chodzi?”
Dlaczego metale ziem alkalicznych reagują w taki sposób
Więc, czy metale ziem alkalicznych są reaktywne ? Tak, a ogólna odpowiedź brzmi: ich reaktywność wzrasta w miarę przesuwania się w dół grupy. Powodem jest ta sama historia dotycząca elektronów, o której mowa powyżej. Niższe wartości pierwszej i drugiej energii jonizacji oznaczają, że atomy mogą łatwiej stracić dwa elektrony i szybciej osiągnąć typowy stan M 2+.
Ma to wpływ na rzeczywiste reakcje. W miarę przesuwania się w dół grupy reakcje z rozcieńczonymi kwasami przebiegają szybciej, reakcje z tlenem stają się bardziej gwałtowne, a cięższe pierwiastki łatwiej ulegają utlenieniu. Notatki Save My Exams podkreślają, że bar jest na tyle reaktywny, że musi być przechowywany pod olejem – jest to praktyczny dowód, jak daleko może sięgać ten trend reaktywności.
- Promień atomowy rośnie w dół grupy 2.
- Energia jonizacji maleje w dół grupy 2.
- Reaktywność wzrasta, ponieważ utrata dwóch elektronów staje się łatwiejsza.
- Temperatury topnienia i gęstość wykazują nieregularności, więc należy unikać bezwzględnych reguł.
- Wodorotlenki i siarczany wykazują przeciwne trendy rozpuszczalności.
Te wzorce czynią rodzinę przewidywalną, ale nie całkowicie jednolitą. Tuż pod szczytem grupy beryl już zaczyna łamać reguły, a magnez wprowadza kolejny powszedni wyjątek, który ma większe znaczenie, niż wielu początkujących oczekuje.
Metale alkaliczne i metale ziem alkalicznych
Ogólne trendy ułatwiają naukę grupy 2, jednak rodzina traci sens, jeśli każdy jej członek traktowany jest jako identyczny. Największym sygnałem ostrzegawczym jest beryl. Magnez wprowadza bardziej praktyczny, powszedni wyjątek. A gdy ludzie porównują metale alkaliczne i metale ziem alkalicznych , podobne nazwy mogą ukrywać bardzo różną chemię.
Dlaczego beryl nie zachowuje się jak typowy metal grupy 2
BYJU'S opisuje beryl jako wyraźny element odstający w grupie 2. Jego nietypowo mała wielkość, wysoka energia jonizacji oraz silna zdolność do polaryzacji nadają mu właściwości mniej charakterystyczne dla tej rodziny. W prostym języku: Be 2+silnie przyciąga pobliskie chmury elektronowe, więc związki berylu są często bardziej kowalencyjne niż bardziej jonowe związki tworzone przez cięższe pierwiastki tej grupy. Ten sam źródło zauważa również, że beryl ma wyższe temperatury topnienia i wrzenia niż pozostałe pierwiastki tej grupy oraz nie reaguje z wodą tak jak jego towarzysze.
Magnez nie jest tak nietypowy jak beryl, ale nadal może wydawać się mniej reaktywny, niż uczniowie oczekują. LibreTexts podkreśla, że bardzo czysty magnez reaguje jedynie umiarkowanie z zimną wodą, a reakcja szybko zwalnia, ponieważ prawie nierozpuszczalny wodorotlenek magnezu tworzy barierę na powierzchni metalu. Na dole rodziny radon jest zwykle omawiany osobno, ponieważ jego promieniotwórczość dominuje w praktycznych zastosowaniach oraz dyskusjach dotyczących bezpieczeństwa.
Jak metale ziemi alkalicznej różnią się od metali alkalicznych
W prostych alkaliczne vs alkaliczno-ziemne słowach: metale grupy 1 tracą jeden elektron walencyjny, podczas gdy metale grupy 2 tracą dwa elektrony. Ta pojedyncza różnica kształtuje właściwości metali alkalicznych i metali ziemi alkalicznej w znacznie większym stopniu niż prawie wszystko inne.
| Cechy | Metale alkaliczne, grupa 1 | Metale ziem alkalicznych, grupa 2 |
|---|---|---|
| Glinu | 1 | 2 |
| Typowy jon | M + | M 2+ |
| Reakcja z zimną wodą | Często gwałtowna lub nawet burzliwa, prowadząca do powstania wodorotlenku i wodoru | Mniej jednolita: beryl nie reaguje z wodą, magnez reaguje łagodnie, a wapń, stront i bar reagują z rosnącą gwałtownością |
| Typowa chemia tlenu | Mogą tworzyć tlenki, nadtlenki lub nadtlenki | Zazwyczaj tworzą monotlenki; większość tych tlenków tworzy wodorotlenki w obecności wody, ale BeO stanowi wyjątek |
Ważne wyjątki, które uczniowie często pomijają
- Nie każdy metal grupy 2 reaguje z wodą w ten sam sposób.
- Związki berylu są bardziej kowalencyjne niż pozostałe pierwiastki tej rodziny.
- Nie mylić metali alkalicznych i metali ziem alkalicznych jako tej samej grupy tylko dlatego, że nazwy brzmią podobnie.
- The właściwości metali alkalicznych i metali ziem alkalicznych najlepiej uczyć się jako wzorców z wyjątkami, a nie sztywnych powtórek.
Jest to również najlepszy sposób na zrozumienie właściwości chemicznych metali alkalicznych i metali ziem alkalicznych . Wzorce elektronowe dają regułę, ale rzeczywiste substancje nadają jej barwę. Ta barwa staje się jeszcze wyraźniejsza, gdy przyjrzymy się temu, gdzie w przyrodzie występują właściwie pierwiastki grupy 2: rzadko jako czyste metale, a znacznie częściej w minerałach, skałach, wodzie morskiej, kościach oraz związkach przemysłowych.
Występowanie metali ziem alkalicznych w przyrodzie
Jeśli wyobrażasz sobie metale ziem alkalicznych jako jasny, czysty próbkę leżącą w skale, natura działa inaczej. Pierwiastki grupy 2 są na tyle reaktywne, że zwykle występują jako jony w minerałach, solach, skałach, wodzie morskiej, kościach i muszelkach, a nie jako wolne metale. Niezależnie od tego, czy ktoś szuka terminu metali ziem alkalicznych czy bardziej standardowego określenia, naturalny wzór pozostaje ten sam: ta rodzina pierwiastków wyraźnie preferuje związki.
Ten wzór wynika bezpośrednio z właściwości chemicznych metali ziem alkalicznych . Mają one tendencję do utraty dwóch elektronów z powłoki zewnętrznej i tworzenia stabilnych jonów M 2+²⁺. Gdy to nastąpi, jony tlenu, węglanowe, siarczanowe oraz halogenkowe łatwo wiążą je w stałych związkach, które mogą utrzymywać się w geologii i biologii.
Dlaczego metale ziem alkalicznych nie występują w przyrodzie w stanie wolnym
Britannica i ThoughtCo obie opisują grupę 2 jako reaktywną, co wyjaśnia, dlaczego pierwiastki tej grupy rzadko występują w stanie wolnym. W powietrzu wiele z nich szybko tworzy warstwy tlenków. W środowisku naturalnym są one jeszcze bardziej stabilizowane jako węglany, siarczany, krzemiany, fluororki lub chlorki. Dlatego wapń występuje w wapieniu i muszlach, magnez – w minerałach i wodzie morskiej, a stront czy bar – w złożach rud. Rad jest jeszcze rzadszy i występuje jedynie w śladowych ilościach w rudach uranu.
Popularne minerały i związki chemiczne grupy 2
| Element | Powszechne źródła naturalne | Znany związek chemiczny | Dlaczego ten związek ma znaczenie |
|---|---|---|---|
| Beryllium | Beryl | BeO | Beryl jest źródłem przemysłowym tego pierwiastka, natomiast tlenek berylu stanowi ważny związek stosowany w materiałach specjalnych |
| Magnez | Magnezyt, dolomit, woda morska | MgCO₃ 3lub Mg(OH)₂ 2 | Wyjaśnia, dlaczego magnez spotyka się częściej w minerałach, wodzie morskiej i medycynie niż jako metal czysty |
| Wapń | Wapień, kreda, marmur, gips, kości, muszle | Caco 3 | Łączy geologię, materiały budowlane i szkielety w jednym bardzo powszechnym związku |
| Strychn | Celestyn, strontyanit | SrSO₄ 4lub SrCO₃ 3 | Te minerały są głównymi naturalnymi źródłami związków strontu |
| Barium | Baryt, witeryt | BaSO 4 | Baryt jest główną rudą, a siarczan baru jest jednym z najbardziej znanych związków baru |
| Rad | Śladowe ilości w pechblendzie i innych rudach uranu | RaCl 2 | Jego rzadkość i promieniotwórczość sprawiają, że związki radu były historycznie ważne, ale są niezwykle rzadkie |
EBSCO zauważa, że woda morska zawiera również wapń i magnez w ilościach odpowiednio około 0,4 g/L i 1,3 g/L. To wyjaśnia, dlaczego ten metale ziem alkalicznych rodzaj wiąże się nie tylko z rudami, ale także z twardą wodą, systemami morskimi oraz tkankami żywymi.
Sposoby izolowania tych metali z ich związków
Ponieważ metale grupy 2 są zwykle związane w związkach chemicznych, proces ich pozyskiwania rozpoczyna się od rud, roztworów solankowych lub złóż mineralnych. Typowym przemysłowym podejściem jest stosunkowo prosta strategia: najpierw przekształca się surowiec w bardziej łatwy do przetwarzania tlenek lub halogenek, a następnie wykorzystuje się elektrolizę lub redukcję chemiczną w celu uwolnienia metalu. W encyklopedii Britannica opisano wcześniejsze izolowanie magnezu, wapnia, strontu i baru metodą elektrolizy, podczas gdy źródło EBSCO zaznacza, że współczesna produkcja nadal najczęściej opiera się na elektrolizie stopionych chlorków, redukcji tlenków lub powiązanych metodach – wybór zależy od konkretnego pierwiastka. Beryl stanowi użyteczne przypomnienie, że ta grupa nie jest całkowicie jednorodna, ponieważ beryl można otrzymać poprzez redukcję fluoroberylu.
W codziennym życiu ludzie zazwyczaj spotykają pierwiastki grupy 2 w postaci wapienia, gipsu, magnezu pochodzącego z wody morskiej, barytu lub wapnia biologicznego, a nie jako próbki surowego metalu. Ten szczegół ma znaczenie, ponieważ rzeczywiste znaczenie tych pierwiastków zależy znacznie bardziej od ich związków i form niż od samych metali w stanie czystym.
Przykłady metali ziem alkalicznych w życiu codziennym
Grupa 2 staje się znacznie łatwiejsza do zapamiętania, gdy każdy jej pierwiastek powiąże się z konkretnym, rzeczywistym obiektem. Kości, leki przeciwwzdorowe, gips, fajerwerki, płyny wiertnicze oraz stare świecące tarcze zegarków to wszystko przydatne przykłady. przykłady metali ziem alkalicznych jeśli kiedykolwiek zastanawiałeś się czy magnez jest metalem czy niemetalem lub czy Ca jest metalem , obie odpowiedzi są proste: magnez i wapń są metalami. W codziennym życiu jednak ludzie zazwyczaj spotykają te substancje w postaci związków, a nie jako próbki czystego metalu.
Codzienne zastosowania związków magnezu i wapnia
- Magnez : Magnez jest jednym z najważniejszych pierwiastków biologicznie pierwiastki ziemi alkalicznej . The Arkusz informacyjny NIH dotyczący magnezu zauważa, że jest on koenzymem w ponad 300 układach enzymatycznych oraz wspiera funkcje mięśni i nerwów, produkcję energii oraz budowę kości. Związki magnezu występują także w niektórych lekach przeciwwzdławiających i środek przeczyszczających, podczas gdy metaliczny magnez jest ceniony w lekkich stopach, gdzie istotne jest zmniejszenie masy.
- Wapń związki wapnia dominują w codziennym życiu. Wapń przyczynia się do nadania struktury kościom i zębom, a takie związki jak węglan wapnia i siarczan wapnia odgrywają kluczową rolę w powstawaniu wapienia, cementu, gipsu i płyt gipsowo-kartonowych. Daje to wapniowi jedno z najbardziej oczywistych połączeń między chemią, biologią a budownictwem.
Zastosowania specjalistyczne strontu i baru
- Strychn sole strontu są najbardziej znane z wywoływania intensywnego czerwonego koloru w fajerwerkach i sygnałach oświetleniowych. Nawet czytelnicy, którzy nie pamiętają pełnej listy pierwiastków grupy 2, często zapamiętują stront, gdy kojarzy się go z określonym kolorem.
- Barium związki baru mają znaczenie w przemyśle i medycynie. Profil baru NLM opisuje główne zastosowania w płuczce wiertniczej, farbach, tworzywach sztucznych, cegłach i szkle. Wskazuje również ważną różnicę medyczną: wysoko nierozpuszczalny siarczan baru stosowany jest jako materiał radioprzezroczysty w niektórych badaniach rentgenowskich, ponieważ zazwyczaj nie jest wchłaniany przez organizm.
- Rad : Rad jest głównie przypadkiem historycznym lub ściśle kontrolowanym zastosowaniem naukowym. Strona NRC poświęcona radowi opisuje jego dawne zastosowanie w farbach luminiscencyjnych oraz w wczesnej terapii raka. Większość tych zastosowań została zastąpiona, choć nadal istnieją niektóre regulowane zastosowania, takie jak określone zastosowania w przemysłowej radiografii.
Dlaczego forma i rodzaj związku mają znaczenie w rzeczywistym użyciu
W grupie 2 najczęściej stosowaną formą jest związek chemiczny, a nie czysty metal.
Ten pojedynczy pomysł wyjaśnia wiele nieporozumień. Magnez w pożywieniu lub lekach nie jest tym samym co palący się pasek magnezu. Wapń w kościach nie jest tym samym co reaktywny metal wapnia. Bar w sposób najbardziej wyraźny ilustruje, dlaczego forma ma znaczenie: nierozpuszczalny siarczan baru może być przydatny w obrazowaniu medycznym, podczas gdy bardziej rozpuszczalne związki baru wymagają znacznie większej ostrożności. Rad przesuwa ten argument jeszcze dalej, ponieważ to jego promieniotwórczość, a nie tylko jego położenie wśród metali, decyduje o sposobie jego obsługi.
Wartość grupy 2 wcale nie jest abstrakcyjna. Te pierwiastki pomagają wyjaśnić, jak ten sam rodzaj pierwiastków może odgrywać rolę w żywieniu, materiałach, medycynie, przetwórstwie przemysłowym oraz zasadach bezpieczeństwa. Krótki wykaz rzeczywistych zastosowań często wystarcza, by ogólny wzór utrzymał się w pamięci.
Główne wnioski dotyczące pierwiastków grupy 2
Do tej pory metale ziem alkalicznych powinny wydawać się mniej jak lista do nauczenia się na pamięć, a bardziej jak wzór, który można bezpośrednio odczytać z grupy 2 w układzie okresowym kolumny. Jeśli ktoś nadal pyta, jakie są metale ziem alkalicznych , krótka odpowiedź pozostaje prosta: beryl, magnez, wapń, stront, bar i rad. Pełniejsza definicja metali ziem alkalicznych jest jeszcze bardziej przydatna: sześć pierwiastków metalicznych z grupy 2, które zwykle tracą dwa elektrony zewnętrznej powłoki i tworzą jony M 2+.
Główne wnioski dotyczące metali ziem alkalicznych
- Położenie ma znaczenie: te sześć pierwiastków grupy 2 znajduje się w drugiej kolumnie od lewej, czyli w sekcji grupy 2 bloku s.
- Członkowie rodziny są stały: Be, Mg, Ca, Sr, Ba i Ra tworzą pełny zbiór.
- Wspólne właściwości chemiczne wyjaśniają podobieństwo rodzinne: ich elektrony walencyjne ns 2wzorzec walencyjny prowadzi do powstawania jonów +2 jako typowego wyniku – kluczowy punkt podsumowany przez LibreTexts.
- Główne trendy w dół grupy są przewidywalne: promień atomowy rośnie, energia jonizacji ogólnie maleje, a reaktywność zwykle wzrasta w miarę przesuwania się w dół grupy.
- Wyjątki mają znaczenie: beryl zachowuje się bardziej kowalencyjnie niż pozostałe pierwiastki, magnez może wydawać się mniej reaktywny ze względu na warstwę powierzchniową, a rad jest omawiany głównie w kontekście swojej radioaktywności.
- W rzeczywistości chodzi zazwyczaj o związki, a nie czyste metale: ludzie spotykają węglan wapnia, tlenek magnezu i siarczan baru znacznie częściej niż pierwiastkowy wapń, magnez lub bar.
The zasadowo-ziemiste układ okresowy kolumna jest najłatwiejsza do zapamiętania jako sześć metali połączonych jedną zasadą: zwykle tworzą jony 2+, ale każdy z członków wyraża tę zasadę nieco inaczej.
Od chemii grupy 2 do zaprojektowanych elementów metalowych
Ta chemia wykracza daleko poza podręczniki. LibreTexts zauważa, że pierwiastkowy magnez jest produkowany w dużych ilościach i stosowany w lekkich stopach przeznaczonych na konstrukcje kadłubów samolotów oraz części silników samochodowych. Szerokie opracowanie dotyczące stopów wyjaśnia, dlaczego to ma znaczenie: inżynierowie dostosowują skład i procesy obróbki, aby osiągnąć odpowiedni balans między masą, wytrzymałością, odpornością na korozję oraz możliwością obróbki skrawaniem w rzeczywistych komponentach.
Od widoku grupy 2 w układzie okresowym do produkcji, Shaoyi Metal Technology przedstawia praktyczny przykład tego związku. Strony poświęcone materiałom motocyklowym i obróbce skrawaniem opisują produkcję części metalowych – od prototypowania po masową produkcję – gdzie zachowanie materiału i kontrola procesu muszą działać w harmonii. To sprawia, że zasadowo-ziemiste układ okresowy stanowi coś więcej niż tylko schemat do nauki w klasie. Jest również częścią logiki stojącej za wyborem metali i stopów do części inżynieryjnych, które muszą być lekkie, niezawodne i nadające się do produkcji.
Często zadawane pytania dotyczące metali ziem alkalicznych
1. Jakie są sześć metali ziem alkalicznych?
Sześcioma metalami ziem alkalicznych są beryl, magnez, wapń, stront, bar i rad. Zajmują one grupę 2 w układzie okresowym pierwiastków i są ze sobą pogrupowane, ponieważ zwykle tracą dwa elektrony zewnętrznej powłoki, co prowadzi do wspólnego wzorca jonów o ładunku 2+ w wielu związkach.
2. W czym różnią się metale ziem alkalicznych od metali alkalicznych?
Metale alkaliczne należą do grupy 1 i zwykle tworzą jony o ładunku 1+, ponieważ posiadają jeden elektron walencyjny. Metale ziem alkalicznych znajdują się w grupie 2, zazwyczaj tworzą jony o ładunku 2+ i są ogólnie mniej reaktywne. Ten jeden dodatkowy elektron walencyjny wpływa na siłę wiązań, sposób reakcji z wodą oraz rodzaje soli i tlenków, które one zwykle tworzą.
3. Dlaczego metale ziem alkalicznych nie występują w przyrodzie w stanie wolnym?
Te metale są wystarczająco reaktywne, aby w naturalnych warunkach nie utrzymywać się długo w czystej postaci pierwiastkowej. Zamiast tego łączą się z jonami tlenu, węglanowymi, siarczanowymi, chlorkowymi lub krzemianowymi i stają się częścią minerałów, skał, wody morskiej, muszli oraz kości. Dlatego ludzie zazwyczaj spotykają się z pierwiastkami grupy 2 w postaci związków, a nie jako próbki czystych metali.
4. Czy wszystkie metale ziem alkalicznych reagują z wodą?
Nie, a to jedno z najbardziej przydatnych wyjątków, które warto zapamiętać. Beryl jest w dużej mierze odporny na działanie wody, magnez reaguje powoli z zimną wodą ze względu na warstwę powierzchniową ograniczającą tę reakcję, natomiast wapń, stront i bar reagują chętniej. Ogólnie rzecz biorąc, aktywność chemiczna względem wody wzrasta w miarę przesuwania się w dół grupy 2.
5. Dlaczego metale ziem alkalicznych są ważne w przemyśle i produkcji?
Ich znaczenie wynika zarówno z ich związków, jak i roli w doborze stopów. Magnez jest ceniony tam, gdzie ważna jest mniejsza masa, związki wapnia odgrywają kluczową rolę w produkcji cementu i gipsu, a związki baru stosuje się w specjalistycznych zastosowaniach przemysłowych i medycznych. W rzeczywistej produkcji zrozumienie zachowania metali pomaga kierować obróbką skrawaniem, zapewniać stabilność procesów oraz utrzymywać wysoką jakość wyrobów – dlatego dostawcy tacy jak Shaoyi Metal Technology podkreślają certyfikowaną obróbkę skrawaniem elementów samochodowych, kontrolę procesu oraz wsparcie od etapu prototypów po masową produkcję.
 Małe partie, wysokie standardy. Nasza usługa szybkiego prototypowania sprawia, że weryfikacja jest szybsza i łatwiejsza —
Małe partie, wysokie standardy. Nasza usługa szybkiego prototypowania sprawia, że weryfikacja jest szybsza i łatwiejsza —
