Was sind die Erdalkalimetalle? Die Gruppe 2 wird endlich verständlich
Was sind Erdalkalimetalle?
Wenn Sie nach was sind Erdalkalimetalle gesucht haben, lautet hier die direkte Antwort: Es handelt sich um die sechs Elemente der Gruppe 2 des Periodensystems. Diese kurze definition von Erdalkalimetallen ist der Ausgangspunkt, doch der Name verrät Ihnen bereits viel über das Verhalten dieser Elementfamilie.
Was sind die Erdalkalimetalle in einem Satz?
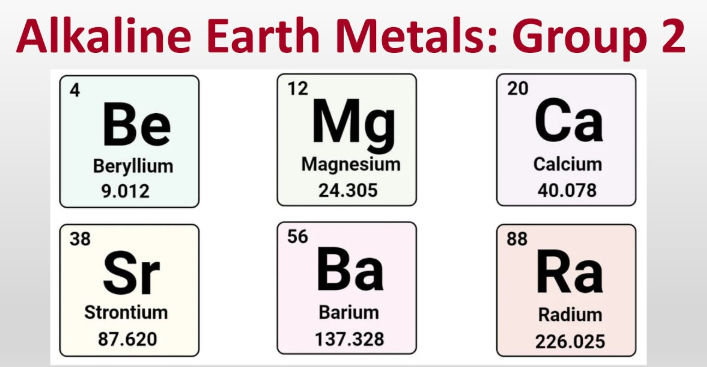
Die Erdalkalimetalle sind Beryllium, Magnesium, Calcium, Strontium, Barium und Radium, die sechs metallischen Elemente der Gruppe 2, die üblicherweise +2-Ionen bilden.
- Beryllium (Be)
- Magnesium (Mg)
- Calcium (Ca)
- Strontium (Sr)
- Barium (Ba)
- Radium (Ra)
Warum der Name Erdalkalimetalle sinnvoll ist
Für Einsteiger wird die definition der Erdalkalimetalle deutlich einfacher, wenn man die Wortgruppe in drei Teile zerlegt.
Alkalin bedeutet, dass ihre Oxide und Hydroxide basisch und nicht sauer sind. Erden ist ein historischer Begriff. Frühe Chemiker verwendeten ihn für wärmebeständige, mineralähnliche Stoffe, die sich weder leicht schmelzen noch leicht in Wasser lösen ließen – ein Punkt, der durch Britannica . Metalle bedeutet, dass die Elemente selbst metallisch sind, typischerweise glänzend und gut darin, bei Reaktionen Elektronen abzugeben.
Damit ergibt sich die grundlegende bedeutung von Erdalkalimetallen ohne dass zuvor fortgeschrittene Chemiekenntnisse erforderlich wären. Es ist zudem eine nützliche kurze beschreibung der Erdalkalimetalle : eine Metallfamilie der Gruppe 2 mit gemeinsamer Chemie, einer gemeinsamen Position im Periodensystem und einer bedeutenden Rolle in der realen Welt. Magnesium kommt in Legierungen und biologischen Systemen vor. Calcium spielt eine wichtige Rolle bei Knochen, Schalen und Baumaterialien. Barium, Strontium und Radium treten in spezialisierteren Anwendungsbereichen auf.
Dieser Artikel beginnt absichtlich einfach. Eine übersichtliche Liste lässt sich leicht auswendig lernen; die Familie wird jedoch erst dann wirklich verständlich, wenn man sieht, wo diese Elemente im Periodensystem stehen und warum gerade diese Position ihnen ein so ähnliches Verhalten verleiht.
Wo die Gruppe 2 im Periodensystem steht
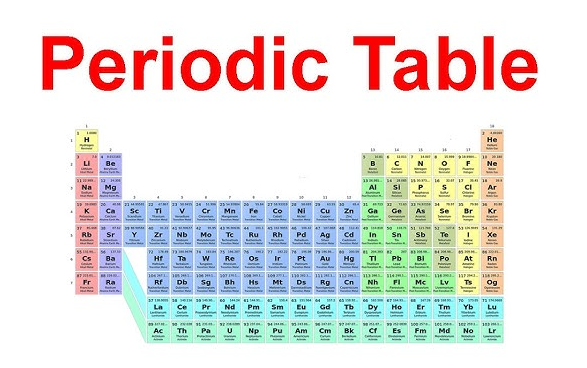
Der Familienname wird deutlich leichter zu merken sein, sobald man sie tatsächlich im Periodensystem lokalisieren kann. Wenn Sie sich fragen wo die Erdalkalimetalle im Periodensystem zu finden sind , schauen Sie in die zweite Spalte von links. Diese senkrechte Spalte ist die Gruppe 2 im Periodensystem , die unmittelbar neben den Alkalimetallen der Gruppe 1 steht. A gruppe 2 des Periodensystems die Darstellung zeigt jedes Mal dieselbe gerade Linie: Beryllium oben, dann Magnesium, Calcium, Strontium, Barium und Radium in Richtung zunehmender Perioden nach unten.
In einem alkalierdmetalle im Periodensystem diagramm gehören diese sechs Elemente zum s-Block. Ihre gemeinsame Position ist bedeutungsvoll, da sie ein gemeinsames Elektronenmuster widerspiegelt. Wie LibreTexts erklärt, besitzen Elemente der Gruppe 2 eine ns- 2valenzkonfiguration, was bedeutet, dass sie zwei Außenelektronen besitzen.
Wo die Alkalierdmetalle im Periodensystem zu finden sind
Visuell ist das Muster einfach. Die elemente der Gruppe 2 des Periodensystems bilden eine Familien-Spalte über die Perioden 2 bis 7. Viele Unterrichtsdiagramme heben die erdalkalimetalle im Periodensystem layouts mit derselben Farbe, weil Elementfamilien vertikal und nicht horizontal gelesen werden. Suchanfragen nach periodensystem Erdalkalimetalle beziehen sich tatsächlich auf diese eine Spalte.
| Elemente | Symbol | Gruppe-2-Position | Typisches Ion | Bekannte Verbindung |
|---|---|---|---|---|
| Beryllium | Be | Periode 2, oberster Platz der Gruppe 2 | Be2+ | BeO |
| Magnesium | Mg | Periode 3 | Mg2+ | MgO |
| Kalzium | Ca | Periode 4 | Ca2+ | Caco 3 |
| Strontium | Sr | Periode 5 | Sr2+ | SrCO 3 |
| Barium | BA | Periode 6 | BA 2+ | BaSO 4 |
| Radium | RA | Periode 7, unteres Ende der Gruppe 2 | RA 2+ | RaCl 2 |
Warum Elemente der Gruppe 2 zweifach positive Ionen bilden
Diese beiden äußeren Elektronen bestimmen die Chemie. Atome der Gruppe 2 neigen dazu, beide Elektronen abzugeben, da dies ihnen eine stabilere Elektronenanordnung verleiht. Das Ergebnis ist ein +2-Ion , wie z. B. Mg 2+ oder Ca 2+. Daher bilden diese Metalle üblicherweise Verbindungen wie Oxide, Chloride, Carbonate und Sulfate. Das Muster in den Formeln ist sofort erkennbar: MgO, CaCl 2, CaCO 3, BaSO 4.
So erkennen Sie die Erdalkalimetalle-Familie schnell
Ein schneller Identifikationstrick besteht darin, gleichzeitig nach drei Merkmalen zu suchen: zweite Spalte, metallische Elemente und typische +2-Ladung. Im Vergleich zu den benachbarten Alkalimetallen, die ein Valenzelektron besitzen und üblicherweise +1-Ionen bilden, halten die Elemente der Gruppe 2 ein zusätzliches äußeres Elektron zurück und sind im Allgemeinen weniger reaktiv. Dennoch gehören sie eindeutig einer gemeinsamen Familie an. Interessant ist, dass jedes Mitglied dieses Musters auf etwas andere Weise Ausdruck verleiht – insbesondere vom Beryllium oben bis zum Radium unten.
Die sechs Erdalkalimetalle
Eine Liste ist nützlich, aber sie ist allein betrachtet nicht besonders einprägsam. Gruppe 2 wirkt erst dann lebendiger, wenn jedes Mitglied eine klare Identität besitzt. Einige treten in Knochen oder Meerwasser auf. Einige färben Feuerwerke. Eines ist vor allem ein historisches Warnsignal. Gemeinsam gehören sie zwar noch immer derselben Familie an, doch jeder hat seine eigene Persönlichkeit.
| Elemente | Symbol | Häufiges Vorkommen | Hervorstechende Eigenschaft | Relevanz im realen Einsatz |
|---|---|---|---|---|
| Beryllium | Be | Kommt in Mineralien wie Beryll vor | Sehr leicht und steif für ein Metall | Wird in speziellen Luft- und Raumfahrtanwendungen sowie bei Röntgenanwendungen eingesetzt; Staub ist gesundheitsgefährdend, wenn eingeatmet |
| Magnesium | Mg | Kommt in Meerwasser und Mineralien vor | Geringe Dichte und hellweiße Flamme beim Verbrennen | Wichtig in Leichtmetalllegierungen, Nahrungsergänzungsmitteln und der Biologie |
| Kalzium | Ca | Häufig in Kalkstein, Knochen, Muschelschalen und Kreide | Biologisch vertrautes Ion der Gruppe 2 | Wichtig in Skeletten, Zement, Gips und vielen natürlichen Mineralien |
| Strontium | Sr | Kommt hauptsächlich in Celestin und Strontianit vor | Salze erzeugen eine lebendige rote Farbe in Flammen | Wird in Feuerwerkskörpern, Leuchtsignalen, Leuchtmaterialien und einigen zahnmedizinischen Produkten verwendet |
| Barium | BA | Trifft meist gemeinsam mit Baryt auf | Dichtes, schweres Erdalkalimetall | Bariumsulfat ist in der Bohrtechnik und der medizinischen Bildgebung von Bedeutung; lösliche Bariumverbindungen erfordern Vorsicht |
| Radium | RA | Kommt in Spuren in Uranerzen vor | Eine starke Radioaktivität prägt seine chemische Geschichte | Heute vorwiegend historische oder streng kontrollierte wissenschaftliche Relevanz |
Beryllium und Magnesium an der Spitze der Gruppe 2
Die element Beryllium steht an der Spitze der Elementfamilie und deutet bereits an, dass die Gruppe 2 nicht vollkommen einheitlich ist. Es ist üblicherweise mit dem Mineral Beryll verbunden, derselben Mineralfamilie, zu der auch Smaragd und Aquamarin gehören. Beryllium fällt dadurch auf, dass es ungewöhnlich leicht und steif ist. Das macht es für Hochleistungskomponenten nützlich, bei denen geringe Masse entscheidend ist. Gleichzeitig ist Beryllium ein Material, das in industriellen Umgebungen besondere Vorsicht erfordert, da feiner Staub bei Einatmung gesundheitsschädlich sein kann. Daher wird es sowohl wegen seiner Leistungsfähigkeit als auch wegen der erforderlichen Handhabungsvorsicht in Erinnerung behalten.
Magnesium wirkt deutlich vertrauter. Das chemische Symbol für Magnesium ist Mg und eines der bekanntesten Metalle dieser Gruppe, da es im Meerwasser, in gewöhnlichen Mineralien und in lebenden Systemen vorkommt. Es ist ein sehr leichtes Metall, und beim Verbrennen erzeugt es ein intensives weißes Licht. Daher ist Magnesium seit langem mit Leuchtsignalen und stark brennbaren Materialien verbunden. Im Alltag begegnen den meisten Menschen jedoch mildere Formen, etwa seine Rolle in der Ernährung, als Bestandteil von Säurebindern oder in leichten Legierungen, die dort eingesetzt werden, wo eine Massereduzierung wichtig ist.
Calcium und Strontium in Alltagsmaterialien
Calcium ist für viele Leser das bekannteste Element der 2. Gruppe. Es kommt in Kalkstein, Kreide, Muschelschalen und Knochen vor und verbindet die Chemie daher nahezu unmittelbar mit der Geologie und Biologie. Calciumcarbonat ist hier die bekannte Verbindung. Sie hilft zu erklären, warum dieselbe Elementfamilie sowohl bei Höhlenbildung, als Baumaterial als auch bei Skeletten eine Rolle spielt. Calciummetall selbst ist reaktiv, doch Calciumverbindungen sind allgegenwärtig – deshalb wirkt dieses Element oft vertrauter als exotisch.
Strontium ist leichter zu merken, sobald man es mit einer Farbe verbindet. Das symbol für Strontium ist Sr und strontium kommt hauptsächlich in den Mineralien Celestinit und Strontianit vor. Die Royal Society of Chemistry beschreibt es als ein weiches, silberfarbenes Metall, das an der Luft brennt und mit Wasser reagiert. Seine Salze sind berühmt dafür, in Feuerwerkskörpern und Leuchtsignalen intensive rote Farben hervorzurufen. Dieselbe Quelle nennt zudem Anwendungen in Leuchtstoffen („Glow-in-the-dark“-Materialien) sowie Strontiumchlorid-Hexahydrat in Zahnpasta für empfindliche Zähne. Damit ist Strontium ein hervorragendes Beispiel dafür, wie ein chemisch reaktives Element dennoch überwiegend in Form seiner Verbindungen begegnet wird.
Barium und Radium in fortgeschrittenen oder spezialisierten Kontexten
Die barium-Element wird oft durch seine Schwere in Erinnerung behalten. Es ist häufig mit Baryt assoziiert, und eine seiner bekanntesten Verbindungen ist Bariumsulfat. Diese Verbindung ist von Bedeutung, weil sie sehr unlöslich ist – dies erklärt, warum Barium in praktischen Anwendungen wie Bohrflüssigkeiten und medizinischer Bildgebung eingesetzt werden kann, während andere lösliche Bariumverbindungen aufgrund ihrer Toxizität sorgfältiger behandelt werden müssen. Barium erinnert die Leser daran, dass die nützliche Form eines Elementes der 2. Hauptgruppe oft eine Verbindung und nicht das glänzende Metall selbst ist.
Radium befindet sich am unteren Ende der Gruppe, doch es fügt sich stillschweigend nicht ein. Auf einer radium-Periodentabelle der Blickwinkel: Ra markiert den Punkt, an dem Radioaktivität zum bestimmenden Merkmal wird. Radium kommt in der Natur nur in Spuren vor, typischerweise in Verbindung mit Uranerzen. Historisch wurde es durch Leuchtfarben und frühe medizinische Experimente berühmt. Heute rührt seine Gefährlichkeit von seiner Radioaktivität her und nicht vom Verhalten eines gewöhnlichen Metalls, weshalb es unter strengen Sicherheitsvorkehrungen gehandhabt wird. Vereinfacht ausgedrückt gehört Radium nach wie vor zur Gruppe 2, doch wird es ebenso sehr im Hinblick auf nukleare Sicherheit wie im Hinblick auf Chemie besprochen.
Stellt man diese sechs Elemente nebeneinander, verliert die Familie das Aussehen einer bloßen Aufzählung von Namen. Größe, Reaktivität, gebräuchliche Verbindungen und sogar die Art und Weise, wie jedes Element im Alltag oder in der Natur vorkommt, ändern sich beim Abstieg innerhalb der Gruppe. Dieses sich wandelnde Muster macht die Gruppe 2 besonders nützlich, denn die Reihenfolge von Beryllium bis Radium beginnt, systematische Trends statt bloßer Einzelheiten aufzuzeigen.
Eigenschaften der Erdalkalimetalle und Trends der Gruppe 2
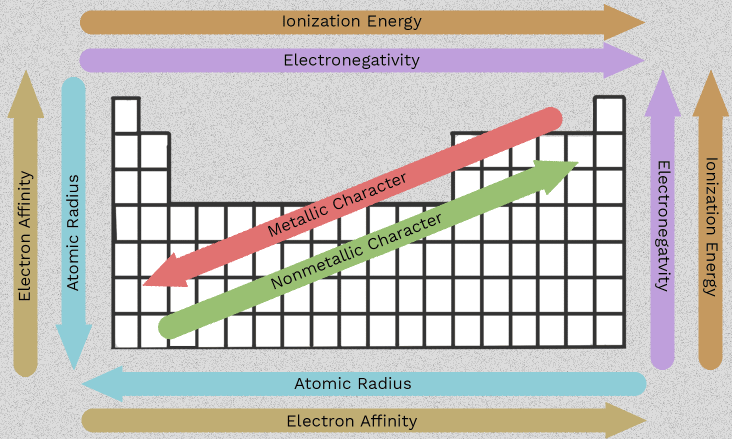
Diese Änderung der Reihenfolge von Beryllium bis Radium macht die 2. Gruppe nützlich. Statt sechs isolierte Fakten auswendig zu lernen, können Sie einer Handvoll Muster folgen, die sich in dieser Spalte wiederholen. Das Wichtigste eigenschaften der Erdalkalimetalle ergibt sich aus einem gemeinsamen Merkmal: Jedes Atom besitzt zwei Außenelektronen, die es tendenziell abgibt.
Sobald Sie verstanden haben, wie sich Größe, Elektronenschirmung und Ionisierungsenergie innerhalb der Gruppe nach unten verändern, wird die Vorhersage des Verhaltens dieser Elementfamilie deutlich einfacher. Diese charakteristika der Erdalkalimetalle sind nicht nur Prüfungswissen. Sie erklären, warum einige Elemente schneller reagieren, warum manche Verbindungen besser löslich sind als andere und warum einige Trends präzise Formulierungen – statt einfacher Pfeile – erfordern.
Gemeinsame Eigenschaften der Erdalkalimetalle
Die meisten Elemente der 2. Gruppe sind silberfarbene Metalle, die üblicherweise M 2+ionen und bilden überwiegend ionische Verbindungen. Sie verhalten sich als Reduktionsmittel, weil sie Elektronen abgeben. Im Vergleich zu den Metallen der Gruppe 1 sind sie im Allgemeinen weniger reaktiv, doch sie sind immer noch chemisch aktiv genug, um zahlreiche gängige Oxide, Chloride, Carbonate und Sulfate zu bilden.
Eine einfache Möglichkeit, die chemischen Eigenschaften der Erdalkalimetalle zu ordnen, besteht darin, das Konstante vom Variablen zu trennen. Konstant bleibt die übliche Oxidationsstufe +2. Variabel ist hingegen, wie leicht jedes Element diese beiden Elektronen abgibt. Genau hier setzen die Trends an.
Trends in der 2. Hauptgruppe nach unten und ihre Bedeutung
Daten von LibreTexts sowie Trenderklärungen von Save My Exams zeigen dasselbe allgemeine Muster: Der Atomradius steigt von 112 pm für Be auf 253 pm für Ba, während die erste Ionisierungsenergie von 900 auf 503 kJ/mol fällt. In einfachen Worten: Die äußeren Elektronen befinden sich weiter vom Kern entfernt und werden durch mehr innere Schalen abgeschirmt, weshalb sie leichter entfernt werden können.
| Entwicklung | Richtung nach unten in der 2. Hauptgruppe | Chemische Ursache | Was dies in der Praxis bedeutet |
|---|---|---|---|
| Atomradius | erhöht | Jedes Element besitzt eine zusätzliche Elektronenschale und mehr Abschirmung | Größere Atome halten ihre äußeren Elektronen weniger fest |
| Erste und zweite Ionisierungsenergie | Gesamtabnahme | Äußere Elektronen befinden sich weiter vom Kern entfernt, daher ist die Anziehung schwächer | Bildung von M 2+ionen wird leichter |
| Reaktivität | Gesamtzunahme | Niedrigere Ionisierungsenergien erleichtern den Elektronenverlust | Schwerere Elemente reagieren heftiger mit Säuren, Sauerstoff und oft auch mit Wasser |
| Schmelzpunkt | Allgemein nimmt sie ab, jedoch nicht gleichmäßig | Größere Metallionen schwächen die metallische Bindung, obwohl auch die Struktur eine Rolle spielt | Verwenden Sie hier das Wort „allgemein“, da Mg und Ca keine perfekt geradlinige Beziehung aufweisen |
| Dichte | Unregelmäßig | Masse, atomare Größe und Metallpackung ändern sich gemeinsam | Die Dichte darf nicht als ein einfacher Abwärtstrend betrachtet werden |
| Hydroxidlöslichkeit | erhöht | Das Verhältnis von Gitterenergie zu Hydratationsenergie verschiebt sich innerhalb der Gruppe nach unten | Schwerere Hydroxide ergeben alkalischere Lösungen |
| Sulfatlöslichkeit | Verringert | Die Hydratationsenergie nimmt ab, wenn der Kationradius zunimmt | Verbindungen wie BaSO 4werden sehr schwer löslich |
Dichte und Schmelzverhalten sind die beiden Trends, die Studierende oft zu stark vereinfachen. Die Dichte verläuft nicht geradlinig, weil sowohl Masse als auch Volumen sich ändern und die Metallatome in jedem Kristall nicht auf dieselbe Weise gepackt sind. Auch die Schmelzpunkte erfordern besondere Aufmerksamkeit. Sie zeigen im Allgemeinen einen Abwärtstrend, da größere Ionen das metallische Gitter schwächen; Magnesium weist jedoch mit 650 °C einen ungewöhnlich niedrigen Schmelzpunkt auf, während Calcium auf 842 °C ansteigt, bevor die Werte erneut fallen. Daher gehört einer der sichersten eigenschaften der Erdalkalimetalle zu dieser Aussage: Das allgemeine Muster ist real, doch die physikalischen Details verlaufen nicht vollkommen glatt.
Auch bei der Löslichkeit gilt dieselbe Warnung. Es gibt keine einzige Regel, die für alle Salze der Gruppe 2 gilt. Die Hydroxide werden im Verlauf der Gruppe löslicher, während die Sulfate weniger löslich werden. Wenn jemand behauptet, „die Löslichkeit nehme in der Gruppe 2 nach unten hin zu“, lautet die entscheidende Frage: „Welche Verbindungen?"
Warum Erdalkalimetalle so reagieren, wie sie es tun
Also, sind Erdalkalimetalle reaktiv ? Ja, und die allgemeine Antwort lautet, dass ihre Reaktivität beim Abstieg in der Gruppe zunimmt. Der Grund ist dieselbe Elektronenkonfiguration wie oben beschrieben. Niedrigere erste und zweite Ionisierungsenergien bedeuten, dass die Atome zwei Elektronen leichter abgeben können und schneller den üblichen M 2+-Zustand erreichen.
Dies wirkt sich auf reale Reaktionen aus. Im Verlauf der Gruppe verlaufen Reaktionen mit verdünnten Säuren schneller, Reaktionen mit Sauerstoff werden heftiger, und schwerere Elemente lassen sich leichter oxidieren. Laut Save My Exams ist Barium so reaktiv, dass es unter Öl aufbewahrt werden muss – ein praktischer Hinweis darauf, wie weit die Reaktivitätsentwicklung gehen kann.
- Der Atomradius nimmt in Gruppe 2 nach unten zu.
- Die Ionisierungsenergie nimmt in Gruppe 2 nach unten ab.
- Die Reaktivität nimmt zu, weil das Abgeben von zwei Elektronen leichter wird.
- Schmelzpunkt und Dichte weisen Unregelmäßigkeiten auf; daher sollten keine absoluten Regeln aufgestellt werden.
- Hydroxide und Sulfate zeigen entgegengesetzte Löslichkeitstrends.
Diese Muster machen die Gruppe vorhersehbar, aber nicht vollkommen einheitlich. Gleich ganz oben in der Gruppe beginnt Beryllium bereits, die Regeln zu brechen, und Magnesium stellt eine weitere alltägliche Ausnahme dar, die wichtiger ist, als viele Anfänger erwarten.
Alkalimetalle und Erdalkalimetalle
Allgemeine Trends erleichtern das Erlernen der Gruppe 2, doch die Gruppe verliert ihren Sinn, wenn jedes Element als identisch behandelt wird. Das deutlichste Warnsignal ist Beryllium. Magnesium stellt eine weitergehende, praktisch relevantere Ausnahme dar. Und wenn Menschen alkalimetalle und Erdalkalimetalle vergleichen, können ähnliche Namen einige sehr unterschiedliche Chemie verbergen.
Warum sich Beryllium nicht wie ein typisches Erdalkalimetall der Gruppe 2 verhält
BYJU'S beschreibt Beryllium als deutlichen Ausreißer innerhalb der Gruppe 2. Seine ungewöhnlich kleine Atomgröße, seine hohe Ionisierungsenergie und seine starke polarisierende Wirkung verleihen ihm ein Verhalten, das weniger typisch für die Gruppe ist. In einfacher Sprache: Be 2+zieht stark an benachbarten Elektronenwolken, weshalb Berylliumverbindungen oft stärker kovalent sind als die stärker ionischen Verbindungen der schwereren Gruppenmitglieder. Dieselbe Quelle weist zudem darauf hin, dass Beryllium höhere Schmelz- und Siedepunkte aufweist als die übrigen Elemente der Gruppe und sich im Gegensatz zu seinen Gruppenmitgliedern nicht mit Wasser reagiert.
Magnesium ist nicht so ungewöhnlich wie Beryllium, wirkt jedoch immer noch weniger reaktiv, als Schüler erwarten würden. LibreTexts vermerkt, dass sehr reines Magnesium nur schwach mit kaltem Wasser reagiert und die Reaktion bald abflaut, weil sich nahezu unlösliches Magnesiumhydroxid als Barriere auf der Oberfläche bildet. Am unteren Ende der Gruppe wird Radium in der Regel separat behandelt, da seine Radioaktivität bei praktischen Anwendungen sowie bei Sicherheitsüberlegungen im Vordergrund steht.
Wie Erdalkalimetalle sich von Alkalimetallen unterscheiden
In einfacher alkali vs. Erdalkali formulierung verlieren die Metalle der Gruppe 1 ein Außenelektron, während die Metalle der Gruppe 2 zwei Außenelektronen abgeben. Dieser einzige Unterschied prägt die eigenschaften von Alkalimetallen und Erdalkalimetallen stärker als fast jede andere Eigenschaft.
| Funktion | Alkalimetalle, Gruppe 1 | Erdalkalimetalle, Gruppe 2 |
|---|---|---|
| Valenzelektronen | 1 | 2 |
| Typisches Ion | M + | M 2+ |
| Reaktion mit kaltem Wasser | Oft heftig oder sogar heftig bis explosiv unter Bildung von Hydroxid und Wasserstoff | Weniger einheitlich: Beryllium reagiert nicht mit Wasser, Magnesium reagiert nur schwach, Calcium, Strontium und Barium reagieren mit zunehmender Heftigkeit |
| Gemeinsame Sauerstoffchemie | Können Oxide, Peroxide oder Superoxide bilden | Bilden üblicherweise Monoxide; die meisten dieser Oxide bilden mit Wasser Hydroxide, doch ist BeO eine Ausnahme |
Wichtige Ausnahmen, die Schüler häufig übersehen
- Nicht jedes Element der Gruppe 2 reagiert auf dieselbe Weise mit Wasser.
- Berylliumverbindungen sind stärker kovalent als die übrigen Elemente dieser Gruppe.
- Verwechseln Sie nicht alkalimetalle und Erdalkalimetalle als dieselbe Gruppe nur deshalb, weil die Namen ähnlich klingen.
- Die eigenschaften der Alkalimetalle und der Erdalkalimetalle werden am besten als Muster mit Ausnahmen gelernt, nicht als starre Schlagwörter.
Das ist auch der beste Weg, um die chemischen Eigenschaften der Alkalimetalle und der Erdalkalimetalle zu verstehen. Elektronenmuster liefern die Regel, doch reale Stoffe verleihen ihr Gewicht. Und diese Gewichtung wird noch deutlicher, wenn man betrachtet, wo die Elemente der Gruppe 2 tatsächlich vorkommen: selten als reine Metalle, weitaus häufiger jedoch in Mineralien, Gesteinen, Meerwasser, Knochen und technischen Verbindungen.
Wie Erdalkalimetalle in der Natur vorkommen
Wenn Sie sich ein erdalkalimetall als helle, reine Probe vorstellen, die in einem Gestein liegt, funktioniert die Natur anders. Elemente der Gruppe 2 sind so reaktiv, dass sie normalerweise als Ionen in Mineralien, Salzen, Gesteinen, Meerwasser, Knochen und Schalen vorkommen – nicht als freie Metalle. Egal, ob jemand nach erdalkalimetallen oder dem gebräuchlicheren Begriff sucht: Das natürliche Muster ist dasselbe – diese Elementfamilie bevorzugt stark Verbindungen.
Dieses Muster ergibt sich unmittelbar aus den chemischen Eigenschaften der Erdalkalimetalle . Sie neigen dazu, zwei Außenelektronen abzugeben und stabile M 2+-Ionen zu bilden. Sobald dies geschieht, binden Sauerstoff-, Carbonat-, Sulfat- und Halogenid-Ionen sie leicht in feste Verbindungen ein, die sich sowohl in der Geologie als auch in der Biologie langfristig erhalten können.
Warum Erdalkalimetalle in der Natur nicht elementar vorkommen
Britannica und ThoughtCo beide beschreiben die Gruppe 2 als reaktiv, was erklärt, warum diese Elemente nur selten unverbunden vorkommen. In Luft bilden viele von ihnen schnell Oxidschichten. In natürlichen Umgebungen werden sie noch stärker als Carbonate, Sulfate, Silikate, Fluoride oder Chloride stabilisiert. Daher kommt Calcium in Kalkstein und Muschelschalen vor, Magnesium in Mineralien und Meerwasser sowie Strontium oder Barium in Erzlagerstätten. Radium ist noch seltener und tritt nur in Spuren in Uranerzen auf.
Häufige Mineralien und Verbindungen der Gruppe 2
| Elemente | Häufige natürliche Quelle | Bekannte Verbindung | Warum diese Verbindung von Bedeutung ist |
|---|---|---|---|
| Beryllium | Beryl | BeO | Beryll ist eine kommerzielle Quelle des Elements, während Berylliumoxid eine wichtige Verbindung in Spezialwerkstoffen ist |
| Magnesium | Magnesit, Dolomit, Meerwasser | MgCO₃ 3oder Mg(OH)₂ 2 | Erklärt, warum Magnesium häufiger in Mineralien, Meerwasser und Medizin als reines Metall vorkommt |
| Kalzium | Kalkstein, Kreide, Marmor, Gips, Knochen, Muschelschalen | Caco 3 | Verbindet Geologie, Baumaterialien und Skelette in einer sehr häufigen Verbindung |
| Strontium | Celestit, Strontianit | SrSO 4oder SrCO 3 | Diese Mineralien sind die wichtigsten natürlichen Quellen für Strontiumverbindungen |
| Barium | Baryt, Witherit | BaSO 4 | Baryt ist das Schlüsselerz, und Bariumsulfat ist eine der bekanntesten Bariumverbindungen |
| Radium | Spuren in Pechblende und anderen Uranerzen | RaCl 2 | Seine Seltenheit und Radioaktivität machen Radiumverbindungen historisch bedeutend, aber ungewöhnlich |
EBSCO weist darauf hin, dass Calcium und Magnesium auch im Meerwasser in einer Konzentration von etwa 0,4 g/L bzw. 1,3 g/L vorkommen. Das hilft zu erklären, warum dieses erdalkalimetall familie nicht nur mit Erzen, sondern auch mit hartem Wasser, marinen Systemen und lebendem Gewebe verbunden ist.
Wie diese Metalle aus ihren Verbindungen gewonnen werden
Da die Metalle der Gruppe 2 üblicherweise in Verbindungen gebunden sind, beginnt die Gewinnung mit Erzen, Sole oder mineralischen Ablagerungen. Eine gängige industrielle Vorgehensweise ist einfach: Zunächst wird das Ausgangsmaterial in ein leichter verarbeitbares Oxid oder Halogenid umgewandelt; anschließend erfolgt die Freisetzung des Metalls mittels Elektrolyse oder chemischer Reduktion. Die Britannica beschreibt die frühe Isolierung von Magnesium, Calcium, Strontium und Barium durch Elektrolyse, während EBSCO darauf hinweist, dass die moderne Produktion nach wie vor häufig auf geschmolzenen Chloriden, Oxid-Reduktion oder verwandten Verfahren beruht – je nach betreffendem Element. Beryllium ist eine nützliche Erinnerung daran, dass die Familie nicht vollständig einheitlich ist, da es durch Reduktion von Berylliumfluorid hergestellt werden kann.
Im Alltag begegnen Menschen der Gruppe 2 daher üblicherweise durch Kalkstein, Gips, Magnesium aus Meerwasser, Baryt oder biologisches Calcium – nicht jedoch durch reine Metallproben. Dieses Detail ist wichtig, denn die reale Bedeutung dieser Elemente hängt weitaus stärker von ihren Verbindungen und Erscheinungsformen ab als vom reinen Metall selbst.
Beispiele für Erdalkalimetalle im Alltag
Die Gruppe 2 wird deutlich einprägsamer, wenn man jedes Element mit etwas Konkretem verknüpft: Knochen, Säurehemmer, Gips, Feuerwerkskörper, Bohrflüssigkeiten und alte Leuchtzifferblätter sind alle hilfreich. beispiele für Erdalkalimetalle wenn Sie sich jemals gefragt haben ist Magnesium ein Metall oder ein Nichtmetall? oder ist Ca ein Metall? , lauten beide Antworten einfach: Magnesium und Calcium sind Metalle. Im gewöhnlichen Leben begegnen Menschen diesen Stoffen jedoch meist in Form von Verbindungen – nicht als reine Metallproben.
Alltägliche Anwendungen von Magnesium- und Calciumverbindungen
- Magnesium : Magnesium gehört zu den biologisch wichtigsten erdalkalimetalle . Der NIH-Magnesium-Faktenblatt weist darauf hin, dass es ein Cofaktor in mehr als 300 Enzymsystemen ist und die Funktion von Muskeln und Nerven, die Energieproduktion sowie die Knochenstruktur unterstützt. Magnesiumverbindungen finden sich zudem in einigen Säurebindern und Abführmitteln, während Magnesiummetall aufgrund seiner geringen Dichte in leichten Legierungen geschätzt wird, bei denen eine Massereduktion entscheidend ist.
- Kalzium calciumverbindungen prägen den Alltag. Calcium trägt zur Struktur von Knochen und Zähnen bei, und Verbindungen wie Calciumcarbonat und Calciumsulfat sind zentral für Kalkstein, Zement, Gips und Trockenbauplatten. Damit stellt Calcium eine der deutlichsten Verbindungen zwischen Chemie, Biologie und Bauwesen dar.
Spezialanwendungen von Strontium und Barium
- Strontium strontiumsalze sind vor allem dafür bekannt, in Feuerwerkskörpern und Signalraketen intensive rote Farben zu erzeugen. Selbst Leser, die sich nicht die vollständige Liste der Gruppe-2-Elemente merken können, erinnern sich oft an Strontium, sobald es mit einer Farbe assoziiert wird.
- Barium bariumverbindungen spielen sowohl in der Industrie als auch in der Medizin eine wichtige Rolle. Das NLM-Barium-Profil beschreibt die wichtigsten Anwendungen in Bohrspülmitteln, Lacken, Kunststoffen, Ziegeln und Glas. Es weist zudem auf eine wichtige medizinische Kontrastanwendung hin: hochgradig unlösliches Bariumsulfat wird als röntgendichtes Material bei bestimmten Röntgenuntersuchungen eingesetzt, da es vom Körper im Allgemeinen nicht resorbiert wird.
- Radium : Radium ist heute vorwiegend ein historisches oder streng reguliertes wissenschaftliches Thema. NRC-Radium-Seite beschreibt dessen frühere Verwendung in Leuchtfarben und der frühen Krebstherapie. Die meisten dieser Anwendungen wurden mittlerweile durch andere Verfahren ersetzt; einige regulierte Anwendungen bestehen jedoch weiterhin, beispielsweise bestimmte industrielle Anwendungen der Strahlenprüfung.
Warum Form und Verbindungstyp in der praktischen Anwendung entscheidend sind
Bei den Elementen der Gruppe 2 wird in der Praxis häufig die Verbindung und nicht das reine Metall verwendet.
Diese einzige Idee klärt viel Verwirrung. Magnesium in Lebensmitteln oder Medikamenten ist nicht dasselbe wie brennendes Magnesiumband. Calcium in Knochen ist nicht dasselbe wie reaktives Calciummetall. Barium ist das deutlichste Beispiel dafür, warum die chemische Form entscheidend ist: unlösliches Bariumsulfat kann in der medizinischen Bildgebung nützlich sein, während löslichere Bariumverbindungen weitaus größere Vorsicht erfordern. Radium unterstreicht diesen Aspekt noch stärker, da seine Radioaktivität – und nicht nur seine Stellung unter den Metallen – bestimmt, wie damit umgegangen wird.
Der Wert der 2. Hauptgruppe ist also keineswegs abstrakt. Diese Elemente helfen zu erklären, wie dieselbe Elementfamilie in Ernährung, Werkstoffkunde, Medizin, industrieller Verarbeitung und Sicherheitsvorschriften von Bedeutung sein kann. Oft genügt bereits eine kurze Liste konkreter Anwendungen, damit sich das übergeordnete Muster einprägt.
Wichtige Erkenntnisse zu den Elementen der 2. Hauptgruppe
Zu diesem Zeitpunkt sollte die erdalkalimetalle-Gruppe weniger wie eine auswendig zu lernende Liste und vielmehr wie ein Muster erscheinen, das Sie direkt aus der 2. Gruppe im Periodensystem spalte ablesen können. Falls jemand dennoch fragt, was sind die Erdalkalimetalle , die kurze Antwort bleibt einfach: Beryllium, Magnesium, Calcium, Strontium, Barium und Radium. Eine umfassendere definition der Erdalkalimetalle ist noch nützlicher: sechs metallische Elemente der Gruppe 2, die normalerweise zwei äußere Elektronen verlieren und M 2+-Ionen bilden.
Wichtige Erkenntnisse zu den Erdalkalimetallen
- Der Ort ist entscheidend: diese sechs gruppe-2-Elemente befinden sich in der zweiten Spalte von links, im Gruppe-2-Bereich des s-Blocks.
- Die Familienmitglieder sind festgelegt: Be, Mg, Ca, Sr, Ba und Ra bilden die gesamte Gruppe.
- Gemeinsame Chemie erklärt die familienähnliche Eigenschaft: ihr ns 2valenzmuster führt gewöhnlich zur Bildung von +2-Ionen – ein zentraler Punkt, der von LibreTexts zusammengefasst wird.
- Die wichtigsten Trends nach unten sind vorhersehbar: der Atomradius nimmt zu, die Ionisierungsenergie nimmt im Allgemeinen ab und die Reaktivität steigt normalerweise beim Abstieg innerhalb der Gruppe.
- Die Ausnahmen sind bedeutsam: beryllium verhält sich stärker kovalent als die anderen, Magnesium kann aufgrund seiner Oberflächenschicht weniger reaktiv erscheinen, und Radium wird hauptsächlich im Zusammenhang mit seiner Radioaktivität behandelt.
- Im Alltag bedeutet ‚real life‘ meist Verbindungen und nicht reine Metalle: menschen treffen viel häufiger auf Calciumcarbonat, Magnesiumoxid und Bariumsulfat als auf elementares Ca, Mg oder Ba.
Die erdalkalimetalle im Periodensystem die Spalte lässt sich am leichtesten als sechs Metalle merken, die durch eine gemeinsame Regel verbunden sind: Sie bilden üblicherweise 2+-Ionen, doch jeder Vertreter dieser Gruppe folgt dieser Regel auf seine eigene Weise.
Von der Chemie der Gruppe 2 zu konstruierten Metallteilen
Diese Chemie reicht weit über Lehrbücher hinaus. LibreTexts weist darauf hin, dass elementares Magnesium in großem Maßstab hergestellt und in leichten Legierungen für Flugzeugrahmen sowie Motorteile von Kraftfahrzeugen eingesetzt wird. Ein umfassenderer Leitfaden zu Legierungen zeigt, warum dies von Bedeutung ist: Ingenieure passen Zusammensetzung und Verarbeitung an, um Gewicht, Festigkeit, Korrosionsbeständigkeit und Bearbeitbarkeit in realen Komponenten auszugleichen.
Für Leser, die vom 2. Gruppe im Periodensystem blickwinkel zur Fertigung übergehen, Shaoyi Metal Technology bietet ein praktisches Beispiel für diese Verbindung. Auf seinen Seiten zu Automobilmaterialien und zur Bearbeitung werden die Herstellung von Metallteilen – von der Prototypenerstellung bis zur Serienfertigung – beschrieben, wobei das Materialverhalten und die Prozesskontrolle Hand in Hand gehen müssen. Dadurch wird die erdalkalimetalle im Periodensystem mehr als nur ein Unterrichtsdiagramm. Sie ist zudem Teil der Logik, die bei der Auswahl von Metallen und Legierungen für technisch ausgelegte Bauteile zum Tragen kommt, die leicht, zuverlässig und fertigungsgerecht sein müssen.
FAQ zu Erdalkalimetallen
1. Welche sechs Erdalkalimetalle gibt es?
Die sechs Erdalkalimetalle sind Beryllium, Magnesium, Calcium, Strontium, Barium und Radium. Sie befinden sich in Gruppe 2 des Periodensystems und sind aufgrund ihrer gemeinsamen Eigenschaft, typischerweise zwei Außenelektronen abzugeben, zu einer Gruppe zusammengefasst; dies führt in vielen Verbindungen zu einem charakteristischen 2+-Ionenmuster.
2. Wie unterscheiden sich Erdalkalimetalle von Alkalimetallen?
Alkalimetalle gehören zur Gruppe 1 und bilden typischerweise 1+-Ionen, da sie ein Außenelektron besitzen. Erdalkalimetalle befinden sich in Gruppe 2, bilden meist 2+-Ionen und sind insgesamt weniger reaktiv. Dieses eine zusätzliche Valenzelektron beeinflusst die Bindungsstärke, die Reaktion mit Wasser sowie die Art der Salze und Oxide, die sie üblicherweise bilden.
3. Warum kommen Erdalkalimetalle nicht frei in der Natur vor?
Diese Metalle sind so reaktiv, dass sie in natürlichen Umgebungen normalerweise nicht lange in reiner elementarer Form verbleiben. Stattdessen verbinden sie sich mit Sauerstoff-, Carbonat-, Sulfat-, Chlorid- oder Silikat-Ionen und werden Bestandteil von Mineralien, Gesteinen, Meerwasser, Muschelschalen und Knochen. Daher begegnen Menschen Gruppe-2-Elemente üblicherweise in Form von Verbindungen und nicht als reine Metallproben.
4. Reagieren alle Erdalkalimetalle mit Wasser?
Nein, und dies ist eine der nützlichsten Ausnahmen, an die man sich erinnern sollte. Beryllium ist weitgehend widerstandsfähig gegenüber Wasser; Magnesium reagiert langsam mit kaltem Wasser, da eine Oberflächenschicht die Reaktion begrenzt; Calcium, Strontium und Barium reagieren dagegen leichter. Im Allgemeinen nimmt die Reaktivität mit Wasser von oben nach unten in Gruppe 2 zu.
5. Warum sind Erdalkalimetalle in Industrie und Fertigung wichtig?
Ihre Bedeutung ergibt sich sowohl aus ihren Verbindungen als auch aus ihrer Rolle bei der Legierungsauswahl. Magnesium ist dort wertvoll, wo geringes Gewicht entscheidend ist; Calciumverbindungen spielen eine zentrale Rolle bei Zement und Putz; Bariumverbindungen werden für spezialisierte industrielle und medizinische Anwendungen eingesetzt. In der praktischen Produktion hilft das Verständnis des metallischen Verhaltens bei der Auswahl geeigneter Bearbeitungsverfahren, der Sicherstellung der Prozessstabilität und der Gewährleistung der Bauteilqualität – daher betonen Lieferanten wie Shaoyi Metal Technology zertifizierte Automobilbearbeitung, Prozesskontrolle sowie Unterstützung von Prototyp-Teilen bis hin zur Serienfertigung.
 Kleine Chargen, hohe Standards. Unser Rapid-Prototyping-Dienst macht die Validierung schneller und einfacher —
Kleine Chargen, hohe Standards. Unser Rapid-Prototyping-Dienst macht die Validierung schneller und einfacher —
