Vad är alkaliska jordmetaller? Grupp 2 blir äntligen begriplig
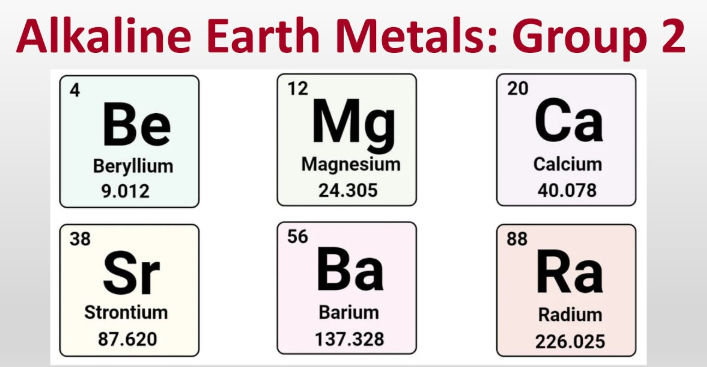
Vad är alkaliska jordmetaller?
Om du sökte efter vad är alkaliska jordmetaller , här är det direkta svaret: de är de sex elementen i Grupp 2 grupp 2 definitionen av alkaliska jordmetaller är utgångspunkten, men namnet säger också mycket om hur denna grupp beter sig.
Vad är alkaliska jordmetaller i en mening
Alkaliska jordmetaller är beryllium, magnesium, kalcium, strontium, barium och radium, de sex metalliska elementen i grupp 2 som vanligtvis bildar +2-joner.
- Beryllium (Be)
- Magnesium (Mg)
- Kalcium (Ca)
- Strontium (Sr)
- Barium (Ba)
- Radium (Ra)
Varför namnet alkalisk jordmetaller är meningsfullt
För nybörjare blir definitionen av alkalisk jordmetaller mycket lättare att förstå när man delar frasen upp i tre delar.
Alkalisk betyder att deras oxider och hydroxider är basiska, inte sura. Jorden är ett historiskt ord. Tidiga kemister använde det för värmebeständiga, mineralliknande ämnen som inte smälte eller löste sig lätt i vatten, en punkt som förklaras av Britannica . Metaller betyder att elementen själva är metalliska, vanligtvis glänsande och bra på att förlora elektroner i reaktioner.
Det ger dig den grundläggande betydelsen av alkalisk jordmetaller utan att behöva avancerad kemi först. Det är också en användbar kort beskrivning av alkaliska jordmetaller : en grupp 2-metallfamilj med gemensam kemi, en gemensam position i det periodiska systemet och en stor roll i den verkliga världen. Magnesium förekommer i legeringar och biologi. Kalcium är viktigt för ben, skal och byggmaterial. Barium, strontium och radium förekommer i mer specialiserade sammanhang.
Den här artikeln börjar medvetet enkelt. En tydlig lista är lätt att memorera, men familjen förstås verkligen först när man ser var dessa grundämnen finns placerade och varför just den platsen ger dem så likartat beteende.
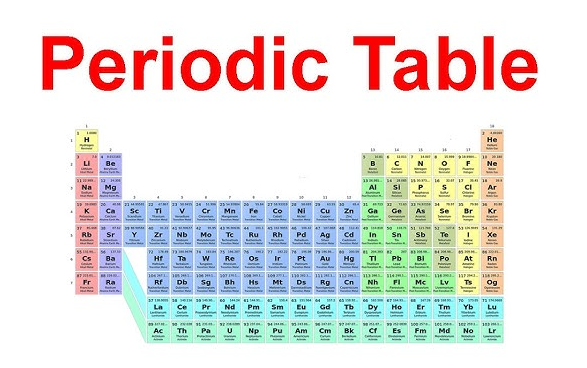
Var grupp 2 finns i det periodiska systemet
Familjenamnet blir mycket lättare att komma ihåg när man faktiskt kan identifiera den. Om du undrar var alkaliska jordmetaller finns i det periodiska systemet , titta på den andra kolumnen från vänster. Den lodräta kolumnen är grupp 2 i det periodiska systemet , placerad direkt bredvid alkalimetallerna i grupp 1. En grupp 2 i periodiska systemet vyn visar samma räta linje varje gång: beryllium överst, sedan magnesium, kalcium, strontium, barium och radium som går nedåt genom perioderna.
I en alkalisk jordmetaller i periodiska systemet diagrammet tillhör dessa sex element s-blocket. Deras gemensamma placering är betydelsefull eftersom den speglar ett gemensamt elektronmönster. Som LibreTexts förklarar har grupp 2-element en ns 2-valenselektronkonfiguration, vilket innebär att de har två yttre elektroner.
Var alkaliska jordmetaller finns i periodiska systemet
Visuellt är mönstret enkelt. Den grupp 2 i periodiska systemet utgör en familjekolumn över perioderna 2 till 7. Många klassrumsdiagram markerar tydligt denna alkaliska jordmetaller i periodiska systemet layouter med samma färg eftersom elementfamiljer läses vertikalt, inte horisontellt. Sökningar efter periodiska systemet alkaliska jordmetaller avser egentligen den här ena kolumnen.
| Element | Symbol | Grupp 2-position | Typisk jon | Känt förening |
|---|---|---|---|---|
| Beryllium | Be | Period 2, toppen av grupp 2 | Be2+ | BeO |
| Magnesium | Mg | Period 3 | Mg2+ | Mgo |
| Kalcium | Ca | Period 4 | Ca2+ | CaCO 3 |
| Strontium | Sr | Period 5 | Sr2+ | SrCO 3 |
| Barium | - Ba | Period 6 | - Ba 2+ | BaSO 4 |
| Radium | RA | Period 7, nedersta delen av grupp 2 | RA 2+ | RaCl 2 |
Varför grupp-2-element bildar +2-joner
Dessa två yttre elektroner styr kemin. Atomer i grupp 2 tenderar att förlora båda elektronerna eftersom det ger dem en mer stabil elektronkonfiguration. Resultatet är en +2-jon , såsom Mg 2+eller Ca 2+. Därför bildar dessa metaller vanligen föreningar som oxider, klorider, karbonater och sulfater. Du ser mönstret i formlerna direkt: MgO, CaCl 2, CaCO 3, BaSO 4.
Hur man snabbt känner igen alkalisk jordmetallgruppen
En snabb identifieringsmetod är att leta efter tre ledtrådar samtidigt: andra kolumnen, metalliska grundämnen och en vanlig +2-laddning. Jämfört med de intilliggande alkalimetallerna, som har en valenselektron och vanligtvis bildar +1-joner, har grupp 2-elementen en extra yttre elektron och är i allmänhet mindre reaktiva. Ändå tillhör de tydligt en gemensam grupp. Det intressanta är att varje medlem uttrycker detta mönster lite olika, särskilt från beryllium högst upp till radium längst ner.
Möt de sex alkaliska jordmetallerna
En lista är användbar, men den är inte särskilt minnesvärd i sig. Grupp 2 börjar kännas mer verklig när varje medlem har en tydlig identitet. Vissa förekommer i ben eller havsvatten. Vissa färgar fyrverkerier. En är främst ett historiskt varningstecken. Tillsammans tillhör de fortfarande samma familj, men var och en har sin egen personlighet.
| Element | Symbol | Vanlig förekomst | Utmärkande egenskap | Relevans i verkligheten |
|---|---|---|---|---|
| Beryllium | Be | Förekommer i mineraler såsom beryll | Mycket lätt och styv för en metall | Används i specialiserade luft- och rymdfartsapplikationer samt röntgenapplikationer; damm är farligt om det andas in |
| Magnesium | Mg | Förekommer i havsvatten och mineraler | Låg densitet och starkt vitt låga när den brinner | Viktigt i lättviktslegeringar, kosttillskott och biologi |
| Kalcium | Ca | Vanligt i kalksten, ben, skal och krita | Biologiskt bekant jon av grupp 2 | Nyckelkomponent i skelett, cement, gips och många naturliga mineraler |
| Strontium | Sr | Huvudsakligen förekommer i celestit och strontianit | Salter ger en levande röd färg i lågor | Används i fyrverkerier, signalraketer, lysmaterial och vissa tandvårdsprodukter |
| Barium | - Ba | Vanligtvis associerat med baryt | Tung, dens metall av alkaliska jordartsmetaller | Bariumsulfat är viktigt inom borrning och medicinsk avbildning; lösliga bariumföreningar kräver försiktighet |
| Radium | RA | Förekommer i spårmängder i uranmalmer | Kraftig radioaktivitet dominerar dess kemihistoria | Idag främst av historisk eller strikt kontrollerad vetenskaplig relevans |
Beryllium och magnesium högst upp i grupp 2
Den grundämnet beryllium finns högst upp i familjen och antyder redan att grupp 2 inte är helt enhetlig. Det är vanligtvis kopplat till mineralen beryll, samma mineralfamilj som omfattar smaragd och akvamarin. Beryllium sticker ut eftersom det är ovanligt lätt och styvt. Det gör det användbart i högpresterande komponenter där låg massa är avgörande. Samtidigt är beryllium ett material som kräver försiktighet i industriella miljöer, eftersom fin damm kan vara skadlig om den andas in. Det minns därför både för sin prestanda och för den försiktighet som krävs vid hantering.
Magnesium känns mycket mer bekant. magnesiums kemiska symbol är Mg och är en av de mest kända metallerna i denna grupp eftersom den förekommer i havsvatten, vanliga mineraler och levande system. Det är en mycket lätt metall, och när den brinner producerar den ett intensivt vitt ljus. Därför har magnesium länge kopplats till signalraketer och material som brinner kraftfullt. I vardagslivet möter de flesta dock magnesium i mildare former, till exempel i kosthållning, som syrabindande föreningar eller i lättviktiga legeringar där minskning av massa är viktig.
Kalcium och strontium i vardagliga material
Kalcium är den mest kända grupp 2-elementet för många läsare. Den förekommer i kalksten, krita, skal och ben, så den knyter samman kemi med både geologi och biologi nästan omedelbart. Kalciumkarbonat är den välbekanta föreningen här. Den hjälper till att förklara varför samma grupp kan spela roll vid grottbildning, byggmaterial och skelett. Rent kalciummetall är reaktivt, men kalciumföreningar finns överallt, vilket är anledningen till att detta grundämne ofta upplevs som mer bekant än exotiskt.
Strontium är lättare att komma ihåg när man kopplar det till färg. symbolen för strontium är Sr och strontium finns främst i mineralen celestit och strontianit. Royal Society of Chemistry beskriver det som ett mjukt, silvervitt metall som brinner i luft och reagerar med vatten. Dess salter är kända för att ge intensiva röda färger i fyrverkerier och signalraketer. Samma källa nämner också användningen i lysande material och strontiumkloridhexahydrat i tandkräm för känsliga tänder. Det gör strontium till ett utmärkt exempel på hur ett grundämne kan vara kemiskt reaktivt men ändå främst mötas i form av föreningar.
Barium och radium i avancerade eller specialiserade sammanhang
Den bariumelementet kommer ofta ihåg genom sin tyngd. Det är vanligt att associera det med baryt, och en av dess mest kända föreningar är bariumsulfat. Den här föreningen är viktig eftersom den är mycket olöslig, vilket förklarar varför barium kan förekomma i praktiska sammanhang såsom borrvätskor och medicinsk bildbehandling, medan andra lösliga bariumföreningar hanteras med större försiktighet på grund av toxikologiska risker. Barium påminner läsarna om att den användbara formen av ett grupp 2-element ofta är en förening, inte det blanka metallet självt.
Radium står längst ner i familjen, men det blandar sig inte diskret. radium-periodiska systemet vy, Ra markerar den punkt där radioaktivitet blir den avgörande egenskapen. Radium förekommer naturligt endast i mycket små mängder, vanligtvis i samband med uranmalm. Historiskt sett blev det berömt för sina lysande färger och tidiga medicinska experiment. Idag härrör dess farlighet från radioaktiviteten snarare än från vanliga metallbeteenden, så det hanteras under strikta kontroller. I enkla termer tillhör radium fortfarande grupp 2, men diskuteras lika mycket med hänsyn till kärnsäkerhet som till kemi.
Ställ dessa sex sida vid sida och familjen slutar se ut som en blott lista över namn. Storlek, reaktivitet, vanliga föreningar och även det sätt på vilket varje grundämne förekommer i livet förändras när man går nedåt i gruppen. Detta föränderliga mönster är där grupp 2 blir särskilt användbar, eftersom ordningen från beryllium till radium börjar avslöja trender istället för oviktiga fakta.
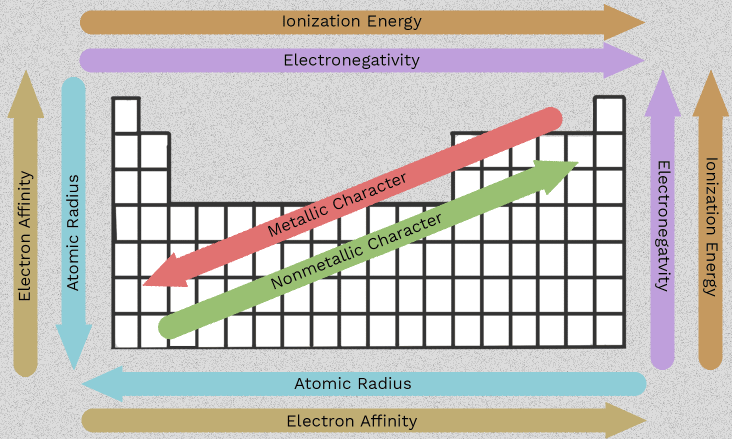
Egenskaper hos alkaliska jordmetaller och trender i grupp 2
Den förändringen av ordningen från beryllium till radium är vad som gör grupp 2 användbar. Istället for att memorera sex isolerade fakta kan du följa ett fåtal mönster som upprepas längs kolumnen. Det viktigaste egenskaper hos alkaliska jordmetaller utgår alla från en gemensam egenskap: varje atom har två yttre elektroner som den tenderar att förlora.
När du förstår hur storlek, elektronskärmning och jonisationsenergi förändras nedåt i gruppen blir familjen mycket lättare att förutsäga. Dessa egenskaper hos alkaliska jordmetaller är inte bara tentamensfakta. De förklarar varför vissa medlemmar reagerar snabbare, varför vissa föreningar löser sig bättre än andra och varför vissa trender kräver noggrann formulering istället for enkla pilarsymboler.
Gemensamma egenskaper hos alkaliska jordmetaller
De flesta medlemmarna i grupp 2 är silverglänsande metaller som vanligtvis bildar M 2+joner och bildar främst jonföreningar. De beter sig som reduktionsmedel eftersom de förlorar elektroner. Jämfört med grupp 1-metaller är de i allmänhet mindre reaktiva, men de är fortfarande kemiskt aktiva nog för att bilda många vanliga oxider, klorider, karbonater och sulfater.
Ett enkelt sätt att organisera de kemiska egenskaperna hos alkalijordmetaller är att separera det som förblir konstant från det som förändras. Det som förblir konstant är den vanliga +2-oxidationsstaten. Det som förändras är hur lätt varje grundämne avger dessa två elektroner. Det är där trenderna börjar bli relevanta.
Trender nedåt i grupp 2 och vad de betyder
Data insamlade av LibreTexts och trendförklaringar från Save My Exams visar samma övergripande mönster. Atomradien ökar från 112 pm för Be till 253 pm för Ba, medan den första joniseringsenergin minskar från 900 till 503 kJ/mol. Med andra ord befinner sig de yttre elektronerna längre från kärnan och skärms av fler inre skal, vilket gör dem lättare att avlägsna.
| Trenden | Riktning nedåt i grupp 2 | Kemisk orsak | Vad detta betyder i praktiken |
|---|---|---|---|
| Atomradie | Ökars | Varje element har ett extra elektronskal och mer skärmning | Större atomer håller yttre elektroner mindre hårt |
| Första och andra joniseringsenergin | Minskar totalt | Yttre elektroner befinner sig längre från kärnan, så attraktionen är svagare | Bildning av M 2+joner blir lättare |
| Reaktivitet | Ökar totalt | Lägre joniseringsenergier gör det lättare att förlora elektroner | Tungare medlemmar reagerar mer kraftfullt med syror, syre och ofta vatten |
| Smältpunkt | Minskar i allmänhet, men inte på ett jämnt sätt | Större metalljoner försvagar metallbindningen, även om strukturen också spelar roll | Använd ordet "allmänt" här, eftersom Mg och Ca inte följer en perfekt linjär trend |
| Densitet | Irreguljärt | Massa, atomstorlek och metallpackning ändras alla samtidigt | Du kan inte behandla densiteten som en enkel nedåtgående trend |
| Löslighet av hydroxider | Ökars | Balansen mellan gitterenergi och hydreringsenergi förskjuts nedåt i gruppen | Tungare hydroxider ger mer alkaliska lösningar |
| Sulfatlöslighet | Minskar | Hydrateringsenergin minskar när kationen blir större | Föreningar såsom BaSO 4blir mycket olösliga |
Densitet och smältbeteende är de två trenderna som elever ofta förenklar för mycket. Densiteten följer inte en rak linje eftersom både massa och volym förändras, och metallatomerna packas inte på samma sätt i varje kristall. Smältpunkter kräver också noggrannhet. De tenderar i allmänhet att minska eftersom större joner försvagar den metalliska gitterstrukturen, men Mg har en ovanligt låg smältpunkt på 650 °C, medan Ca stiger till 842 °C innan värdena sjunker igen. En av de säkraste egenskaperna hos alkalisk jordmetaller är därför detta: den generella trenden är verklig, men de fysikaliska detaljerna är inte helt jämnt fördelade.
Löslighet har samma varningsetikett. Det finns ingen enda regel som omfattar alla grupp 2-salter. Hydroxider blir mer lösliga nedåt i gruppen, medan sulfater blir mindre lösliga. Om någon säger "lösligheten ökar nedåt i grupp 2" är den viktiga frågan: "Vilka föreningar?"
Varför alkalisk jordmetaller reagerar som de gör
Så, är alkalisk jordmetaller reaktiva ? Ja, och det allmänna svaret är att deras reaktivitet ökar när man går nedåt i gruppen. Anledningen är samma elektronhistoria som beskrivs ovan. Lägre första och andra joniseringsenergier innebär att atomerna lättare kan förlora två elektroner och snabbare nå den vanliga M 2+-staten.
Det påverkar verkliga reaktioner. När man går nedåt i gruppen blir reaktioner med utspädda syrlösningar snabbare, reaktioner med syre mer våldsamma och tyngre gruppmedlemmar lättare att oxidera. Save My Exams noterar att barium är så reaktivt att det måste förvaras under olja, vilket är ett praktiskt tecken på hur långt reaktivitetstrenden kan gå.
- Atomradien ökar nedåt i grupp 2.
- Joniseringsenergin minskar nedåt i grupp 2.
- Reaktiviteten ökar eftersom det blir lättare att förlora två elektroner.
- Smältpunkter och densitet visar oregelbundenheter, så undvik absoluta regler.
- Hydroxider och sulfater visar motsatta löslighetstrender.
Dessa mönster gör familjen förutsägbar, men inte fullständigt enhetlig. Precis nära toppen av gruppen börjar beryllium redan att bryta reglerna, och magnesium lägger till en annan vardaglig undantagsregel som är viktigare än många nybörjare förväntar sig.
Alkalimetaller och jordalkalimetaller
Breda trender gör grupp 2 lättare att lära sig, men familjen slutar ha mening om varje medlem behandlas som identisk. Det största varningstecknet är beryllium. Magnesium lägger till en mer praktisk vardaglig undantagsregel. Och när människor jämför alkalimetaller och jordalkalimetaller , kan liknande namn dölja vissa mycket olika kemiska egenskaper.
Varför beryllium inte beter sig som en typisk grupp-2-metall
BYJU'S beskriver beryllium som den tydliga avvikaren i grupp 2. Dess ovanligt små storlek, höga joniseringsenergi och stark polariserande förmåga ger det ett beteende som är mindre typiskt för familjen. Med andra ord, Be 2+drar kraftfullt på närliggande elektronmoln, så berylliumföreningar är ofta mer kovalenta än de mer joniska föreningar som bildas av de tyngre gruppmedlemmarna. Samma källa noterar också att beryllium har högre smältpunkt och kokpunkt än övriga gruppmedlemmar och inte reagerar med vatten på samma sätt som dess sysslingsgrupp.
Magnesium är inte lika ovanligt som beryllium, men det kan ändå verka mindre reaktivt än vad eleverna förväntar sig. LibreTexts noterar att mycket rent magnesium reagerar endast svagt med kallt vatten, och reaktionen avtar snabbt eftersom nästan olösligt magnesiumhydroxid bildar en barriär på ytan. I botten av gruppen diskuteras radium vanligtvis separat, eftersom dess radioaktivitet dominerar praktiska användningsområden och säkerhetsdiskussioner.
Hur alkalijordartsmetaller skiljer sig från alkalimetaller
I enkla alkali kontra alkalisk jordart termer förlorar metallerna i grupp 1 en yttre elektron, medan metallerna i grupp 2 förlorar två. Den enda skillnaden formar egenskaperna hos alkalimetaller och alkalijordartsmetaller mer än nästan något annat. mer än nästan något annat.
| Funktion | Alkalimetaller, grupp 1 | Alkaliska jordartsmetaller, grupp 2 |
|---|---|---|
| Valenselektroner | 1 | 2 |
| Typisk jon | M + | M 2+ |
| Reaktion med kallt vatten | Ofta kraftfull eller till och med våldsam, bildar hydroxid och vätgas | Mindre enhetlig: Be reagerar inte med vatten, Mg reagerar mildt, Ca, Sr och Ba reagerar med ökande kraft |
| Vanlig syre-kemi | Kan bilda oxider, peroxider eller superoxider | Bildar vanligen monoxider; de flesta av dessa oxider bildar hydroxider i vatten, men BeO är en undantagsfall |
Viktiga undantag som elever ofta missar
- Inte alla metaller i grupp 2 reagerar på samma sätt med vatten.
- Berylliumföreningar är mer kovalenta än resten av gruppen.
- Förväxla inte alkalimetaller och alkalisk jordartsmetaller som samma grupp bara för att namnen låter besläktade.
- Den egenskaper hos alkalimetaller och alkalisk jordartsmetaller lär man sig bäst som mönster med undantag, inte som stelbent slogans.
Det är också det bästa sättet att förstå kemiska egenskaper hos alkalimetaller och alkalisk jordartsmetaller . Elektronmönster ger dig regeln, men verkliga ämnen tillför struktur. Och den strukturen blir ännu tydligare när man undersöker var grupp 2-elementen faktiskt förekommer: sällan som rena metaller och långt oftare i mineraler, bergarter, havsvatten, ben och industriella föreningar.
Hur alkalisk jordartsmetaller förekommer i naturen
Om du föreställer dig en alkalisk jordmetall som en ljus, ren provbit som ligger i en sten, fungerar naturen på ett annat sätt. Grundämnen i grupp 2 är reaktiva nog för att vanligtvis förekomma som joner i mineraler, salter, bergarter, havsvatten, ben och skal snarare än som fria metaller. Oavsett om någon söker efter alkaliska jordmetaller eller den mer standardiserade termen är mönstret i naturen detsamma: denna ämnensfamilj föredrar starkt kemiska föreningar.
Detta mönster härrör direkt från de kemiska egenskaperna hos alkaliska jordmetaller . De tenderar att förlora två yttre elektroner och bilda stabila M 2+joner. När detta sker binder sygen, karbonatjoner, sulfatjoner och halogenjoner dem lätt i fasta föreningar som kan bestå i geologi och biologi.
Varför alkaliska jordmetaller inte förekommer fritt i naturen
Britannica och ThoughtCo båda beskriver grupp 2 som reaktiv, vilket förklarar varför dessa grundämnen sällan förekommer i oombundet tillfälle. I luft bildar många snabbt oxidbeläggningar. I naturliga miljöer stabiliseras de ytterligare som karbonater, sulfater, silikater, fluorider eller klorider. Därför förekommer kalcium i kalksten och skal, magnesium i mineraler och havsvatten samt strontium eller barium i malmfyndigheter. Radium är ännu sällsyntare och förekommer endast i spårkvantiteter i uranmalm.
Vanliga mineraler och föreningar i grupp 2
| Element | Vanlig naturlig källa | Känt förening | Varför denna förening är viktig |
|---|---|---|---|
| Beryllium | Beryl | BeO | Beryll är en kommersiell källa till grundämnet, medan berylliumoxid är en viktig förening i specialmaterial |
| Magnesium | Magnesit, dolomit, havsvatten | MgCO₃ 3eller Mg(OH)₂ 2 | Visar varför magnesium ofta påträffas i mineraler, havsvatten och läkemedel snarare än som rent metall |
| Kalcium | Kalksten, krita, marmor, gips, ben, skal | CaCO 3 | Sammanbinder geologi, byggmaterial och skelett i en mycket vanlig förening |
| Strontium | Celestit, strontianit | SrSO₄ 4eller SrCO₃ 3 | Dessa mineral är de främsta naturliga källorna till strontiumföreningar |
| Barium | Baryt, witherit | BaSO 4 | Baryt är den viktigaste malmarten, och bariumsulfat är en av de mest kända bariumföreningarna |
| Radium | Spårkvantiteter i pitchblende och andra uranmalmer | RaCl 2 | Dess sällsynthet och radioaktivitet gör radiumföreningar historiskt betydelsefulla men ovanliga |
EBSCO noterar att kalcium och magnesium också förekommer i havsvatten i koncentrationer av cirka 0,4 g/L respektive 1,3 g/L. Detta hjälper till att förklara varför denna alkalisk jordart grupp inte bara är kopplad till malm, utan även till hårt vatten, marina system och levande vävnad.
Hur dessa metaller isoleras från sina föreningar
Eftersom grupp 2-metaller vanligtvis är inlåsta i föreningar börjar utvinningen med malm, saltvatten (briner) eller mineralavlagringar. En vanlig industriell idé är enkel: omvandla först materialet till en mer hanterbar oxid eller halid, och använd sedan elektrolys eller kemisk reduktion för att frigöra metallen. Britannica beskriver den tidiga isoleringen av magnesium, kalcium, strontium och barium genom elektrolys, medan EBSCO påpekar att modern produktion fortfarande ofta bygger på smält klorider, oxidreduktion eller relaterade vägar beroende på vilket grundämne det gäller. Beryllium är en användbar påminnelse om att gruppen inte är helt enhetlig, eftersom berylliumfluorid kan reduceras för att framställa beryllium.
Så i vardagliga sammanhang möter människor vanligtvis grupp 2 genom kalksten, gips, magnesium från havsvatten, baryt eller biologisk kalcium, inte genom råmetallprover. Den här detaljen är viktig, eftersom dessa grundämnes verkliga betydelse i verkligheten snarare beror på deras föreningar och former än på de rena metallerna själva.
Exempel på alkaliska jordartsmetaller i vardagslivet
Grupp 2 blir mycket mer minnesvärd när du kopplar varje grundämne till något konkret. Ben, magmedel, gips, fyrverkerier, borrvätskor och gamla lysande urtavlor är alla användbara exempel på alkaliska jordartsmetaller . Om du någonsin har undrat är magnesium en metall eller en icke-metall eller är Ca en metall , är båda svaren enkla: magnesium och kalcium är metaller. I vardagliga sammanhang möter människor dock vanligtvis dessa ämnen som föreningar, inte som rena metallprover.
Vanliga användningsområden för magnesium- och kalciumföreningar
- Magnesium : Magnesium är ett av de biologiskt viktigaste alkaliska jordartselement . Den NIH:s faktablad om magnesium noterar att det är en koenzymfaktor i mer än 300 enzymsystem och stödjer muskel- och nervfunktion, energiproduktion samt benstruktur. Magnesiumföreningar förekommer också i vissa magmedel och avföringsmedel, medan magnesiummetall uppskattas i lättviktliga legeringar där minskning av massa är avgörande.
- Kalcium kalciumföreningar dominerar vardagslivet. Kalcium bidrar till benens och tändernas struktur, och föreningar såsom kalciumkarbonat och kalciumsulfat är centrala i kalksten, cement, gips och gipsplattor. Det gör kalcium till en av de tydligaste kopplingarna mellan kemi, biologi och byggteknik.
Specialiserade tillämpningar av strontium och barium
- Strontium strontiumsalter är främst kända för att ge djupt röda färger i fyrverkerier och signalraketer. Även läsare som inte minns hela grupp 2-listan minns ofta strontium så snart färg kopplas till det.
- Barium bariumföreningar är betydelsefulla inom industri och medicin. Den NLM:s profil på barium beskriver stora användningsområden i borrslam, färger, plaster, tegel och glas. Det noterar också en viktig medicinsk kontrast: starkt olöslig bariumsulfat används som ett radiopakt material i vissa röntgenundersökningar eftersom det i allmänhet inte absorberas av kroppen.
- Radium : Radium är främst ett historiskt eller strikt reglerat vetenskapligt fall. Den NRC:s radiumsida beskriver dess tidigare användning i lysfärger och tidig cancerbehandling. De flesta av dessa användningsområden har ersatts, även om vissa reglerade användningar fortfarande finns, till exempel vissa industriella radiografiapplikationer.
Varför form och föreningstyp spelar roll i praktisk användning
Inom grupp 2 är den form som människor använder ofta föreningen, inte renmetallen.
Den enda idén klargör mycket förvirring. Magnesium i mat eller medicin är inte samma sak som brinnande magnesiumband. Kalcium i ben är inte samma sak som reaktivt kalciummetall. Barium är det tydligaste exemplet på varför formen spelar roll: olösligt bariumsulfat kan vara användbart vid avbildning, medan mer lösliga bariumföreningar kräver betydligt större försiktighet. Radium förstärker ännu mer denna punkt, eftersom dess radioaktivitet – inte bara dess placering bland metallerna – styr hur det hanteras.
Så värdet av grupp 2 är alls inte abstrakt. Dessa element hjälper till att förklara hur samma grupp kan vara relevant för näring, material, medicin, industriell bearbetning och säkerhetsregler. En kort lista över verkliga användningsområden räcker ofta för att den större mönstret ska fastna.
Nyckelpunkter om grupp 2-element
Vid detta laget bör alkaliska jordartsmetaller-gruppen kännas mindre som en lista att memorera och mer som ett mönster som du kan läsa direkt från grupp 2 i periodiska systemet kolumnen. Om någon fortfarande frågar, vad är alkaliska jordmetaller? , är det korta svaret enkelt: beryllium, magnesium, kalcium, strontium, barium och radium. En fullare definition av alkaliska jordmetaller är ännu mer användbart: sex metalliska element i grupp 2 som vanligtvis förlorar två yttre elektroner och bildar M 2+- Ioner.
Viktiga fakta om alkaliska jordmetaller
- Platsen spelar roll. dessa sex grupp 2-element sitt i den andra kolumnen från vänster, grupp 2-sektionen av s-blocket.
- Familjemedlemmarna är fasta: Be, Mg, Ca, Sr, Ba och Ra utgör hela gruppen.
- Delad kemi förklarar familjelikheten: deras ns 2valensmönster gör +2-joner till den vanliga produkten, en central punkt som sammanfattas av LibreTexts.
- De främsta nedåtgående trenderna är förutsägbara: atomradien ökar, joniseringsenergin minskar i allmänhet och reaktiviteten stiger oftast när man går neråt i gruppen.
- Undantagen är viktiga: beryllium beter sig mer kovalent än de andra, magnesium kan verka mindre reaktiv på grund av sin ytbeläggning, och radium diskuteras främst utifrån sin radioaktivitet.
- I verkliga livet handlar det vanligtvis om föreningar, inte rena metaller: människor stöter på kalciumkarbonat, magnesiumoxid och bariumsulfat långt oftare än på grundämnesformerna Ca, Mg eller Ba.
Den alkaliska jordartsmetaller i det periodiska systemet kolumnen är lättast att komma ihåg som sex metaller som förbinder en regel: de bildar vanligtvis 2+-joner, men varje medlem uttrycker den regeln lite olika.
Från grupp 2-kemi till konstruerade metallkomponenter
Denna kemi sträcker sig långt bortom läroböcker. LibreTexts noterar att grundämnesmagnesium framställs i stor skala och används i lättviktiga legeringar för flygplansramar och bilmotordelar. En mer omfattande legeringsguide visar varför detta är viktigt: ingenjörer justerar sammansättning och bearbetning för att balansera vikt, hållfasthet, korrosionsbeständighet och bearbetbarhet i verkliga komponenter.
För läsare som går från grupp 2 i periodiska systemet vyen till tillverkning, Shaoyi Metal Technology erbjuder ett praktiskt exempel på den kopplingen. Dess sidor om automaterial och bearbetning beskriver tillverkning av metallkomponenter från prototypning till massproduktion, där materialbeteende och processkontroll måste samverka. alkaliska jordartsmetaller i det periodiska systemet mer än en klassrumsdiagram. Det är också en del av logiken bakom valet av metaller och legeringar för konstruerade komponenter som behöver vara lätta, pålitliga och tillverkningsbara.
Vanliga frågor om alkaliska jordmetaller
1. Vilka är de sex alkaliska jordmetallerna?
De sex alkaliska jordmetallerna är beryllium, magnesium, kalcium, strontium, barium och radium. De ingår i grupp 2 i det periodiska systemet och är samlade i samma grupp eftersom de vanligtvis förlorar två yttre elektroner, vilket leder till ett gemensamt 2+-jonmönster i många föreningar.
2. Hur skiljer sig alkaliska jordmetaller från alkalimetaller?
Alkalimetaller tillhör grupp 1 och bildar vanligtvis 1+-joner eftersom de har en yttre elektron. Alkaliska jordartsmetaller finns i grupp 2, bildar vanligtvis 2+-joner och är i allmänhet mindre reaktiva. Den ena extra valenselektronen påverkar hur starkt de binder, hur de reagerar med vatten samt vilka typer av salter och oxider de vanligen bildar.
3. Varför förekommer alkaliska jordartsmetaller inte fritt i naturen?
Dessa metaller är tillräckligt reaktiva för att sällan finnas kvar i ren elementär form under längre tid i naturliga miljöer. Istället kombinerar de sig med syre-, karbonat-, sulfat-, klorid- eller silikatjoner och ingår i mineraler, bergarter, havsvatten, skal och ben. Därför stöter människor vanligtvis på grupp 2 genom föreningar snarare än genom råmetallprover.
4. Reagerar alla alkaliska jordartsmetaller med vatten?
Nej, och detta är en av de mest användbara undantagen att komma ihåg. Beryllium är i stort sett motståndskraftigt mot vatten, magnesium reagerar långsamt i kallt vatten eftersom ett ytskikt begränsar reaktionen, och kalcium, strontium och barium reagerar lättare. I allmänhet ökar vattenreaktiviteten ju längre ner i grupp 2 man går.
5. Varför är alkaliska jordmetaller viktiga inom industri och tillverkning?
Deras betydelse beror både på deras föreningar och deras roll vid legeringsval. Magnesium är värdefullt där lägre vikt är avgörande, kalciumföreningar är centrala för cement och gips, och bariumföreningar väljs för specialiserade industriella och medicinska användningsområden. I verklig produktion hjälper förståelsen av metallernas beteende till att styra bearbetning, processstabilitet och delkvalitet, vilket är anledningen till att leverantörer som Shaoyi Metal Technology betonar certifierad bilindustribearbetning, processkontroll samt stöd från prototypdelar till massproduktion.
 Lilla partier, höga standarder. Vår snabba prototypservice gör validering snabbare och enklare —
Lilla partier, höga standarder. Vår snabba prototypservice gör validering snabbare och enklare —
