Что такое щелочноземельные металлы? Группа 2 наконец-то становится понятной
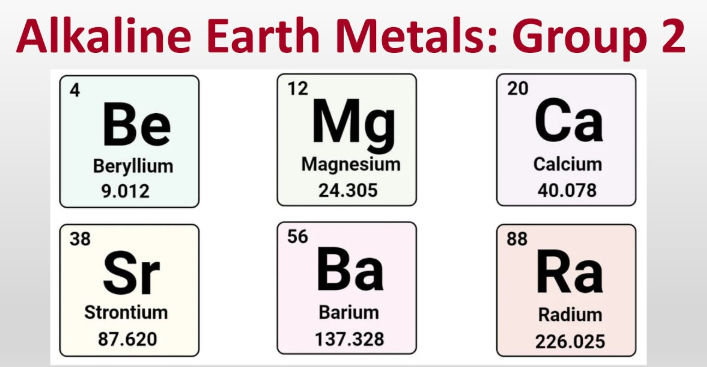
Что такое щелочноземельные металлы?
Если вы искали что такое щелочноземельные металлы , вот прямой ответ: это шесть элементов в Группа 2 группе 2 определение щелочноземельных металлов является отправной точкой, однако название также многое говорит о поведении этой группы элементов.
Щелочноземельные металлы в одном предложении
Щелочноземельные металлы — это бериллий, магний, кальций, стронций, барий и радий, шесть металлических элементов второй группы, которые обычно образуют ионы с зарядом +2.
- Вольфрам (Be)
- Магний (Mg)
- Кальций (Ca)
- Стронций (Sr)
- Барий (Ba)
- Радий (Ra)
Почему название «щелочноземельные металлы» является обоснованным
Для начинающих определение щелочноземельных элементов становится значительно проще, если разбить это выражение на три части.
Щелочной означает, что их оксиды и гидроксиды являются основными, а не кислотными. Земле — это исторический термин. Ранние химики использовали его для обозначения термостойких, минералоподобных веществ, которые не плавились и плохо растворялись в воде; этот момент поясняется в Британика . Металлы означает, что сами элементы являются металлами, как правило, блестящими и легко отдающими электроны в химических реакциях.
Это даёт вам базовое значение термина «щелочноземельные металлы» без необходимости сначала осваивать сложную химию. Это также полезное краткое описание щелочноземельных металлов : металлического семейства II группы с общими химическими свойствами, общей позицией в периодической таблице и важной ролью в реальном мире. Магний присутствует в сплавах и биологических системах. Кальций играет ключевую роль в строении костей, раковин и строительных материалах. Барий, стронций и радий встречаются в более узкоспециализированных областях.
Эта статья намеренно начинается с простого. Чёткий перечень легко запомнить, однако истинное понимание этого семейства приходит, когда вы видите, где именно расположены эти элементы и почему именно это положение обуславливает их сходное поведение.
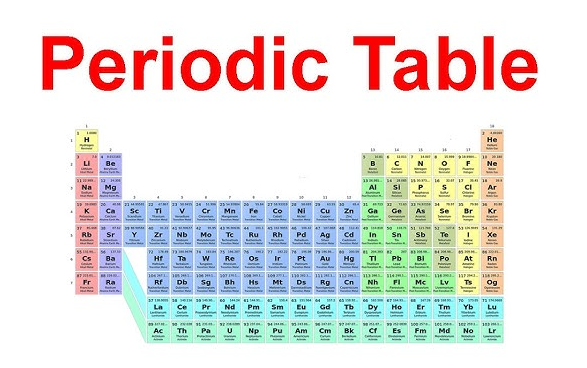
Расположение II группы в периодической таблице
Название семейства становится значительно легче запомнить, если вы можете буквально указать на него. Если вы задаётесь вопросом где находятся щелочноземельные металлы в периодической таблице , взгляните на второй столбец слева. Этот вертикальный столбец — это iI группа периодической таблицы , расположенная непосредственно справа от щелочных металлов I группы. А группа 2 периодической таблицы на рисунке каждый раз отображается одна и та же прямая линия: бериллий вверху, затем магний, кальций, стронций, барий и радий — по мере движения вниз через периоды.
В периодическая таблица щелочноземельных металлов на этой схеме эти шесть элементов относятся к s-блоку. Их общее расположение имеет значение, поскольку оно отражает общую электронную конфигурацию. LibreTexts как объясняется 2валентную конфигурацию ns², что означает наличие у них двух электронов во внешней оболочке.
Где находятся щелочноземельные металлы в периодической таблице
Визуально эта закономерность проста. элементы группы 2 периодической таблицы образуют один семейственный столбец, охватывающий периоды со 2-го по 7-й. Во многих учебных диаграммах этот столбец выделяется. щелочноземельные металлы в периодической таблице макеты одного цвета, поскольку семейства элементов читаются по вертикали, а не по горизонтали. Поисковые запросы на тему периодическая таблица щелочноземельных металлов на самом деле относятся к этому одному столбцу.
| Элемент | Символ | Положение в группе 2 | Типичный ион | Известное соединение |
|---|---|---|---|---|
| Бериллий | Be | Период 2, верхняя часть группы 2 | Be2+ | BeO |
| Магний | Mg | Период 3 | Mg2+ | MgO |
| Кальций | Ca | Период 4 | Ca2+ | Како 3 |
| Стронций | Sr | Период 5 | Sr2+ | SrCO 3 |
| Барий | BA | Период 6 | BA 2+ | BaSO 4 |
| Радий | RA | Период 7, нижняя часть группы 2 | RA 2+ | RaCl 2 |
Почему элементы группы 2 образуют ионы с зарядом +2
Эти два внешних электрона определяют химические свойства. Атомы группы 2 склонны терять оба электрона, поскольку это обеспечивает им более устойчивое электронное строение. В результате образуется +2 ион , например, Mg 2+ или Ca 2+. Именно поэтому эти металлы обычно образуют соединения, такие как оксиды, хлориды, карбонаты и сульфаты. Вы сразу замечаете закономерность в формулах: MgO, CaCl 2, CaCO 3, BaSO 4.
Как быстро распознать семейство щелочноземельных металлов
Быстрый способ идентификации — одновременно обратить внимание на три признака: элементы второй группы, металлические элементы и типичный заряд +2. По сравнению с соседними щелочными металлами, имеющими один валентный электрон и обычно образующими ионы с зарядом +1, элементы группы 2 имеют на один внешний электрон больше и, как правило, менее реакционноспособны. Тем не менее они явно относятся к единому семейству. Интересно то, что каждый из них проявляет эту закономерность по-своему, особенно от бериллия вверху до радия внизу.
Шесть щелочноземельных металлов
Список полезен, но сам по себе он плохо запоминается. Группа 2 начинает ощущаться более реальной, когда каждый её член обладает чёткой индивидуальностью. Некоторые встречаются в костях или морской воде. Некоторые придают цвет фейерверкам. Один из них в основном служит историческим предупреждающим знаком. Вместе они всё ещё принадлежат к одной и той же группе, однако у каждого — своя собственная «личность».
| Элемент | Символ | Распространённое явление | Выделяющееся свойство | Релевантность в реальных условиях |
|---|---|---|---|---|
| Бериллий | Be | Встречается в минералах, таких как берилл | Очень лёгкий и жёсткий для металла | Используется в специализированных аэрокосмических и рентгеновских применениях; пыль опасна при вдыхании |
| Магний | Mg | Присутствует в морской воде и минералах | Низкая плотность и ярко-белое пламя при горении | Важен в лёгких сплавах, пищевых добавках и биологии |
| Кальций | Ca | Распространён в известняке, костях, раковинах и мелу | Биологически знакомый ион группы 2 | Ключевой элемент в скелетах, цементе, штукатурке и многих природных минералах |
| Стронций | Sr | Встречается преимущественно в целестине и стронцианите | Соли придают пламени яркий красный цвет | Используется в пиротехнике, сигнальных ракетах, светящихся материалах и некоторых стоматологических продуктах |
| Барий | BA | Обычно ассоциируется с баритом | Плотный, тяжёлый щёлочноземельный металл | Сульфат бария важен при бурении и медицинской визуализации; растворимые соединения бария требуют осторожности |
| Радий | RA | Встречается в следовых количествах в урановых рудах | Сильная радиоактивность определяет его химическую историю | В основном историческая или строго контролируемая научная значимость сегодня |
Бериллий и магний в верхней части группы 2
Трубы элемент бериллий находится в верхней части подгруппы и уже указывает на то, что группа 2 не является совершенно однородной. Чаще всего он ассоциируется с минералом бериллом — тем же минералом, к которому относятся изумруд и аквамарин. Бериллий выделяется тем, что он необычайно лёгкий и жёсткий. Это делает его полезным в высокопроизводительных компонентах, где важна небольшая масса. В то же время бериллий — это материал, требующий особой осторожности при промышленном использовании, поскольку мелкодисперсная пыль может быть вредной при вдыхании. Поэтому его помнят как за высокие эксплуатационные характеристики, так и за необходимость соблюдения мер предосторожности при обращении.
Магний кажется гораздо более знакомым. химический символ магния это Mg, и он является одним из наиболее известных металлов этой группы, поскольку встречается в морской воде, обычных минералах и живых системах. Это очень лёгкий металл, а при горении он даёт интенсивный белый свет. Именно поэтому магний давно ассоциируется с сигнальными ракетами и материалами, ярко горящими при сгорании. В повседневной жизни, однако, большинство людей сталкиваются с ним в более мягких формах — например, как компонент пищевых продуктов, в составе антацидных препаратов или в лёгких сплавах, применяемых там, где важно снизить массу.
Кальций и стронций в повседневных материалах
Для многих читателей кальций — самый узнаваемый элемент II группы. Он присутствует в известняке, мелу, раковинах и костях, поэтому химия кальция практически сразу связывает геологию и биологию. Кальций карбонат — это знакомое соединение, объясняющее, почему один и тот же химический элемент играет важную роль в формировании пещер, в качестве строительного камня и в скелетах живых организмов. Сам по себе металлический кальций химически активен, однако его соединения повсеместно распространены, поэтому этот элемент часто воспринимается как привычный, а не экзотический.
Стронций легче запомнить, если ассоциировать его с цветом. символ стронция — Sr, и стронций встречается в основном в минералах целестине и стронцианите. Королевское химическое общество описывает его как мягкий серебристый металл, который горит на воздухе и реагирует с водой. Его соли известны тем, что придают ярко-красный цвет фейерверкам и сигнальным ракетам. То же самое издание отмечает также применение стронция в светящихся в темноте материалах и гексагидрате хлорида стронция в зубной пасте для чувствительных зубов. Таким образом, стронций является отличным примером того, как химически активный элемент чаще всего встречается в виде соединений.
Барий и радий в продвинутых или специализированных контекстах
Трубы элемент барий часто ассоциируется с тяжёлостью. Обычно его связывают с баритом, а одним из наиболее известных его соединений является сульфат бария. Это соединение имеет важное значение, поскольку оно крайне малорастворимо, что объясняет, почему барий может применяться в практических целях — например, в буровых растворах и медицинской визуализации, — в то время как другие растворимые соединения бария требуют более осторожного обращения из-за их токсичности. Барий напоминает читателям, что полезной формой элемента II группы зачастую является не сам блестящий металл, а его соединение.
Радий занимает нижнее положение в этой группе, однако он не остаётся незаметным. периодической таблице с радием просмотр: Ra обозначает точку, в которой радиоактивность становится определяющей характеристикой. Радий встречается в природе лишь в микроскопических количествах, обычно в составе урановых руд. Исторически он прославился благодаря использованию в люминесцентных красках и ранних медицинских экспериментах. Сегодня его опасность связана исключительно с радиоактивностью, а не с обычными свойствами металла, поэтому с ним обращаются в строгом соответствии с установленными нормами безопасности. Проще говоря, радий по-прежнему относится к группе 2, однако при его рассмотрении столь же важны соображения ядерной безопасности, сколь и химические аспекты.
Расположите эти шесть элементов рядом друг с другом — и семейство перестаёт выглядеть как простой перечень названий. Размер атомов, реакционная способность, распространённые соединения и даже то, как каждый элемент проявляется в повседневной жизни, изменяются при движении вниз по группе. Именно эта закономерная смена свойств делает группу 2 особенно полезной: упорядоченное расположение от бериллия до радия позволяет выявить общие тенденции, а не просто запоминать отдельные факты.
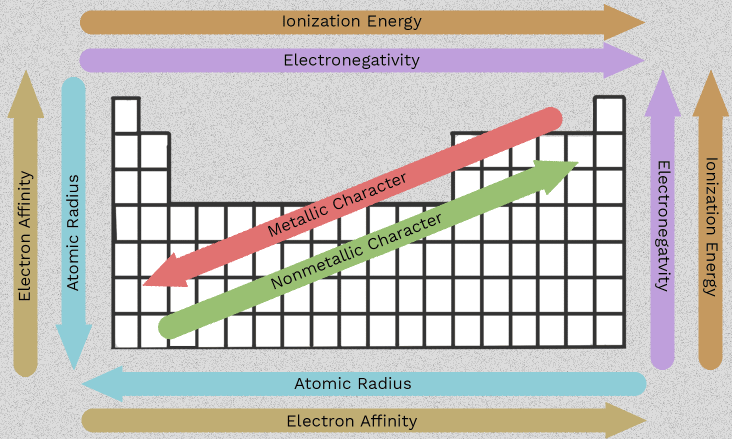
Свойства щелочноземельных металлов и закономерности группы 2
Именно изменение свойств от бериллия к радию делает II группу полезной. Вместо того чтобы запоминать шесть изолированных фактов, вы можете проследить несколько закономерностей, повторяющихся в пределах этой группы. свойства щелочноземельных металлов все проистекают из одной общей особенности: каждый атом имеет два внешних электрона, которые он склонен терять.
Как только вы поймёте, как изменяются атомный радиус, экранирование электронов и энергия ионизации при движении вниз по группе, поведение элементов этой подгруппы становится значительно легче прогнозировать. Эти характерные особенности щелочноземельных металлов — это не просто сведения для экзамена. Они объясняют, почему одни элементы реагируют быстрее других, почему одни соединения лучше растворяются, чем другие, и почему некоторые тенденции требуют осторожной формулировки вместо простого указания стрелкой.
Общие свойства щелочноземельных металлов
Большинство элементов II группы — серебристые металлы, которые обычно образуют катионы M 2+ионы и образуют преимущественно ионные соединения. Они проявляют себя как восстановители, поскольку отдают электроны. По сравнению с металлами первой группы они, как правило, менее реакционноспособны, однако всё ещё достаточно химически активны для образования многих распространённых оксидов, хлоридов, карбонатов и сульфатов.
Простой способ систематизировать химические свойства щелочноземельных металлов состоит в разделении того, что остаётся неизменным, и того, что изменяется. Неизменным остаётся характерная степень окисления +2. То, что изменяется, — это лёгкость, с которой каждый элемент отдаёт эти два электрона. Именно здесь начинают проявляться закономерности.
Закономерности при движении вниз по второй группе и их значение
Данные, собранные LibreTexts, и объяснения закономерностей от Save My Exams демонстрируют одну и ту же общую тенденцию. Атомный радиус увеличивается от 112 пм у Be до 253 пм у Ba, а первая энергия ионизации снижается с 900 до 503 кДж/моль. Простыми словами: внешние электроны расположены дальше от ядра и экранируются большим числом внутренних электронных оболочек, поэтому их легче удалить.
| Тенденция | Направление движения вниз по второй группе | Химическая причина | Что это означает на практике |
|---|---|---|---|
| Атомный радиус | Увеличивает | У каждого элемента имеется дополнительная электронная оболочка и большее экранирование | Более крупные атомы удерживают внешние электроны менее прочно |
| Первая и вторая энергии ионизации | В целом уменьшаются | Внешние электроны расположены дальше от ядра, поэтому притяжение слабее | Образование M 2+ионов становится проще |
| Реакционность | В целом возрастает | Более низкие энергии ионизации облегчают потерю электронов | Более тяжелые элементы реагируют более энергично с кислотами, кислородом и часто с водой |
| Температура плавления | В целом уменьшается, но не плавно | Более крупные ионы металлов ослабляют металлическую связь, хотя структура также имеет значение | Используйте слово «в целом», поскольку магний и кальций не укладываются в идеально прямую зависимость |
| Плотность | Нерегулярный | Масса, атомный размер и упаковка металла изменяются одновременно | Нельзя рассматривать плотность как одну простую нисходящую тенденцию |
| Растворимость гидроксидов | Увеличивает | Соотношение энергии решетки и энергии гидратации изменяется при движении вниз по группе | Более тяжелые гидроксиды образуют более щелочные растворы |
| Растворимость сульфатов | Уменьшается | Энергия гидратации уменьшается по мере увеличения размера катиона | Соединения, такие как BaSO 4становятся крайне малорастворимыми |
Плотность и поведение при плавлении — это две тенденции, которые студенты зачастую чрезмерно упрощают. Плотность не изменяется линейно, поскольку одновременно изменяются как масса, так и объём, а атомы металлов упаковываются в кристаллической решётке по-разному. За температурами плавления также необходимо внимательно следить. В целом они снижаются вниз по группе, поскольку увеличение размера ионов ослабляет металлическую решётку, однако у магния необычно низкая температура плавления — 650 °C, тогда как у кальция она возрастает до 842 °C, после чего снова начинает снижаться. Таким образом, одним из самых надёжных характеристик щелочноземельных металлов является следующее: общая закономерность действительно существует, однако физические детали проявляются не вполне гладко.
Для растворимости действует то же предупреждение. Не существует единого правила, применимого ко всем солям второй группы. Гидроксиды становятся более растворимыми при движении вниз по группе, тогда как сульфаты — менее растворимыми. Если кто-то утверждает: «растворимость возрастает вниз по второй группе», важнейшим уточняющим вопросом будет: «растворимость каких соединений?»
Почему щелочноземельные металлы реагируют именно так
Итак, являются ли щелочноземельные металлы реакционноспособными ? Да, и общий ответ заключается в том, что их реакционная способность возрастает при движении вниз по группе. Причина та же — история с электронами, описанная выше. Более низкие значения первой и второй энергий ионизации означают, что атомы могут легче терять два электрона и быстрее достигать характерного для них состояния M 2+.
Это влияет на реальные химические реакции. При движении вниз по группе реакции с разбавленными кислотами ускоряются, реакции с кислородом становятся более бурными, а более тяжёлые элементы легче окисляются. В материалах Save My Exams отмечается, что барий настолько реакционноспособен, что его хранят под слоем масла — это практическое свидетельство того, насколько далеко может простираться эта тенденция изменения реакционной способности.
- Атомный радиус увеличивается при движении вниз по группе 2.
- Энергия ионизации уменьшается при движении вниз по группе 2.
- Реакционная способность возрастает, поскольку потеря двух электронов становится проще.
- Температуры плавления и плотность демонстрируют нерегулярности, поэтому не следует формулировать абсолютные правила.
- Гидроксиды и сульфаты проявляют противоположные тенденции растворимости.
Эти закономерности делают семейство предсказуемым, но отнюдь не абсолютно однородным. Прямо в верхней части группы бериллий уже начинает нарушать общие правила, а магний добавляет ещё одно повседневное исключение, которое имеет большее значение, чем ожидают многие новички.
Щелочные и щелочноземельные металлы
Общие тенденции упрощают изучение группы 2, однако семейство перестаёт быть логичным, если каждый его элемент рассматривать как полностью идентичный остальным. Крупнейшим «тревожным сигналом» является бериллий. Магний добавляет более практичное, повседневно значимое исключение. А когда люди сравнивают щелочные и щелочноземельные металлы , схожие названия могут скрывать весьма различную химию.
Почему бериллий ведёт себя не как типичный металл группы 2
BYJU'S описывает бериллий как очевидный выброс в группе 2. Его необычно малый атомный радиус, высокая энергия ионизации и сильная поляризующая способность обусловливают поведение, менее характерное для этого семейства. Простыми словами, Be 2+сильно притягивает близлежащие электронные облака, поэтому соединения бериллия зачастую носят более ковалентный, а не ионный характер по сравнению с соединениями более тяжёлых элементов этой группы. В том же источнике отмечается, что бериллий обладает более высокими температурами плавления и кипения по сравнению с остальными элементами группы и не реагирует с водой так, как это делают его «собратья».
Магний менее необычен, чем бериллий, однако он всё ещё может показаться менее реакционноспособным, чем ожидают учащиеся. В ресурсе LibreTexts указано, что очень чистый магний реагирует лишь слабо с холодной водой, причём реакция вскоре замедляется из-за образования почти нерастворимого гидроксида магния, который образует защитный барьер на поверхности металла. В нижней части подгруппы радий обычно рассматривается отдельно, поскольку его радиоактивность определяет практическое применение и вопросы безопасности.
Чем щелочноземельные металлы отличаются от щелочных металлов
В простых щелочные против щелочноземельных терминах металлы первой группы теряют один внешний электрон, тогда как металлы второй группы теряют два. Именно это единственное различие определяет свойства щелочных и щелочноземельных металлов в большей степени, чем практически любой другой фактор. более чем почти что-либо другое.
| Особенность | Щелочные металлы, группа 1 | Щелочноземельные металлы, группа 2 |
|---|---|---|
| Валентные электроны | 1 | 2 |
| Типичный ион | М + | М 2+ |
| Реакция с холодной водой | Часто бурная или даже взрывоопасная, с образованием гидроксида и водорода | Менее однородная: бериллий не реагирует с водой, магний реагирует слабо, кальций, стронций и барий реагируют с возрастающей интенсивностью |
| Характерная химия кислорода | Могут образовывать оксиды, пероксиды или супероксиды | Обычно образуют монооксиды; большинство этих оксидов при взаимодействии с водой дают гидроксиды, однако BeO является исключением |
Важные исключения, которые учащиеся часто упускают из виду
- Не все металлы группы 2 реагируют с водой одинаково.
- Соединения бериллия более ковалентны, чем соединения остальных элементов этой группы.
- Не путайте щелочные и щелочноземельные металлы с одной и той же группой только потому, что их названия звучат сходно.
- Трубы свойства щелочных металлов и щелочноземельных металлов лучше всего усваивать как закономерности с исключениями, а не как жёсткие формулировки.
Это также наилучший способ понять химические свойства щелочных металлов и щелочноземельных металлов . Электронные конфигурации задают общее правило, однако реальные вещества придают ему «текстуру». Эта «текстура» становится ещё отчётливее, если рассмотреть, где на самом деле встречаются элементы II группы: крайне редко в виде чистых металлов и значительно чаще — в составе минералов, горных пород, морской воды, костей и промышленных соединений.
Как щелочноземельные металлы встречаются в природе
Если вы представите себе щелочноземельный металл в виде яркого, чистого образца, лежащего в породе, природа действует иначе. Элементы II группы достаточно реакционноспособны, поэтому обычно встречаются в виде ионов внутри минералов, солей, горных пород, морской воды, костей и раковин, а не в виде свободных металлов. Независимо от того, ищет ли кто-то щелочноземельные металлы или более устоявшийся термин, естественная закономерность остаётся той же: эта группа элементов сильно предпочитает существовать в виде соединений.
Эта закономерность напрямую обусловлена химическими свойствами щелочноземельных металлов их атомы склонны терять два внешних электрона и образовывать устойчивые ионы M 2+²⁺. Как только это происходит, ионы кислорода, карбоната, сульфата и галогенов легко связывают их в твёрдые соединения, способные сохраняться в геологических и биологических системах.
Почему щелочноземельные металлы не встречаются в природе в свободном виде
Британика и ThoughtCo оба описывают группу 2 как реакционноспособную, что объясняет, почему эти элементы редко встречаются в свободном виде. На воздухе многие из них быстро образуют оксидные плёнки. В природных условиях они стабилизируются ещё сильнее в виде карбонатов, сульфатов, силикатов, фторидов или хлоридов. Именно поэтому кальций присутствует в известняке и раковинах, магний — в минералах и морской воде, а стронций и барий — в рудных месторождениях. Радий встречается ещё реже и присутствует лишь в следовых количествах в урановых рудах.
Распространённые минералы и соединения группы 2
| Элемент | Распространённый природный источник | Известное соединение | Почему это соединение имеет значение |
|---|---|---|---|
| Бериллий | Берилл | BeO | Берилл является промышленным источником этого элемента, а оксид бериллия представляет собой важное соединение, применяемое в специализированных материалах |
| Магний | Магнезит, доломит, морская вода | MgCO₃ 3или Mg(OH)₂ 2 | Объясняет, почему магний чаще встречается в минералах, морской воде и медицине, чем в виде чистого металла |
| Кальций | Известняк, мел, мрамор, гипс, кости, раковины | Како 3 | Связывает геологию, строительные материалы и скелеты в одном очень распространенном соединении |
| Стронций | Целестин, стронцианит | SrSO 4или SrCO 3 | Эти минералы являются основными природными источниками соединений стронция |
| Барий | Барит, витерит | BaSO 4 | Барит является ключевой рудой, а сульфат бария — одно из самых известных соединений бария |
| Радий | Следовые количества в урановой смоле и других урановых рудах | RaCl 2 | Её редкость и радиоактивность делают соединения радия исторически важными, но малораспространенными |
EBSCO отмечает, что кальций и магний также присутствуют в морской воде в концентрации около 0,4 г/л и 1,3 г/л соответственно. Это помогает объяснить, почему данный щелочноземельный семейство связано не только с рудами, но и с жёсткой водой, морскими системами и живыми тканями.
Как эти металлы выделяются из их соединений
Поскольку металлы II группы обычно находятся в составе соединений, их извлечение начинается с руд, рассолов или минеральных залежей. Общепринятая промышленная стратегия проста: сначала преобразовать исходное сырьё в более удобный для обработки оксид или галогенид, а затем применить электролиз или химическое восстановление для получения свободного металла. В энциклопедии «Британника» описывается раннее получение магния, кальция, стронция и бария методом электролиза, тогда как в источнике EBSCO отмечается, что современное производство по-прежнему часто основывается на электролизе расплавленных хлоридов, восстановлении оксидов или других аналогичных методах — в зависимости от конкретного элемента. Бериллий служит полезным напоминанием о том, что это семейство не является абсолютно однородным: его можно получать путём восстановления фторида бериллия.
Таким образом, в повседневной жизни люди обычно сталкиваются с элементами группы 2 через известняк, гипс, магний из морской воды, барит или биологический кальций, а не через образцы чистых металлов. Этот нюанс имеет значение, поскольку практическая значимость этих элементов в реальном мире определяется в первую очередь их соединениями и формами, а не самими чистыми металлами.
Примеры щелочноземельных металлов в повседневной жизни
Группа 2 становится гораздо более запоминающейся, если связать каждый элемент с конкретным реальным объектом: кости, антациды, гипс, фейерверки, буровые растворы и старые светящиеся циферблаты — всё это полезные примеры. примеры щелочноземельных металлов если вы когда-либо задавались вопросом является ли магний металлом или неметаллом или является ли Ca металлом , ответы просты: магний и кальций — металлы. Однако в обычной жизни люди обычно встречают эти вещества в виде соединений, а не в виде образцов чистых металлов.
Повседневное применение соединений магния и кальция
- Магний : магний является одним из наиболее биологически важных щелочноземельные элементы . Справочный лист Национального института здоровья (NIH) о магнии отмечает, что он является кофактором более чем 300 ферментных систем и поддерживает функции мышц и нервов, выработку энергии и структуру костей. Соединения магния также присутствуют в некоторых антацидах и слабительных средствах, а металлический магний ценится в лёгких сплавах, где важна минимизация массы.
- Кальций соединения кальция доминируют в повседневной жизни. Кальций придаёт костям и зубам их структуру, а такие соединения, как карбонат кальция и сульфат кальция, играют ключевую роль в составе известняка, цемента, штукатурки и гипсокартона. Это делает кальций одним из наиболее наглядных примеров связи между химией, биологией и строительством.
Специализированные применения стронция и бария
- Стронций соли стронция наиболее известны своей способностью придавать пиротехническим изделиям и сигнальным ракетам насыщенный красный цвет. Даже те читатели, которые не помнят полный список элементов II группы, зачастую вспоминают стронций, как только ассоциируют его с цветом.
- Барий соединения бария имеют значение в промышленности и медицине. Профиль бария Национальной медицинской библиотеки (NLM) описывает основные области применения в буровых растворах, красках, пластмассах, кирпичах и стекле. Также отмечается важное медицинское применение: малорастворимый сульфат бария используется в качестве рентгеноконтрастного вещества при некоторых рентгенологических исследованиях, поскольку он, как правило, не всасывается организмом.
- Радий : Радий в основном представляет собой исторический или строго регламентируемый научный случай. Страница НРК (Комиссии по ядерному регулированию США) о радии описывает его прошлые применения в люминесцентных красках и ранней лучевой терапии рака. Большинство из этих применений были заменены, хотя некоторые регламентируемые применения сохраняются до сих пор, например, определённые виды промышленной радиографии.
Почему форма и тип соединения имеют значение на практике
Для элементов II группы форма, используемая на практике, зачастую представляет собой соединение, а не чистый металл.
Эта единственная идея устраняет множество недоразумений. Магний в пище или лекарствах — это не то же самое, что горящая магниевая лента. Кальций в костях — это не то же самое, что реакционноспособный металлический кальций. Барий является наиболее ярким примером того, почему форма вещества имеет решающее значение: нерастворимый сульфат бария может быть полезен при медицинской визуализации, тогда как более растворимые соединения бария требуют значительно большей осторожности. Радий подчёркивает этот тезис ещё сильнее, поскольку его обращение определяется не только принадлежностью к щелочноземельным металлам, но и радиоактивностью.
Таким образом, ценность II группы вовсе не абстрактна. Эти элементы помогают объяснить, как один и тот же семейственный ряд может играть важную роль в питании, материаловедении, медицине, промышленной переработке и правилах техники безопасности. Часто достаточно краткого перечня реальных применений, чтобы устойчиво закрепился общий закономерный паттерн.
Ключевые выводы о элементах II группы
К этому моменту щелочноземельные металлы должны восприниматься не как список для заучивания, а как закономерность, которую можно напрямую прочитать из группы 2 периодической таблицы колонки. Если кто-то всё ещё спрашивает, что такое щелочноземельные металлы , краткий ответ остается простым: бериллий, магний, кальций, стронций, барий и радий. Более полное определение щелочноземельных металлов еще более полезно: шесть металлических элементов второй группы, которые обычно теряют два внешних электрона и образуют ионы M 2+²⁺.
Ключевые выводы о щелочноземельных металлах
- Расположение имеет значение: эти шесть элементов второй группы находятся во втором столбце слева — в разделе «Группа 2» s-блока.
- Состав семьи фиксирован: Be, Mg, Ca, Sr, Ba и Ra составляют всю группу.
- Общая химия объясняет сходство внутри группы: их ns 2валентный характер приводит к образованию катионов +2 как наиболее типичному результату — ключевой вывод, обобщённый в LibreTexts.
- Основные тенденции при движении вниз по группе предсказуемы: атомный радиус увеличивается, энергия ионизации, как правило, уменьшается, а реакционная способность обычно возрастает при движении вниз по группе.
- Исключения имеют значение: бериллий проявляет более ковалентный характер по сравнению с остальными элементами, магний может казаться менее реакционноспособным из-за поверхностного слоя, а радий рассматривается преимущественно с точки зрения его радиоактивности.
- На практике речь обычно идёт о соединениях, а не о чистых металлах: люди сталкиваются с карбонатом кальция, оксидом магния и сульфатом бария значительно чаще, чем с элементарным кальцием, магнием или барием.
Трубы щелочноземельные элементы периодической таблицы столбец проще всего запомнить как шесть металлов, объединённых одним правилом: они обычно образуют ионы с зарядом 2+, однако каждый из них проявляет это правило по-своему.
От химии элементов II группы к инженерным металлическим деталям
Эта химия выходит далеко за пределы учебников. В LibreTexts отмечается, что элементарный магний производится в промышленных масштабах и применяется в лёгких сплавах для изготовления каркасов самолётов и деталей автомобильных двигателей. Более обширное руководство по сплавам показывает, почему это имеет значение: инженеры корректируют состав и технологию обработки, чтобы достичь оптимального баланса между массой, прочностью, коррозионной стойкостью и обрабатываемостью в реальных компонентах.
Для читателей, переходящих от группы 2 периодической таблицы теоретического взгляда к производству, Shaoyi Metal Technology предоставляет практический пример этой связи. На страницах, посвящённых автомобильным материалам и обработке металлов, описывается производство металлических деталей — от прототипирования до массового производства, где поведение материала и контроль технологического процесса должны работать в тесной взаимосвязи. Это делает щелочноземельные элементы периодической таблицы более чем просто учебной схемой. Она также лежит в основе логики выбора металлов и сплавов для инженерных деталей, которым необходимо быть лёгкими, надёжными и пригодными для производства.
Часто задаваемые вопросы об щелочноземельных металлах
1. Какие шесть металлов относятся к группе щелочноземельных?
Шесть щелочноземельных металлов — это бериллий, магний, кальций, стронций, барий и радий. Они расположены во 2-й группе периодической таблицы и объединены в одну группу, поскольку обычно теряют два внешних электрона, что приводит к образованию катионов с зарядом +2 во многих соединениях.
2. Чем щелочноземельные металлы отличаются от щелочных металлов?
Щелочные металлы относятся к группе 1 и обычно образуют катионы с зарядом 1+, поскольку имеют один валентный электрон. Щелочноземельные металлы находятся в группе 2, обычно образуют катионы с зарядом 2+ и в целом проявляют меньшую реакционную способность. Этот один дополнительный валентный электрон влияет на прочность их химических связей, характер взаимодействия с водой, а также типы солей и оксидов, которые они обычно образуют.
3. Почему щелочноземельные металлы не встречаются в природе в свободном виде?
Эти металлы достаточно реакционноспособны, чтобы не сохраняться в чистой элементарной форме в течение длительного времени в естественных условиях. Вместо этого они соединяются с ионами кислорода, карбоната, сульфата, хлорида или силиката и входят в состав минералов, горных пород, морской воды, раковин и костей. Именно поэтому люди, как правило, сталкиваются с элементами группы 2 в виде соединений, а не в виде образцов чистого металла.
4. Реагируют ли все щелочноземельные металлы с водой?
Нет, и это одно из самых полезных исключений, которое следует запомнить. Бериллий в значительной степени устойчив к воздействию воды, магний реагирует медленно с холодной водой из-за поверхностного слоя, ограничивающего реакцию, а кальций, стронций и барий реагируют более активно. В целом реакционная способность с водой усиливается при движении вниз по II группе.
5. Почему щелочноземельные металлы важны в промышленности и производстве?
Их важность обусловлена как их соединениями, так и их ролью при выборе сплавов. Магний ценится там, где имеет значение меньший вес; соединения кальция играют ключевую роль в производстве цемента и штукатурки; соединения бария применяются в специализированных промышленных и медицинских целях. На практике понимание поведения металлов помогает оптимизировать механическую обработку, обеспечивать стабильность технологических процессов и поддерживать высокое качество изделий — именно поэтому такие поставщики, как Shaoyi Metal Technology, делают акцент на сертифицированной обработке деталей для автомобильной промышленности, контроле технологических процессов и комплексной поддержке — от изготовления прототипов до массового производства.
 Малые партии, высокие стандарты. Наша служба быстрого прототипирования делает проверку точнее и проще —
Малые партии, высокие стандарты. Наша служба быстрого прототипирования делает проверку точнее и проще —
