Apa Itu Logam Tanah Alkali? Kelompok 2 Akhirnya Menjadi Jelas
Apa Itu Logam Alkali Tanah?
Jika Anda mencari apa itu logam alkali tanah , berikut adalah jawaban langsungnya: yaitu enam unsur dalam Grup 2 kolom 2 definisi logam alkali tanah ini merupakan titik awal, namun nama tersebut juga memberi banyak petunjuk tentang perilaku kelompok unsur ini.
Apa itu logam alkali tanah dalam satu kalimat
Logam alkali tanah adalah berilium, magnesium, kalsium, stronsium, barium, dan radium, yaitu enam unsur logam dalam Golongan 2 yang umumnya membentuk ion +2.
- Berilium (Be)
- Magnesium (Mg)
- Kalsium (Ca)
- Stronsium (Sr)
- Barium (Ba)
- Radium (Ra)
Mengapa nama logam alkali tanah masuk akal
Bagi pemula, definisi logam alkali tanah menjadi jauh lebih mudah ketika Anda membagi frasa tersebut menjadi tiga bagian.
Alkalin berarti oksida dan hidroksida mereka bersifat basa, bukan asam. Bumi adalah istilah historis. Para kimiawan awal menggunakannya untuk zat-zat tahan panas yang mirip mineral dan tidak mudah meleleh atau larut dalam air, suatu penjelasan yang diuraikan dalam Britannica . Logam berarti unsur-unsur tersebut bersifat logam, umumnya mengilap dan memiliki kecenderungan kuat melepaskan elektron dalam reaksi.
Hal itu memberi Anda dasar makna logam alkali tanah tanpa perlu mempelajari kimia tingkat lanjut terlebih dahulu. Ini juga merupakan deskripsi singkat yang berguna tentang logam alkali tanah : sebuah keluarga logam Golongan 2 dengan sifat kimia yang serupa, posisi bersama di tabel periodik, serta peran besar dalam dunia nyata. Magnesium muncul dalam paduan dan biologi. Kalsium penting bagi tulang, cangkang, dan bahan bangunan. Barium, stronsium, dan radium muncul dalam konteks yang lebih khusus.
Artikel ini sengaja dimulai dari hal yang sederhana. Daftar yang jelas mudah dihafal, tetapi pemahaman sebenarnya tentang keluarga ini baru muncul ketika Anda melihat di mana unsur-unsur ini berada dan mengapa posisi tersebut memberikan sifat yang sangat mirip.
Posisi Golongan 2 di Tabel Periodik
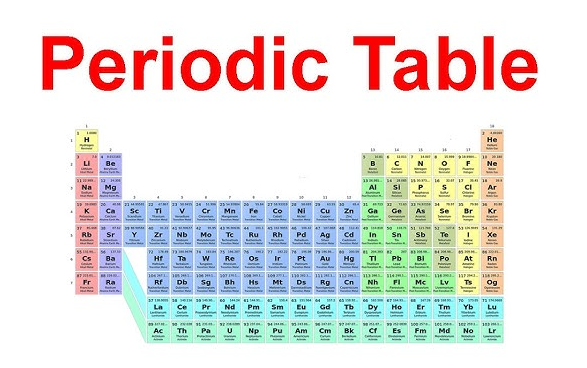
Nama keluarga ini menjadi jauh lebih mudah diingat ketika Anda benar-benar dapat menemukannya. Jika Anda bertanya-tanya di mana logam alkali tanah berada di tabel periodik , lihatlah kolom kedua dari kiri. Kolom vertikal ini adalah golongan 2 di tabel periodik , yang berada tepat di sebelah logam alkali pada Golongan 1. Sebuah golongan 2 tabel periodik tampilan menunjukkan garis lurus yang sama setiap kali: berilium di bagian atas, kemudian magnesium, kalsium, stronsium, barium, dan radium berurutan ke bawah melalui periode-periode tersebut.
Di sebuah tabel periodik logam alkali tanah grafik, keenam unsur ini termasuk dalam blok-s. Lokasi bersama mereka penting karena mencerminkan pola konfigurasi elektron yang sama. Sebagaimana LibreTexts dijelaskan, unsur-unsur golongan 2 memiliki konfigurasi valensi ns 2, yang berarti mereka memiliki dua elektron pada kulit terluar.
Lokasi logam alkali tanah pada tabel periodik
Secara visual, polanya sederhana. unsur-unsur golongan 2 tabel periodik membentuk satu kolom keluarga yang membentang dari periode 2 hingga periode 7. Banyak diagram kelas menyoroti logam alkali tanah dalam tabel periodik tata letak dengan warna yang sama karena keluarga unsur dibaca secara vertikal, bukan horizontal. Pencarian untuk tabel periodik logam alkali tanah benar-benar mengacu pada satu kolom tersebut.
| Elemen | Simbol | Posisi Golongan 2 | Ion khas | Senyawa umum |
|---|---|---|---|---|
| Beryllium | Be | Periode 2, bagian atas Golongan 2 | Be2+ | BeO |
| Magnesium | Mg | Periode 3 | Mg2+ | MgO |
| Kalsium | Ca | Periode 4 | Ca2+ | CaCO 3 |
| Stronsium | Sr | Periode 5 | Sr2+ | SrCO 3 |
| Barium | BA | Periode 6 | BA 2+ | BaSO 4 |
| Radium | RA | Periode 7, bagian bawah Golongan 2 | RA 2+ | RaCl 2 |
Mengapa unsur-unsur Golongan 2 membentuk ion positif dua
Kedua elektron luar tersebut menentukan sifat kimia. Atom-atom Golongan 2 cenderung melepaskan kedua elektron tersebut karena hal itu memberikan susunan elektron yang lebih stabil. Hasilnya adalah sebuah +2 ion , seperti Mg 2+atau Ca 2+. Itulah sebabnya logam-logam ini umumnya membentuk senyawa seperti oksida, klorida, karbonat, dan sulfat. Pola tersebut langsung terlihat dalam rumus kimianya: MgO, CaCl 2, CaCO 3, BaSO 4.
Cara cepat mengenali keluarga logam alkali tanah
Triks identifikasi cepat adalah mencari tiga petunjuk sekaligus: berada di kolom kedua, merupakan unsur logam, dan umumnya memiliki muatan +2. Dibandingkan dengan logam alkali yang bersebelahan, yang memiliki satu elektron valensi dan biasanya membentuk ion +1, unsur-unsur Golongan 2 memiliki satu elektron luar tambahan serta umumnya kurang reaktif. Namun, unsur-unsur ini jelas termasuk dalam satu keluarga yang sama. Bagian yang menarik adalah bahwa masing-masing anggotanya mengekspresikan pola tersebut dengan cara yang sedikit berbeda, khususnya dari berilium di puncak hingga radium di dasar.
Kenalan dengan Enam Logam Alkali Tanah
Daftar memang berguna, tetapi daftar itu sendiri tidak begitu mudah diingat. Kelompok 2 mulai terasa lebih nyata ketika masing-masing anggotanya memiliki identitas yang jelas. Sebagian muncul dalam tulang atau air laut. Sebagian lain memberi warna pada kembang api. Salah satunya terutama berfungsi sebagai tanda peringatan sejarah. Secara bersama-sama, unsur-unsur ini masih termasuk dalam keluarga yang sama, namun masing-masing memiliki kepribadian tersendiri.
| Elemen | Simbol | Kejadian umum | Sifat unggulan | Relevansi Dunia Nyata |
|---|---|---|---|---|
| Beryllium | Be | Ditemukan dalam mineral seperti beril | Sangat ringan dan kaku untuk sebuah logam | Digunakan dalam aplikasi khusus di bidang dirgantara dan sinar-X; debunya berbahaya jika terhirup |
| Magnesium | Mg | Hadis dalam air laut dan mineral | Kepadatan rendah dan menghasilkan nyala api putih terang saat terbakar | Penting dalam paduan ringan, suplemen, dan biologi |
| Kalsium | Ca | Umum ditemukan dalam batu kapur, tulang, cangkang, dan kapur | Ion golongan 2 yang secara biologis familier | Komponen kunci dalam kerangka, semen, plester, dan banyak mineral alami |
| Stronsium | Sr | Ditemukan terutama dalam celestite dan strontianite | Garam-garamnya menghasilkan warna merah mencolok dalam nyala api | Digunakan dalam kembang api, lampu isyarat, bahan bercahaya, dan beberapa produk gigi |
| Barium | BA | Biasanya terkait dengan barit | Logam alkali tanah yang padat dan berat | Barium sulfat penting dalam pengeboran dan pencitraan medis; senyawa barium yang larut memerlukan kehati-hatian |
| Radium | RA | Terjadi dalam jumlah jejak di bijih uranium | Radioaktivitas kuat mendominasi kisah kimianya | Sebagian besar bersifat historis atau memiliki relevansi ilmiah yang sangat terkendali saat ini |
Berilium dan magnesium di bagian atas Golongan 2
The unsur berilium berada di puncak keluarga ini dan sudah menunjukkan bahwa Golongan 2 tidak sepenuhnya seragam. Unsur ini umumnya dikaitkan dengan mineral beril, yaitu keluarga mineral yang sama yang mencakup zamrud dan akwamarin. Berilium menonjol karena memiliki massa jenis yang tidak biasa ringan namun kaku. Hal ini membuatnya berguna dalam komponen berkinerja tinggi di mana massa rendah menjadi faktor penting. Di sisi lain, berilium merupakan bahan yang memerlukan penanganan hati-hati dalam lingkungan industri, karena debu halusnya dapat berbahaya jika terhirup. Oleh sebab itu, berilium dikenang baik karena kinerjanya maupun karena kehati-hatiannya dalam penanganan.
Magnesium terasa jauh lebih akrab. lambang kimia magnesium adalah Mg, dan merupakan salah satu logam paling dikenal dalam golongan ini karena terdapat dalam air laut, mineral umum, serta sistem kehidupan. Magnesium adalah logam yang sangat ringan, dan ketika terbakar menghasilkan cahaya putih yang sangat terang. Itulah sebabnya magnesium telah lama dikaitkan dengan lampu isyarat (flare) dan bahan-bahan yang membakar dengan terang. Namun, dalam kehidupan sehari-hari, kebanyakan orang menjumpainya dalam bentuk yang lebih lembut, seperti perannya dalam nutrisi, senyawa antasid, atau paduan ringan yang digunakan di mana pengurangan massa menjadi penting.
Kalsium dan stronsium dalam bahan-bahan sehari-hari
Kalsium merupakan anggota Golongan 2 yang paling dikenal oleh banyak pembaca. Unsur ini terdapat dalam batu gamping, kapur, cangkang, dan tulang, sehingga menghubungkan kimia dengan geologi maupun biologi secara langsung. Senyawa kalsium karbonat merupakan senyawa yang akrab dalam konteks ini. Senyawa tersebut membantu menjelaskan mengapa keluarga unsur yang sama berperan penting dalam pembentukan gua, batuan bangunan, dan kerangka. Logam kalsium itu sendiri bersifat reaktif, namun senyawa kalsium tersebar luas di mana-mana, itulah sebabnya unsur ini sering terasa lebih akrab daripada eksotis.
Stronsium lebih mudah diingat setelah Anda mengaitkannya dengan warna. lambang stronsium adalah Sr, dan stronsium ditemukan terutama dalam mineral celestite dan strontianite. Royal Society of Chemistry menggambarkannya sebagai logam keperakan yang lunak dan terbakar di udara serta bereaksi dengan air. Garam-garamnya terkenal menghasilkan warna merah terang dalam kembang api dan lampu isyarat. Sumber yang sama juga mencatat penggunaannya dalam bahan bercahaya dalam gelap serta strontium chloride hexahydrate dalam pasta gigi untuk gigi sensitif. Hal ini menjadikan stronsium contoh yang sangat baik tentang bagaimana suatu unsur dapat bersifat reaktif secara kimia namun kebanyakan dijumpai melalui senyawanya.
Barium dan radium dalam konteks lanjutan atau khusus
The unsur barium sering diingat melalui beratnya. Unsur ini umumnya dikaitkan dengan barit, dan salah satu senyawa paling dikenalnya adalah barium sulfat. Senyawa tersebut penting karena sangat tidak larut, yang membantu menjelaskan mengapa barium dapat muncul dalam penerapan praktis seperti cairan pengeboran dan pencitraan medis, sedangkan senyawa barium lain yang larut ditangani lebih hati-hati karena kekhawatiran akan toksisitasnya. Barium mengingatkan pembaca bahwa bentuk berguna dari unsur Golongan 2 sering kali berupa senyawa, bukan logam mengilapnya sendiri.
Radium berada di dasar kelompok ini, tetapi tidak berbaur secara diam-diam. Pada tabel periodik radium tampilan, Ra menandai titik di mana radioaktivitas menjadi ciri khas utama. Radium terjadi secara alami hanya dalam jumlah sangat kecil, biasanya terkait dengan bijih uranium. Secara historis, unsur ini menjadi terkenal karena cat berpendar dan eksperimen medis awal. Saat ini, bahayanya berasal dari sifat radioaktifnya, bukan dari perilaku logam biasa, sehingga penanganannya dilakukan di bawah pengawasan ketat. Secara sederhana, radium tetap termasuk dalam Golongan 2, namun pembahasannya lebih mempertimbangkan aspek keselamatan nuklir sebanyak hal-hal kimia.
Susun keenam unsur ini berdampingan, dan keluarga ini tidak lagi tampak seperti daftar nama kosong. Ukuran, kereaktifan, senyawa umum, serta bahkan cara masing-masing unsur muncul dalam kehidupan nyata berubah saat Anda bergerak ke bawah. Pola perubahan inilah yang membuat Golongan 2 menjadi khusus berguna, karena urutan dari berilium hingga radium mulai mengungkap tren, bukan sekadar fakta-fakta tak berarti.
Sifat Logam Tanah Alkali dan Tren Golongan 2
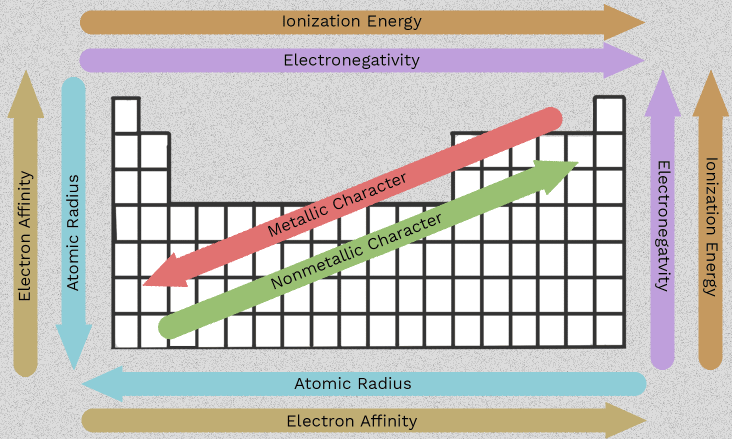
Urutan perubahan dari berilium hingga radium itulah yang membuat Golongan 2 menjadi berguna. Alih-alih menghafal enam fakta terpisah, Anda dapat mengikuti sejumlah pola yang berulang di sepanjang kolom tersebut. Yang paling penting sifat logam alkali tanah semuanya berasal dari satu ciri bersama: setiap atom memiliki dua elektron di kulit terluarnya yang cenderung dilepaskan.
Begitu Anda memahami bagaimana ukuran atom, pelindungan elektron, dan energi ionisasi berubah ke bawah sepanjang golongan, keluarga unsur ini menjadi jauh lebih mudah diprediksi. Sifat-sifat ini karakteristik logam alkali tanah bukan sekadar fakta untuk ujian. Sifat-sifat ini menjelaskan mengapa beberapa anggotanya bereaksi lebih cepat, mengapa beberapa senyawa lebih mudah larut dibandingkan yang lain, serta mengapa beberapa tren memerlukan perumusan yang cermat—bukan sekadar panah sederhana.
Sifat-sifat bersama logam alkali tanah
Sebagian besar anggota Golongan 2 adalah logam keperakan yang biasanya membentuk M 2+ion dan membentuk senyawa ionik terutama. Mereka berperilaku sebagai agen pereduksi karena melepaskan elektron. Dibandingkan dengan logam Golongan 1, secara umum mereka kurang reaktif, namun tetap cukup aktif secara kimia untuk membentuk banyak oksida, klorida, karbonat, dan sulfat umum.
Cara sederhana untuk mengorganisasi sifat-sifat kimia logam alkali tanah adalah dengan membedakan antara apa yang tetap konstan dan apa yang berubah. Yang tetap konstan adalah keadaan oksidasi biasa +2. Yang berubah adalah seberapa mudah masing-masing unsur melepaskan dua elektron tersebut. Di sinilah tren mulai penting.
Tren ke bawah Golongan 2 dan maknanya
Data yang dikumpulkan oleh LibreTexts serta penjelasan tren dari Save My Exams menunjukkan pola keseluruhan yang sama. Jari-jari atom meningkat dari 112 pm untuk Be menjadi 253 pm untuk Ba, sedangkan energi ionisasi pertama menurun dari 900 menjadi 503 kJ/mol. Dalam bahasa awam, elektron terluar berada semakin jauh dari inti dan terlindungi oleh lebih banyak kulit dalam, sehingga lebih mudah dilepaskan.
| Tren | Arah ke bawah Golongan 2 | Alasan kimia | Apa Arti Ini dalam Praktik |
|---|---|---|---|
| Jari-jari atom | Meningkatkan | Setiap unsur memiliki satu kulit elektron tambahan dan lebih banyak pelindungan | Atom yang lebih besar mengikat elektron luar dengan kekuatan lebih rendah |
| Energi ionisasi pertama dan kedua | Menurun secara keseluruhan | Elektron luar berada lebih jauh dari inti, sehingga gaya tarik lebih lemah | Pembentukan M 2+ion menjadi lebih mudah |
| Reaktifitas | Meningkat secara keseluruhan | Energi ionisasi yang lebih rendah memudahkan kehilangan elektron | Unsur-unsur yang lebih berat bereaksi lebih kuat dengan asam, oksigen, dan sering kali juga dengan air |
| Titik leleh | Umumnya menurun, tetapi tidak secara mulus | Ion logam yang lebih besar melemahkan ikatan logam, meskipun struktur juga berperan | Gunakan kata "umum" di sini, karena Mg dan Ca tidak mengikuti garis yang sempurna |
| Kepadatan | Tidak teratur | Massa, ukuran atom, dan pengemasan logam semuanya berubah bersamaan | Anda tidak dapat memperlakukan densitas sebagai satu tren penurunan sederhana |
| Kelarutan hidroksida | Meningkatkan | Keseimbangan antara energi kisi dan energi hidrasi bergeser ke bawah golongan | Hidroksida yang lebih berat menghasilkan larutan yang lebih basa |
| Kelarutan sulfat | Berkurang | Energi hidrasi menurun seiring bertambahnya ukuran kation | Senyawa seperti BaSO 4menjadi sangat tidak larut |
Kerapatan dan perilaku peleburan merupakan dua tren yang sering disederhanakan secara berlebihan oleh siswa. Kerapatan tidak berubah secara linier karena baik massa maupun volume mengalami perubahan, dan atom logam tidak memiliki cara pengemasan yang sama di setiap kristal. Titik lebur juga memerlukan perhatian khusus. Secara umum, titik lebur cenderung menurun karena ion yang lebih besar melemahkan kisi logam, namun Mg memiliki titik lebur yang tidak biasa rendah, yaitu 650 °C, sedangkan Ca naik menjadi 842 °C sebelum nilai-nilai tersebut kembali turun. Jadi, salah satu sifat paling andal logam alkali tanah adalah ini: pola umum memang nyata, tetapi detail fisiknya tidak sepenuhnya mulus.
Kelarutan memiliki peringatan yang sama. Tidak ada satu aturan tunggal yang berlaku untuk semua garam Golongan 2. Hidroksida menjadi semakin larut ke bawah golongan, sedangkan sulfat menjadi semakin tidak larut. Jika seseorang mengatakan "kelarutan meningkat ke bawah Golongan 2", pertanyaan penting yang harus diajukan adalah, "Senyawa mana yang dimaksud?"
Mengapa logam alkali tanah bereaksi seperti yang mereka lakukan
Jadi, apakah logam alkali tanah reaktif ? Ya, dan jawaban umumnya adalah bahwa kereaktifan mereka meningkat saat bergerak ke bawah. Alasannya sama dengan kisah elektron yang dijelaskan di atas. Energi ionisasi pertama dan kedua yang lebih rendah berarti atom-atom tersebut dapat kehilangan dua elektron lebih mudah dan mencapai keadaan umum M 2+lebih cepat.
Hal ini memengaruhi reaksi nyata. Sepanjang golongan, reaksi dengan asam encer menjadi lebih cepat, reaksi dengan oksigen menjadi lebih hebat, dan anggota yang lebih berat lebih mudah teroksidasi. Catatan Save My Exams menyebutkan bahwa barium cukup reaktif sehingga harus disimpan di bawah minyak, yang merupakan tanda praktis sejauh mana tren kereaktifan ini dapat berlangsung.
- Jari-jari atom meningkat ke bawah Golongan 2.
- Energi ionisasi menurun ke bawah Golongan 2.
- Kereaktifan meningkat karena kehilangan dua elektron menjadi lebih mudah.
- Titik leleh dan densitas menunjukkan ketidakteraturan, sehingga hindari aturan mutlak.
- Hidroksida dan sulfat menunjukkan tren kelarutan yang berlawanan.
Pola-pola tersebut membuat keluarga unsur ini dapat diprediksi, namun tidak sepenuhnya seragam. Tepat di dekat puncak kelompok ini, berilium sudah mulai melanggar aturan-aturan tersebut, dan magnesium menambahkan pengecualian sehari-hari lainnya yang lebih signifikan daripada yang diperkirakan banyak pemula.
Logam alkali dan logam alkali tanah
Tren umum memudahkan pembelajaran Kelompok 2, tetapi keluarga unsur ini kehilangan maknanya jika setiap anggotanya diperlakukan secara identik. Tanda peringatan terbesar adalah berilium. Magnesium menambahkan pengecualian sehari-hari yang lebih praktis. Dan ketika orang membandingkan logam alkali dan logam alkali tanah , nama-nama yang mirip dapat menyamarkan beberapa perbedaan kimia yang sangat mendasar.
Mengapa berilium tidak berperilaku seperti logam Kelompok 2 pada umumnya
BYJU'S menggambarkan berilium sebagai penyimpangan jelas dalam Kelompok 2. Ukurannya yang tidak biasa kecil, energi ionisasinya yang tinggi, serta daya polarisasinya yang kuat memberikan sifat-sifat yang kurang khas dibandingkan anggota keluarga ini. Dengan kata sederhana, Be 2+menarik secara kuat awan elektron di sekitarnya, sehingga senyawa berilium sering lebih kovalen dibandingkan senyawa yang lebih ionik yang terbentuk oleh anggota kelompok yang lebih berat. Sumber yang sama juga mencatat bahwa berilium memiliki titik leleh dan titik didih yang lebih tinggi dibandingkan anggota kelompok lainnya serta tidak bereaksi dengan air seperti kerabatnya.
Magnesium tidak seaneh berilium, tetapi tetap tampak kurang reaktif dibandingkan yang diperkirakan siswa. LibreTexts mencatat bahwa magnesium yang sangat bersih hanya bereaksi ringan dengan air dingin, dan reaksi tersebut segera melambat karena magnesium hidroksida yang hampir tidak larut membentuk penghalang di permukaan. Di bagian bawah kelompok ini, radium biasanya dibahas secara terpisah karena sifat radioaktifnya mendominasi pembahasan penerapan praktis dan keselamatan.
Perbedaan logam alkali tanah dengan logam alkali
Secara sederhana alkali vs alkali tanah logam Golongan 1 kehilangan satu elektron luar, sedangkan logam Golongan 2 kehilangan dua elektron. Perbedaan tunggal ini membentuk sifat-sifat logam alkali dan logam alkali tanah lebih daripada hampir semua faktor lain.
| Fitur | Logam alkali, Golongan 1 | Logam alkali tanah, Golongan 2 |
|---|---|---|
| Valensi aluminium | 1 | 2 |
| Ion khas | M + | M 2+ |
| Reaksi dengan air dingin | Sering kali kuat atau bahkan hebat, menghasilkan hidroksida dan hidrogen | Kurang seragam: Be tidak bereaksi dengan air, Mg bereaksi secara ringan, sedangkan Ca, Sr, dan Ba bereaksi dengan intensitas yang meningkat |
| Kimia oksigen umum | Dapat membentuk oksida, peroksida, atau superoksida | Umumnya membentuk monoksida; sebagian besar oksida ini menghasilkan hidroksida ketika bereaksi dengan air, tetapi BeO merupakan pengecualian |
Pengecualian penting yang sering terlewat oleh siswa
- Tidak semua logam Golongan 2 bereaksi dengan air dengan cara yang sama.
- Senyawa berilium lebih bersifat kovalen dibandingkan anggota keluarga lainnya.
- Jangan keliru logam alkali dan logam alkali tanah sebagai satu golongan yang sama hanya karena namanya terdengar terkait.
- The sifat-sifat logam alkali dan logam alkali tanah paling baik dipelajari sebagai pola-pola dengan pengecualian, bukan sebagai jargon-jargon kaku.
Itu juga merupakan cara terbaik untuk memahami sifat-sifat kimia logam alkali dan logam alkali tanah . Pola elektron memberi Anda aturannya, tetapi zat-zat nyata menambahkan dimensi tekstur. Dan tekstur tersebut menjadi semakin jelas ketika Anda memperhatikan keberadaan sebenarnya unsur-unsur Golongan 2 di alam: sangat jarang dalam bentuk logam murni, dan jauh lebih sering terdapat di dalam mineral, batuan, air laut, tulang, serta senyawa industri.
Keterjadian Logam Alkali Tanah di Alam
Jika Anda membayangkan sebuah logam alkali tanah sebagai sampel yang cerah dan murni tergeletak di dalam batuan, alam bekerja dengan cara yang berbeda. Unsur-unsur Golongan 2 cukup reaktif sehingga biasanya muncul sebagai ion di dalam mineral, garam, batuan, air laut, tulang, dan cangkang—bukan sebagai logam bebas. Baik seseorang mencari istilah logam alkali tanah atau istilah yang lebih baku, pola alami tetap sama: keluarga unsur ini sangat menyukai senyawa.
Pola tersebut muncul langsung dari sifat kimia logam alkali tanah . Unsur-unsur ini cenderung melepaskan dua elektron terluar dan membentuk ion M 2+yang stabil. Setelah hal ini terjadi, ion oksigen, karbonat, sulfat, dan halida dengan mudah mengikatnya menjadi senyawa padat yang dapat bertahan dalam geologi maupun biologi.
Mengapa logam alkali tanah tidak ditemukan secara bebas di alam
Britannica dan ThoughtCo keduanya menggambarkan Golongan 2 sebagai reaktif, yang menjelaskan mengapa unsur-unsur ini jarang ditemukan dalam bentuk bebas. Di udara, banyak di antaranya dengan cepat membentuk lapisan oksida. Di lingkungan alami, unsur-unsur ini menjadi lebih stabil lagi sebagai karbonat, sulfat, silikat, fluorida, atau klorida. Oleh karena itu, kalsium ditemukan dalam batu kapur dan cangkang, magnesium dalam mineral dan air laut, serta stronsium atau barium dalam endapan bijih. Radium jauh lebih langka lagi, hanya terdapat dalam jumlah jejak di bijih uranium.
Mineral dan senyawa umum Golongan 2
| Elemen | Sumber alami umum | Senyawa umum | Mengapa senyawa tersebut penting |
|---|---|---|---|
| Beryllium | Beryl | BeO | Beryl merupakan sumber komersial unsur tersebut, sedangkan oksida berilium merupakan senyawa penting dalam bahan khusus |
| Magnesium | Magnesit, dolomit, air laut | MgCO₃ 3atau Mg(OH)₂ 2 | Menunjukkan mengapa magnesium lebih sering ditemui dalam mineral, air laut, dan obat-obatan dibandingkan dalam bentuk logam murni |
| Kalsium | Batu kapur, kapur, marmer, gips, tulang, cangkang | CaCO 3 | Menghubungkan geologi, bahan bangunan, dan kerangka dalam satu senyawa yang sangat umum |
| Stronsium | Celestit, stronsianit | SrSO 4atau SrCO 3 | Mineral-mineral ini merupakan sumber alami utama senyawa stronsium |
| Barium | Barit, witerit | BaSO 4 | Barit adalah bijih utama, dan barium sulfat merupakan salah satu senyawa barium yang paling dikenal |
| Radium | Jumlah jejak dalam pitchblende dan bijih uranium lainnya | RaCl 2 | Kelangkaan dan sifat radioaktifnya membuat senyawa radium secara historis penting namun jarang ditemukan |
EBSCO mencatat bahwa kalsium dan magnesium juga terdapat dalam air laut masing-masing sekitar 0,4 g/L dan 1,3 g/L. Hal ini membantu menjelaskan mengapa logam alkali tanah kelompok ini tidak hanya terkait dengan bijih, tetapi juga dengan air sadah, sistem kelautan, dan jaringan hidup.
Cara logam-logam ini diisolasi dari senyawa-senyawanya
Karena logam Golongan 2 umumnya terikat dalam senyawa, proses ekstraksi dimulai dari bijih, air payau, atau endapan mineral. Prinsip industri umum yang diterapkan cukup sederhana: pertama-tama mengubah bahan menjadi oksida atau halida yang lebih mudah diolah, kemudian menggunakan elektrolisis atau reduksi kimia untuk membebaskan logamnya. Britannica menjelaskan bahwa isolasi awal magnesium, kalsium, stronsium, dan barium dilakukan melalui elektrolisis, sedangkan EBSCO mencatat bahwa produksi modern saat ini masih sering mengandalkan klorida lebur, reduksi oksida, atau jalur terkait lainnya, tergantung pada unsur yang bersangkutan. Berilium merupakan pengingat penting bahwa kelompok ini tidak sepenuhnya seragam, karena berilium dapat diproduksi melalui reduksi berilium fluorida.
Jadi, dalam kehidupan sehari-hari, orang biasanya menjumpai Golongan 2 melalui batu kapur, plester, magnesium dari air laut, barit, atau kalsium biologis, bukan melalui sampel logam murni. Detail ini penting, karena relevansi unsur-unsur ini dalam dunia nyata jauh lebih terkait dengan senyawa dan bentuknya daripada dengan logam murninya sendiri.
Contoh Logam Alkali Tanah dalam Kehidupan Sehari-hari
Golongan 2 menjadi jauh lebih mudah diingat ketika Anda mengaitkan setiap unsurnya dengan sesuatu yang nyata. Tulang, obat antasida, plester, kembang api, cairan pengeboran, dan dial bercahaya lama semuanya merupakan contoh yang berguna contoh logam alkali tanah . Jika Anda pernah bertanya-tanya apakah magnesium logam atau bukan logam atau apakah Ca logam , kedua jawabannya sederhana: magnesium dan kalsium adalah logam. Namun, dalam kehidupan sehari-hari, orang biasanya menjumpai zat-zat ini dalam bentuk senyawanya, bukan sebagai sampel logam murni.
Penggunaan sehari-hari senyawa magnesium dan kalsium
- Magnesium : Magnesium merupakan salah satu unsur yang paling penting secara biologis unsur tanah alkali . Lembar Fakta Magnesium NIH menyebutkan bahwa magnesium berperan sebagai kofaktor dalam lebih dari 300 sistem enzim serta mendukung fungsi otot dan saraf, produksi energi, dan struktur tulang. Senyawa magnesium juga terdapat dalam beberapa antasida dan pencahar, sedangkan logam magnesium dihargai dalam paduan ringan di mana pengurangan massa menjadi pertimbangan penting.
- Kalsium senyawa kalsium mendominasi kehidupan sehari-hari. Kalsium membantu memberikan struktur pada tulang dan gigi, dan senyawa seperti kalsium karbonat serta kalsium sulfat merupakan komponen utama batu kapur, semen, plester, dan drywall. Hal ini menjadikan kalsium salah satu hubungan paling jelas antara kimia, biologi, dan konstruksi.
Aplikasi khusus stronsium dan barium
- Stronsium garam stronsium paling dikenal karena menghasilkan warna merah tua dalam kembang api dan lampu isyarat. Bahkan pembaca yang tidak mengingat seluruh daftar Golongan 2 sering kali tetap mengingat stronsium begitu warna dikaitkan dengannya.
- Barium senyawa barium penting dalam industri dan kedokteran. Profil Barium NLM menggambarkan penggunaan utama dalam lumpur pengeboran, cat, plastik, batu bata, dan kaca. Teks ini juga mencatat kontras medis penting: barium sulfat yang sangat tidak larut digunakan sebagai bahan radiopak dalam beberapa pemeriksaan sinar-X karena umumnya tidak diserap oleh tubuh.
- Radium : Radium sebagian besar merupakan kasus historis atau ilmiah yang dikendalikan secara ketat. Halaman radium NRC menggambarkan penggunaan masa lalunya dalam cat berpendar dan terapi kanker awal. Sebagian besar penggunaan tersebut telah digantikan, meskipun beberapa penggunaan yang diatur masih ada, seperti penerapan radiografi industri tertentu.
Mengapa bentuk dan jenis senyawa penting dalam penggunaan nyata
Dengan Golongan 2, bentuk yang digunakan orang sering kali adalah senyawanya, bukan logam murninya.
Gagasan tunggal itu menghilangkan banyak kebingungan. Magnesium dalam makanan atau obat tidak sama dengan magnesium pita yang terbakar. Kalsium dalam tulang tidak sama dengan logam kalsium reaktif. Barium merupakan contoh paling jelas mengapa bentuk zat sangat penting: barium sulfat yang tidak larut dapat bermanfaat dalam pencitraan medis, sedangkan senyawa barium yang lebih larut memerlukan kehati-hatian jauh lebih besar. Radium memperkuat argumen ini bahkan lebih jauh, karena sifat radioaktifnya—bukan hanya posisinya di antara logam—yang menentukan cara penanganannya.
Jadi, nilai Golongan 2 sama sekali tidak abstrak. Unsur-unsur ini membantu menjelaskan bagaimana satu golongan yang sama dapat berperan penting dalam nutrisi, bahan material, kedokteran, pengolahan industri, serta aturan keselamatan. Daftar singkat penggunaan nyata sering kali cukup untuk membuat pola besar ini mudah diingat.
Poin-Poin Utama Mengenai Unsur Golongan 2
Pada tahap ini, logam alkali tanah seharusnya terasa kurang seperti daftar yang harus dihafal dan lebih seperti suatu pola yang dapat Anda baca langsung dari golongan 2 pada tabel periodik kolom tersebut. Jika seseorang masih bertanya, apa itu logam alkali tanah , jawaban singkatnya tetap sederhana: berilium, magnesium, kalsium, stronsium, barium, dan radium. Definisi yang lebih lengkap logam alkali tanah bahkan lebih bermanfaat: enam unsur logam dalam Golongan 2 yang biasanya kehilangan dua elektron terluar dan membentuk ion M 2+²⁺.
Poin penting mengenai logam alkali tanah
- Lokasi penting: keenam unsur Golongan 2 berada di kolom kedua dari kiri, yaitu bagian Golongan 2 dalam blok-s.
- Anggota keluarga ini bersifat tetap: Be, Mg, Ca, Sr, Ba, dan Ra membentuk keseluruhan himpunan tersebut.
- Kesamaan sifat kimia menjelaskan kemiripan antaranggota keluarga: konfigurasi elektron ns-nya 2pola valensi menghasilkan ion bermuatan +2 sebagai hasil yang umum, suatu poin inti yang dirangkum oleh LibreTexts.
- Tren utama ke arah bawah bersifat dapat diprediksi: jari-jari atom meningkat, energi ionisasi umumnya menurun, dan reaktivitas biasanya meningkat seiring pergerakan ke bawah golongan.
- Pengecualian-pengecualian ini penting: berilium berperilaku lebih kovalen dibandingkan unsur lainnya, magnesium dapat tampak kurang reaktif karena lapisan permukaannya, dan radium umumnya dibahas melalui sifat radioaktivitasnya.
- Dalam kehidupan nyata, yang umumnya dimaksud adalah senyawa, bukan logam murni: orang lebih sering menjumpai kalsium karbonat, magnesium oksida, dan barium sulfat dibandingkan unsur Ca, Mg, atau Ba secara murni.
The tabel periodik logam alkali tanah kolom ini paling mudah diingat sebagai enam logam yang dihubungkan oleh satu aturan: umumnya membentuk ion 2+, tetapi masing-masing anggotanya menerapkan aturan tersebut dengan cara yang sedikit berbeda.
Dari kimia Golongan 2 hingga komponen logam rekayasa
Kimia tersebut meluas jauh di luar buku teks. LibreTexts mencatat bahwa magnesium unsur diproduksi dalam skala besar dan digunakan dalam paduan ringan untuk rangka pesawat terbang serta komponen mesin mobil. Panduan paduan yang lebih luas menunjukkan mengapa hal ini penting: insinyur menyesuaikan komposisi dan proses pengolahan untuk menyeimbangkan bobot, kekuatan, ketahanan korosi, dan kemampuan mesin pada komponen nyata.
Untuk pembaca yang beralih dari golongan 2 pada tabel periodik tampilan ke manufaktur, Shaoyi Metal Technology menawarkan contoh praktis dari hubungan tersebut. Halaman bahan otomotif dan pemesinan menjelaskan produksi komponen logam, mulai dari pembuatan prototipe hingga produksi massal, di mana perilaku bahan dan pengendalian proses harus bekerja secara bersamaan. Hal ini menjadikan tabel periodik logam alkali tanah lebih dari sekadar diagram kelas. Ini juga merupakan bagian dari logika dalam memilih logam dan paduan untuk komponen rekayasa yang perlu ringan, andal, serta dapat diproduksi secara efisien.
FAQ Mengenai Logam Tanah Alkali
1. Apa saja enam logam tanah alkali?
Enam logam tanah alkali adalah berilium, magnesium, kalsium, stronsium, barium, dan radium. Unsur-unsur ini menempati Golongan 2 dalam tabel periodik dan dikelompokkan bersama karena umumnya kehilangan dua elektron terluar, sehingga menghasilkan pola ion 2+ yang umum dalam banyak senyawa.
2. Bagaimana perbedaan logam tanah alkali dengan logam alkali?
Logam alkali termasuk dalam Golongan 1 dan biasanya membentuk ion 1+ karena memiliki satu elektron di kulit terluar. Logam alkali tanah berada dalam Golongan 2, umumnya membentuk ion 2+, serta cenderung kurang reaktif secara keseluruhan. Satu elektron valensi tambahan tersebut mengubah kekuatan ikatan yang mereka bentuk, cara mereka bereaksi dengan air, serta jenis garam dan oksida yang biasa mereka hasilkan.
3. Mengapa logam alkali tanah tidak ditemukan dalam bentuk bebas di alam?
Logam-logam ini cukup reaktif sehingga biasanya tidak bertahan lama dalam bentuk unsur murni di lingkungan alami. Sebagai gantinya, mereka bergabung dengan ion oksigen, karbonat, sulfat, klorida, atau silikat dan menjadi bagian dari mineral, batuan, air laut, cangkang, serta tulang. Oleh karena itu, orang umumnya menjumpai Golongan 2 melalui senyawa-senyawanya, bukan dalam bentuk logam murni.
4. Apakah semua logam alkali tanah bereaksi dengan air?
Tidak, dan ini merupakan salah satu pengecualian paling berguna yang perlu diingat. Berilium sebagian besar tahan terhadap air, magnesium bereaksi lambat dalam air dingin karena lapisan permukaan membatasi reaksi tersebut, sedangkan kalsium, stronsium, dan barium bereaksi lebih mudah. Secara umum, kereaktifan terhadap air menjadi semakin kuat seiring bergerak ke bawah Golongan 2.
5. Mengapa logam alkali tanah penting dalam industri dan manufaktur?
Pentingnya logam-logam ini berasal dari senyawa-senyawanya serta perannya dalam pemilihan paduan. Magnesium bernilai tinggi di aplikasi yang memerlukan bobot lebih ringan, senyawa kalsium merupakan komponen utama dalam semen dan plester, sedangkan senyawa barium dipilih untuk keperluan industri dan medis khusus. Dalam produksi nyata, pemahaman terhadap perilaku logam membantu mengarahkan proses pemesinan, stabilitas proses, dan kualitas komponen—oleh karena itu, pemasok seperti Shaoyi Metal Technology menekankan pemesinan otomotif bersertifikat, pengendalian proses, serta dukungan mulai dari komponen prototipe hingga produksi massal.
 Produksi dalam jumlah kecil, standar tinggi. Layanan prototipisasi cepat kami membuat validasi lebih cepat dan mudah —
Produksi dalam jumlah kecil, standar tinggi. Layanan prototipisasi cepat kami membuat validasi lebih cepat dan mudah —
