Mi az alkalik földfémek? A 2. csoport végre érthetővé válik
Mi az alkalik földfémek?
Ha a következő kifejezésre kerestél mi az alkalik földfémek , itt a közvetlen válasz: ezek a periódusos rendszer Csoport 2 csoportjában található hat elem. Ez a rövid az alkalik földfémek meghatározása a kiindulási pont, de a név szintén sokat elárul arról, hogyan viselkedik ez a csoport.
Mi az alkalik földfémek egy mondatban?
Az alkalik földfémek a berillium, a magnézium, a kalcium, a stroncium, a bárium és a rádium, azaz a 2. csoport hat fémes eleme, amelyek általában +2 töltésű ionokat képeznek.
- Beryllium (Be)
- Magnézium (Mg)
- Kalcium (Ca)
- Stroncium (Sr)
- Bárium (Ba)
- Rádium (Ra)
Miért értelmes az „alkáliföldfémek” elnevezés
Kezdőknek a alkáliföldfémek definíciója sokkal könnyebben érthetővé válik, ha a kifejezést három részre bontjuk.
Alkális ez azt jelenti, hogy oxidjaik és hidroxidjaik bázisosak, nem savasak. Földön ez egy történeti kifejezés. A korai vegyészek ezt a kifejezést olyan hőálló, ásvány-szerű anyagokra használták, amelyek nem olvadtak vagy oldódtak könnyen vízben, amit a Britannica . Fémek azt jelenti, hogy maguk az elemek fémek, általában fényesek, és jól veszítik el elektronjaikat reakciókban.
Ez adja a alapvető alkáliföldfémek jelentését anélkül, hogy először összetett kémiai ismeretekre lenne szükség. Egy hasznos rövid leírás az alkáliföldfémekről : egy 2. csoportba tartozó fémcsalád, amelynek közös a kémiai viselkedése, közös helye van a periódusos rendszerben, és jelentős szerepe van a valós világban. A magnézium ötvözetekben és a biológiában fordul elő. A kalcium fontos a csontokban, a héjakban és az építőanyagokban. A bárium, a stroncium és a rádium speciálisabb alkalmazási területeken jelennek meg.
Ez a cikk szándékosan egyszerűen kezdődik. Egy áttekinthető lista könnyen megjegyezhető, de a család igazán érthetővé válik, ha látható, hol helyezkednek el ezek az elemek, és miért adja e helyzetük olyan hasonló viselkedést.
A 2. csoport helye a periódusos rendszerben
A család neve sokkal könnyebben megjegyezhető, ha ténylegesen felismerhető a helye. Ha azt kérdezi magától hol találhatók az alkáliföldfémek a periódusos rendszerben , nézze meg a bal oldali második oszlopot. Ez a függőleges oszlop a periódusos rendszer 2. csoportja , amely közvetlenül mellette helyezkedik el az 1. csoportban található alkáli fémekkel. A 2. csoport – periódusos rendszer a nézet minden alkalommal ugyanazt az egyenes vonalat mutatja: a berillium a tetején, majd lefelé haladva magnézium, kalcium, stroncium, bárium és rádium az egyes periódusokban.
Egy lúgföldfémek – periódusos rendszer ábrán ezek a hat elem az s-mezőhöz tartoznak. Közös helyzetük fontos, mert egy közös elektronszerkezetet tükröz. Ahogyan LibreTexts magyarázza, a 2. csoport elemeinek vegyértékelektron-konfigurációja ns 2, azaz két külső héjon lévő elektronjuk van.
Hol találhatók a lúgföldfémek a periódusos rendszerben
Látványosan egyszerű a minta. A periódusos rendszer 2. csoportjának elemei egy családos oszlopot alkotnak a 2–7. periódusokban. Sok tantermi ábra kiemeli a alkáliföldfémek a periódusos rendszerben elrendezések ugyanazzal a színnel, mert az elemcsaládokat függőlegesen, nem vízszintesen olvassák. Keresések: periódusos rendszer alkáliföldfémek valójában ezt az egy oszlopot keresik.
| Elemens | Szimbólum | 2. csoport helyzete | Tipikus ion | Ismert vegyület |
|---|---|---|---|---|
| Berillium | Be | 2. periódus, a 2. csoport teteje | Be2+ | BeO |
| Magnesium | Mg | 3. periódus | Mg2+ | MgO |
| Kalcium | Ca | 4. időszak | Ca2+ | CaCO 3 |
| Stroncium | Sr | 5. időszak | Sr2+ | SrCO 3 |
| Bárium | BA | 6. időszak | BA 2+ | BaSO 4 |
| Rádium | RA | 7. időszak, a 2. csoport alja | RA 2+ | RaCl 2 |
A 2. csoport elemeinek miért képeznek két pozitív töltésű ionokat
Azok a két külső elektron határozzák meg a kémiai viselkedést. A 2. csoport atomjai hajlamosak mindkét elektront elveszíteni, mert ez stabilabb elektronszerkezetet eredményez. Az eredmény egy +2 ion , például Mg 2+vagy Ca 2+. Ezért ezek a fémek gyakran olyan vegyületeket alkotnak, mint az oxidok, kloridok, karbonátok és szulfátok. A képletekben azonnal észre lehet venni a mintát: MgO, CaCl 2, CaCO 3, BaSO 4.
Az alkaliföldfémek csoportjának gyors felismerése
Egy gyors azonosítási trükk az, ha egyszerre három jellemzőt keresünk: a második oszlopot, a fémes elemeket és a tipikus +2 töltést. Az alkálifémekkel összehasonlítva, amelyeknek egy vegyértékelektronja van és általában +1 ionokat alkotnak, a 2. csoport elemei egy további külső elektront tartalmaznak, és általában kevésbé reaktívak. Ennek ellenére egyértelműen ugyanahhoz a csoportba tartoznak. Érdekes módon mindegyik tag kissé másképp fejezi ki ezt a mintát, különösen berilliumtól, a csoport tetején, radiumig, a csoport alján.
Ismerkedjünk meg a hat alkaliföldfémmel
Egy lista hasznos, de önmagában nem igazán marad meg az ember emlékezetében. A 2. csoport akkor kezd valódi érzetet kelteni, ha minden tagjának egyértelmű az identitása. Néhányuk csontokban vagy tengervízben fordul elő. Néhányuk színezi a tűzijátékokat. Az egyik főként történelmi figyelmeztető jel. Együtt ugyanazon családhoz tartoznak, de mindegyiknek saját személyisége van.
| Elemens | Szimbólum | Gyakori előfordulás | Kiemelkedő tulajdonság | Gyakorlati jelentőség |
|---|---|---|---|---|
| Berillium | Be | Beryl ásványokban található | Nagyon könnyű és merev fémmént | Speciális űrkutatási és röntgenalkalmazásokban használják; pora belégzése veszélyes |
| Magnesium | Mg | Tengervízben és ásványokban fordul elő | Alacsony sűrűségű, és égés közben világos fehér lángot ad | Fontos a könnyűfém ötvözetekben, kiegészítőként és a biológiában |
| Kalcium | Ca | Gyakori mészkőben, csontokban, kagylóhéjakban és krétában | Biológiailag ismert 2. csoportos ion | Kulcsfontosságú a csontvázban, a cementben, a gipszben és számos természetes ásványban |
| Stroncium | Sr | Főként a celestitben és a strónianitban található | Sói élénkvörös színt adnak a lángokban | Tűzijátékokban, jelzőrakétákban, fénylő anyagokban és egyes fogászati termékekben használják |
| Bárium | BA | Általában a bárium-szulfáttal társul | Sűrű, nehéz alkáliföldfém | A bárium-szulfát fontos a fúrástechnikában és az orvosi képalkotásban; a vízben oldódó báriumvegyületek óvatos kezelést igényelnek |
| Rádium | RA | Nyomokban fordul elő uránércekben | Erős radioaktivitása dominálja kémiai történetét | Ma főként történelmi vagy szigorúan szabályozott tudományos jelentőséggel bír |
Berillium és magnézium a 2. csoport tetején
A berillium elem az elem a család tetején helyezkedik el, és már ebből is látszik, hogy a 2. csoport nem teljesen homogén. Gyakran kapcsolódik a berilhez, ugyanannak a ásványcsaládnak a tagjához, amelybe az smaragd és az akvamarin is beletartozik. A berillium kiemelkedik, mert rendkívül könnyű és merev. Ezért hasznos olyan nagy teljesítményű alkatrészek gyártásában, ahol a kis tömeg döntő fontosságú. Ugyanakkor a berillium olyan anyag, amely ipari környezetben különös óvatosságot igényel, mivel a finom por belégzése káros hatással lehet az egészségre. Ezért emlékeznek rá egyaránt a kiváló teljesítményéről és a kezelésével kapcsolatos óvintézkedésekről.
A magnézium sokkal ismerősebb érzést kelt. A magnézium vegyjele a magnézium (Mg) az egyik legismertebb fém ebben a csoportban, mivel előfordul a tengervízben, gyakori ásványokban és élő rendszerekben. Nagyon könnyű fém, és égésekor intenzív fehér fényt bocsát ki. Ezért a magnéziumot régóta kapcsolják össze jelzőrakétákkal és erősen égő anyagokkal. A mindennapi életben azonban a legtöbb ember enyhébb formáiban találkozik vele, például táplálkozási szerepében, savsemlegesítő vegyületekben vagy akkor használt könnyű ötvözetekben, amikor a tömeg csökkentése fontos.
Kalcium és stroncium a mindennapi anyagokban
A kalcium a második csoport legismertebb eleme számos olvasó számára. Előfordul a mészkőben, a krétában, a kagylóhéjakban és a csontokban, így a kémiát majdnem azonnal összekapcsolja a geológiával és a biológiával. A kalcium-karbonát itt a jól ismert vegyület. Megmagyarázza, miért lehet ugyanazon elemcsoport fontos a barlangképződményekben, építőanyagokban és a vázrendszerben. Maga a kalciumfém reaktív, de kalciumvegyületek mindenütt megtalálhatók, ezért ezt az elemet gyakran ismerősebbnek érezzük, mint exotikusnak.
A stroncium könnyebben emlékeztethető, ha a színhez kötöd. A sztrontzium jelképe sr, és stroncium a sztrontián főleg a celestit és a strontianit ásványokban található. A Királyi Kémiai Társaság úgy írja le, mint egy puha, ezüstes fémet, amely levegőben ég és vízhez reagál. A sói híresek a fényes vörös színek előállításáért a tűzijátékokban és a villámcsapásokban. Ugyanez a forrás megjegyzi, hogy a fényes anyagokat a sötétben is használhatják, és a stroncium-klorid-hexahidrátot a fogkrémben is, ha az érzékeny fogak kezelésére készül. Ez a stroncium egy nagyszerű példa arra, hogy egy elem kémiailag reaktívan reagálhat, de leginkább vegyületeken keresztül fordul elő.
Bárium és rádium fejlett vagy speciális felhasználásban
A bárium elem gyakran a súlyosságával marad meg az emlékezetben. Gyakran társítják a bárium-kén-vegyülettel (barit), és egyik legismertebb vegyülete a bárium-szulfát. Ez a vegyület fontos, mert nagyon oldhatatlan, ami magyarázatot ad arra, hogy miért jelenhet meg a bárium gyakorlati alkalmazásokban – például fúrási folyadékokban és orvosi képalkotásban –, miközben más, oldható bárium-vegyületekkel óvatosabban bánunk, mivel mérgező hatásuk miatt különösen figyelni kell rájuk. A bárium emlékeztet a olvasókat arra, hogy egy 2. csoportba tartozó elem hasznos formája gyakran egy vegyület, nem pedig maga a fémes, csillogó elem.
Rádium az elemek családjának alján helyezkedik el, de nem marad észrevétlenül. rádium periódusos rendszer a nézet szerint a Ra jelöli azt a pontot, ahol a radioaktivitás válik meghatározó tulajdonsággá. A rádium természetes körülmények között csak nyomnyi mennyiségben fordul elő, általában uránércekkel társulva. Történelmileg a lumineszkáló festékek és a korai orvosi kísérletek miatt vált híressé. Ma veszélyessége elsősorban a radioaktivitásából fakad, nem pedig az általános fémtulajdonságaiból, ezért szigorú ellenőrzés alatt kezelik. Egyszerű szavakkal fogalmazva: a rádium továbbra is a 2. csoportba tartozik, de a kémián túl a nukleáris biztonság szempontjából is meg kell vizsgálni.
Ha ezeket a hat elemet egymás mellé helyezzük, a csoport már nem egy üres névlista formájában jelenik meg. A méret, a reaktivitás, a gyakori vegyületek, sőt még az is, ahogyan az egyes elemek a mindennapi életben megjelennek, mind változik lefelé haladva. Ez a változó minta teszi különösen hasznosnak a 2. csoportot, mert a berilliumtól a rádiumig terjedő sorrendből trendek bontakoznak ki, nem csupán véletlenszerű tények.
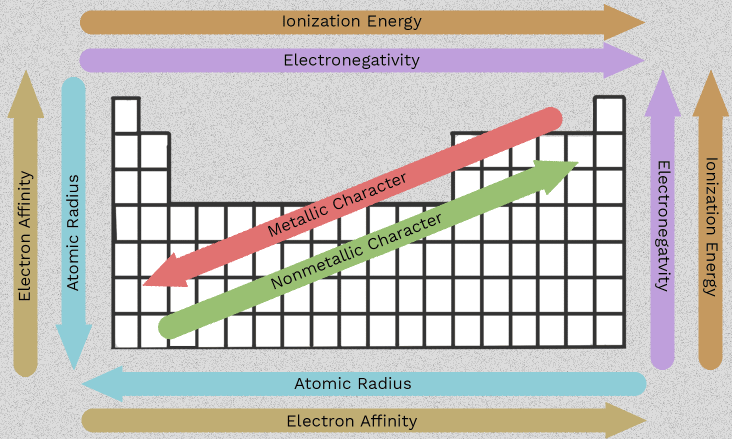
Lúgos földfémek tulajdonságai és a 2. csoport irányzatai
Az a tény, hogy a berilliumtól a rádiumig változik a sorrend, teszi hasznossá a 2. csoportot. Hat elkülönült tény helyett egy handfult ismétlődő mintát követhetünk lefelé az oszlopon. A legfontosabb lúgos földfémek tulajdonságai mind egy közös jellemzőből erednek: minden atomnak két külső elektronja van, amelyeket általában elveszít.
Ha észrevesszük, hogyan változnak a méret, az elektronpajzsolás és az ionizációs energia lefelé a csoportban, a csoport tagjainak viselkedése sokkal könnyebben előrejelezhetővé válik. Ezek a lúgos földfémek jellemzői nem csupán vizsgatények. Megmagyarázzák, miért reagálnak egyes elemek gyorsabban, miért oldódnak jobban egyes vegyületek, mint mások, és miért szükséges néhány tendenciát óvatos megfogalmazással, nem egyszerű nyilakkal leírni.
A lúgos földfémek közös tulajdonságai
A 2. csoport legtöbb tagja ezüstös fémes anyag, amely általában M 2+ionokat alkotnak, és főként ionos vegyületeket képeznek. Redukálószerként viselkednek, mert elektronokat veszítenek. Az 1. csoport fémjeihez képest általában kevésbé reaktívak, de továbbra is elegendően kémiai aktivitással rendelkeznek ahhoz, hogy számos gyakori oxidot, klóridot, karbonátot és szulfátot alkossanak.
Egy egyszerű módja a lúzföldfémek kémiai tulajdonságainak szervezésének az, ha elkülönítjük azt, ami állandó, attól, ami változik. Ami állandó, az a szokásos +2 oxidációs állapot. Ami változik, az az egyes elemek képessége, hogy leadják ezt a két elektront. Itt kezdődnek a tendenciák értelmezése.
A 2. csoport lefelé mutató tendenciái és jelentésük
A LibreTexts által gyűjtött adatok és a Save My Exams által megadott tendencia-magyarázatok ugyanazt az általános mintát mutatják. Az atomrádiusz 112 pm-ről (Be) 253 pm-re (Ba) nő, miközben az első ionizációs energia 900 kJ/mol-ról 503 kJ/mol-ra csökken. Egyszerű nyelven: a külső elektronok távolabb helyezkednek el az atommagtól, és több belső héj árnyékolja őket, ezért könnyebben eltávolíthatók.
| Trend | Irány a 2. csoportban lefelé | Kémiai ok | Mit jelent ez gyakorlatban |
|---|---|---|---|
| Atom sugár | Növeli | Minden elemnek egy további elektronhéja és nagyobb képernyőzése van | A nagyobb atomok kevésbé szorosan tartják a külső elektronokat |
| Első és második ionizációs energia | Általában csökken | A külső elektronok távolabb vannak az atommagtól, így a vonzás gyengébb | Az M 2+ionok képződése könnyebbé válik |
| Reaktivitás | Általában növekszik | Az alacsonyabb ionizációs energiák könnyebbé teszik az elektronok elvesztését | A nehezebb elemek hevesebben reagálnak savakkal, oxigénnel és gyakran vízzel is |
| Olvadáspont | Általában csökken, de nem simán | A nagyobb fémionok gyengítik a fémes kötést, bár a szerkezet is szerepet játszik | Használja a „általános” szót itt, mert a Mg és a Ca nem illeszkedik tökéletesen egy egyenes vonalba |
| Sűrűség | Nem szabályos | A tömeg, az atomméret és a fémcsomagolás egyszerre változik | A sűrűséget nem lehet egyszerű, lefelé mutató tendenciaként kezelni |
| Hidroxid-oldhatóság | Növeli | A rácsenergia és a hidratációs energia egyensúlya a csoportban lefelé tolódik | A nehezebb hidroxidok lúgosabb oldatokat alkotnak |
| Szulfát-oldhatóság | Csökken | A hidratációs energia csökken, ahogy a kation mérete nő | Olyan vegyületek, mint a BaSO 4rendkívül rosszul oldódnak |
A sűrűség és az olvadási viselkedés két olyan tendencia, amelyet a diákok gyakran túlegyszerűsítenek. A sűrűség nem egyenes vonalban változik, mert a tömeg és a térfogat is változik, és a fématomok nem ugyanúgy rendeződnek el minden kristályrácsban. Az olvadáspontokra is figyelmet érdemelni kell. Általában lefelé mutatnak, mert a nagyobb ionok gyengítik a fémes rácsot, de a magnézium rendkívül alacsony olvadáspontja 650 °C, míg a kalciumnál ez 842 °C-ra emelkedik, majd újra csökken. Így az egyik legbiztonságosabb jellemző az alkaliföldfémekre az, hogy a széles körű mintázat valós, de a fizikai részletek nem teljesen simák.
Az oldhatóságnál is ugyanez a figyelmeztetés érvényes. Nincs egyetlen szabály, amely minden 2. csoportba tartozó sóra vonatkozna. A hidroxidok oldhatósága a csoportban lefelé haladva nő, míg a szulfátoké csökken. Ha valaki azt állítja, hogy „az oldhatóság a 2. csoportban lefelé haladva nő”, akkor a fontos kérdés az: „Mely vegyületekre vonatkozik ez?”
Miért reagálnak az alkáliföldfémek úgy, ahogy teszik
Tehát, reaktív-e az alkáliföldfémek ? Igen, és az általános válasz az, hogy reaktivitásuk nő a csoportban lefelé haladva. Az ok ugyanaz az elektronszerkezeti magyarázat, amelyet fentebb láttunk. Alacsonyabb első és második ionizációs energia azt jelenti, hogy az atomok könnyebben veszítenek el két elektront, és gyorsabban érik el a gyakori M 2+állapotot.
Ez hatással van a valós kémiai reakciókra. A csoportban lefelé haladva a híg savakkal zajló reakciók gyorsabbá válnak, az oxigénnel zajló reakciók intenzívebbé válnak, és a nehezebb elemeket egyszerűbb oxidálni. A Save My Exams megjegyzi, hogy a bárium annyira reaktív, hogy olaj alatt kell tárolni, ami gyakorlati bizonyítéka annak, milyen messzire juthat a reaktivitás irányultsága.
- Az atom sugara nő a 2. csoportban lefelé haladva.
- Az ionizációs energia csökken a 2. csoportban lefelé haladva.
- A reaktivitás nő, mert két elektron elvesztése egyre könnyebbé válik.
- Az olvadáspont és a sűrűség szabálytalan változást mutat, ezért kerülni kell az abszolút szabályokat.
- A hidroxidok és szulfátok ellentétes oldhatósági irányultságot mutatnak.
Ezek a minták előrejelezhetővé teszik a családot, de nem teszik teljesen egységesé.
Alkálifémeket és alkáliföldfémeket
A széles körű tendenciák miatt a 2. csoport tanulása egyszerűbb, de a család akkor veszíti értelmét, ha minden tagját azonosként kezeljük. A legnagyobb figyelmeztető jel a berillium. A magnézium egy gyakorlatiasabb, mindennapi kivételt jelent. És amikor az emberek összehasonlítják alkálifémeket és alkáliföldfémeket , a hasonló nevek néhány nagyon eltérő kémiai viselkedést rejthetnek.
Miért nem viselkedik a berillium tipikus 2. csoportos fémként
BYJU'S a berilliumot a 2. csoport nyilvánvaló kilógó elemeként írja le. Szokatlanul kis mérete, magas ionizációs energiája és erős polarizáló képessége olyan viselkedést eredményez, amely kevésbé jellemző a családra. Egyszerű nyelven: Be 2+erősen vonzza a szomszédos elektronfelhőket, ezért a berilliumvegyületek gyakran inkább kovalens jellegűek, mint az ionosabb vegyületek, amelyeket a nehezebb elemek képeznek. Ugyanez a forrás megjegyzi, hogy a berillium magasabb olvadásponttal és forrásponttal rendelkezik, mint a csoport többi tagja, és nem reagál vízzel úgy, mint társai.
A magnézium nem olyan szokatlan, mint a berillium, de mégis kevésbé reaktívnak tűnhet a diákok számára, mint amire számítanak. A LibreTexts megjegyzi, hogy a nagyon tiszta magnézium csak enyhén reagál a hideg vízzel, és a reakció hamar lelassul, mivel majdnem oldhatatlan magnézium-hidroxid képződik a felületén, és egy gátat alkot. A család alján lévő rádiumot általában külön tárgyalják, mivel radioaktivitása meghatározza a gyakorlati alkalmazását és a biztonsági megbeszéléseket.
Az alkaliföldfémek és az alkálfémek közötti különbségek
Egyszerű alkálfémek vs. alkaliföldfémek kifejezésekben a 1. csoportba tartozó fémek egy külső elektront veszítenek, míg a 2. csoportba tartozó fémek két külső elektront veszítenek. Ez az egyetlen különbség formálja az alkálfémek és az alkaliföldfémek tulajdonságait majdnem bármi mást jobban.
| Funkció | Alkálifémek, 1. csoport | Alkáliföldfémek, 2. csoport |
|---|---|---|
| Vegyértékelektronjai | 1 | 2 |
| Tipikus ion | M + | M 2+ |
| Reakció hideg vízzel | Gyakran heves vagy akár erőszakos is, hidroxid és hidrogén keletkezése közben | Kevésbé egységes: a berillium nem reagál vízzel, a magnézium enyhén reagál, a kalcium, stroncium és bárium egyre hevesebben reagál |
| Jellemző oxigén-kémia | Oxidokat, peroxidokat vagy szuperoxidokat képezhetnek | Általában monoxidokat képeznek; ezek többsége vízzel hidroxidot ad, de a BeO kivétel |
Fontos kivételek, amelyeket a tanulók gyakran figyelmen kívül hagynak
- Nem minden 2. csoportba tartozó fém reagál ugyanúgy vízzel.
- A berilliumvegyületek inkább kovalens jellegűek, mint a család többi tagja.
- Ne keverje össze az alkáli- és az alkaliföldfémeket ugyanazon csoportként pusztán azért, mert a neveik hasonlóan hangzanak.
- A az alkálimetálok és az alkaliföldfémek tulajdonságait a legjobban mint mintákat – kivételekkel együtt – tanulhatjuk meg, nem merev szlogensekként.
Ez az a legjobb módja annak, hogy megértsük a kémiai tulajdonságokat az alkálimetálok és az alkaliföldfémek esetében . Az elektronszerkezetek adják a szabályt, de a valós anyagok színre hozzák a finomabb részleteket. És ezek a részletek még élesebben kirajzolódnak, ha megnézzük, hol fordulnak elő ténylegesen a 2. csoport elemei: ritkán tisztán fémként, sokkal gyakrabban ásványokban, kőzetekben, tengervízben, csontokban és ipari vegyületekben.
Az alkaliföldfémek előfordulása a természetben
Ha elképzel egy lúgföldfémet mint egy fényes, tiszta mintát, amely egy kőben nyugszik, a természet másképp működik. A 2. csoport elemei annyira reaktívak, hogy általában ionok formájában jelennek meg ásványokban, sókban, kőzetekben, tengervízben, csontokban és héjakban, nem pedig szabad fémként. Akár az lúgföldfémeket keresi valaki, akár a szokásosabb kifejezést használja, a természetes minta ugyanaz: ez a csoport erősen preferálja a vegyületeket.
Ez a minta közvetlenül a lúgföldfémek kémiai tulajdonságaiból származik. Hajlamosak két külső elektront elveszíteni, és stabil M 2+ionokat képezni. Miután ez megtörténik, az oxigén-, karbonát-, szulfát- és halogénionok könnyen rögzítik őket szilárd vegyületekbe, amelyek geológiai és biológiai környezetben is tartósan fennmaradhatnak.
Miért nem fordulnak elő a lúgföldfémek szabad állapotban a természetben
Britannica és ThoughtCo mindkét forrás a 2. csoportot reaktívnak írja le, ami magyarázza, hogy miért ritkán fordulnak elő ezek az elemek elemi állapotban. A levegőben sokuk gyorsan oxidréteget képez. Természetes környezetben még tovább stabilizálódnak karbonátokként, szulfátokként, szilikátokként, fluoridokként vagy klóridokként. Ezért található meg a kalcium a mészkőben és a csigaházakban, a magnézium ásványokban és tengervízben, a stroncium és a bárium érctelepekben. A rádium még ritkább, csupán nyomokban fordul elő uránércekben.
A 2. csoport gyakori ásványai és vegyületei
| Elemens | Gyakori természetes forrás | Ismert vegyület | Miért fontos ez a vegyület |
|---|---|---|---|
| Berillium | Beryl | BeO | A beril egy kereskedelmi forrása ennek az elemnek, míg a berillium-oxid speciális anyagokban fontos vegyület |
| Magnesium | Magnézit, dolomit, tengervíz | MgCO₃ 3vagy Mg(OH)₂ 2 | Megmutatja, hogy miért fordul elő a magnézium gyakrabban ásványokban, tengervízben és gyógyszerekben, mint tiszta fémként |
| Kalcium | Mészkő, kréta, márvány, gipsz, csontok, héjak | CaCO 3 | Összekapcsolja a geológiát, az építőanyagokat és a csontvázat egy nagyon gyakori vegyületben |
| Stroncium | Sztróncium-karbonát, sztróncium-karbonát | SrSO₄ 4vagy SrCO₃ 3 | Ezek a ásványok a sztróncium-vegyületek fő természetes forrásai |
| Bárium | Bárium-szulfát, bárium-karbonát | BaSO 4 | A bárium-szulfát a kulcsásvány, és a bárium-szulfát az egyik legismertebb bárium-vegyület |
| Rádium | Nyomokban uraninitban és más uránércekben | RaCl 2 | Ritkasága és radioaktivitása miatt a rádium-vegyületek történetileg fontosak, de ritkák |
EBSCO megjegyzi, hogy a kalcium és a magnézium szintén előfordulnak a tengervízben kb. 0,4 g/L és 1,3 g/L koncentrációban. Ez segít megérteni, miért alkáliföldfém család nem csupán a ércekhez, hanem a kemény vízhez, a tengeri rendszerekhez és az élő szövetekhez is kapcsolódik.
Hogyan nyerik ki ezeket a fémeket vegyületeikből
Mivel a 2. csoportba tartozó fémek általában vegyületekbe zárva fordulnak elő, a kinyerésük ércekből, sós vizekből vagy ásványi lelőhelyekből indul ki. Egy gyakori ipari elv egyszerű: először az anyagot egy kezelhetőbb oxidra vagy halidra alakítják át, majd elektrolízissel vagy kémiai redukcióval szabadítják fel a fémet. A Britannica a magnézium, kalcium, stroncium és bárium korai elektrolitikus kinyerését írja le, míg az EBSCO megjegyzi, hogy a modern termelés továbbra is gyakran támaszkodik olvadt klóridokra, oxidok redukciójára vagy az adott elemre jellemző hasonló eljárásokra. A berillium jól illusztrálja, hogy a család nem teljesen homogén, mivel a berillium-fluorid redukciójával állítható elő.
Így a mindennapi életben az emberek általában a 2. csoportot mészkőn, gipszen, tengervízből nyert magnéziumon, bárium-szulfáton (barit) vagy biológiai eredetű kalciumon keresztül ismerik meg, nem pedig nyers fém minták formájában. Ez a részlet fontos, mert ezeknek az elemeknek a való világbeli jelentősége sokkal inkább összefügg vegyületeikkel és formáikkal, mint magukkal a tisztán fém állományokkal.
Lúgos földfémek példái a mindennapi életből
A 2. csoport sokkal emlékezetesebbé válik, ha minden elemhez valós tárgyat vagy jelenséget kapcsolunk. A csontok, a gyomorsav-csökkentők, a gipsz, a tűzijátékok, a fúrási folyadékok és a régi, fénylő számjegyek mind hasznos példák. lúgos földfémek példái ha valaha eltűnődöttél a magnézium fém-e vagy nemfém vagy a Ca fém-e , mindkét kérdésre egyszerű a válasz: a magnézium és a kalcium fémek. A mindennapi életben azonban az emberek általában ezeket az anyagokat vegyületük formájában, nem pedig tisztán fém mintaként találják meg.
A magnézium- és kalciumvegyületek mindennapi felhasználása
- Magnesium : A magnézium egyik legfontosabb biológiai szerepet játszó elem lúgképző földfémek . A NIH magnézium ténylap megjegyzi, hogy több mint 300 enzimrendszer koenzime, és támogatja az izmok és idepek működését, az energiatermelést, valamint a csontok szerkezetét. A magnézium-vegyületek egyes gyomornedv-csökkentő és hashajtó készítményekben is előfordulnak, míg a magnézium-fém könnyű ötvözetekben értékes, ahol a tömeg csökkentése fontos.
- Kalcium a kalcium-vegyületek uralkodnak a mindennapi életben. A kalcium hozzájárul a csontok és fogak szerkezetének kialakításához, és olyan vegyületek, mint a kalcium-karbonát és a kalcium-szulfát, központi szerepet játszanak a mészkőben, a cementben, a gipszben és a gipszkartonban. Ezért a kalcium egyik legnyilvánvalóbb kapcsolatot teremt a kémiában, a biológiában és az építészetben.
Stroncium és bárium specializált alkalmazásai
- Stroncium a stroncium-sók leginkább a tűzijátékokban és jelzőrakétákban előállított mélyvörös színük miatt ismertek. Még azok a olvasók is, akik nem emlékeznek a teljes 2. csoport elemeire, gyakran megjegyzik a stronciumot, ha a színhez kötik.
- Bárium a bárium-vegyületek ipari és orvosi szempontból is jelentősek. A NLM bárium-profil leírja a fő felhasználási területeket: fúrási folyadékok, festékek, műanyagok, téglák és üveg. Emellett megemlíti egy fontos orvosi ellentétet: a nagyon oldhatatlan bárium-szulfátot röntgenkontrasztanyagként használják bizonyos röntgenvizsgálatok során, mivel általában nem szívódik fel a szervezetben.
- Rádium : A rádium főként történelmi vagy szigorúan szabályozott tudományos eset. A NRC rádium-oldala leírja a múltban történő felhasználását fénykibocsátó festékekben és a korai rákterápiában. Ezek közül a felhasználások többsége ma már kiváltásra került, bár néhány szabályozott alkalmazás továbbra is létezik, például bizonyos ipari röntgenfelvételek során.
Miért fontos a forma és az összetétel típusa a gyakorlati felhasználás során
A 2. csoport elemeinél az emberek által használt forma gyakran a vegyület, nem a tiszta fém.
Ez az egyetlen gondolat sok zavarodottságot eloszlat. A magnézium élelmiszerekben vagy gyógyszerekben nem ugyanaz, mint a magnéziumszalag égése. A kalcium a csontban nem ugyanaz, mint a reaktív kalciumfém. A bárium a legkifejezőbb példa arra, miért számít az elem formája: az oldhatatlan báriumszulfát hasznos lehet képalkotásra, míg a jobban oldódó báriumvegyületek sokkal nagyobb óvatosságot igényelnek. A rádium még tovább fokozza ezt a különbséget, mivel kezelését nemcsak a fémek között elfoglalt helye, hanem elsősorban a rádióaktivitása határozza meg.
Tehát a 2. csoport értéke egyáltalán nem absztrakt. Ezek az elemek segítenek megérteni, hogyan lehet ugyanazon elemcsoport fontos a táplálkozásban, az anyagokban, az orvostudományban, az ipari feldolgozásban és a biztonsági szabályokban is. Gyakran elegendő egy rövid, valós alkalmazásokat tartalmazó lista ahhoz, hogy a nagyobb minta megmaradjon a memóriában.
Kulcstényezők a 2. csoport elemeiről
Ezen a ponton a alkáliföldfémek csoportja már kevésbé tűnik egy megtanulandó felsorolásnak, és inkább olyan mintázatnak, amelyet közvetlenül leolvashatunk a 2. csoport a periódusos rendszerben oszlopból. Ha valaki mégis megkérdezi, mi az alkáliföldfémek? , a rövid válasz egyszerű marad: berillium, magnézium, kalcium, stroncium, bárium és rádium. Egy teljesebb alkáliföldfémek definíciója még hasznosabb: hat fémes elem a 2. csoportban, amelyek általában két külső elektront veszítenek el, és M 2+ionokat képeznek.
Fontos megjegyzendő tények az alkáliföldfémekről
- A helyzet számít: ez a hat 2. csoportba tartozó elem a bal oldaltól számított második oszlopban, az s-mező 2. csoportjában helyezkedik el.
- A családtagok rögzítettek: Be, Mg, Ca, Sr, Ba és Ra alkotják az egész csoportot.
- A közös kémiai viselkedés magyarázza a családi hasonlóságot: ns 2külső elektronhéjuk konfigurációja miatt a +2 töltésű ionok képződése a leggyakoribb eredmény, amit a LibreTexts összefoglal egy alapvető állításban.
- A fő irányok lefelé előrejelezhetők: az atom sugara nő, a ionizációs energia általában csökken, és a reaktivitás általában nő a csoport lefelé haladásával.
- A kivételek fontosak: a berillium inkább kovalens jellegű, mint a többi elem; a magnézium látszólag kevésbé reaktív lehet a felületi oxidrétege miatt; a rádiumot főként radioaktivitása miatt tárgyalják.
- A mindennapi életben általában vegyületekről, nem tisztán fémekről van szó: az emberek sokkal gyakrabban találkoznak kalcium-karbonáttal, magnézium-oxiddal és bárium-szulfáttal, mint az elemi Ca, Mg vagy Ba anyagokkal.
A lúgösszetevők periódusos rendszer az oszlop a legkönnyebben hat fémként jegyezhető meg, amelyeket egy szabály köt össze: általában 2+ töltésű ionokká válnak, de mindegyik tag ezt a szabályt kissé eltérő módon fejezi ki.
A 2. csoport kémiai ismereteitől az üzembe helyezett fémpartokig
Ez a kémia messze túlmutat a tankönyveken. A LibreTexts megjegyzi, hogy az elemi magnéziumot nagy mennyiségben állítják elő, és könnyű ötvözetekként használják repülőgép-hidak és autómotor-alkatrészek gyártásához. Egy átfogóbb ötvözet-útmutató bemutatja, miért is fontos ez: a mérnökök a komponensek összetételét és feldolgozását úgy igazítják, hogy egyensúlyt teremtsenek a súly, a szilárdság, a korrózióállóság és a megmunkálhatóság között a gyakorlati alkatrészekben.
Olvasók számára, akik a 2. csoport a periódusos rendszerben nézeteiktől a gyártás felé haladnak, Shaoyi Metal Technology gyakorlati példát nyújt erre a kapcsolatra. Az autóipari anyagok és megmunkálás oldalai a fémalkatrészek gyártását írják le a prototípuskészítéstől a tömeggyártásig, ahol az anyagviselkedésnek és a folyamatiránynak együtt kell működnie. lúgösszetevők periódusos rendszer több mint egy tanteremben használt táblázat. Ugyanakkor ez a logika áll a fémes és ötvözetes anyagok kiválasztása mögött is olyan mérnöki alkotásokhoz, amelyeknek könnyűnek, megbízhatónak és gyárthatónak kell lenniük.
GYIK az alkaliföldfémekről
1. Melyek a hat alkaliföldfém?
A hat alkaliföldfém a berillium, a magnézium, a kalcium, a stroncium, a bárium és a rádium. A periódusos rendszer 2. csoportját alkotják, és azért sorolják őket közös csoportba, mert általában két külső elektront veszítenek el, ami sok vegyületben egy közös 2+ töltésű ionmintát eredményez.
2. Miben különböznek az alkaliföldfémek az alkálfémektől?
Az alkáli fémek az 1. csoportba tartoznak, és általában 1+ töltésű ionokat képeznek, mivel egy darab külső elektronjuk van. Az alkáliföldfémek a 2. csoportba tartoznak, általában 2+ töltésű ionokat képeznek, és általában kevésbé reaktívak. Az egyetlen további vegyértékelektron megváltoztatja kötésük erősségét, vízzel való reakciójukat, valamint azokat a sókat és oxidokat, amelyeket általában képeznek.
3. Miért nem fordulnak elő szabad elemi formájukban a természetben az alkáliföldfémek?
Ezek a fémek annyira reaktívak, hogy természetes környezetben általában nem maradnak hosszú ideig tiszta elemi formában. Ehelyett oxigénnel, karbonát-, szulfát-, klór- vagy szilikátionokkal kötődnek, és ásványok, kőzetek, tengervíz, csigaházak és csontok részévé válnak. Ezért az emberek általában a 2. csoport elemeit vegyületek formájában, nem pedig nyers fém mintákban találják meg.
4. Reagálnak-e az összes alkáliföldfém vízzel?
Nem, és ez az egyik leghasznosabb kivétel, amelyre érdemes emlékezni. A berillium nagyrészt ellenáll a víz hatásának, a magnézium lassan reagál a hideg vízzel, mert egy felületi réteg korlátozza a reakciót, míg a kalcium, a stroncium és a bárium könnyebben reagál. Általánosságban elmondható, hogy a csoporton belül lefelé haladva a vízreaktivitás erősödik.
5. Miért fontosak az alkáliföldfémek az iparban és a gyártásban?
Fontosságuk mind az összetett vegyületeikből, mind az ötvözetválasztásban betöltött szerepükből fakad. A magnézium akkor értékes, ha a kisebb tömeg számít, a kalciumvegyületek központi szerepet töltenek be a cement és a gipsz gyártásában, míg a báriumvegyületeket speciális ipari és orvosi alkalmazásokra választják. A gyakorlati termelés során a fémek viselkedésének megértése segít irányítani a megmunkálást, a folyamatstabilitást és a alkatrészek minőségét, ezért olyan beszállítók – például a Shaoyi Metal Technology – kiemelik a tanúsított autóipari megmunkálást, a folyamatszabályozást és a prototípusalkatrészektől a tömeggyártásig nyújtott támogatást.
 Kis szeletek, magas szabványok. Gyors prototípuskészítési szolgáltatásunk gyorsabbá és egyszerűbbé teszi az ellenőrzést —
Kis szeletek, magas szabványok. Gyors prototípuskészítési szolgáltatásunk gyorsabbá és egyszerűbbé teszi az ellenőrzést —
