Ce sunt metalele alcalino-pământoase? Grupa 2 devine în sfârșit clară
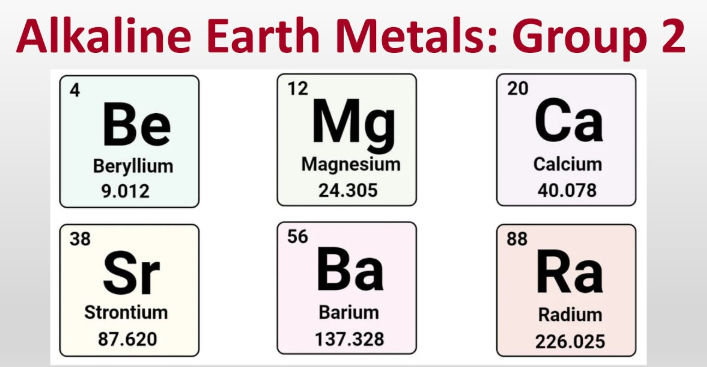
Ce sunt metalele alcalino-pământoase?
Dacă ați căutat ce sunt metalele alcalino-pământoase , iată răspunsul direct: sunt cele șase elemente din Grupul 2 grupa 2 definiție rapidă a metalelor alcalino-pământoase este punctul de plecare, dar numele ne spune, de asemenea, multe despre modul în care se comportă această familie de elemente.
Care sunt metalele alcalino-pământoase, într-o singură propoziție
Metalele alcalino-pământoase sunt beriliul, magneziul, calciul, stronțiul, bariul și radiul, cele șase elemente metalice din Grupa 2 care formează, de obicei, ioni +2.
- Beriliu (Be)
- Magneziu (Mg)
- Calcium (Ca)
- Stronțiu (Sr)
- Bariul (Ba)
- Radium (Ra)
De ce denumirea de metale alcalino-pământoase este potrivită
Pentru începători, definiția metalelor alcalino-pământoase devine mult mai ușoară atunci când împărțiți expresia în trei părți.
Alcalin înseamnă că oxizii și hidroxizii lor sunt bazici, nu acizi. Pamânt este un termen istoric. Chimistii timpurii l-au folosit pentru substanțe rezistente la căldură, de tip mineral, care nu se topesc sau nu se dizolvă ușor în apă, un aspect explicat de Britannica . Alte metale înseamnă că elementele în sine sunt metalice, de obicei lucioase și bune în cedarea electronilor în reacții.
Acest lucru vă oferă sensul de bază al metalelor alcalino-pământoase fără a avea nevoie mai întâi de cunoștințe avansate de chimie. Este, de asemenea, o descriere concisă și utilă a metalelor alcalino-pământoase : o familie de metale din Grupa 2, care împart aceeași chimie, aceeași poziție în tabelul periodic și un rol important în lumea reală. Magneziul apare în aliaje și în biologie. Calciul este esențial pentru oase, cochilii și materiale de construcție. Bariul, stronțiul și radiul apar în contexte mai specializate.
Acest articol începe intenționat într-un mod simplu. O listă clară este ușor de memorat, dar familia devine cu adevărat intuitivă atunci când observi unde se află aceste elemente și de ce această poziție le conferă un comportament atât de similar.
Unde se află Grupa 2 în tabelul periodic
Numele familiei devine mult mai ușor de reținut atunci când o poți identifica efectiv. Dacă te întrebi unde se găsesc metalele alcalino-pământoase în tabelul periodic , uită-te la a doua coloană din stânga. Această coloană verticală este grupa 2 din tabelul periodic , situată imediat învecinată metalelor alcaline din Grupa 1. A grupul 2 din tabelul periodic vizualizarea arată aceeași linie dreaptă de fiecare dată: beriliul în partea de sus, apoi magneziul, calciul, stronțiul, bariul și radiul, dispuse în ordine descendentă pe parcursul perioadelor.
Într-un tabelul periodic al metalelor alcalino-pământoase grafic, aceste șase elemente aparțin blocului s. Poziția lor comună este importantă, deoarece reflectă un model comun de electroni. Așa cum LibreTexts explică, elementele din grupul 2 au o configurație de valență ns 2, ceea ce înseamnă că posedă doi electroni în stratul exterior.
Unde se găsesc metalele alcalino-pământoase în tabelul periodic
Vizual, modelul este simplu. elementele din grupul 2 al tabelului periodic formează o singură coloană familială, care se întinde pe perioadele 2 până la 7. Multe diagrame utilizate în clase subliniază acest metale alcalino-pământoase din tabelul periodic aranjamente cu aceeași culoare deoarece familiile de elemente se citesc vertical, nu orizontal. Căutările pentru tabelul periodic al metalelor alcalino-pământoase se referă de fapt la acea coloană specifică.
| Element | Simbol | Poziția Grupului 2 | Ion tipic | Compus cunoscut |
|---|---|---|---|---|
| Beriliu | Be | Perioada 2, partea superioară a Grupului 2 | Be2+ | BeO |
| Magnesiu | Mg | Perioada 3 | Mg2+ | MgO |
| Calciu | Ca | Perioada 4 | Ca2+ | Caco 3 |
| Stronțiul | Sr | Perioada 5 | Sr2+ | SrCO 3 |
| Barium | BA | Perioada 6 | BA 2+ | BaSO 4 |
| Radiu | RA | Perioada 7, partea inferioară a Grupului 2 | RA 2+ | RaCl 2 |
De ce elementele din Grupul 2 formează ioni cu sarcină plus doi
Acei doi electroni exteriori determină comportamentul chimic. Atomii din Grupul 2 tind să piardă ambele electroni, deoarece această pierdere le conferă o configurație electronică mai stabilă. Rezultatul este un +2 ioni , cum ar fi Mg 2+sau Ca 2+. De aceea, aceste metale formează în mod obișnuit compuși precum oxizi, cloruri, carbonați și sulfați. Observați imediat modelul din formule: MgO, CaCl 2, CaCO 3, BaSO 4.
Cum să recunoașteți rapid familia metalelor alcalino-pământoase
O metodă rapidă de identificare constă în căutarea simultană a trei indicii: colțul al doilea (grupa 2), elemente metalice și o sarcină obișnuită de +2. Comparativ cu metalele alcaline vecine, care au un singur electron de valență și formează în mod obișnuit ioni +1, elementele Grupului 2 au un electron suplimentar în stratul exterior și sunt, în general, mai puțin reactive. Totuși, ele aparțin clar aceleiași familii. Partea interesantă este că fiecare membru exprimă acest model într-un mod ușor diferit, în special de la beriliu, situat în vârful grupei, până la radiu, aflat la baza acesteia.
Cunoașteți cele șase metale alcalino-pământoase
O listă este utilă, dar nu este foarte memorabilă în sine. Grupul 2 începe să pară mai real atunci când fiecare membru are o identitate clară. Unii apar în oase sau în apă de mare. Unii colorează focurile de artificii. Unul este în principal un semn istoric de avertizare. Împreună, ei continuă să aparțină aceleiași familii, dar fiecare are propria personalitate.
| Element | Simbol | Apariție comună | Proprietate remarcabilă | Relevanță în practică |
|---|---|---|---|---|
| Beriliu | Be | Găsit în minerale precum berilul | Foarte ușor și rigid pentru un metal | Utilizat în aplicații specializate din domeniul aerospace și al radiografiilor; praful este periculos dacă este inhalat |
| Magnesiu | Mg | Prezent în apă de mare și în minerale | Densitate scăzută și flacără alb-strălucitor la ardere | Important în aliaje ușoare, suplimente și biologie |
| Calciu | Ca | Comun în calcar, oase, cochilii și cretă | Ion din Grupul 2 biologic familiar | Esential în schelete, ciment, ipsos și numeroase minerale naturale |
| Stronțiul | Sr | Se găsește în principal în celestina și strontianită | Sărurile produc o culoare roșie intensă în flăcări | Este utilizat în artificii, rachete de semnalizare, materiale luminescente și unele produse dentare |
| Barium | BA | Este de obicei asociat cu barita | Metal alcalino-pământos dens și greu | Sulfatul de bariu este important în foraj și imagistică medicală; compușii solubili de bariu necesită precauție |
| Radiu | RA | Apare în cantități urmăre în minereurile de uraniu | Radioactivitatea puternică domină povestea sa chimică | În prezent, în principal de relevanță istorică sau științifică strict controlată |
Beriliul și magneziul de la începutul Grupului 2
The elementul beriliu se află în vârful familiei și sugerează deja că Grupul 2 nu este perfect uniform. Este frecvent asociat cu mineralul beril, aceeași familie de minerale care include smaraldul și acvamarina. Beriliul se remarcă prin faptul că este neobișnuit de ușor și rigid. Acest lucru îl face util în componente de înaltă performanță, unde masa redusă este esențială. În același timp, beriliul este un material care necesită precauție în mediile industriale, deoarece prafurile fine pot fi dăunătoare dacă sunt inhalate. Astfel, este reținut atât pentru performanța sa, cât și pentru necesitatea măsurilor de precauție în manipulare.
Magneziul pare mult mai familiar. simbolul chimic al magneziului este Mg și este unul dintre cele mai cunoscute metale din acest grup, deoarece apare în apa de mare, minerale comune și sisteme vii. Este un metal foarte ușor, iar când arde, produce o lumină albă intensă. De aceea, magneziul a fost asociat de mult timp cu semnalele luminoase și materialele care ard strălucitor. În viața de zi cu zi, totuși, majoritatea oamenilor îl întâlnesc sub forme mai blânde, cum ar fi rolurile sale nutriționale, compușii antiacizi sau aliajele ușoare utilizate acolo unde reducerea masei este esențială.
Calciul și stronțiul în materialele de uz comun
Calciul este membrul Grupului 2 cel mai recunoscut pentru mulți cititori. Apare în calcar, cretă, cochilii și oase, astfel încât leagă chimia de geologie și biologie aproape imediat. Carbonatul de calciu este compusul familiar în acest context. El ajută la explicarea motivului pentru care aceeași familie poate avea importanță atât în formările de peșteri, cât și în piatra de construcții și în schelete. Metalul calciu în sine este reactiv, dar compușii săi sunt peste tot, ceea ce face ca acest element să pară adesea mai familiar decât exotic.
Stronțiul este mai ușor de reținut odată ce îl asociezi cu o culoare. simbolul pentru stronțiu este Sr, iar stronțiul se găsește în principal în mineralele celestina și stronțianită. Societatea Regală de Chimie îl descrie ca un metal moale, argintiu, care arde în aer și reacționează cu apa. Sărurile sale sunt cunoscute pentru producerea unor culori roșii strălucitoare în petarde și rachete de semnalizare. Aceeași sursă menționează, de asemenea, utilizări în materialele care strălucesc în întuneric și în clorura de stronțiu hexahidrată din pasta de dinți pentru dinții sensibili. Acest lucru face din stronțiu un excelent exemplu de element care poate fi chimic reactiv, dar cu care ne confruntăm în principal sub formă de compuși.
Bariul și radiul în contexte avansate sau specializate
The elementul bariu este adesea amintit prin greutatea sa. Este frecvent asociat cu barita, iar unul dintre cele mai cunoscute compuși ai săi este sulfatul de bariu. Acest compus este important deoarece este foarte puțin solubil, ceea ce explică de ce bariul poate apărea în domenii practice, cum ar fi fluidele de foraj și imagistica medicală, în timp ce alți compuși solubili de bariu sunt tratați cu mai multă atenție din cauza preocupărilor legate de toxicitate. Bariul reamintește cititorilor că forma utilă a unui element din Grupa 2 este adesea un compus, nu metalul strălucitor în sine.
Radiumul se află în partea de jos a familiei, dar nu rămâne discret. tabel periodic al radiumului vedere, Ra marchează punctul în care radioactivitatea devine caracteristica definitorie. Radiul apare în mod natural doar în cantități minuscule, de obicei asociat cu minereurile de uraniu. În trecut, a devenit faimos datorită vopselelor luminescente și experimentelor medicale timpurii. Astăzi, pericolul său provine din radioactivitate, nu din comportamentul obișnuit al unui metal, astfel încât este manipulat în condiții de control strict. În termeni simpli, radiul aparține în continuare Grupului 2, dar este discutat având în vedere siguranța nucleară la fel de mult ca și chimia.
Așezați aceste șase elemente unul lângă altul și familia nu mai pare o simplă listă de nume. Mărimea, reactivitatea, compușii obișnuiți și chiar modul în care fiecare element apare în viață se modifică pe măsură ce coborâm în grup. Acest model în schimbare este locul în care Grupul 2 devine deosebit de util, deoarece ordinea de la beriliu la radiu începe să evidențieze tendințe, nu doar informații izolate.
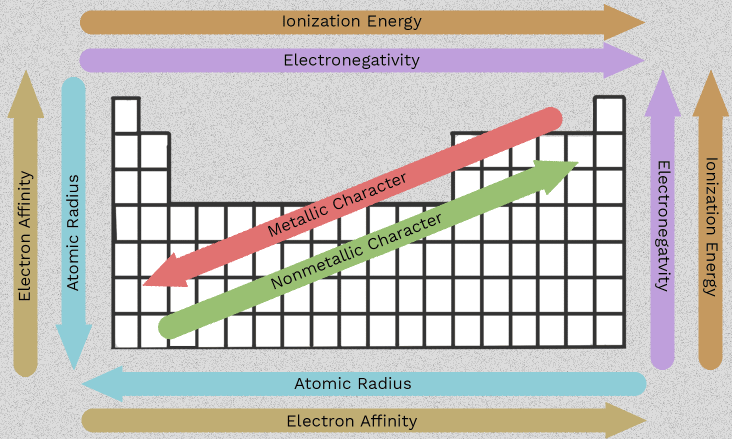
Proprietățile metalelor alcalino-pământoase și tendințele Grupului 2
Această ordine descrescătoare, de la beriliu la radiu, este ceea ce face Grupa 2 utilă. În loc să învățați pe de rost șase fapte izolate, puteți urmări un număr mic de modele care se repetă pe întreaga coloană. Cel mai important proprietăți ale metalelor alcalino-pământoase derivă dintr-o caracteristică comună: fiecare atom are doi electroni de valență pe care tinde să îi piardă.
Odată ce observați cum variază dimensiunea atomică, ecranarea electronică și energia de ionizare în coborârea grupei, comportamentul acestei familii devine mult mai ușor de prevăzut. Aceste caracteristici ale metalelor alcalino-pământoase nu sunt doar informații pentru examene. Ele explică de ce unii membri reacționează mai rapid, de ce unele compuși se dizolvă mai bine decât alții și de ce unele tendințe necesită o formulare atentă, nu doar săgeți simple.
Proprietăți comune ale metalelor alcalino-pământoase
Majoritatea membrilor Grupei 2 sunt metale argintii care formează, de obicei, M 2+ioni și formează în principal compuși ionici. Se comportă ca agenți reducători deoarece își pierd electronii. În comparație cu metalele din Grupa 1, sunt în general mai puțin reactive, dar rămân totuși suficient de active din punct de vedere chimic pentru a forma numeroase oxizi, cloruri, carbonați și sulfați comuni.
Un mod simplu de a organiza proprietățile chimice ale metalelor alcalino-pământoase este să se distingă ceea ce rămâne constant de ceea ce se modifică. Ceea ce rămâne constant este starea obișnuită de oxidare +2. Ceea ce se modifică este ușurința cu care fiecare element cedează acei doi electroni. Aici încep să conteze tendințele.
Tendințe în sensul coborârii Grupului 2 și semnificația lor
Datele colectate de LibreTexts și explicațiile privind tendințele provenite de la Save My Exams arată același model general. Raza atomică crește de la 112 pm pentru Be la 253 pm pentru Ba, în timp ce prima energie de ionizare scade de la 900 la 503 kJ/mol. În termeni simpli, electronii din exterior se află la o distanță mai mare față de nucleu și sunt ecranați de un număr mai mare de straturi interioare, astfel că sunt mai ușor de eliminat.
| Tendință | Direcția coborârii Grupului 2 | Motiv chimic | Ce înseamnă acest lucru în practică |
|---|---|---|---|
| Raza atomică | Crește | Fiecare element are un strat electronic suplimentar și o ecranare mai mare | Atomii mai mari rețin electronii din exterior mai puțin strâns |
| Prima și a doua energie de ionizare | Scad în ansamblu | Electronii din exterior sunt mai departe de nucleu, deci atracția este mai slabă | Formarea ionilor M 2+devine mai ușoară |
| Reactivitate | Crește în ansamblu | Energiile mai mici de ionizare fac pierderea electronilor mai ușoară | Elementele mai grele reacționează mai energic cu acizii, oxigenul și, adesea, cu apa |
| Punctul de topire | Scade în general, dar nu în mod uniform | Ionii metalici mai mari slăbesc legătura metalică, deși structura are, de asemenea, importanță | Folosiți cuvântul „general” aici, deoarece Mg și Ca nu se încadrează perfect într-o linie clar definită |
| Densitate | Neregulat | Masa, dimensiunea atomică și împachetarea metalelor se modifică simultan | Nu puteți trata densitatea ca pe o tendință simplă descendentă |
| Solubilitatea hidroxidului | Crește | Echilibrul dintre energia reticulară și energia de hidratare se deplasează în josul grupei | Hidroxizii mai grei formează soluții mai alcaline |
| Solubilitatea sulfaților | Scade | Energia de hidratare scade pe măsură ce cationul devine mai mare | Compuși precum BaSO 4devin foarte puțin solubili |
Densitatea și comportamentul la topire sunt cele două tendințe pe care studenții le simplifică adesea în exces. Densitatea nu evoluează în linie dreaptă, deoarece atât masa, cât și volumul se modifică, iar atomii metalici nu se împachetează în același mod în fiecare cristal. Punctele de topire necesită, de asemenea, o analiză atentă. În general, acestea scad în josul grupei, deoarece ionii mai mari slăbesc rețeaua metalică, dar Mg are un punct de topire neobișnuit de scăzut, de 650 °C, în timp ce Ca crește până la 842 °C, înainte ca valorile să scadă din nou. Așadar, una dintre cele mai sigure caracteristici ale metalelor alcalino-pământoase este următoarea: tendința generală este reală, dar detaliile fizice nu sunt perfect uniforme.
Solubilitatea are aceeași etichetă de avertizare. Nu există o singură regulă care să acopere toate sărurile din Grupa 2. Hidroxizii devin mai solubili în josul grupei, în timp ce sulfații devin mai puțin solubili. Dacă cineva spune «solubilitatea crește în josul Grupei 2», întrebarea importantă este: «Despre care compuși vorbim?»
De ce metalele alcalino-pământoase reacționează în modul în care o fac
Deci, sunt metalele alcalino-pământoase reactive ? Da, iar răspunsul general este că reactivitatea lor crește pe măsură ce coborâm în grup. Motivul este același fenomen legat de electroni descris mai sus. Energia mai scăzută de prima și a doua ionizare înseamnă că atomii pot ceda mai ușor doi electroni și pot atinge starea comună M 2+mai repede.
Acest lucru influențează reacțiile reale. În josul grupului, reacțiile cu acizii diluați devin mai rapide, reacțiile cu oxigenul devin mai violente, iar membrii mai grei sunt mai ușor de oxidat. Notele Save My Exams subliniază faptul că bariul este suficient de reactiv pentru a fi stocat sub ulei, ceea ce constituie un semn practic al intensității acestei tendințe de reactivitate.
- Raza atomică crește în josul Grupului 2.
- Energia de ionizare scade în josul Grupului 2.
- Reactivitatea crește deoarece cedarea a doi electroni devine mai ușoară.
- Punctul de topire și densitatea prezintă neregularități, așadar evitați regulile absolute.
- Hidroxizii și sulfații prezintă tendințe opuse de solubilitate.
Aceste modele fac familia previzibilă, dar nu perfect uniformă. Chiar în partea superioară a grupului, beriliul începe deja să încalce regulile, iar magneziul adaugă o altă excepție cotidiană care are o importanță mai mare decât mulți începători ar presupune.
Metalele alcaline și metalele alcalino-pământoase
Tendințele generale fac Grupul 2 mai ușor de învățat, dar familia își pierde sensul dacă fiecare membru este tratat ca fiind identic. Cel mai semnificativ semn de avertizare este beriliul. Magneziul adaugă o excepție mai practică, din viața de zi cu zi. Și atunci când oamenii compară metalele alcaline și metalele alcalino-pământoase , denumirile similare pot ascunde unele diferențe chimice foarte mari.
De ce beriliul nu se comportă ca un metal tipic din Grupul 2
BYJU'S descrie beriliul ca fiind clarul excepție din Grupul 2. Dimensiunea sa neobișnuit de mică, energia ridicată de ionizare și puterea sa de polarizare accentuată îi conferă un comportament mai puțin tipic pentru această familie. În limbaj simplu, Be 2+atrage puternic norii de electroni din apropiere, astfel încât compuşii beriliului sunt adesea mai covalenţi decât compuşii mai ioniçi formaţi de elementele mai grele din grup. Aceeaşi sursă observă, de asemenea, că beriliul are puncte de topire și de fierbere mai ridicate decât celelalte elemente din grup și nu reacționează cu apa, spre deosebire de omologii săi.
Magneziul nu este la fel de neobișnuit ca beriliul, dar poate părea totuși mai puțin reactiv decât se așteaptă studenții. LibreTexts subliniază faptul că magneziul foarte curat reacționează doar ușor cu apa rece, iar reacția încetinește rapid, deoarece hidroxidul de magneziu, practic insolubil, formează o barieră pe suprafață. În partea de jos a grupei, radiul este de obicei discutat separat, deoarece radioactivitatea sa domină atât aplicațiile practice, cât și discuțiile privind siguranța.
Cum diferă metalele alcalino-pământoase de metalele alcaline
În termeni simpli alcaline vs. alcalino-pământoase metalele din Grupa 1 pierd un electron exterior, în timp ce metalele din Grupa 2 pierd doi electroni. Această singură diferență modelează proprietățile metalelor alcaline și ale metalelor alcalino-pământoase mai mult decât orice alt factor.
| Caracteristică | Metale alcaline, Grupa 1 | Metale alcalino-pământoase, Grupa 2 |
|---|---|---|
| Electronii de valență | 1 | 2 |
| Ion tipic | M + | M 2+ |
| Reacție cu apa rece | Adesea viguroasă sau chiar violentă, formând hidroxid și hidrogen | Mai puțin uniformă: Be nu reacționează cu apa, Mg reacționează ușor, iar Ca, Sr și Ba reacționează cu o intensitate în creștere |
| Chimie obișnuită a oxigenului | Pot forma oxizi, peroxizi sau superoxizi | Formează în mod obișnuit monoxizi; majoritatea acestor oxizi formează hidroxizi în reacție cu apa, dar BeO este o excepție |
Excepții importante pe care elevii le omit adesea
- Nu toate metalele din Grupa 2 reacționează cu apa în același mod.
- Compușii beriliului sunt mai covalenți decât restul familiei.
- Nu confunda metalele alcaline și metalele alcalino-pământoase ca fiind același grup doar pentru că denumirile lor sună asemănător.
- The proprietățile metalelor alcaline și ale metalelor alcalino-pământoase sunt mai bine învățate ca modele cu excepții, nu ca sloganuri rigide.
Aceasta este, de asemenea, cea mai bună modalitate de a înțelege proprietățile chimice ale metalelor alcaline și ale metalelor alcalino-pământoase . Modelele electronice îți oferă regula, dar substanțele reale adaugă nuanță. Această nuanță devine chiar mai clară atunci când analizezi unde se găsesc, de fapt, elementele Grupului 2: rar ca metale pure și mult mai frecvent în interiorul mineralelor, rocilor, apei de mare, oaselor și compușilor industriali.
Modul în care metalele alcalino-pământoase apar în natură
Dacă vă imaginați un metal alcalino-pământos ca pe o mostră strălucitoare și pură așezată într-o rocă, natura acționează într-un mod diferit. Elementele din Grupa 2 sunt suficient de reactive încât, de obicei, apar ca ioni în interiorul mineralelor, sărurilor, rocilor, apei de mare, oaselor și scoicelor, nu ca metale libere. Indiferent dacă cineva caută metale alcalino-pământoase sau termenul mai standard, modelul natural este același: această familie preferă în mod evident compușii.
Acest model provine direct din proprietățile chimice ale metalelor alcalino-pământoase . Acestea tind să piardă doi electroni din stratul exterior și să formeze ioni stabili M 2+²⁺. Odată ce acest lucru se întâmplă, ionii de oxigen, carbonat, sulfat și halogeni le fixează ușor în compuși solizi care pot persista în geologie și biologie.
De ce metalele alcalino-pământoase nu se găsesc libere în natură
Britannica și ThoughtCo ambele descriu Grupul 2 ca fiind reactiv, ceea ce explică de ce aceste elemente sunt rar întâlnite în stare ne combinată. În aer, multe formează rapid straturi de oxizi. În mediile naturale, ele sunt stabilizate și mai mult sub formă de carbonați, sulfați, silicați, fluoruri sau cloruri. De aceea calciul apare în calcar și cochilii, magneziul în minerale și apă de mare, iar stronțiul sau bariul în zăcăminte de minereu. Radiul este și mai rar, apărând doar în urme în minereurile de uraniu.
Minerale și compuși comuni ai Grupului 2
| Element | Sursă naturală comună | Compus cunoscut | De ce acest compus este important |
|---|---|---|---|
| Beriliu | Beryl | BeO | Berilul este o sursă comercială a elementului, iar oxidul de beriliu este un compus important în materiale specializate |
| Magnesiu | Magnesit, dolomit, apă de mare | MgCO₃ 3sau Mg(OH)₂ 2 | Arată de ce magneziul este întâlnit mai frecvent în minerale, apă de mare și medicină decât sub formă de metal pur |
| Calciu | Calcar, cretă, marmură, gips, oase, cochilii | Caco 3 | Leagă geologia, materialele de construcție și scheletele într-un compus foarte comun |
| Stronțiul | Celestita, strontianita | SrSO 4sau SrCO 3 | Aceste minerale sunt principalele surse naturale de compuși ai stronțiului |
| Barium | Barita, witherita | BaSO 4 | Barita este minereul esențial, iar sulfatul de bariu este unul dintre cei mai cunoscuți compuși ai bariului |
| Radiu | Cantități urmă în pitchblenda și alte minereuri de uraniu | RaCl 2 | Raritatea și radioactivitatea sa au făcut ca compușii radiului să fie istoric importanți, dar puțin întâlniți |
EBSCO observă că calciul și magneziul apar, de asemenea, în apa de mare în concentrații de aproximativ 0,4 g/L, respectiv 1,3 g/L. Acest lucru ajută la explicarea faptului că acest grup al pământurilor alcaline cuprinde nu doar minereuri, ci și apă dură, sisteme marine și țesuturi vii.
Modul în care aceste metale sunt izolate din compușii lor
Deoarece metalele din Grupa 2 sunt de obicei încorporate în compuși, extracția începe cu minereuri, ape sărate (brine) sau depozite minerale. O idee industrială comună este simplă: mai întâi se transformă materialul într-un oxid sau halogenură mai ușor de prelucrat, apoi se folosește electroliza sau reducerea chimică pentru a elibera metalul. Encyclopædia Britannica descrie izolarea inițială a magneziului, calciului, stronțiului și bariului prin electroliză, în timp ce EBSCO subliniază faptul că producția modernă se bazează încă frecvent pe cloruri topite, reducerea oxizilor sau alte metode similare, în funcție de elementul respectiv. Beriliul reprezintă un exemplu util care evidențiază faptul că acest grup nu este perfect uniform, deoarece poate fi obținut prin reducerea fluorurii de beriliu.
Astfel, în viața de zi cu zi, oamenii întâlnesc de obicei Grupa 2 prin calcar, gips, magneziu din apă de mare, barită sau calciu biologic, nu prin eșantioane de metal brut. Acest detaliu este important, deoarece importanța acestor elemente în lumea reală este legată mult mai mult de compușii și formele lor decât de metalele pure în sine.
Exemple de metale alcalino-pământoase în viața de zi cu zi
Grupa 2 devine mult mai ușor de reținut atunci când asociați fiecare element cu ceva concret: oase, antiacide, gips, artificii, fluide de foraj și vechi cadranuri luminescente sunt toate exemple utile. exemple de metale alcalino-pământoase . Dacă v-ați întrebat vreodată este magneziul un metal sau un nemetal sau este Ca un metal , ambele răspunsuri sunt simple: magneziul și calciul sunt metale. În viața obișnuită, totuși, oamenii întâlnesc de obicei aceste substanțe sub formă de compuși, nu ca eșantioane de metal pur.
Utilizări zilnice ale compușilor de magneziu și calciu
- Magnesiu : Magneziul este unul dintre cele mai importante elemente din punct de vedere biologic elemente alcalino-pământoase . Fișa informativă NIH despre magneziu subliniază faptul că este un cofactor în peste 300 de sisteme enzimatice și susține funcția musculară și nervoasă, producția de energie și structura osoasă. Compușii de magneziu apar, de asemenea, în unele antiacide și laxative, iar metalul magneziu este valoros în aliaje ușoare, acolo unde reducerea masei este esențială.
- Calciu compușii de calciu domină viața de zi cu zi. Calciul contribuie la structura oaselor și a dinților, iar compușii precum carbonatul de calciu și sulfatul de calciu sunt esențiali pentru calcar, ciment, ipsos și rigips. Acest lucru face din calciu una dintre cele mai evidente legături între chimie, biologie și construcții.
Aplicații specializate ale stronțiului și bariului
- Stronțiul sărurile de stronțiu sunt cele mai cunoscute pentru producerea nuanțelor roșii intense în artificii și rachete semnalizatoare. Chiar și cititorii care nu-și amintesc întreaga listă a Grupului 2 își aduc adesea aminte de stronțiu odată ce acesta este asociat cu o culoare.
- Barium compușii de bariu au importanță în industrie și medicină. Profilul bariului NLM descrie utilizările majore în noroiurile de foraj, vopsele, materialele plastice, cărămizi și sticlă. Se menționează, de asemenea, un contrast medical important: sulfatul de bariu, extrem de insolubil, este utilizat ca material radiopac în unele examinări radiologice, deoarece nu este, în general, absorbit de organism.
- Radiu : Radiul este în principal un caz istoric sau unul strict controlat din punct de vedere științific. Pagina NRC despre radiu descrie utilizarea sa anterioară în vopsele luminescente și în terapia precoce a cancerului. Majoritatea acestor utilizări au fost înlocuite, deși mai există încă unele utilizări reglementate, cum ar fi anumite aplicații industriale de radiografie.
De ce forma și tipul de compus sunt importante în utilizarea practică
În cadrul grupului 2, forma utilizată de oameni este adesea compusul, nu metalul pur.
Această singură idee clarifică multă confuzie. Magneziul din alimente sau din medicamente nu este același lucru cu magneziul care arde sub formă de bandă. Calciul din oase nu este același lucru cu metalul reactiv de calciu. Bariul este cel mai clar exemplu de ce forma este esențială: sulfatul de bariu, insolubil, poate fi util în imagistică, în timp ce compușii mai solubili de bariu necesită o atenție mult mai mare. Radiul accentuează și mai mult acest punct, deoarece radioactivitatea sa, nu doar poziția sa printre metale, determină modul în care este manipulat.
Valoarea grupului 2 nu este deloc abstractă. Aceste elemente ajută la explicarea modului în care aceeași familie poate avea importanță în nutriție, materiale, medicină, procesare industrială și reguli de siguranță. O listă scurtă de utilizări reale este adesea suficientă pentru ca modelul general să rămână fixat în memorie.
Concluzii cheie privind elementele grupului 2
Până în acest moment, metalele alcalino-pământoase ar trebui să pară mai puțin o listă de memorat și mai degrabă un model pe care îl puteți citi direct din coloana grupului 2 din tabelul periodic dacă cineva întreabă încă, care sunt metalele alcalino-pământoase , răspunsul scurt rămâne simplu: beriliul, magneziul, calciul, stronțiul, bariul și radiul. O definiție mai completă a metalelor alcalino-pământoase este chiar mai utilă: șase elemente metalice din Grupa 2 care, de obicei, pierd doi electroni din stratul exterior și formează ioni M 2+.
Concluzii cheie despre metalele alcalino-pământoase
- Locația este importantă: aceste șase elemente din Grupa 2 se află în a doua coloană de la stânga, în secțiunea Grupa 2 a blocului s.
- Membrii familiei sunt fixați: Be, Mg, Ca, Sr, Ba și Ra formează întreaga mulțime.
- Chimia comună explică asemănarea familială: configurația lor electronică ns 2modelul de valență determină formarea ionilor +2 ca rezultat comun, un punct esențial sintetizat de LibreTexts.
- Tendințele principale în sens descendent sunt previzibile: raza atomică crește, energia de ionizare scade în general, iar reactivitatea crește de obicei pe măsură ce coborâți în grup.
- Excepțiile sunt importante: beriliul se comportă mai degrabă covalent decât ceilalți, magneziul poate părea mai puțin reactiv din cauza stratului său superficial, iar radiul este discutat în principal în contextul radioactivității.
- În viața reală, este vorba de obicei despre compuși, nu despre metale pure: oamenii întâlnesc carbonatul de calciu, oxidul de magneziu și sulfatul de bariu mult mai des decât calciul, magneziul sau bariul elementar.
The tabelul periodic al metalelor alcalino-pământoase coloana este cea mai ușor de reținut ca fiind formată din șase metale legate de o singură regulă: ele devin, de obicei, ioni 2+, dar fiecare membru exprimă această regulă într-un mod puțin diferit.
De la chimia grupului 2 la piesele metalice proiectate
Această chimie se extinde mult dincolo de manualele școlare. LibreTexts observă că magneziul elementar este produs la scară largă și este utilizat în aliaje ușoare pentru cadrele avioanelor și piesele motorului autovehiculelor. Un ghid mai amplu privind aliajele arată de ce acest lucru este important: inginerii ajustează compoziția și procesarea pentru a echilibra greutatea, rezistența, rezistența la coroziune și prelucrabilitatea în componente reale.
Pentru cititorii care trec de la coloana grupului 2 din tabelul periodic perspectiva teoretică la fabricație, Shaoyi Metal Technology oferă un exemplu practic al acestei conexiuni. Paginile sale dedicate materialelor și prelucrării în domeniul automotive descriu producția pieselor metalice, de la prototipare până la producția de masă, unde comportamentul materialului și controlul procesului trebuie să funcționeze împreună. Acest lucru face ca tabelul periodic al metalelor alcalino-pământoase să fie mai mult decât un grafic pentru clasă. Este, de asemenea, parte integrantă a raționamentului din spatele alegerii metalelor și aliajelor pentru piese inginerite care trebuie să fie ușoare, fiabile și ușor de fabricat.
Întrebări frecvente despre metalele alcalino-pământoase
1. Care sunt cele șase metale alcalino-pământoase?
Cele șase metale alcalino-pământoase sunt beriliul, magneziul, calciul, stronțiul, bariul și radiul. Ele ocupă Grupa 2 din tabelul periodic și sunt grupate împreună deoarece, în mod obișnuit, cedează doi electroni din stratul exterior, determinând astfel o configurație comună de ioni 2+ în numeroase compuși.
2. Cum diferă metalele alcalino-pământoase de metalele alcaline?
Metalele alcaline aparțin Grupului 1 și formează, de obicei, ioni cu sarcină 1+ deoarece au un singur electron în stratul exterior. Metalele alcalino-pământoase se află în Grupul 2, formează, în mod uzual, ioni cu sarcină 2+ și tind să fie mai puțin reactive în ansamblu. Acel electron de valență suplimentar modifică intensitatea legăturilor pe care le formează, modul în care reacționează cu apa și tipurile de săruri și oxizi pe care le formează în mod obișnuit.
3. De ce nu se găsesc metalele alcalino-pământoase în stare liberă în natură?
Aceste metale sunt suficient de reactive încât să nu rămână mult timp în stare elementală pură în mediile naturale. În schimb, se combină cu ioni de oxigen, carbonat, sulfat, clorură sau silicat și devin componente ale mineralelor, rocilor, apei de mare, scoicelor și oaselor. De aceea, oamenii întâlnesc, de obicei, Grupul 2 sub formă de compuși, nu ca eșantioane de metal brut.
4. Reacționează toate metalele alcalino-pământoase cu apa?
Nu, iar aceasta este una dintre cele mai utile excepții de reținut. Beriliul este în mare parte rezistent la apă, magneziul reacționează lent în apă rece din cauza unui strat superficial care limitează reacția, iar calciul, stronțiul și bariul reacționează mai ușor. În general, reactivitatea față de apă devine mai intensă pe măsură ce coborâți în Grupa 2.
5. De ce sunt importante metalele alcalino-pământoase în industrie și fabricație?
Importanța lor provine atât din compușii lor, cât și din rolul lor în alegerea aliajelor. Magneziul este valoros acolo unde contează reducerea greutății, compușii de calciu sunt esențiali pentru ciment și ipsos, iar compușii de bariu sunt aleși pentru utilizări industriale și medicale specializate. În producția reală, înțelegerea comportamentului metalelor ajută la orientarea prelucrării prin așchiere, a stabilității proceselor și a calității pieselor, motiv pentru care furnizori precum Shaoyi Metal Technology subliniază prelucrarea automotive certificată, controlul proceselor și sprijinul oferit, de la piesele prototip până la producția de masă.
 Serii mici, standarde ridicate. Serviciul nostru de prototipare rapidă face validarea mai rapidă și mai ușoară —
Serii mici, standarde ridicate. Serviciul nostru de prototipare rapidă face validarea mai rapidă și mai ușoară —
