Kas ir sārmzemju metāli? 2. grupa beidzot kļūst saprotama
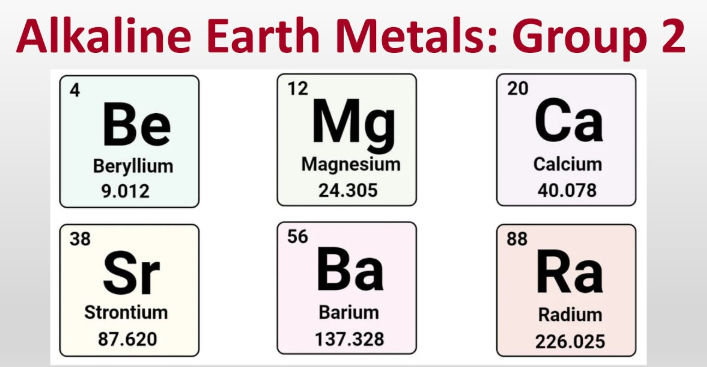
Kas ir sārmzemju metāli?
Ja jūs meklējāt kas ir sārmzemju metāli , šeit ir tiešā atbilde: tie ir seši elementi Grupa 2 periodiskajā tabulā. šī īsa sārmzemju metālu definīcija ir izходpunkts, taču nosaukums arī daudz pastāsta par šīs elementu grupas uzvedību.
Kas ir sārmzemju metāli vienā teikumā
Sārmzemju metāli ir berilijs, magnijs, kalcija, stroncijs, bārijs un radis — seši metāliskie elementi 2. grupā, kas parasti veido +2 lādētus jonus.
- Berilijs (Be)
- Magnijs (Mg)
- Kalcijs (Ca)
- Stroncijs (Sr)
- Bārijs (Ba)
- Rādijs (Ra)
Kāpēc nosaukums „sārmzemju metāli” ir pamatots
Sākotnējiem lietotājiem sārmzemju definīcija kļūst daudz vieglāk saprotama, ja frāzi sadala trīs daļās.
Bāze nozīmē, ka to oksīdi un hidroksīdi ir bāziski, nevis skābi. Zeme ir vēsturisks vārds. Agrīnie ķīmiķi to izmantoja, lai apzīmētu siltumstabīlas, minerālveida vielas, kas nekust nekādā temperatūrā un grūti šķīst ūdenī, ko skaidro Britannica . Metāli nozīmē, ka paši elementi ir metāliski — parasti spīdīgi un labi zaudē elektronus reakcijās.
Tas jums dod pamata alkalīnzemju metālu nozīme neprasot iepriekš sarežģītas ķīmijas zināšanas. Tas ir arī noderīgs īss apraksts par alkalīnzemju metāliem : 2. grupas metālu ģimene ar kopīgu ķīmisko uzvedību, kopīgu atrašanās vietu periodiskajā tabulā un būtisku lomu reālajā pasaulē. Magnijs sastopams sakausējumos un bioloģijā. Kalcija nozīme ir kaulos, čaulās un būvmateriālos. Bārijs, stroncijs un radis sastopami specializētākos kontekstos.
Šis raksts apzināti sākas vienkārši. Skaidrs saraksts ir viegli iemācāms, taču ģimenes būtība kļūst pilnīgi skaidra, kad redz, kur šie elementi atrodas un kāpēc tieši šī vieta nodrošina tiem tik līdzīgu uzvedību.
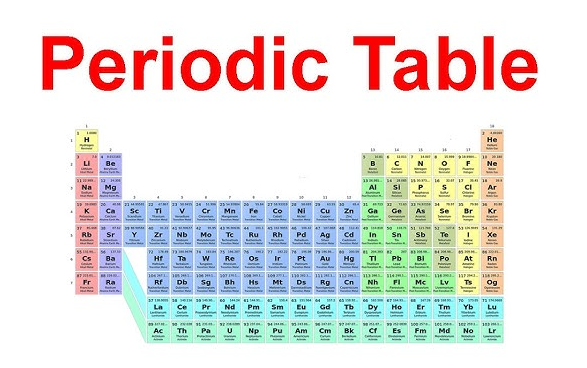
2. grupas atrašanās vieta periodiskajā tabulā
Ģimenes nosaukums kļūst daudz vieglāk iegaumējams, ja to patiešām var atrast. Ja jūs jautājat sev kur alkalīnzemju metālus atrast periodiskajā tabulā , paskatieties uz otro kolonnu no kreisās puses. Šī vertikālā kolonna ir 2. grupa periodiskajā tabulā , tieši blakus alkāliemetalļiem 1. grupā. 2. grupas periodiskā tabula attēls katru reizi parāda to pašu taisni: augšā berilijs, tad magnijs, kalcija, stroncijs, bārijs un radis, kas pārvietojas lejup pa periodiem.
Akvarijā alkalizemju metālu periodiskā tabula diagrammā šie seši elementi pieder s-apakšblokam. To kopīgā atrašanās vieta ir nozīmīga, jo tā atspoguļo kopīgu elektronu izkārtojumu. Kā LibreTexts skaidro, 2. grupas elementiem ir ns 2vērtības elektronkonfigurācija, kas nozīmē, ka tiem ir divi ārējā slāņa elektroni.
Kur alkalizemju metālus atrod periodiskajā tabulā
Vizuāli šis raksturs ir vienkāršs. periodiskās tabulas 2. grupas elementi veido vienu ģimenes kolonnu periodos no 2. līdz 7. Dažādi klasē izmantotie diagrammu attēlojumi izceļ alkaliski zemju metālus periodiskajā tabulā izkārtojumus ar to pašu krāsu, jo elementu ģimenes tiek lasītas vertikāli, nevis horizontāli. Meklējumi pēc periodiskās tabulas alkaliski zemju metālu patiesībā attiecas uz šo vienu kolonnu.
| Elements | Sīkāku informāciju | 2. grupas pozīcija | Tipisks jons | Pazīstama savienojuma forma |
|---|---|---|---|---|
| Berilijs | Be | 2. periods, 2. grupas augšdaļa | Be2+ | BeO |
| Magnijs | Mg | 3. periods | Mg2+ | MgO |
| Kalciju | Ca | 4. periods | Ca2+ | CaCO 3 |
| Stroncijs | Sr | 5. periods | Sr2+ | SrCO 3 |
| Bārijs | Ba | 6. periods | Ba 2+ | BaSO 4 |
| Rādijs | Ra | 7. periods, 2. grupas apakšdaļa | Ra 2+ | RaCl 2 |
Kāpēc 2. grupas elementi veido +2 jonus
Šie divi ārējie elektroni nosaka ķīmisko aktivitāti. 2. grupas atomi parasti zaudē abus elektronus, jo tas nodrošina stabilitāku elektronu izkārtojumu. Rezultātā rodas +2 jons , piemēram, Mg 2+vai Ca 2+. Tāpēc šie metāli bieži veido savienojumus, piemēram, oksīdus, hlorīdus, karbonātus un sulfātus. Šo modeli var redzēt uzreiz formulās: MgO, CaCl 2, CaCO 3, BaSO 4.
Kā ātri atpazīt alkaliski zemju metālu grupu
Ātra identifikācijas viltība ir meklēt vienlaicīgi trīs norādījumus: otrā kolonna, metāliskie elementi un parasti +2 lādiņš. Salīdzinot ar blakus esošajiem alkālijskābajiem metāliem, kuriem ir viens valences elektrons un kuri parasti veido +1 jonus, 2. grupas elementiem ir viens papildu ārējais elektrons, un tie parasti ir mazāk reaģētspējīgi. Tomēr tie acīmredzami pieder pie vienas un tās pašas grupas. Interesantākais ir tas, ka katrs dalībnieks šo modeli izpauž nedaudz citādā veidā, īpaši no berilija augšgalā līdz radiju apakšgalā.
Iepazīstieties ar sešiem alkaliski zemju metāliem
Saraksts ir noderīgs, taču pats par sevi tas nav īpaši atmiņā paliekams. 2. grupa kļūst reālāka, kad katram tās dalībniekam ir skaidra identitāte. Daži sastopami kaulos vai jūras ūdenī. Daži krāso uguņošanas izrādes. Viens galvenokārt ir vēsturisks brīdinājuma signāls. Kopā tie joprojām pieder pie vienas un tās pašas grupas, taču katram ir savs raksturs.
| Elements | Sīkāku informāciju | Bieža izplatība | Izceļošā īpašība | Pielietojums reālajā pasaulē |
|---|---|---|---|---|
| Berilijs | Be | Atrodams minerālos, piemēram, berilā | Ļoti viegls un stingrs metāls | Izmantots specializētās aviācijas un rentgena lietojumprogrammās; putekļi ir bīstami, ja tie tiek ieelpoti |
| Magnijs | Mg | Sastopams jūras ūdenī un minerālos | Zema blīvuma un spilgti balta uguns, degot | Svarīgs vieglo sakausējumu, papildinājumu un bioloģijas jomā |
| Kalciju | Ca | Sastopams klintīs, kaulos, vēžu čaulās un mēlītē | Bioloģiski pazīstams 2. grupas jons | Būtisks skeletam, cementam, ģipsim un daudziem dabiskajiem minerāliem |
| Stroncijs | Sr | Galvenokārt sastopams celestitā un stroncijitā | Sāls sadegšanas laikā rada spilgti sarkanu liesmu | Izmantots ugunskuršu, signāllukturu, spožo materiālu un dažu zobārsta produktu ražošanā |
| Bārijs | Ba | Parasti saistīts ar barītu | Blīvs, smags alkalizemju metāls | Bārija sulfāts ir svarīgs urbšanā un medicīniskajā attēlošanā; šķīstošiem bārija savienojumiem jāpievērš uzmanība |
| Rādijs | Ra | Sastopams pēdu daudzumos urāna rūdās | Spēcīgā radioaktivitāte dominē tā ķīmijas vēsturē | Mūsdienās galvenokārt vēsturiska vai stingri kontrolēta zinātniska nozīme |
Berilijs un magnijs — 2. grupas augšējās pozīcijās
Laiks elements berilijs atrodas šīs ģimenes augšgalā un jau norāda, ka 2. grupa nav pilnīgi vienmērīga. To bieži saista ar minerālu berilu, kas pieder pie tās pašas minerālu ģimenes, kurā ietilpst arī smaragds un akvamarīns. Berilijs izceļas ar to, ka tas ir neparasti viegls un stingrs. Tas padara to noderīgu augstas veiktspējas detaļās, kur svarīga maza masa. Tajā pašā laikā berilijs ir materiāls, kuram rūpnieciskajā vidē jāpievērš uzmanība, jo smalks putekļains berilijs var būt kaitīgs, ja tiek ieelpots. Tāpēc to atceras gan kā augstas veiktspējas materiālu, gan kā materiālu, ar ko jārīkojas uzmanīgi.
Magnijs izjūtas daudz pazīstamāks. magnija ķīmiskais simbols ir Mg, un tas ir viens no viszinātākajiem šīs grupas metāliem, jo tas sastopams jūras ūdenī, parastos minerālos un dzīvajos organismos. Tas ir ļoti viegls metāls, un, degot, tas rada spilgtu baltu gaismu. Tāpēc magnijs jau sen ir saistīts ar signālluktām un spilgti degošiem materiāliem. Ikdienas dzīvē tomēr lielākā daļa cilvēku ar to saskaras mierīgākās formās, piemēram, kā uztura komponentu, kā antacīdu savienojumu vai kā vieglās sakausējumus, kurus izmanto tad, kad svarīga masas samazināšana.
Kalcija un stroncija izmantošana ikdienas materiālos
Kalcija elements ir visvairāk pazīstamais 2. grupas pārstāvis daudziem lasītājiem. Tas sastopams kaļķakmenī, krītā, vēžu čaulās un kaulos, tāpēc tas ķīmiju saista gan ar ģeoloģiju, gan ar bioloģiju gandrīz uzreiz. Kalcija karbonāts šajā kontekstā ir pazīstamā viela. Tas palīdz izskaidrot, kāpēc viena un tā pati ķīmisko elementu grupa ir nozīmīga gan alūnu veidošanā, gan būvmateriālu ražošanā, gan skeletu veidošanā. Pats kalcija metāls ir reaktīvs, taču kalcija savienojumi ir visur, tāpēc šis elements bieži šķiet pazīstamāks nekā eksotisks.
Stronciju ir vieglāk atcerēties, ja to saista ar krāsu. stroncija simbols ir Sr, un stroncijs tas ir galvenokārt atrasts minerālos cēlestītā un stroncijītā. Karaliskā ķīmijas sabiedrība to apraksta kā mīkstu, sudrabbaltu metālu, kas deg gaisā un reaģē ar ūdeni. Tā sāļi ir slaveni ar spilgti sarkano krāsu rašanos uguņošanas izstrādājumos un signālluktās. Tas pats avots min arī lietojumu gaismu izstarojošos materiālos un stroncija hlorīda heksahidrātu zobiem jutīgai zobu pastai. Tas padara stronciju par lielisku piemēru tam, kā elements var būt ķīmiski reaktīvs, tomēr lielākoties tiek sastapts caur savienojumiem.
Bārijs un rādijs uzlabotajos vai specializētajos kontekstos
Laiks bārija elements bieži tiek atcerēts pēc smaguma. Tas bieži saistīts ar barītu, un viena no tā pazīstamākajām savienojumu ir bārija sulfāts. Šis savienojums ir svarīgs, jo tas ir ļoti nešķīstošs, kas palīdz izskaidrot, kāpēc bārijs var parādīties praktiskos pielietojumos, piemēram, urbšanas šķidrumos un medicīniskajā attēlošanā, kamēr citus šķīstošus bārija savienojumus apstrādā uzmanīgāk to toksicitātes dēļ. Bārijs atgādina lasītājiem, ka Grupas 2 elementa noderīgā forma bieži ir savienojums, nevis spīdošais metāls pats par sevi.
Rādijs atrodas ģimenes apakšā, taču tas neiekļaujas klusējoši. Uz rādijs periodiskajā tabulā skatoties uz Ra, tas norāda punktu, kur radioaktivitāte kļūst par noteicošo īpašību. Rādijs dabā sastopams tikai niecīgos daudzumos, parasti saistīts ar urāna rūdām. Vēsturiski tas kļuva slavens dēļ luminiscējošajiem krāsas maisījumiem un agrīnajiem medicīniskajiem eksperimentiem. Mūsdienās tā bīstamība rodas no radioaktivitātes, nevis no parastās metāla īpašībām, tāpēc to apstrādā stingrā kontroles režīmā. Vienkāršotā veidā — rādijs joprojām pieder 2. grupai, taču to apspriež gan ķīmijas, gan kodoldrošības aspektā.
Ja šos sešus elementus novieto vienu blakus otram, šī ģimene vairs neatgādina vienkāršu vārdu sarakstu. Elementu izmērs, reaktivitāte, biežāk sastopamās savienojumu formas un pat to, kā katrs elements parādās ikdienas dzīvē, mainās, pārvietojoties lejup pa grupu. Šī mainīgā rakstura paradigma ir tieši tā, kur 2. grupa kļūst īpaši noderīga, jo secība no berilija līdz rādijam sāk atklāt likumsakarības, nevis vienkārši nevajadzīgu informāciju.
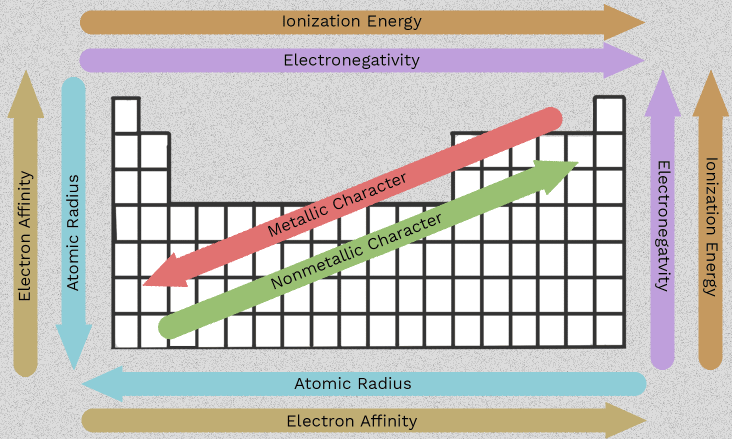
Sārmzemju metālu īpašības un 2. grupas likumsakarības
Tas, ka kārtība mainās no berilija līdz radijam, ir tas, kas padara 2. grupu noderīgu. Nevis jāiegaumē seši atsevišķi fakti, bet gan var sekot dažiem paraugiem, kas atkārtojas visā kolonnā. Svarīgākais alkaliski zemju metālu īpašības visi izriet no vienas kopīgas iezīmes: katram atomam ir divi ārējie elektroni, kurus tas parasti zaudē.
Kad redzat, kā lielums, elektronu aizsegšana un jonizācijas enerģija mainās grupā uz leju, šī elementu ģimene kļūst daudz vieglāk prognozējama. Šīs alkaliski zemju metālu raksturīgās īpašības nav tikai eksāmenu faktu. Tās skaidro, kāpēc daži grupas locekļi reaģē ātrāk, kāpēc daži savienojumi labāk šķīst nekā citi un kāpēc daži trendi prasa rūpīgu formulēšanu, nevis vienkāršus bultu zīmējumus.
Alkaliski zemju metālu kopīgās īpašības
Vairums 2. grupas locekļu ir sudrabbalti metāli, kas parasti veido M 2+joni un veido galvenokārt joniskus savienojumus. Tie rīkojas kā reducētāji, jo zaudē elektronus. Salīdzinājumā ar 1. grupas metāliem tie parasti ir mazāk reaktīvi, tomēr viņi joprojām ir pietiekami ķīmiski aktīvi, lai veidotu daudzus izplatītos oksīdus, hlorīdus, karbonātus un sulfātus.
Vienkāršs veids, kā sistematizēt sārmzemju metālu ķīmiskās īpašības ir atdalīt to, kas paliek nemainīgs, no tā, kas mainās. Nemainīgs paliek parastais +2 oksidācijas pakāpes stāvoklis. Mainās tas, cik viegli katrs elements atdod šos divus elektronus. Tieši šeit sāk uzrādīties tendences.
Tendences 2. grupā virzienā uz leju un to nozīme
Datus, ko savācis LibreTexts, un tendenču skaidrojumus no Save My Exams rāda vienu un to pašu vispārējo modeli. Atomu rādiuss palielinās no 112 pm (Be) līdz 253 pm (Ba), kamēr pirmās ionizācijas enerģija samazinās no 900 līdz 503 kJ/mol. Vienkāršā valodā — ārējie elektroni atrodas tālāk no kodola un ir aizsargāti ar vairāk iekšējām apvalku slāņiem, tāpēc tos ir vieglāk noņemt.
| Riedonu | Virziens 2. grupā uz leju | Ķīmiskais iemesls | Ko tas praktiski nozīmē |
|---|---|---|---|
| Atomu rādiuss | Palielina | Katram elementam ir vēl viena elektronu apvalka slānis un lielāka aizsegšana | Lielāki atomi ārējos elektronus tur mazāk cieši |
| Pirmā un otrā jonizācijas enerģija | Samazinās kopumā | Ārējie elektroni atrodas tālāk no kodola, tāpēc pievilkšana ir vājāka | M veidošanās 2+kļūst vieglāka |
| Reaktivitāte | Palielinās kopumā | Zemākas jonizācijas enerģijas padara elektronu zudumu vieglāku | Smagākie elementi reaģē intensīvāk ar skābēm, skābekli un bieži arī ar ūdeni |
| Šķidrumtemperatūra | Parasti samazinās, taču nevienmērīgi | Lielāki metālu joni vājina metālisko saiti, tomēr arī struktūra ir svarīga | Izmantojiet vārdu "vispārīgi", jo Mg un Ca neatbilst pilnīgi vienmērīgai līnijai |
| Blīvums | Neregulārs | Masa, atomlielums un metālu iepakojums mainās vienlaikus | Blīvumu nevar uzskatīt par vienkāršu lejupejošu tendenci |
| Hidroksīdu šķīstamība | Palielina | Režģa enerģijas un hidratācijas enerģijas līdzsvars mainās grupā uz leju | Smagākie hidroksīdi veido spēcīgāk alkaliskas šķīdumus |
| Sulfātu šķīstamība | Samazina | Hidratācijas enerģija samazinās, kad kations kļūst lielāks | Savienojumi, piemēram, BaSO 4kļūst ļoti nešķīstoši |
Blīvums un kušanas uzvedība ir divas tendences, kurās skolēni bieži pārvērtē vienkāršošanu. Blīvums nemainās taisnā līnijā, jo gan masa, gan tilpums mainās, un metāla atomi kristālos nepakojas vienādi katrā gadījumā. Arī kušanas temperatūrām jāpievērš uzmanība. Parasti tās samazinās, jo lielāki joni vājina metālisko režģi, taču Mg ir nenobīdīti zema kušanas temperatūra — 650 °C, kamēr Ca tā palielinās līdz 842 °C, pirms vērtības atkal samazinās. Tāpēc viena no drošākajām alikaliski zemes metālu raksturīgajām īpašībām ir šī: vispārējā tendence ir reāla, bet fiziskie detalizētie rādītāji nav pilnīgi gludi.
Šķīstamībai arī piemīt tāda pati brīdinājuma etiķete. Nav neviena vienota noteikuma, kas attiektos uz visiem 2. grupas sāļiem. Hidroksīdi kļūst šķīstāki, ejot lejup pa grupu, savukārt sulfāti kļūst mazāk šķīstoši. Ja kāds saka: «šķīstamība palielinās, ejot lejup pa 2. grupu», svarīgākais jautājums ir: «Kuri savienojumi?»
Kāpēc zemes alkālijs metāli reaģē tā, kā viņi to dara
Tātad, vai zemes alkālijs metāli ir reaktīvi ? Jā, un vispārīgā atbilde ir, ka viņu reaktīvums palielinās, pārvietojoties uz leju. Iemesls ir tas pats elektronu stāsts, ko redzējām iepriekš. Zemākas pirmās un otrās jonizācijas enerģijas nozīmē, ka atomiem ir vieglāk zaudēt divus elektronus un ātrāk sasniegt parasto M 2+stāvokli.
Tas ietekmē reālās reakcijas. Grupā uz leju reakcijas ar atšķaidītām skābēm notiek ātrāk, reakcijas ar skābekli kļūst intensīvākas, un smagākie elementi ir vieglāk oksidēt. Save My Exams norāda, ka bārijs ir tik reaktīvs, ka to jāglabā zem eļļas, kas ir praktisks pierādījums tam, cik tālu var aizvest reaktīvuma tendenci.
- Atomu rādiuss palielinās 2. grupā uz leju.
- Jonizācijas enerģija samazinās 2. grupā uz leju.
- Reaktīvums palielinās, jo divu elektronu zaudēšana kļūst vieglāka.
- Kausēšanās temperatūrai un blīvumam raksturīgas neatbilstības, tāpēc izvairieties no absolūtiem noteikumiem.
- Hidroksīdi un sulfāti parāda pretējas šķīstošuma tendences.
Šie raksturīgie pazīmes padara šo elementu grupu paredzamu, bet ne pilnīgi vienmērīgu. Tieši grupas augšdaļā berilija jau sāk pārkāpt noteikumus, un magnijs pievieno vēl vienu ikdienišķu izņēmumu, kas ir svarīgāks, nekā daudzi iesācēji sagaida.
Sārmiskos un sārmzemju metālus
Vispārīgie raksturīgie pazīmes padara 2. grupu vieglāk apgūstamu, taču šī elementu grupa zaudē nozīmi, ja katru tās locekli uzskata par identisku. Lielākais brīdinājuma signāls ir berilijs. Magnijs pievieno praktiskāku ikdienišķu izņēmumu. Un kad cilvēki salīdzina sārmiskos un sārmzemju metālus , līdzīgi nosaukumi var slēpt ļoti atšķirīgu ķīmisko uzvedību.
Kāpēc berilijs neuzvedas kā tipisks 2. grupas metāls
BYJU'S apraksta beriliju kā acīmredzamu izņēmumu 2. grupā. Tā nenobrieduši mazais izmērs, augstā jonizācijas enerģija un spēcīgā polarizējošā ietekme rada uzvedību, kas ir mazāk raksturīga šai elementu grupai. Vienkāršā valodā: Be 2+spēcīgi pievelk tuvējās elektronu mākoņus, tāpēc berilija savienojumi bieži ir vairāk kovalenti nekā smagāko grupas locekļu veidotie jonišķākie savienojumi. Tas pats avots norāda arī, ka berilijam ir augstāka kušanas un viršanas temperatūra nekā pārējiem grupas elementiem un ka tas nereaģē ar ūdeni tāpat kā tās grupas pārējie locekļi.
Magnijs nav tik neparasts kā berilijums, tomēr tas var šķist mazāk reaktīvs, nekā skolēni sagaida. LibreTexts norāda, ka ļoti tīrs magnijs reaģē tikai vāji ar aukstu ūdeni, un reakcija drīz palēninās, jo gandrīz nešķīstošais magnija hidroksīds veido barjeru uz virsmas. Grupas apakšā radiju parasti apspriež atsevišķi, jo tā radioaktivitāte dominē praktiskajā izmantošanā un drošības diskusijās.
Kā alkalizemju metāli atšķiras no alkāliemetāliem
Vienkārši alkālijs vs alkalizemju izteiksmē, 1. grupas metāli zaudē vienu ārējo elektronu, kamēr 2. grupas metāli zaudē divus. Šis vienīgais atšķirības faktors vairāk nekā jebkas cits nosaka alkāliemetālu un alkalizemju metālu īpašības vairāk nekā gandrīz jebkas cits.
| Iezīme | Sārmu metāli, 1. grupa | Sārmzemju metāli, 2. grupa |
|---|---|---|
| Vērtības elektroni | 1 | 2 |
| Tipisks jons | M + | M 2+ |
| Reakcija ar aukstu ūdeni | Bieži strauja vai pat vardarbīga, veidojot hidroksīdu un ūdeņradi | Mazāk vienmērīga: berilijs nereaģē ar ūdeni, magnijs reaģē mierīgi, kalcija, stroncija un bārija reakcija kļūst arvien straujāka |
| Raksturīgā skābekļa ķīmija | Var veidot oksīdus, peroksīdus vai superoksīdus | Parasti veido monoksīdus; lielākā daļa šo oksīdu ūdenī veido hidroksīdus, taču BeO ir izņēmums |
Svarīgi izņēmumi, kurus skolēni bieži nepamanā
- Ne katrs 2. grupas metāls reaģē ar ūdeni vienādi.
- Berilija savienojumi ir vairāk kovalenti nekā pārējās šīs grupas vielas.
- Nesajauciet sārmu un sārmzemju metālus kā vienu un to pašu grupu tikai tāpēc, ka to nosaukumi skan līdzīgi.
- Laiks sārmu metālu un sārmzemju metālu īpašības ir vislabāk apgūt kā paraugus ar izņēmumiem, nevis kā stingrus devīzus.
Tas ir arī labākais veids, kā saprast ķīmiskās īpašības sārmu metāliem un sārmzemju metāliem . Elektronu struktūras jums sniedz likumu, bet reālās vielas pievieno papildu nianses. Un šīs nianses kļūst vēl skaidrākas, ja aplūkojat, kur faktiski sastopamas 2. grupas elementu vielas: reti kā tīri metāli un daudz biežāk minerālos, akmeņos, jūras ūdenī, kaulos un rūpnieciskos savienojumos.
Kā sārmzemju metāli sastopami dabā
Ja jūs iedomājaties zemes alkālijs metālu kā spožu, tīru paraugu, kas atrodas klintī, daba rīkojas citādi. 2. grupas elementi ir pietiekami reaktīvi, lai parasti parādītos kā joni minerālos, sāļos, klintīs, jūras ūdenī, kaulos un vāku ādā, nevis kā brīvie metāli. Neatkarīgi no tā, vai kāds meklē zemes alkālijs metālus vai vairāk standarta terminu, dabiskais raksts ir vienāds: šī elementu ģimene stingri izvēlas savienojumus.
Šis raksts tieši izriet no zemes alkālijs metālu ķīmiskajām īpašībām tie parasti zaudē divus ārējos elektronus un veido stabili M 2+jonus. Kad tas notiek, skābeklis, karbonāta, sulfāta un halīda joni viegli saista tos cietos savienojumos, kas var pastāvēt ģeoloģijā un bioloģijā.
Kāpēc zemes alkālijs metāli dabā netiek atrasti brīvā veidā
Britannica un ThoughtCo abi apraksta 2. grupu kā reaktīvu, kas izskaidro, kāpēc šie elementi reti tiek atrasti neatombinētā veidā. Gaisā daudzi ātri veido oksīdu pārklājumus. Dabiskajās vides apstākļos tie tiek stabilizēti vēl vairāk kā karbonāti, sulfāti, silikāti, fluorīdi vai hlorīdi. Tāpēc kalcija savienojumi sastopami mēlītā un gliemežu čaulās, magnijs — minerālos un jūras ūdenī, stroncijs vai bārijs — rudas atradnēs. Rādijs ir vēl retāk sastopams, tas rodas tikai pēdas daudzumos urāna rudos.
Bieži sastopamie 2. grupas minerāli un savienojumi
| Elements | Bieži sastopamais dabiskais avots | Pazīstama savienojuma forma | Kāpēc šis savienojums ir nozīmīgs |
|---|---|---|---|
| Berilijs | Berils | BeO | Berils ir komerciāls šī elementa avots, bet berilija oksīds ir svarīgs savienojums specializētu materiālu ražošanā |
| Magnijs | Magnīta, dolomīts, jūras ūdens | MgCO₃ 3vai Mg(OH)₂ 2 | Paskaidro, kāpēc magnijs biežāk sastopams minerālos, jūras ūdenī un medicīnā nekā tīrā metāla veidā |
| Kalciju | Dolomīts, mēls, marmors, ģipsis, kauli, vākuļi | CaCO 3 | Sasaista ģeoloģiju, būvmateriālus un skeletus vienā ļoti izplatītā savienojumā |
| Stroncijs | Celestits, stroncijanīts | SrSO₄ 4vai SrCO₃ 3 | Šie minerāli ir galvenie naturālie stroncija savienojumu avoti |
| Bārijs | Bārīts, viterīts | BaSO 4 | Bārīts ir galvenais rūdas veids, un bārija sulfāts ir viens no pazīstamākajiem bārija savienojumiem |
| Rādijs | Uzskaitīti pēdās urāna rūdās — pītblendē un citās | RaCl 2 | Tā retums un radioaktivitāte padarīja rādija savienojumus vēsturiski svarīgus, bet reti sastopamus |
EBSCO norāda, ka kalcija un magnija savienojumi jūras ūdenī ir arī aptuveni 0,4 g/L un 1,3 g/L attiecīgi. Tas palīdz izskaidrot, kāpēc šis alkaliski zemīgie metāli elements saistās ne tikai ar rūdām, bet arī ar cieto ūdeni, jūras sistēmām un dzīvām audu struktūrām.
Kā šos metālus izolē no to savienojumiem
Tā kā 2. grupas metāli parasti ir iekļauti savienojumos, to iegūšana sākas ar rūdām, brīnēm vai minerālu nogulsnēm. Visizplatītākā rūpnieciskā metode ir vienkārša: vispirms pārvērst materiālu vieglāk apstrādājamā oksīdā vai halīdā, pēc tam izmantot elektrolīzi vai ķīmisko reducēšanu, lai atbrīvotu metālu. Encyclopædia Britannica apraksta magnija, kalcija, stroncija un bārija agrīno izolāciju ar elektrolīzi, kamēr EBSCO norāda, ka mūsdienu ražošanā joprojām bieži izmanto kausētu hlorīdu, oksīdu reducēšanu vai citus līdzīgus procesus, atkarībā no konkrētā elementa. Berilija piemērs noder kā noderīgs atgādinājums, ka šī elementu grupa nav pilnīgi vienveidīga, jo beriliju var iegūt, reducējot berilija fluorīdu.
Tāpēc ikdienas dzīvē cilvēki parasti sastop 2. grupu kalcija karbonātā (kaļķakmenī), ģipsī, jūras ūdens magnijā, barijā vai bioloģiskajā kalcijā, nevis kā čistus metāla paraugus. Šis nianses ir svarīgas, jo šo elementu reālās pasaules nozīme daudz vairāk saistīta ar to savienojumiem un formām nekā ar pašiem čistajiem metāliem.
Šķeldmetālu piemēri ikdienas dzīvē
2. grupa kļūst daudz atmiņā paliekamāka, ja katru elementu saista ar kaut ko reālu. Kauli, zobu pastas, ģipsis, uguņošanas izstrādājumi, urbšanas šķidrumi un vecās luminiscējošās ciparnīcas ir visi noderīgi piemēri. šķeldmetālu piemēri ja jums kādreiz radusies šāda doma vai magnijs ir metāls vai nemetāls vai vai Ca ir metāls , abu jautājumu atbildes ir vienkāršas: magnijs un kalcija ir metāli. Tomēr ikdienas dzīvē cilvēki parasti sastop šīs vielas kā savienojumus, nevis kā čistus metāla paraugus.
Magnija un kalcija savienojumu ikdienas lietojumi
- Magnijs : Magnijs ir viens no bioloģiski svarīgākajiem sārmzemju elementi - Jā. Parasti NIH magnija informācijas lapa norāda, ka tas ir kofaktors vairāk nekā 300 enzīmu sistēmās un atbalsta muskuļu un nervu funkcijas, enerģijas ražošanu un kaulu struktūru. Magnija savienojumi arī ietilpst dažos zobu līdzekļos un caurejas līdzekļos, kamēr magnija metāls tiek vērtēts vieglo sakausējumu ražošanā, kur svarīga ir masas samazināšana.
- Kalciju kalcija savienojumi dominē ikdienas dzīvē. Kalcijam ir būtiska nozīme kaulu un zobiem, nodrošinot to struktūru, un savienojumi, piemēram, kalcija karbonāts un kalcija sulfāts, ir centrāli materiāli dolomītā, cementā, ģipsī un sausajās sienās. Tādējādi kalcijam ir viena no skaidrākajām saitēm starp ķīmiju, bioloģiju un būvniecību.
Stroncija un bārija specializētas lietojumprogrammas
- Stroncijs stroncija sāļi visvairāk pazīstami ar spilgti sarkano krāsu ražošanu uguņošanas izrādēs un signālu ugunīs. Pat lasītāji, kuri neatceras pilnu 2. grupas elementu sarakstu, bieži atceras stronciju, tiklīdz tam tiek piesaistīta krāsa.
- Bārijs bārija savienojumi ir nozīmīgi rūpniecībā un medicīnā. NLM bārija profils apraksta galvenās lietošanas vietas urbšanas šķidrumos, krāsās, plastmasās, ķieģeļos un stiklā. Tajā minēts arī svarīgs medicīniskais kontrasts: ļoti nešķīstošais bārija sulfāts tiek izmantots kā rentgenopārredzams materiāls dažās rentgena pārbaudēs, jo tas parasti netiek uzsūkts organismā.
- Rādijs : Rādijs lielākoties ir vēsturisks vai stingri kontrolēts zinātnisks gadījums. NRC rādija lapa apraksta tā iepriekšējo lietošanu luminiscējošajās krāsās un agrīnajā vēža terapijā. Lielākā daļa no šiem lietojumiem ir aizvietota, tomēr daži regulēti lietojumi joprojām pastāv, piemēram, noteiktas rūpnieciskās radiogrāfijas lietojumprogrammas.
Kāpēc forma un savienojuma tips ir svarīgi praktiskā lietošanā
II grupā cilvēki bieži izmanto savienojumu, nevis tīro metālu.
Šī vienīgā ideja novērš daudz neskaidrību. Magnijs pārtikā vai zālēs nav tas pats, kas degošs magnija lentīte. Kalcija kaulos nav tas pats, kas reaģējošs kalcija metāls. Bārijs ir visskaidrākais piemērs tam, kāpēc forma ir būtiska: nešķīstošais bārija sulfāts var būt noderīgs attēlošanā, kamēr šķīdīgāki bārija savienojumi prasa daudz lielāku uzmanību. Rādijs vēl vairāk pastiprina šo domu, jo tā radioaktivitāte, nevis tikai tā vieta starp metāliem, nosaka to, kā ar to jārīkojas.
Tātad 2. grupas vērtība vispār nav abstrakta. Šie elementi palīdz izskaidrot, kā viena un tā pati ģimene var būt nozīmīga uzturā, materiālos, medicīnā, rūpnieciskajā apstrādē un drošības noteikumos. Bieži vien pietiek ar īsu reālu lietojumu sarakstu, lai lielāks modelis paliktu prātā.
Galvenie secinājumi par 2. grupas elementiem
Šajā brīdī zemesalkaliskie metāli vajadzētu likties mazāk kā jāiegaudo saraksts un vairāk kā modelis, ko var lasīt tieši no 2. grupas periodiskajā tabulā kolonnas. Ja kāds joprojām jautā, kas ir zemes alkālijskābju metāli , īsā atbilde paliek vienkārša: berilijs, magnijs, kalcija, stroncijs, bārijs un radiums. Pilnīgāka zemes alkālijskābju metālu definīcija ir pat vēl noderīgāka: seši metāliskie elementi 2. grupā, kas parasti zaudē divus ārējos elektronus un veido M 2+jonus.
Galvenie secinājumi par zemes alkālijskābju metāliem
- Atrašanās vieta ir svarīga: šie seši 2. grupas elementi atrodas otrajā kolonnā no kreisās puses, s-bloka 2. grupas daļā.
- Ģimenes locekļi ir fiksēti: Be, Mg, Ca, Sr, Ba un Ra veido visu kopu.
- Kopīgā ķīmija izskaidro ģimenes līdzību: viņu ns 2vērtības modelis rada +2 jonus kā parasto rezultātu — galveno punktu kopsavilkumā sniedz LibreTexts.
- Galvenās tendences lejup ir paredzamas: atomu rādiuss palielinās, jonizācijas enerģija parasti samazinās un reaktivitāte parasti palielinās, pārvietojoties grupā uz leju.
- Izņēmumi ir svarīgi: berilija uzvedība ir vairāk kovalenta nekā citu elementu, magnijs var šķist mazāk reaktīvs tāpēc, ka tam ir virsmas kārta, un radiju galvenokārt apspriež saistībā ar tā radioaktivitāti.
- Ik ikdienas dzīvē parasti runa ir par savienojumiem, nevis par tīriem metāliem: cilvēki sastop kalcija karbonātu, magnija oksīdu un bārija sulfātu daudz biežāk nekā elementāro Ca, Mg vai Ba.
Laiks skaņas zemes metālu periodiskā tabula kolonna ir visvieglāk atcerēties kā seši metāli, kas saistīti ar vienu likumu: parasti tie veido 2+ jonus, taču katrs šīs grupas loceklis šo likumu izpauž nedaudz citādā veidā.
No 2. grupas ķīmijas līdz inženierētiem metāla komponentiem
Šī ķīmija aptver daudz vairāk nekā tikai mācību grāmatas. LibreTexts norāda, ka elementāro magniju ražo lielos daudzumos un izmanto vieglo sakausējumu izgatavošanai lidmašīnu korpusiem un automobiļu dzinēju daļām. Plašāks sakausējumu pamācības materiāls parāda, kāpēc tas ir svarīgi: inženieri pielāgo sakausējuma sastāvu un apstrādes procesus, lai reālos komponentos sasniegtu optimālu līdzsvaru starp svaru, izturību, korozijas izturību un apstrādājamību.
Lasītājiem, kas pāriet no 2. grupas periodiskajā tabulā skatpunkta uz ražošanu, Shaoyi Metal Technology sniedz praktisku piemēru šai saistībai. Tās automašīnu materiālu un apstrādes lapas apraksta metāla daļu ražošanu no prototipēšanas līdz masveida ražošanai, kur materiāla uzvedībai un procesa kontrolei ir jādarbojas kopā. Tas padara skaņas zemes metālu periodiskā tabula vairāk nekā klases tāfeles diagrammu. Tas ir arī loģikas pamatā, izvēloties metālus un sakausējumus inženierijas daļām, kurām ir jābūt vieglām, uzticamām un ražojamām.
Bieži uzdotie jautājumi par zemes alkāliju metāliem
1. Kuri ir seši zemes alkāliju metāli?
Seši zemes alkāliju metāli ir berilijs, magnijs, kalcija, stroncijs, bārijs un radiums. Tie aizņem 2. grupu periodiskajā elementu tabulā un ir savākti kopā, jo parasti zaudē divus ārējos elektronus, kas rada kopīgu 2+ jona modeli daudzos savienojumos.
2. Kā zemes alkāliju metāli atšķiras no alkāliju metāliem?
Alkālijs metāli pieder 1. grupai un parasti veido 1+ jonus, jo tiem ir viens ārējais elektrons. Alkālzemju metāli atrodas 2. grupā, parasti veido 2+ jonus un vispārīgi ir mazāk reaktīvi. Tas viens papildu vērtības elektrons maina to saistīšanās stiprumu, to reakciju ar ūdeni un sāļu un oksīdu veidus, ko tie parasti veido.
3. Kāpēc alkālzemju metālus dabā neatrod brīvā veidā?
Šie metāli ir pietiekami reaktīvi, lai dabiskos apstākļos ilgu laiku neuzglabātos kā tīri elementāri metāli. Vismazāk viņi savienojas ar skābekli, karbonāta, sulfāta, hlorīda vai silikāta joniem un kļūst par minerālu, akmens, jūras ūdens, čaulu un kaulu sastāvdaļu. Tāpēc cilvēki parasti sastop 2. grupas elementus caur to savienojumiem, nevis kā tīrus metāla paraugus.
4. Vai visi alkālzemju metāli reaģē ar ūdeni?
Nē, un tas ir viens no noderīgākajiem izņēmumiem, ko vajag atcerēties. Berilija reakcija ar ūdeni ir ļoti maza, magnijs reaģē lēni ar aukstu ūdeni, jo virsmas kārtiņa ierobežo reakciju, bet kalcija, stroncija un bārija reakcija notiek vieglāk. Vispārīgi ņemot, ūdens reaktivitāte palielinās, pārvietojoties lejup pa 2. grupu.
5. Kāpēc alkālzemju metāli ir svarīgi rūpniecībā un ražošanā?
To nozīme izriet gan no to savienojumiem, gan no to lomas sakausējumu izvēlē. Magnijs ir vērtīgs tajos gadījumos, kad ir svarīgs zemāks svars, kalcija savienojumi ir centrāli cementa un ģipša ražošanā, bet bārija savienojumi tiek izvēlēti specializētām rūpnieciskām un medicīniskām lietojumprogrammām. Patiesajā ražošanā metālu uzvedības izpratne palīdz vadīt apstrādi, procesa stabilitāti un detaļu kvalitāti, tāpēc piegādātāji, piemēram, Shaoyi Metal Technology, uzsvēr certificētu automobiļu apstrādi, procesa kontroli un atbalstu no prototipa detaļām līdz masveida ražošanai.
 Mažas partijas, augsti standarti. Mūsu ātra prototipēšanas pakalpojums padara validāciju ātrāku un vieglāku —
Mažas partijas, augsti standarti. Mūsu ātra prototipēšanas pakalpojums padara validāciju ātrāku un vieglāku —
