Kokie yra metalai periodinėje elementų lentelėje? Skaičius, kurį dauguma puslapių praleidžia
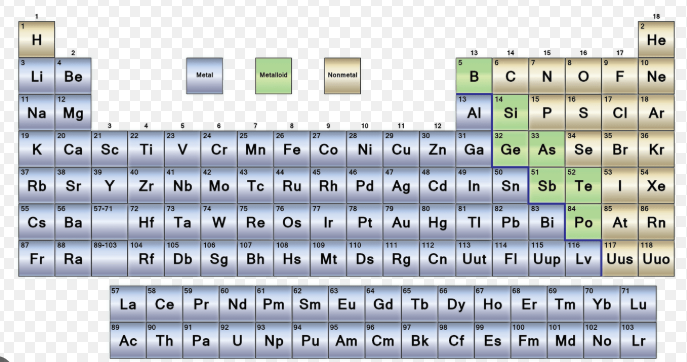
Kokie yra metalai periodinėje elementų lentelėje?
Jei ieškojote, kokie yra metalai periodinėje elementų lentelėje, trumpas atsakymas paprastesnis, nei atrodo iš pirmo žvilgsnio. Metalai – tai elementai, kurie dažniausiai elgiasi įprastu metaliniu būdu, pvz., laiduoja elektros srovę, atspindi šviesą, lenkiami be įtrūkimų ir reaguodami praranda elektronus.
Tiesioginis atsakymas į klausimą „Kokie yra metalai periodinėje elementų lentelėje?“
Metalai – tai periodinės elementų lentelės elementai, kurie dažniausiai parodo metalinį elgesį. Dauguma jų gerai laiduoja šilumą ir elektros srovę, dažnai turi blizgesį, paprastai yra plastiški ir vilkiami bei linkę sudaryti teigiamus jonų praradę elektronus. Dauguma žinomų elementų yra metalai, nors tikslus jų skaičius gali šiek tiek skirtis priklausomai nuo to, kaip klasifikuojami ribiniai elementai.
Paprasčiausiai tariant, skaitytojai, kurie klausia, kokie yra metalinių elementų periodinėje lentelėje klausiama apie didžiąją grupę, kurioje yra žinomi pavyzdžiai, tokie kaip natrius, aliuminis, geležis, varis, sidabras ir aukso.
Kodėl dauguma elementų priskiriami metalams
Dauguma elementų priskiriama metalų kategorijai dėl jų išorinių elektronų elgesio. Metalai paprastai praranda elektronus lengviau nei nemetalai, todėl jie sudaro teigiamus jonų ir daugelis jų gerai laiduoja šilumą bei elektros srovę. Britannica nurodo, kad maždaug trys ketvirtadaliai žinomų cheminių elementų yra metalai, ir LibreTexts apibūdina metalus kaip elementus, kurie dažnai sudaro teigiamus jonų prarasdami elektronus.
- Dauguma elementų lentelėje yra metalai.
- Pagrindinės savybės apima laidumą, blizgesį, plastiškumą ir tempimą.
- Metalai paprastai praranda elektronus cheminių reakcijų metu.
- Periodinės elementų lentelės metalų ir nemetalų modelis tampa lengviau suprantamas, kai pastebite ir ribinę metaloidų grupę.
- Tikslus metalų skaičius ne visada pateikiamas vienodai kiekviename grafike.
Paskutinė ši detalė yra svarbesnė, nei atrodo, nes klasifikacija prasideda nuo savybių, tačiau periodinės elementų lentelės išdėstymas rodo, kur paprastai randami metalai, nemetalai ir pusmetaliai.
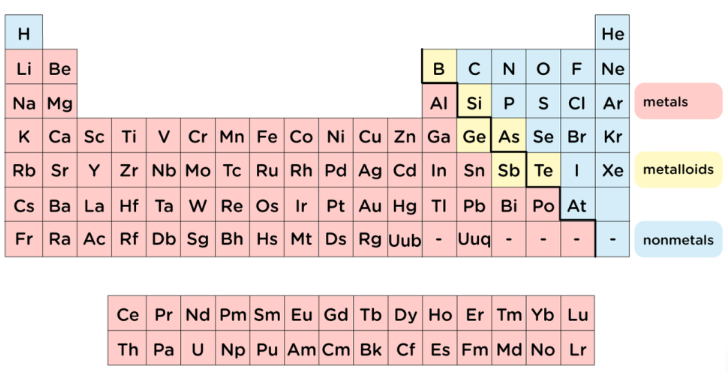
Kur periodinėje elementų lentelėje yra metalai?
Greitas žvilgsnis į spalvomis pažymėtą schemą atskleidžia pagrindinį modelį. Jei klausiate, kur periodinėje elementų lentelėje yra metalai, pažvelkite į lentelės kairiąją pusę ir platią jos centrą. Natrius yra labai kairėje , geležis užima vidurį, o tokie metalai kaip aliuminis ir auksas parodo, kad metaliniai elementai išsisklaidę didelėje lentelės dalyje. Netgi dvi eilutės, kurios dažniausiai ištraukiamos žemiau pagrindinės lentelės – lantano elementai ir aktinoidai – taip pat yra metalai.
Kur periodinėje elementų lentelėje yra metalai
Mokiniai, kurie klausia, kur periodinėje elementų lentelėje yra metalai, gali naudoti žigzago arba laiptų liniją kaip orientyrą. Elementai kairėje nuo šios linijos paprastai yra metalai. Elementai dešinėje – daugiausia ne metalai. Elementai palei ribą yra metaloidai. Išdėstymo santrauka iš ThoughtCo daugumą metalų padėsta į periodinės elementų lentelės kairiąją pusę, o ChemistryTalk apibūdina ne metalus kaip susitelkusius dešinėje pusėje, o metaloidus – palei žigzago ribą.
Taigi, kur praktikoje randami metalai periodinėje elementų lentelėje? Daugiausia kairėje nuo laiptų linijos ir visoje centre. Tai taip pat atsako į klausimą, kur metalai yra pavaizduoti daugumoje vadovėlių. Vienas žinomiausias išimtis – vandenilis. Jis pavaizduotas viršutinėje kairiojoje lentelės dalyje, tačiau yra ne metalas.
| Lentelės sritis | Tipinė klasifikacija | Pavyzdžiai |
|---|---|---|
| Kairioji pusė ir centras | Daugiausia metalai | Natrius, aliuminis, geležis, auksas |
| Žigzaginė riba | Daugiausia metaloidai | Silicis, arsenas, telūras |
| Viršutinė dešinė | Daugiausia nemetalai | Deguonis, azotas, chloras |
Paprasta spalvomis pažymėta periodinė elementų lentelė padaro šį modelį daug lengviau įsiminti iškart pažvelgus.
Kaip keičiasi metalinis pobūdis eilutėse ir grupėse
Elementų padėtis nėra atsitiktinė. Ji atspindi elektronų elgesį. LibreTexts paaiškina, kad metalinis pobūdis bendrai didėja judant žemyn grupėje ir kairėn per eilutę. Judant žemyn grupėje atomai tampa didesni, o jonizacijos energija mažėja, todėl išoriniai elektronai lengviau pašalinami. Judant per eilutę iš kairės į dešinę atomai laiko elektronus stipriau, todėl metalinis elgesys mažėja.
Ši tendencija paaiškina, kodėl natrius yra metalingesnis nei elementai, esantys toje pačioje eilutėje deščiau, ir kodėl reaktyviausi metalai yra apatinėje kairėje lentelės kraštinėje. Geležis, aliuminis ir auksas visi yra metalai, tačiau jų pozicijos rodo, kad ne visi metalai elgiasi vienodai. Žemėlapis aiškus. Skaičiavimas, tačiau, tampa sudėtingesnis, nes ribiniai atvejai ne visada vienodai telpa į visas diagramas.
Periodinės lentelės metalai, nemetalai ir pusmetaliai
Šis kairysis ir centrinis modelis padaro metalus lengvai atpažįstamus, tačiau jų skaičiavimas yra mažiau tvarkingas, nei manytų daugelis puslapių. Karališkoji draugija nurodo, kad daugiau kaip dvi trečiosios visų elementų yra metalai aplinkos sąlygomis. Nepaisant to, skirtingi šaltiniai ne visada pateikia tikslų tą patį bendrą skaičių, nes atsakymas priklauso nuo to, kaip lentelėje „metalai, nemetalai ir pusmetaliai“ įvertinami ribiniai elementai.
Kodėl šaltiniai nesutaria dėl metalų skaičiaus
Nesutarimai dažniausiai kyla dėl klasifikavimo taisyklių, o ne dėl netikslaus skaičiavimo. Tas pats Karališkosios draugijos apžvalgos straipsnis pabrėžia svarbų niuansą: periodinė elementų lentelė sąrašo elementus, tačiau žymės kaip „metalas“ ir „nemetalas“ aprašo, kaip šie elementai elgiasi savo elementarioje būsenoje įprastomis sąlygomis. Šaltkalviškojo („laiptų“) regiono srityje toks elgesys nėra visada aiškiai atskiriamas. Apžvalga taip pat pabrėžia, kad kai kurios p-plokštumos dalys, ypač grupėse 14 ir 15, gali būti ties metalų ir nemetalų riba. Taigi, nors mokyklinė periodinės lentelės metalų schema nemetalai, metaloidai yra naudinga, ji supaprastina sudėtingesnę tikrovę.
Jei puslapis nurodo vieną tikslų metalų skaičių, nepateikdamas savo klasifikavimo taisyklių, tvarkingumas gali laimėti prieš tikslumą.
Kaip klasifikavimo taisyklės keičia bendrąjį skaičių
Konservatyvus bendrasis skaičius prasideda nuo aiškiai metalinių elementų šeimų. Plačiau apibrėžtas skaičius gali taip pat apimti metalinius p-plokštumos elementus, tuo tarpu šaltkalviškojo regiono šalia esančius elementus vertinti atsargiau. IUPAC palaiko naujausią periodinę elementų lentelę ir pastebi, kad net struktūriniai klausimai, pvz., III grupės elementų vieta, buvo diskutuojami. Ši diskusija nešalina bendros nuotraukos, tačiau primena skaitytojams, kad mokslinė klasifikacija apima tiek konvencijas, tiek stebėjimus. Praktikoje didžiausią skaičiavimo problemą dažniausiai kelia ribos regionas, kuriame metalo, nemetalo ar metaloido žymė gali skirtis nuo vienos lentelės prie kitos.
| Kategorija | Tipiškas požiūris | Kodėl tai svarbu |
|---|---|---|
| Aiškiai metalinės šeimos | Beveik visada skaitomi kaip metalai | Apima pagrindinius metalinius blokus ir sukelia mažai nesutarimų |
| Metaliniai p-bloko elementai | Dažniausiai skaitomi kaip metalai | Vis dar metaliniai, bet arti laiptų ribos |
| Ribos regionas | Gali būti žymimi kaip metaloidai arba tarpiniai | Čia metaloidų, metalų ir netmetalų palyginimai sukuria skirtingus visuminius rezultatus |
Todėl naudingas atsakymas – tai ne tik skaičius. Tai yra po šeimų žiūrėjimas į tas grupes, kurios visada įtraukiamos, ir į tas, kurios yra pakankamai arti ribos, kad sukeltų nesusipratimų.
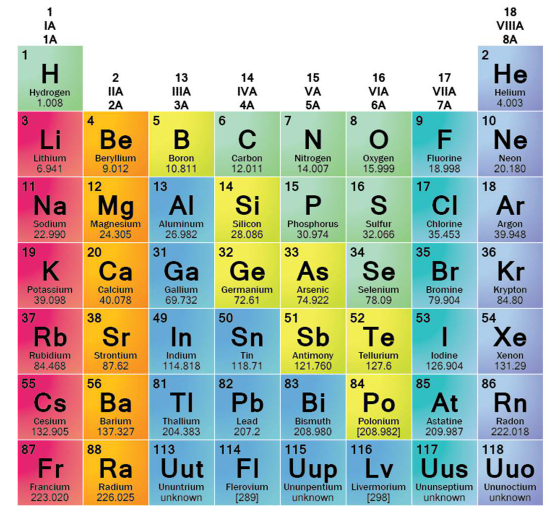
Cheminių elementų periodinės lentelės šeimos
Žiūrėjimas po šeimų labai supaprastina metalų pusės supratimą periodinėje lentelėje. Chemijoje periodinės lentelės elementų šeima apima elementus, turinčius panašias išorines elektronų struktūras ir, kaip rezultatą, panašų elgesį. Būtent todėl metalų klasifikacija yra naudingesnė nei paprastas kairės–dešinės padalijimas. Trumpas „ThoughtCo“ tinklapio apžvalgos, kartu su „Los Alamos“ naudojama metalų klasifikacija, suteikia skaitytojams praktinį būdą suskirstyti pagrindines metalų šeimas. Los Alamos , suteikia skaitytojams praktinį būdą suskirstyti pagrindines metalų šeimas.
Metalų šeimos periodinėje lentelėje
Šešios šeimos, kurios daugumai skaitytojų reikia, yra alkaliniai metalai, žemės šarminiai metalai, perėjimo metalai, po perėjimo metalai, lantanoidai ir aktinoidai. Jei esate matę kitokius periodinės elementų lentelės grupių pavadinimus, tai visiškai normalu. Šiuolaikinėse lentelėse stulpeliai sunumeruoti nuo 1 iki 18, tačiau šeimų pavadinimai pabrėžia bendras chemines savybes, o kai kurios šeimos apima daugiau nei vieną stulpelį ar net atskirus eilutes po pagrindine lentele.
| Metalų šeima | Kur pasitaiko | Prisimintinos savybės |
|---|---|---|
| Alkaliniai metalai | 1 grupė, išskyrus vandenilį | Po vieną valentinį elektroną, minkšti, blizgūs, labai reaktyvūs, dažniausiai sudaro +1 jonų |
| Žemės šarminiai metalai | 2-ojoje grupėje | Po du valentinius elektronus, kietesni ir tankesni už alkalinius metalus, dažniausiai sudaro +2 jonų |
| Perėjimo metalai | Grupės 3–12, centrinė d-blokko dalis | Kieti, tankūs, laidūs, dažnai aukštos lydymosi temperatūros, keli oksidaciniai laipsniai |
| Po perėjimo metalai | p-blokas, esantis dešinėje nuo perėjimo elementų bloko | Minkštesni metalai, kurie laiduoja prasčiau nei perėjimo metalai |
| Lantano elementai | Elementai nuo 57 iki 71, pirmoji atskira eilutė | Labai panašios cheminės savybės, priklauso f-blokui |
| Aktinoidai | Elementai nuo 89 iki 103, antroji atskira eilutė | f-blokų metalai, visi radioaktyvūs |
Kas daro kiekvieną metalų grupę skirtinga
Pradėkite nuo pačios kairės. Alkalinių metalų grupė periodinėje elementų lentelėje yra lengviausia pastebėti, nes jie turi po vieną valentinį elektroną ir reaguoja smarkiai, ypač su vandeniu. 2-osios grupės metalai taip pat reaguoja, bet jų du išoriniai elektronai daro juos mažiau aktyviuosius ir bendrai kietesnius nei 1-osios grupės metalai. Viduryje esančioje periodinės elementų lentelės perėjimo metalų dalyje įtraukta plati centrinė bloko dalis, žinoma dėl kietų metalinių kietųjų kūnų, gerų laidumo savybių ir įvairių oksidacinės būsenos laipsnių.
Perkelkite šiek tiek toliau į dešinę, ir šablonas sušvelnėja. Postperėjimo metalai išlieka metaliniai, tačiau paprastai būna minkštesni ir prastesni laidininkai nei perėjimo metalai. Žemiau lentelės pavaizduotos dvi eilutės dar labiau sudėtingina situaciją. Lantano elementai turi labai panašią chemiją, o aktinoidai išsiskiria radioaktyvumu. Kai kurie šaltiniai netgi abiejų eilučių elementus vadinami specialiaisiais perėjimo metalais, kas rodo, kodėl periodinės elementų lentelės grupių pavadinimai gali būti naudingi, bet negali pakeisti tikrosios cheminės elgsenos.
- 1 grupė reiškia minkštus ir labai reaktyvius elementus.
- 2 grupė reiškia reaktyvius, bet paprastai kietesnius nei 1 grupės elementus.
- 3–12 grupės reiškia centrinį bloką, kuriame yra daug klasikinių metalų.
- Postperėjimo metalai reiškia minkštesnius metalus, esančius arti laiptų regiono.
- Lantano elementai ir aktinoidai reiškia dvi f-poblokio eilutes, išdėstytas pagrindinio lentelės kūno apačioje.
Šie šeimos žymėjimai padaro lentelę labiau organizuotą, tačiau tikroji metalo išbandymo sąlyga yra ne vien jo šeimos pavadinimas. laidumas, blizgesys, kovojamumas ir elektronų praradimas paaiškina, kodėl visos šios grupės iš pradžių priskiriamos prie metalų pusės.
Kokios yra metalų savybės?
Šeimos žymėjimai padaro periodinę elementų lentelę lengviau peržvelgti, tačiau chemikai metalą nustato pagal jo elgesį, o ne tik pagal pavadinimą. Kai mokiniai klausia, kokios yra metalų savybės, atsakymas prasideda bendrų fizinių ir cheminių bruožų modeliu. „ LibreTexts metalinio ryšio aprašyme metalo atomai traukiami į judančių, delokalizuotų elektronų baseiną. Šis paprastas modelis padeda paaiškinti metalų metalines savybes ir kodėl tiek daug skirtingų metalų šeimų vis dėlto turi atpažįstamą elgesio savybių rinkinį.
Daugumos metalų bendros savybės
Jei palyginsite metalų ir nemetalų savybes, metalai dažniausiai išsiskiria keletu aiškių būdų.
- Elektrinė laidumas: Judrūs elektronai leidžia metalams gerai laiduoti elektros srovę. Klasikinis pavyzdys – vario laidas.
- Šilumos laidumas: Tie patys elektronai padeda perduoti šilumą, todėl metalai, tokie kaip varis ir aliuminis, yra naudingi ten, kur svarbi šilumos perdavimas.
- Blizgesys: LibreTexts paaiškina, kad metalų elektronai gali sugerti energiją ir vėliau išskleisti šviesą, todėl metalai turi blizgantį paviršių. Tai aiškiai matyti aukso, sidabro ir vario atveju.
- Kovojamumas: Metalus galima plakti arba ritinėti į lakštus, o ne tik sulaužyti. Paprasti pavyzdžiai – aliuminio folija ir plonas auksinis lapelis.
- Plastiškumas: Metalus galima tempti į vielas. Vėlgi, dažnai paminimas varis.
- Teigiamų jonų susidarymas: Daugelis metalų reakcijų metu praranda elektronus. Natrius sudaro Na+, magnis – Mg2+, o aliuminis – Al3+.
| Savybė | Tipinis elementas | Ką tai rodo |
|---|---|---|
| Elektrinis laidumas | Varį | Naudinga laidams ir grandinėms |
| Šilumos laidumas | Aliuminio | Efektyviai perduoda šilumą |
| Spalva | Sidabras | Šviečianti, poliruota paviršiaus |
| Plastiškumas | Auksinis | Gali būti suformuota į labai plonus lakštus |
| Sudugnumas | Varį | Gali būti ištempta į ilgus laidus |
Pavyzdžiai, kurie rodo, kad metalai nėra visi vienodi
Šios savybės yra stiprūs polinkiai, o ne tobula sąrašo tikrinimo schema. LibreTexts pažymi, kad gyvsidabris kambario temperatūroje yra skystas, nors metalai paprastai būna kieti. Tas pats šaltinis nurodo, kad natriis ir kalio yra tokie minkšti, kad juos galima pjauti peiliu, todėl jie labai skiriasi nuo kieto metalo, tokio kaip geležis. Laidumas taip pat kinta. Sidabras ir varis yra ypač stiprūs laidininkai, tuo tarpu kai kurie metalai prasčiau laidina. Taip pat labai skiriasi reaktyvumas. Auksas išlaiko savo išvaizdą geriau nei daugelis kitų metalų, nes jis daug efektyviau pasipriešina korozijai nei metalai, tokie kaip geležis.
Todėl metalų savybės geriausiai turi būti laikomos kaip požymių rinkinys. Vienu tik švytėjimu nepasitenkinama. Taip pat nepasitenkinama vien tik laidumu. Chemikai nagrinėja visą modelį: kaip elementas laiduoja, lankstomas ir kaip elgiasi praradęs elektronus reakcijose. Tokiu požiūriu kyla kitas praktinis klausimas, kurio atsakyti tampa daug lengviau: kurie konkrečiai elementai priklauso metalų kategorijai, juos grupuojant šeimomis?
Metalų sąrašas pagal periodinės lentelės šeimas
Skaitytojai, norintys praktinio metalų sąrašo dažniausiai neturi reikėti ilgo elementų pavadinimų sąrašo. Jiems reikia struktūros. Metalinių elementų grupavimas pagal šeimas padaro modelį lengvesnį tiriant, palyginant ir įsimenant. Žemiau pateikta pagrindinė lentelė remiasi „Science Notes“ ir „ThoughtCo“ naudojamomis bendromis metalų klasifikacijomis, taip pat pažymėdama kelis atvejus, kuriuos chemijos šaltiniai kartais traktuoja skirtingai. Tai aiškiausias būdas atsakyti į klausimą, kurie elementai yra metalai periodinėje lentelėje, nebandant daryti išvados, kad kiekvienas ribinis žymėjimas yra visuotinai nustatytas. Science Notes ir ThoughtCo
Metalų elementų šeimų sąrašas
| Serija | Elementai šeimoje | Klasifikavimo pastaba |
|---|---|---|
| Alkaliniai metalai | Litijus, natrius, kalis, rubidis, cezis, francis | Vandenilis yra 1-osios grupės elementas, tačiau įprastomis sąlygomis dažniausiai laikomas nemetalu. |
| Žemės šarminiai metalai | Berilis, magnis, kalcis, stroncis, barijus, radis | Šie elementai nuosekliai priskiriami metalams. |
| Perėjimo metalai | Skandis, titanas, vanadis, chromas, mangano, geležis, kobaltas, nikelis, varis, cinkas, itris, cirkonis, niobis, molibdenas, technecijus, rutenis, rodijus, paladis, sidabras, kadmis, hafnis, tantalias, volframas, renetis, osmis, iridis, platinos, auksas, gyvsidabris, ruterfordis, dubnis, seaborgis, bohris, hasis, meitneris, darmštadis, rentgenis, kopernicis | Daugelis mokyklinių periodinės lentelės variantų šiuos elementus (Zn, Cd ir Hg) įtraukia į šią grupę, nors kai kuriose chemijos diskusijose jie traktuojami šiek tiek kitaip. |
| Po-perėjimo arba paprastieji metalai | Aliuminis, galis, indis, cinas, talis, švinas, bizmis, polonis, nihonijus, flerovijus, moskovijus, livermorijus | Moksliniai užrašai apie paprastuosius metalus pažymi, kad šios grupės sudėtis labiausiai skiriasi priklausomai nuo šaltinio. Polonis dažnai įtraukiamas, tačiau kartais kyla ginčų. Livermorijus dažnai laikomas galimu arba prognozuojamu metalu. |
| Lantano elementai | Lantanas, ceris, prazeodimis, neodimis, prometis, samaris, europis, gadolinis, terbis, disprozis, holmis, erbis, tulis, iterbis, lutecijus | Tai pirmoji atskira eilutė po pagrindinės lentelės ir ji yra metalinė. |
| Aktinoidai | Aktinidas, toris, protaktinis, uranas, neptunijus, plutonijus, amerikis, kuris, berkelis, kalifornijus, ainstainis, fermis, mendelevis, nobelis, laurencijus | Tai antroji atskira eilutė po pagrindinės lentelės ir ji yra metalinė, nors daugelis šių elementų žymimi daugiau dėl radioaktyvumo nei dėl kasdieninio metalinio elgesio. |
Kaip skaityti pagrindinį sąrašą be painiavos
Jei reikia greito metalų sąrašo namų darbams ar peržiūrai pirmiausia naudokite šeimos stulpelį, o antra – pastabų stulpelį. Šeima nurodo, kur periodinėje elementų lentelėje priklauso elementas. Pastaba nurodo, kur klasifikacija tampa neaiški. Tai svarbiausia ypač arti laiptų formos linijos ir sunkiausių p bloko elementų.
Kai mokytojai prašo mokinių išvardyti metalus , jie paprastai ieško šių šeimų stabiliosios šerdies, o ne ginčų dėl kiekvieno kraštutinio atvejo. Jei norite tik pačių žymiausių metalų pavadinimų , pradėkite nuo geriausiai žinomų kiekvienos grupės narių ir nuo jų plėskitės toliau.
- Šarminiai metalai: natrius, kalis
- Žemės šarminiai metalai: magnis, kalcis
- Perėjimo metalai: geležis, varis, sidabras, auksas
- Po perėjimo metalai: aliuminis, alvas, švinas
- Lantano elementai: lantanas, neodimis
- Aktinoidai: uranas, plutonis
Tai yra keli metalų pavyzdžiai kuriuos dauguma skaitytojų jau pažįsta. Jie taip pat puikiai tinka kaip atminties atramos, kai visa lentelė atrodo perpildyta. Mokymosi užrašuose naudinga prisiminti, kad įprasti metalų pavadinimų dažniausiai kilę iš perėjimo ir po perėjimo grupių, o lantano elementai bei aktinoidai lengviau įsimenami kaip eilės.
Dar viena įspėjimo priemonė padeda šiam pagrindiniam sąrašui išlikti tiksliai: ne visos schemos vienodai klasifikuoja elementus, tokius kaip polonis ar sunkiausi sintetiniai p bloko nariai. Todėl naudingas šaltinis turi daryti daugiau nei tiesiog nurodyti elementų pavadinimus. Jame taip pat turėtų būti parodyta, kur ribos išsisklaido, nes metalo žymė yra labiausiai patikima tuomet, kai galima aiškiai atskirti ją nuo pusmetalių ar nemetalų.
Metalai prieš nemetalus – periodinės elementų lentelės vadovas
Ilgas pagrindinis sąrašas yra naudingas, tačiau daugumai skaitytojų reikia greitesnio būdo elementui klasifikuoti iš pirmo žvilgsnio. Gera naujiena ta, kad periodinė elementų lentelė suteikia aiškų vizualinį ženklą. Dar geresnė naujiena – kad chemija suteikia papildomą patikrinimą, kai vien tik išdėstymas nepakanka.
Kaip atskirti metalus nuo metaloidų ir nemetalų
Mokslininkų pastabų (Science Notes) vizualinė žemėlapis aiškiai rodo pagrindinį modelį: metalai daugiausia išsidėstę kairėje ir centre, o nemetalai susitelkę dešinėje. Tarp jų yra pažįstama laiptų formos riba. Jei klausiate, kur periodinėje elementų lentelėje yra metaloidai, juos paprastai galima rasti šioje zigzago formos riboje. UMD chemijos vadovas naudoja tą patį modelį greitai identifikavimui.
Vis dėlto metalų ir nemetalų periodinės lentelės klausimas negali būti išspręstas tik vien pagal jų vietą. Periodinėje lentelėje esančius metalus ir nemetalus geriausia atskirti ne tik pagal jų padėtį, bet ir pagal jų elgesį. Metalai dažnai gerai laiduoja šilumą ir elektros srovę bei dažnai praranda elektronus, kad susidarytų teigiamieji jonai. Periodinėje lentelėje esantys nemetalai labiau linkę priimti arba bendrinti elektronus, o daugelis jų yra prasti laidininkai. Periodinėje lentelėje esantys metaloidai yra tarp jų, dažnai parodantys mišrius savybių požymius ir puslaidininkišką elgesį.
- Raskite laiptų formos liniją lentelėje.
- Pirmiausia pažvelkite į kairę arba centrą. Dauguma ten esančių elementų yra metalai.
- Pažvelkite į viršutinį dešinįjį lentelės kampą. Dauguma ten esančių elementų yra nemetalai.
- Patikrinkite patį ribos plotą. Ten esantys elementai dažnai yra metaloidai.
- Jei reikia, išbandykite elgesį. Gerasis laidininkas rodo, kad tai metalas, prastas laidininkas – kad tai nemetalas, o tarpinis arba puslaidininkiškas elgesys – kad tai metaloidas.
- Stebėkite išimtis. Vandenilis yra įrašytas kairėje, bet dažniausiai yra nemetalas. Jei paklaustumėte, ar silicis yra metalas, nemetalas ar metaloidas, silicis dažniausiai klasifikuojamas kaip metaloidas. Jo puslaidininkinės savybės pabrėžiamos MISUMI metaloidų gidoje.
Laipstų forma – tai tik orientyras, o ne garantija. Ribinės ribos elementai gali būti žymimi skirtingai priklausomai nuo lentelės ir jos klasifikavimo taisyklių.
Paprasčiausi atminties pagalbiniai priemonės greitesniam atpažinimui
- Kairėje ir centre – galvokite apie metalus.
- Viršutinėje dešinėje – galvokite apie nemetalus.
- Laipstų formos linijoje – galvokite apie metaloidus.
- Prisiminkite elgsenos užuominą: laidumas, pasipriešinimas arba puslaidininkinės savybės.
Šis greitasis rėmas padaro periodinės elementų lentelės diagramose esančius metalus ir nemetalus daug lengviau suprantamus stresinėmis sąlygomis. Jis taip pat nurodo kažką didesnio nei vien tik faktų įsiminimas, nes skirtumas tarp laidžiojo metalo ir puslaidininkinio metaloido lemia realių medžiagų pasirinkimą elektronikoje ir gamyboje.

Kodėl periodinėje elementų lentelėje esantys metalai svarbūs gamyboje
Laiptų modelis padeda mokiniams ne tik rūšiuoti elementus. Projektavime ir gamyboje klausimas „kas yra metalas?“ greitai virsta praktiniu sprendimu dėl našumo. Žinodami, kur periodinėje elementų lentelėje yra metalai, inžinieriai gauna pirmąją nuovoką apie laidumą, stiprumą, plastikumą ir šilumos perdavimą, tačiau tikroji gamyba eina toliau nei mokyklinės etiketės.
Kodėl metalų klasifikacija svarbi tikrojoje gamyboje
Metalinis cheminis elementas dažnai yra pradžios taškas, o ne galutinis rezultatas. AJProTech apibūdina medžiagų pasirinkimą kaip apkrovų, aplinkos, svorio, gamybos galimybės, prieinamumo, kainos ir atitikties reikalavimams pusiausvyrą. Todėl skirtingų rūšių metalai sprendžia skirtingas problemas. TIRapid aiškiai parodo šį modelį: varis vertinama dėl elektros ir šilumos laidumo, aliuminis – dėl mažo tankio ir korozijos atsparumo, plienas – dėl stiprumo ir naudingumo kainos atžvilgiu, o titanas – dėl aukšto specifinio stiprio reikalaujančiose aplinkose. Praktikoje daugelis baigtų detalių gaminama iš lydinių, o ne iš grynos metalinės cheminės elementų, nes darbo užduotis paprastai reikalauja geriau subalansuotų savybių.
- Transportavimas: Aliuminis ir magnis padeda sumažinti svorį, tuo tarpu plienas išlieka dažnai pasirenkama medžiaga konstrukcinėms detalėms, nes jis derina stiprumą su praktiška kaina.
- Elektronika: Varis yra pageidautinas ten, kur svarbūs elektros srovės tekėjimas ir šilumos perdavimas.
- Griežtos aplinkos: Nerūdijantis plienas, titanas ir nikeliu pagrįstos medžiagos yra naudingos, kai kyla korozijos atsparumo ar aukštos temperatūros stabilumo reikalavimai.
- Gamybos planavimas: Svarbu ir apdirbamosios medžiagos savybės. Medžiaga, kuri atrodo idealiai tinkama teorinėje analizėje, vis tiek gali padidinti įrankių nusidėvėjimą, gamybos ciklo trukmę arba tikrinimo reikalavimus.
Kur ieškoti tikslaus metalų apdirbimo paslaugų
Cheminių elementų periodinėje lentelėje esantis metalinis elementas tampa naudinga dalimi tik tada, kai gamybos procesas atitinka medžiagos savybes. Aliuminis leidžia greitai apdirbti ir sukurti lengvą konstrukciją, tuo tarpu kietesniems plienams ar titano lydiniams gali prireikti tikresnio proceso valdymo. Todėl inžinieriai domisi ne tik medžiagos chemine sudėtimi, bet taip pat tikslumo ribomis, paviršiaus apdorojimu, patvirtinimu ir pakartojamumu.
Praktiniam pavyzdžiui, Shaoyi Metal Technology pateikiamas automobilių pramonės apdirbimo darbo eilių procesas, kuris susieja greitą prototipavimą, mažo tūrio gamybą ir masinę gamybą su IATF 16949 kokybės valdymo sistema ir statistiniu procesų valdymu. Tokiu būdu periodinė lentelė nustoja būti tik mokytina schema ir virsta vadovu, padedančiu pasirinkti medžiagas, kurios gali būti apdirbtos, patikrintos ir kuriose galima pasitikėti realiuose komponentuose.
- Naudokite chemiją, kad susiaurintumėte pasirinkimą.
- Naudokite inžinerinius kriterijus, kad pasirinktumėte galutinį medžiagų tipą.
- Naudokite procesų valdymą, kad iš tinkamo metalo būtų pagaminta patikima detalė.
Tikroji vertė, mokantis, kurie elementai yra metalai periodinėje elementų lentelėje, slypi ne tik juos pavadindami, bet ir suprasdami, kaip metalų klasifikacija formuoja tas dalis, kurios kasdien naudojamos automobiliuose, laiduose, aušinimo sistemose ir statybose.
Dažniausiai užduodami klausimai apie metalus periodinėje elementų lentelėje
kiek metalų yra periodinėje elementų lentelėje?
Nėra vieno skaičiaus, kurį visi šaltiniai laikytų galutiniu. Dauguma elementų yra metalai, tačiau tikslus bendras skaičius gali keistis priklausomai nuo to, kaip konkrečioje lentelėje įvertinami ribiniai atvejai, ypač šešėlinėje („laiptų“) srityje ir tarp kai kurių sunkesnių p bloko elementų. Tikslus atsakymas aiškiai atskiria akivaizdžiai metalines grupes nuo tų elementų, kuriems kartais priskiriamos skirtingos klasifikacijos, o ne priverčia nustatyti vieną perdaug supaprastintą skaičių.
kur periodinėje elementų lentelėje randami metalai?
Metalai randami daugiausia periodinės elementų lentelės kairėje pusėje ir per jos centrą. Dvi atskirtos eilutės apačioje – lantano elementai ir aktinoidai – taip pat yra metalai. Greitas būdas suprasti išdėstymą – naudoti laiptų liniją: dauguma elementų kairėje yra metalai, dauguma dešinėje – nemetalai, o ribinėje srityje dauguma yra pusrūdžiai. Vandenilis yra įprastas vizualinis išimtis, nes jis yra kairėje, bet dažniausiai priskiriamas prie nemetalų.
3. Kokie yra pagrindiniai metalų šeimų periodinėje elementų lentelėje?
Pagrindinės metalų šeimos yra alkaliniai metalai, žemės šarminiai metalai, perėjimo metalai, po-perėjimo metalai, lantano elementai ir aktinoidai. Kiekviena šeima turi savo savybių modelį. Alkaliniai metalai yra labai reaktyvūs, žemės šarminiai metalai mažiau reaktyvūs, bet vis tiek aktyvūs, perėjimo metalai apima daugelį įprastų konstrukcinių ir inžinerinių metalų, po-perėjimo metalai paprastai minkštesni, o lantano elementai ir aktinoidai sudaro dvi metalines eilutes, parodytas pagrindinės lentelės apačioje.
4. Kokie savybės daro elementą metalu?
Chemikai paprastai nustato metalą pagal keletą požymių, o ne vieną tikrą požymį. Metalai dažnai gerai laiduoja šilumą ir elektros srovę, atspindi šviesą, lankomi be įtrūkimų, ištempiami į vielas ir reakcijose linkę prarasti elektronus. Vis dėlto ne visi metalai elgiasi vienodai. Kai kurie yra minkšti, kai kurie puikiai atsparūs korozijai, o vienas žinomiausių pavyzdžių – gyvsidabris – kambario temperatūroje yra skystas.
5. Kodėl svarbu, ar elementas yra metalas gamyboje?
Metalų klasifikacija padeda susieti chemiją su tikrais medžiagų pasirinkimais. Kai inžinieriai žino, kad medžiaga yra metalinė, jie gali pradėti mąstyti apie laidumą, stiprumą, korozijos atsparumą, svorį ir apdirbamumą. Tai svarbu elektronikoje, transporto dalyse ir pramonės komponentuose. Praktikoje metalinio elemento ar lydinio paverčiant naudinga detalė taip pat svarbi technologinio proceso kontrolė ir tikslus apdirbimas. Pavyzdžiui, „Shaoyi Metal Technology“ taiko IATF 16949 standarto sertifikuotą apdirbimą ir statistinės proceso kontrolės (SPC) pagrįstą kokybės valdymą, kad būtų galima perkelti metalines dalis iš prototipų etapo į gamybos naudojimą.
 Maži serijos dydžiai, aukšti standartai. Mūsų greito prototipavimo paslauga leidžia patvirtinti rezultatus greičiau ir lengviau —
Maži serijos dydžiai, aukšti standartai. Mūsų greito prototipavimo paslauga leidžia patvirtinti rezultatus greičiau ir lengviau —
