- Reduzca los costos de extrusión de aluminio con 5 consejos esenciales de DFM
- El verdadero ROI de matrices de extrusión personalizadas para producción masiva
- Prototipado de metal para automoción: una guía para una innovación más rápida
- Piezas del Aire Acondicionado Automotriz: Desde el Compresor hasta el Evaporador Explicado
¿Qué son los metales alcalinotérreos? El grupo 2 finalmente tiene sentido
Time : 2026-04-02
¿Qué son los metales alcalinotérreos?
Si buscó ¿qué son los metales alcalinotérreos? , aquí tiene la respuesta directa: son los seis elementos del Grupo 2 del sistema periódico. Esta breve definición de los metales alcalinotérreos es el punto de partida, pero el nombre también le indica mucho acerca del comportamiento de esta familia.
¿Qué son los metales alcalinotérreos en una sola oración?
Los metales alcalinotérreos son berilio, magnesio, calcio, estroncio, bario y radio, los seis elementos metálicos del Grupo 2 que normalmente forman iones +2.
- Berilio (Be)
- Magnesio (Mg)
- Calcio (Ca)
- Estroncio (Sr)
- Bario (Ba)
- Radio (Ra)
Por qué el nombre «metales alcalinotérreos» tiene sentido
Para principiantes, la definición de metales alcalinotérreos se vuelve mucho más sencilla cuando se divide la expresión en tres partes.
Alcalino significa que sus óxidos e hidróxidos son básicos, no ácidos. La Tierra es una palabra histórica. Los primeros químicos la usaban para referirse a sustancias estables al calor, similares a minerales, que no fundían ni se disolvían fácilmente en agua, un aspecto explicado por Britannica . Los metales significa que los propios elementos son metálicos, típicamente brillantes y buenos perdiendo electrones en las reacciones.
Esto le da el significado básico de metales alcalinotérreos sin necesidad de conocer primero la química avanzada. También es una breve descripción útil de los metales alcalinotérreos : una familia de metales del grupo 2 con química compartida, una posición común en la tabla periódica y un papel importante en el mundo real. El magnesio aparece en aleaciones y en procesos biológicos. El calcio es fundamental en los huesos, las conchas y los materiales de construcción. El bario, el estroncio y el radio aparecen en contextos más especializados.
Este artículo comienza de forma sencilla intencionadamente. Una lista clara es fácil de memorizar, pero la familia resulta mucho más comprensible cuando se observa dónde se sitúan estos elementos y por qué esa ubicación les confiere un comportamiento tan similar.
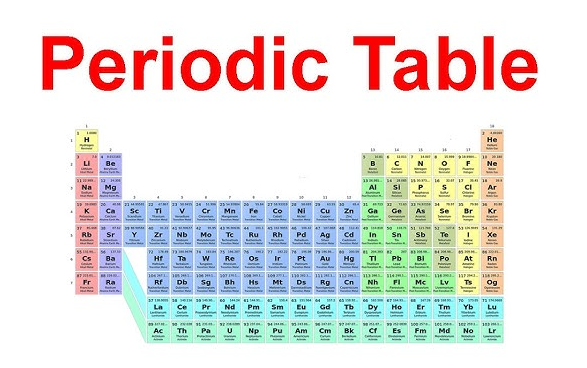
Ubicación del grupo 2 en la tabla periódica
El nombre de la familia resulta mucho más fácil de recordar cuando realmente se puede identificar. Si te preguntas ¿dónde se encuentran los metales alcalinotérreos en la tabla periódica? , mira la segunda columna desde la izquierda. Esa columna vertical es el grupo 2 de la tabla periódica , situado inmediatamente al lado de los metales alcalinos del grupo 1. A grupo 2 de la tabla periódica la vista muestra siempre la misma línea recta: berilio en la parte superior, seguido de magnesio, calcio, estroncio, bario y radio, descendiendo a lo largo de los periodos.
En un tabla periódica de los metales alcalinotérreos gráfico, estos seis elementos pertenecen al bloque s. Su ubicación compartida es relevante porque refleja un patrón compartido de electrones. Como LibreTexts explica, los elementos del grupo 2 tienen una configuración de valencia ns 2, lo que significa que poseen dos electrones en su capa externa.
Dónde se encuentran los metales alcalinotérreos en la tabla periódica
Visualmente, el patrón es sencillo. La tabla periódica: elementos del grupo 2 forman una única columna familiar a lo largo de los periodos 2 al 7. Muchos diagramas didácticos resaltan la metales alcalinotérreos en la tabla periódica diseños con el mismo color porque las familias de elementos se leen verticalmente, no horizontalmente. Las búsquedas de tabla periódica metales alcalinotérreos realmente están solicitando esa única columna.
| El elemento | El símbolo | Posición del grupo 2 | Ion típico | Compuesto conocido |
|---|---|---|---|---|
| El berilo | Be | Periodo 2, parte superior del grupo 2 | Be2+ | BeO |
| Magnesio | Mg | Periodo 3 | Mg2+ | MgO |
| Calcio | Ca | Periodo 4 | Ca2+ | Caco 3 |
| Estróncio | Sr | Periodo 5 | Sr2+ | SrCO 3 |
| El barrio | BA | Periodo 6 | BA 2+ | BaSO 4 |
| Radio | RA | Periodo 7, parte inferior del grupo 2 | RA 2+ | RaCl 2 |
Por qué los elementos del grupo 2 forman iones con carga +2
Esos dos electrones externos determinan la química. Los átomos del grupo 2 tienden a perder ambos electrones porque así adquieren una configuración electrónica más estable. El resultado es un +2 iones , como Mg 2+ o Ca 2+. Por eso, estos metales suelen formar compuestos como óxidos, cloruros, carbonatos y sulfatos. El patrón en las fórmulas se aprecia de inmediato: MgO, CaCl 2, CaCO 3, BaSO 4.
Cómo reconocer rápidamente la familia de los metales alcalinotérreos
Un truco rápido para identificarlos consiste en buscar tres pistas simultáneamente: segundo grupo, elementos metálicos y carga habitual de +2. En comparación con los metales alcalinos vecinos, que tienen un electrón de valencia y suelen formar iones +1, los elementos del grupo 2 poseen un electrón exterior adicional y, por lo general, son menos reactivos. No obstante, claramente pertenecen a una misma familia. Lo interesante es que cada miembro expresa ese patrón de forma ligeramente distinta, especialmente desde el berilio, en la parte superior, hasta el radio, en la parte inferior.
Conozca los seis metales alcalinotérreos
Una lista es útil, pero por sí sola no es muy memorable. El grupo 2 empieza a parecer más real cuando cada miembro tiene una identidad clara. Algunos aparecen en los huesos o en el agua de mar. Algunos dan color a los fuegos artificiales. Uno es, sobre todo, una señal histórica de advertencia. Juntos siguen perteneciendo a la misma familia, pero cada uno tiene su propia personalidad.
| El elemento | El símbolo | Acontecimiento común | Propiedad destacada | Relevancia en condiciones reales |
|---|---|---|---|---|
| El berilo | Be | Presente en minerales como la berilo | Muy ligero y rígido para ser un metal | Se utiliza en aplicaciones especializadas aeroespaciales y de rayos X; el polvo es peligroso si se inhala |
| Magnesio | Mg | Presente en el agua de mar y en minerales | Baja densidad y llama blanca brillante al arder | Importante en aleaciones ligeras, suplementos y biología |
| Calcio | Ca | Común en la piedra caliza, los huesos, las conchas y la tiza | Ion del Grupo 2 biológicamente familiar | Clave en esqueletos, cemento, yeso y muchos minerales naturales |
| Estróncio | Sr | Se encuentra principalmente en la celestina y la estroncianita | Las sales producen un color rojo intenso en las llamas | Se utiliza en fuegos artificiales, bengalas, materiales luminiscentes y algunos productos dentales |
| El barrio | BA | Suele asociarse con la baritina | Metal alcalinotérreo denso y pesado | El sulfato de bario es importante en la perforación y en la imagen médica; los compuestos solubles de bario requieren precaución |
| Radio | RA | Aparece en cantidades traza en minerales de uranio | Su intensa radiactividad domina su historia química | Hoy en día, su relevancia es principalmente histórica o está estrictamente controlada desde el punto de vista científico |
Berilio y magnesio en la parte superior del grupo 2
El elemento berilio se sitúa en la parte superior de la familia y ya sugiere que el grupo 2 no es perfectamente uniforme. Suele asociarse con el mineral berilo, la misma familia mineral que incluye la esmeralda y la acuamarina. El berilio destaca porque es inusualmente ligero y rígido. Eso lo hace útil en componentes de alto rendimiento donde importa la baja masa. Al mismo tiempo, el berilio es un material que exige precaución en entornos industriales, ya que el polvo fino puede ser perjudicial si se inhala. Por ello, se le recuerda tanto por su rendimiento como por la cautela requerida en su manipulación.
El magnesio resulta mucho más familiar. El símbolo químico del magnesio es Mg, y es uno de los metales más conocidos de este grupo porque aparece en el agua de mar, minerales comunes y sistemas vivos. Es un metal muy ligero y, al arder, produce una luz blanca intensa. Por eso, el magnesio ha estado asociado desde hace mucho tiempo con bengalas y materiales que arden con gran intensidad. En la vida cotidiana, sin embargo, la mayoría de las personas lo encuentran en formas más suaves, como su papel en la dieta, compuestos antiácidos o aleaciones ligeras utilizadas allí donde reducir la masa resulta fundamental.
Calcio y estroncio en materiales de uso cotidiano
El calcio es el miembro del Grupo 2 más reconocible para muchos lectores. Aparece en la piedra caliza, la tiza, las conchas y los huesos, por lo que conecta inmediatamente la química tanto con la geología como con la biología. El carbonato cálcico es el compuesto familiar en este contexto. Ayuda a explicar por qué el mismo grupo puede ser relevante tanto en la formación de cuevas, como en la piedra de construcción y en los esqueletos. El calcio metálico en sí es reactivo, pero los compuestos de calcio están presentes en todas partes, razón por la cual este elemento suele percibirse como más familiar que exótico.
El estroncio es más fácil de recordar una vez que lo asocias con el color. el símbolo del estroncio es Sr, y estróncio se encuentra principalmente en los minerales celestita y estroncianita. La Royal Society of Chemistry lo describe como un metal blando y plateado que arde en el aire y reacciona con el agua. Sus sales son famosas por producir colores rojos intensos en fuegos artificiales y bengalas. La misma fuente también menciona su uso en materiales fosforescentes y en el cloruro de estroncio hexahidratado presente en pastas dentales para dientes sensibles. Esto convierte al estroncio en un excelente ejemplo de cómo un elemento puede ser químicamente reactivo, pero, en su mayor parte, encontrarse a través de sus compuestos.
Bario y radio en contextos avanzados o especializados
El elemento bario a menudo se recuerda por su densidad. Se asocia comúnmente con la barita, y uno de sus compuestos más conocidos es el sulfato de bario. Este compuesto es importante porque es muy insoluble, lo que ayuda a explicar por qué el bario puede aparecer en aplicaciones prácticas, como los fluidos de perforación y la imagen médica, mientras que otros compuestos solubles de bario se manejan con mayor precaución debido a su toxicidad.
El radio se sitúa en la parte inferior de la familia, pero no pasa desapercibido. tabla periódica del radio la vista, Ra marca el punto en el que la radiactividad se convierte en la característica definitoria. El radio ocurre de forma natural únicamente en cantidades mínimas, normalmente asociado a minerales de uranio. Históricamente, adquirió fama por sus pinturas luminosas y sus primeros experimentos médicos. Hoy en día, su peligrosidad proviene de su radiactividad más que de su comportamiento como metal ordinario, por lo que se manipula bajo controles estrictos. En términos sencillos, el radio sigue perteneciendo al grupo 2, pero se trata tanto desde la perspectiva de la seguridad nuclear como desde la química.
Coloque estos seis elementos uno al lado del otro y la familia deja de parecer una simple lista de nombres. El tamaño, la reactividad, los compuestos comunes e incluso la forma en que cada elemento aparece en la vida cotidiana cambian al descender en el grupo. Este patrón cambiante es precisamente lo que hace especialmente útil al grupo 2, ya que el orden desde el berilio hasta el radio comienza a revelar tendencias en lugar de meros datos anecdóticos.
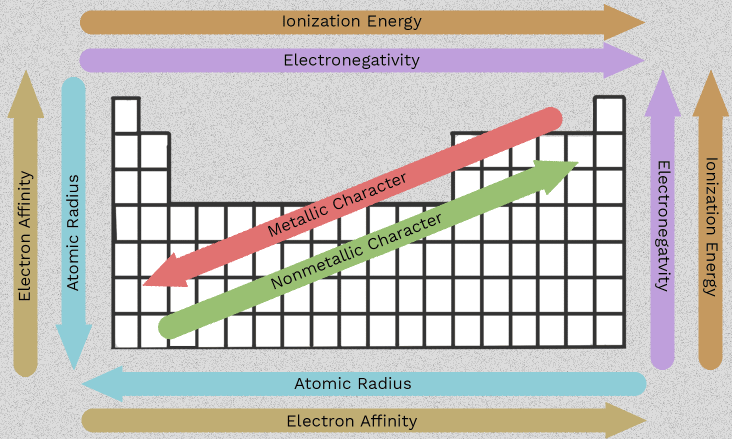
Propiedades de los metales alcalinotérreos y tendencias del grupo 2
Ese cambio de orden desde el berilio hasta el radio es lo que hace útiles a los elementos del Grupo 2. En lugar de memorizar seis hechos aislados, puedes seguir una serie de patrones que se repiten a lo largo de la columna. El más importante propiedades de los metales alcalinotérreos surgen todas de una característica compartida: cada átomo tiene dos electrones en su capa exterior que tiende a perder.
Una vez que comprendes cómo varían el tamaño atómico, el apantallamiento electrónico y la energía de ionización al descender por el grupo, resulta mucho más fácil predecir el comportamiento de esta familia. Estas características de los metales alcalinotérreos no son meros datos para exámenes. Explican por qué algunos elementos reaccionan con mayor rapidez, por qué algunos compuestos se disuelven mejor que otros y por qué ciertas tendencias requieren una formulación cuidadosa, en lugar de simples flechas.
Propiedades comunes de los metales alcalinotérreos
La mayoría de los elementos del Grupo 2 son metales plateados que normalmente forman M 2+iones y forman principalmente compuestos iónicos. Se comportan como agentes reductores porque pierden electrones. En comparación con los metales del Grupo 1, son generalmente menos reactivos, pero siguen siendo lo suficientemente activos químicamente como para formar muchos óxidos, cloruros, carbonatos y sulfatos comunes.
Una forma sencilla de organizar las propiedades químicas de los metales alcalinotérreos consiste en separar lo que permanece constante de lo que cambia. Lo que permanece constante es el estado de oxidación habitual +2. Lo que cambia es la facilidad con la que cada elemento cede esos dos electrones. Ahí es donde comienzan a tener importancia las tendencias.
Tendencias hacia abajo en el Grupo 2 y su significado
Datos recopilados por LibreTexts y explicaciones sobre las tendencias de Save My Exams muestran el mismo patrón general. El radio atómico aumenta de 112 pm para Be a 253 pm para Ba, mientras que la primera energía de ionización disminuye de 900 a 503 kJ/mol. En términos sencillos, los electrones externos se encuentran más lejos del núcleo y están apantallados por más capas internas, por lo que resultan más fáciles de eliminar.
| Tendencia | Dirección hacia abajo en el Grupo 2 | Razón química | Qué significa esto en la práctica |
|---|---|---|---|
| Radio atómico | Aumenta | Cada elemento tiene una capa electrónica adicional y mayor apantallamiento | Los átomos más grandes retienen los electrones externos con menor fuerza |
| Primera y segunda energía de ionización | Disminuyen en conjunto | Los electrones externos están más alejados del núcleo, por lo que la atracción es más débil | Formación de M 2+los iones se vuelve más fácil |
| Reactividad | Aumenta en conjunto | Energías de ionización más bajas facilitan la pérdida de electrones | Los elementos más pesados reaccionan con mayor intensidad con los ácidos, el oxígeno y, a menudo, el agua |
| Punto de fusión | Generalmente disminuye, pero no de forma uniforme | Los iones metálicos de mayor tamaño debilitan el enlace metálico, aunque la estructura también influye | Utilice la palabra "general" aquí, porque el Mg y el Ca no se ajustan perfectamente a una línea clara |
| Densidad | Irregular | La masa, el tamaño atómico y el empaquetamiento metálico cambian simultáneamente | No puede considerar la densidad como una simple tendencia descendente |
| Solubilidad de los hidróxidos | Aumenta | El equilibrio entre la energía reticular y la energía de hidratación se desplaza hacia abajo en el grupo | Los hidróxidos más pesados generan disoluciones más alcalinas |
| Solubilidad de los sulfatos | Disminuye | La energía de hidratación disminuye a medida que el catión aumenta de tamaño | Compuestos como BaSO 4se vuelven muy poco solubles |
La densidad y el comportamiento de fusión son las dos tendencias que los estudiantes suelen simplificar en exceso. La densidad no varía de forma lineal porque tanto la masa como el volumen están cambiando, y los átomos metálicos no se empaquetan del mismo modo en todos los cristales. Los puntos de fusión también requieren atención. En general, disminuyen porque los iones más grandes debilitan la red metálica, pero el magnesio tiene un punto de fusión inusualmente bajo de 650 °C, mientras que el calcio asciende a 842 °C antes de que los valores vuelvan a descender. Por tanto, una de las características más seguras de los metales alcalinotérreos es la siguiente: el patrón general es real, pero los detalles físicos no son perfectamente regulares.
La solubilidad lleva la misma advertencia. No existe una única regla que abarque todas las sales del grupo 2. Los hidróxidos se vuelven más solubles al descender en el grupo, mientras que los sulfatos se vuelven menos solubles. Si alguien afirma «la solubilidad aumenta al descender en el grupo 2», la pregunta clave es: «¿De qué compuestos se trata?»
Por qué los metales alcalinotérreos reaccionan del modo en que lo hacen
Así que, ¿Son reactivos los metales alcalinotérreos ? Sí, y la respuesta general es que su reactividad aumenta al descender en el grupo. La razón es la misma historia de electrones expuesta anteriormente. Energías de ionización primera y segunda más bajas significan que los átomos pueden perder dos electrones con mayor facilidad y alcanzar el estado común M 2+más rápidamente.
Esto afecta las reacciones reales. Al descender en el grupo, las reacciones con ácidos diluidos se vuelven más rápidas, las reacciones con oxígeno se vuelven más vigorosas y los elementos más pesados son más fáciles de oxidar. Las notas de Save My Exams indican que el bario es lo suficientemente reactivo como para almacenarse bajo aceite, lo cual constituye una señal práctica de hasta dónde puede llegar esta tendencia de reactividad.
- El radio atómico aumenta al descender en el grupo 2.
- La energía de ionización disminuye al descender en el grupo 2.
- La reactividad aumenta porque resulta más fácil perder dos electrones.
- Los puntos de fusión y la densidad presentan irregularidades, por lo que deben evitarse reglas absolutas.
- Los hidróxidos y los sulfatos muestran tendencias opuestas de solubilidad.
Esos patrones hacen que la familia sea predecible, pero no perfectamente uniforme. Justo cerca de la parte superior del grupo, el berilio ya comienza a romper las reglas, y el magnesio añade otra excepción cotidiana que resulta más relevante de lo que muchos principiantes esperan.
Metales alcalinos y metales alcalinotérreos
Las tendencias generales hacen que el Grupo 2 sea más fácil de aprender, pero la familia deja de tener sentido si se trata a cada miembro como idéntico. La señal de advertencia más importante es el berilio. El magnesio añade una excepción práctica y cotidiana. Y cuando las personas comparan metales alcalinos y metales alcalinotérreos , nombres similares pueden ocultar una química muy distinta.
Por qué el berilio no se comporta como un metal típico del Grupo 2
BYJU'S describe al berilio como la clara excepción en el Grupo 2. Su tamaño inusualmente pequeño, su alta energía de ionización y su fuerte poder polarizante le confieren un comportamiento menos típico de la familia. En términos sencillos, Be 2+atrae fuertemente las nubes electrónicas cercanas, por lo que los compuestos de berilio suelen ser más covalentes que los compuestos más iónicos formados por los elementos más pesados del grupo. La misma fuente también señala que el berilio tiene puntos de fusión y ebullición más altos que los demás elementos del grupo y no reacciona con el agua como lo hacen sus congéneres.
El magnesio no es tan inusual como el berilio, pero aún puede parecer menos reactivo de lo que los estudiantes esperan. LibreTexts señala que el magnesio muy limpio reacciona solo ligeramente con agua fría, y la reacción pronto se ralentiza porque el hidróxido de magnesio, casi insoluble, forma una barrera sobre la superficie. En la parte inferior de la familia, el radio suele tratarse por separado debido a que su radiactividad domina las discusiones prácticas y de seguridad.
Cómo difieren los metales alcalinotérreos de los metales alcalinos
En términos simples alcalinos frente a alcalinotérreos los metales del Grupo 1 pierden un electrón externo, mientras que los metales del Grupo 2 pierden dos. Esa única diferencia condiciona las propiedades de los metales alcalinos y alcalinotérreos más que casi cualquier otro factor.
| Característica | Metales alcalinos, Grupo 1 | Metales alcalinotérreos, Grupo 2 |
|---|---|---|
| Electrones de valencia | 1 | 2 |
| Ion típico | M + | M 2+ |
| Reacción con agua fría | A menudo vigorosa o incluso violenta, formando hidróxido e hidrógeno | Menos uniforme: el berilio no reacciona con agua, el magnesio reacciona levemente, y el calcio, el estroncio y el bario reaccionan con creciente intensidad |
| Química común del oxígeno | Pueden formar óxidos, peróxidos o superóxidos | Comúnmente forman monóxidos; la mayoría de estos óxidos dan hidróxidos con agua, pero el BeO es una excepción |
Excepciones importantes que los estudiantes suelen pasar por alto
- No todos los metales del Grupo 2 reaccionan con agua de la misma manera.
- Los compuestos de berilio son más covalentes que el resto de la familia.
- No confunda metales alcalinos y alcalinotérreos como si pertenecieran al mismo grupo solo porque sus nombres suenan relacionados.
- El propiedades de los metales alcalinos y de los metales alcalinotérreos se aprenden mejor como patrones con excepciones, no como lemas rígidos.
Esa también es la mejor forma de comprender las propiedades químicas de los metales alcalinos y de los metales alcalinotérreos . Los patrones electrónicos le brindan la regla, pero las sustancias reales aportan matices. Y esos matices se vuelven aún más evidentes cuando se observa dónde ocurren realmente los elementos del Grupo 2: rara vez como metales puros y mucho más frecuentemente dentro de minerales, rocas, agua de mar, huesos y compuestos industriales.
Cómo ocurren los metales alcalinotérreos en la naturaleza
Si imagina un metal alcalinotérreo como una muestra brillante y pura situada en una roca, la naturaleza actúa de manera distinta. Los elementos del grupo 2 son lo suficientemente reactivos como para aparecer normalmente como iones dentro de minerales, sales, rocas, agua de mar, huesos y conchas, en lugar de como metales libres. Ya sea que alguien busque metales alcalinotérreos o el término más habitual, el patrón natural es el mismo: esta familia prefiere fuertemente los compuestos.
Ese patrón proviene directamente de las propiedades químicas de los metales alcalinotérreos 2+ 2+. Tienden a perder dos electrones externos y formar iones M
Por qué los metales alcalinotérreos no se encuentran libres en la naturaleza
Britannica y ThoughtCo ambos describen al Grupo 2 como reactivo, lo que explica por qué estos elementos rara vez se encuentran en estado libre. En el aire, muchos forman rápidamente recubrimientos de óxido. En entornos naturales, se estabilizan aún más como carbonatos, sulfatos, silicatos, fluoruros o cloruros. Por eso el calcio aparece en la piedra caliza y las conchas, el magnesio en minerales y agua de mar, y el estroncio o el bario en yacimientos minerales. El radio es aún más raro, y solo aparece en cantidades traza en minerales de uranio.
Minerales y compuestos comunes del Grupo 2
| El elemento | Fuente natural común | Compuesto conocido | Por qué ese compuesto es importante |
|---|---|---|---|
| El berilo | Beryl | BeO | La berilo es una fuente comercial del elemento, mientras que el óxido de berilio es un compuesto importante en materiales especializados |
| Magnesio | Magnesita, dolomita, agua de mar | MgCO₃ 3o Mg(OH)₂ 2 | Explica por qué el magnesio se encuentra con mayor frecuencia en minerales, agua de mar y medicina que como metal puro |
| Calcio | Piedra caliza, tiza, mármol, yeso, huesos, conchas | Caco 3 | Relaciona la geología, los materiales de construcción y los esqueletos en un compuesto muy común |
| Estróncio | Celestina, estroncianita | SrSO₄ 4o SrCO₃ 3 | Estos minerales son las principales fuentes naturales de compuestos de estroncio |
| El barrio | Baritina, witherita | BaSO 4 | La baritina es el mineral clave, y el sulfato de bario es uno de los compuestos de bario más conocidos |
| Radio | Cantidades traza en pechblenda y otros minerales de uranio | RaCl 2 | Su escasez y radiactividad hacen que los compuestos de radio hayan sido históricamente importantes, pero poco comunes |
EBSCO señala que el calcio y el magnesio también están presentes en el agua de mar a concentraciones aproximadas de 0,4 g/L y 1,3 g/L, respectivamente. Eso ayuda a explicar por qué este grupo de metales alcalinotérreos no solo está vinculado a los minerales, sino también al agua dura, a los sistemas marinos y a los tejidos vivos.
Cómo se aíslan estos metales de sus compuestos
Dado que los metales del grupo 2 suelen encontrarse atrapados dentro de compuestos, la extracción comienza con minerales, salmueras o depósitos minerales. Una idea industrial común es sencilla: primero se convierte el material en un óxido o haluro más manejable y luego se emplea electrólisis o reducción química para liberar el metal. Britannica describe la obtención temprana de magnesio, calcio, estroncio y bario mediante electrólisis, mientras que EBSCO señala que la producción moderna sigue recurriendo habitualmente a cloruros fundidos, reducción de óxidos o rutas relacionadas, según el elemento en cuestión. El berilio constituye un recordatorio útil de que este grupo no es perfectamente uniforme, ya que puede obtenerse mediante la reducción del fluoruro de berilio.
Así pues, en la vida cotidiana, las personas suelen encontrarse con los elementos del Grupo 2 a través de la caliza, el yeso, el magnesio procedente del agua de mar, el bario o el calcio biológico, y no mediante muestras de metal puro. Este detalle es importante, porque la relevancia práctica de estos elementos depende mucho más de sus compuestos y formas que del metal puro en sí.
Ejemplos de metales alcalinotérreos en la vida cotidiana
El Grupo 2 resulta mucho más memorable cuando se asocia cada elemento con algo tangible: huesos, antiácidos, yeso, fuegos artificiales, fluidos de perforación y antiguos esferos luminosos son todos ejemplos útiles. ejemplos de metales alcalinotérreos si alguna vez te has preguntado ¿es el magnesio un metal o un no metal? o ¿es el Ca un metal? , ambas respuestas son sencillas: el magnesio y el calcio son metales. Sin embargo, en la vida cotidiana, las personas suelen encontrarse con estas sustancias en forma de compuestos, y no como muestras de metal puro.
Usos cotidianos de los compuestos de magnesio y calcio
- Magnesio : El magnesio es uno de los elementos biológicamente más importantes elementos alcalinotérreos . El Hoja informativa sobre el magnesio del NIH señala que es un cofactor en más de 300 sistemas enzimáticos y que apoya la función muscular y nerviosa, la producción de energía y la estructura ósea. Algunos compuestos de magnesio también aparecen en ciertos antiácidos y laxantes, mientras que el metal magnesio es valorado en aleaciones ligeras donde la reducción de masa resulta fundamental.
- Calcio los compuestos de calcio dominan la vida cotidiana. El calcio contribuye a dar estructura a los huesos y a los dientes, y compuestos como el carbonato cálcico y el sulfato cálcico son fundamentales en la composición de la piedra caliza, el cemento, el yeso y los paneles de yeso. Esto convierte al calcio en uno de los vínculos más evidentes entre la química, la biología y la construcción.
Aplicaciones especializadas del estroncio y el bario
- Estróncio las sales de estroncio son especialmente conocidas por producir colores rojos intensos en fuegos artificiales y bengalas de señalización. Incluso quienes no recuerdan íntegramente la lista completa del grupo 2 suelen recordar el estroncio una vez que se asocia con su color característico.
- El barrio los compuestos de bario tienen importancia en la industria y en la medicina. El Perfil de bario del NLM describe los principales usos en lodos de perforación, pinturas, plásticos, ladrillos y vidrio. También señala una importante contraindicación médica: el sulfato de bario, altamente insoluble, se utiliza como material radiopaco en algunos exámenes de rayos X porque, en general, no es absorbido por el organismo.
- Radio : El radio es principalmente un caso histórico o científico estrictamente controlado. El Página del NRC sobre el radio describe su uso anterior en pinturas luminiscentes y en la terapia temprana del cáncer. La mayoría de esos usos han sido sustituidos, aunque aún existen algunos usos regulados, como ciertas aplicaciones industriales de radiografía.
Por qué la forma y el tipo de compuesto importan en el uso real
En el grupo 2, la forma que las personas utilizan suele ser el compuesto, no el metal puro.
Esa única idea aclara mucha confusión. El magnesio presente en los alimentos o en medicamentos no es lo mismo que la cinta de magnesio en combustión. El calcio presente en los huesos no es lo mismo que el metal calcio reactivo. El bario constituye el ejemplo más contundente de por qué la forma importa: el sulfato de bario insoluble puede ser útil en estudios de imagen, mientras que los compuestos de bario más solubles requieren una precaución mucho mayor. El radio lleva este punto aún más lejos, ya que su radiactividad —y no solo su ubicación entre los metales— determina cómo debe manipularse.
Por tanto, el valor del grupo 2 no es en absoluto abstracto. Estos elementos ayudan a explicar cómo un mismo grupo puede resultar relevante en nutrición, materiales, medicina, procesamiento industrial y normas de seguridad. A menudo, una breve lista de usos reales es suficiente para que el patrón general quede fijado.
Conclusiones clave sobre los elementos del grupo 2
En este punto, el grupo de metales alcalinotérreos debería parecer menos una lista para memorizar y más un patrón que se puede leer directamente desde la columna del grupo 2 en la tabla periódica ¿Alguien todavía pregunta? ¿Qué son los metales alcalinotérreos? , la respuesta breve sigue siendo sencilla: berilio, magnesio, calcio, estroncio, bario y radio. Una definición más completa de metales alcalinotérreos es aún más útil: seis elementos metálicos del grupo 2 que normalmente pierden dos electrones externos y forman iones M 2+²⁺.
Conclusiones clave sobre los metales alcalinotérreos
- La ubicación importa: estos seis elementos del grupo 2 se sitúan en la segunda columna desde la izquierda, en la sección del grupo 2 del bloque s.
- Los miembros de la familia son fijos: Be, Mg, Ca, Sr, Ba y Ra constituyen el conjunto completo.
- La química compartida explica el parecido familiar: su configuración ns 2el patrón de valencia hace que los iones +2 sean el resultado común, un punto central resumido por LibreTexts.
- Las principales tendencias descendentes son predecibles: el radio atómico aumenta, la energía de ionización disminuye generalmente y la reactividad suele aumentar al descender en el grupo.
- Las excepciones son importantes: el berilio se comporta de forma más covalente que los demás, el magnesio puede parecer menos reactivo debido a su capa superficial y el radio se analiza principalmente desde el punto de vista de su radiactividad.
- En la vida real, normalmente se tratan compuestos, no metales puros: las personas se encuentran con carbonato de calcio, óxido de magnesio y sulfato de bario con mucha mayor frecuencia que con calcio, magnesio o bario elementales.
El tabla periódica de los metales alcalinotérreos la columna es más fácil de recordar como seis metales vinculados por una regla: normalmente forman iones 2+, aunque cada uno de ellos expresa dicha regla de manera ligeramente distinta.
De la química del grupo 2 a las piezas metálicas fabricadas
Esa química va mucho más allá de los libros de texto. LibreTexts señala que el magnesio elemental se produce a gran escala y se utiliza en aleaciones ligeras para estructuras de aeronaves y componentes de motores automotrices. Una guía más amplia sobre aleaciones muestra por qué esto es relevante: los ingenieros ajustan la composición y el procesamiento para equilibrar peso, resistencia mecánica, resistencia a la corrosión y facilidad de mecanizado en componentes reales.
Para los lectores que pasan de la columna del grupo 2 en la tabla periódica visión a la fabricación, Shaoyi Metal Technology ofrece un ejemplo práctico de esa conexión. Sus páginas sobre materiales y mecanizado automotrices describen la producción de piezas metálicas, desde la prototipación hasta la producción en masa, donde el comportamiento del material y el control del proceso deben funcionar conjuntamente. Eso convierte al tabla periódica de los metales alcalinotérreos en algo más que un cuadro para el aula. También forma parte de la lógica subyacente a la selección de metales y aleaciones para piezas ingenieriles que deben ser ligeras, fiables y fabricables.
Preguntas frecuentes sobre los metales alcalinotérreos
1. ¿Cuáles son los seis metales alcalinotérreos?
Los seis metales alcalinotérreos son berilio, magnesio, calcio, estroncio, bario y radio. Ocupan el Grupo 2 de la tabla periódica y se agrupan juntos porque normalmente pierden dos electrones externos, lo que da lugar a un patrón común de ion 2+ en muchos compuestos.
2. ¿En qué se diferencian los metales alcalinotérreos de los metales alcalinos?
Los metales alcalinos pertenecen al Grupo 1 y suelen formar iones 1+ porque tienen un electrón de valencia. Los metales alcalinotérreos se encuentran en el Grupo 2, generalmente forman iones 2+ y tienden a ser menos reactivos en conjunto. Ese electrón de valencia adicional modifica la intensidad con la que se unen, su reacción con el agua y los tipos de sales y óxidos que comúnmente forman.
3. ¿Por qué los metales alcalinotérreos no se encuentran libres en la naturaleza?
Estos metales son lo suficientemente reactivos como para no permanecer mucho tiempo en forma elemental pura en entornos naturales. En cambio, se combinan con iones de oxígeno, carbonato, sulfato, cloruro o silicato y pasan a formar parte de minerales, rocas, agua de mar, conchas y huesos. Por eso, las personas suelen encontrar al Grupo 2 en forma de compuestos, y no como muestras de metal puro.
4. ¿Reaccionan todos los metales alcalinotérreos con el agua?
No, y esta es una de las excepciones más útiles que vale la pena recordar. El berilio es en gran medida resistente al agua; el magnesio reacciona lentamente con el agua fría porque una capa superficial limita la reacción; y el calcio, el estroncio y el bario reaccionan con mayor facilidad. En general, la reactividad con el agua aumenta al descender en el Grupo 2.
5. ¿Por qué son importantes los metales alcalinotérreos en la industria y la fabricación?
Su importancia radica tanto en sus compuestos como en su papel en la selección de aleaciones. El magnesio resulta valioso cuando se requiere menor peso; los compuestos de calcio son fundamentales en la fabricación de cemento y yeso; y los compuestos de bario se seleccionan para usos industriales y médicos especializados. En la producción real, comprender el comportamiento de los metales ayuda a guiar los procesos de mecanizado, la estabilidad de los procesos y la calidad de las piezas, razón por la cual proveedores como Shaoyi Metal Technology destacan el mecanizado automotriz certificado, el control de procesos y el soporte desde piezas prototipo hasta la producción en masa.
 Pequeños lotes, altos estándares. Nuestro servicio de prototipado rápido hace que la validación sea más rápida y fácil —
Pequeños lotes, altos estándares. Nuestro servicio de prototipado rápido hace que la validación sea más rápida y fácil —
