Hvad er de alkaliske jordmetaller? Gruppe 2 giver endelig mening
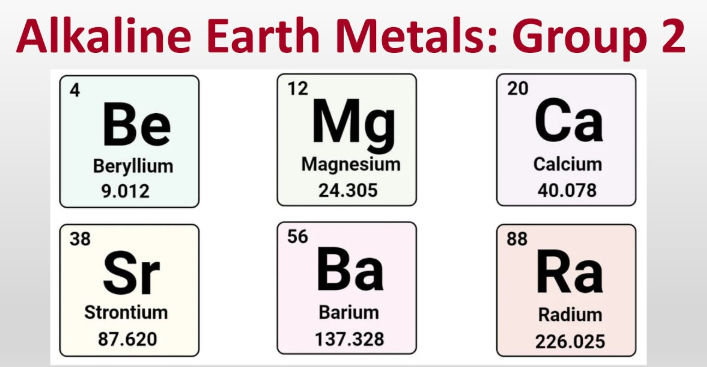
Hvad er alkaliske jordmetaller?
Hvis du har søgt efter hvad er alkaliske jordmetaller , så er her det direkte svar: De er de seks elementer i Gruppe 2 gruppe 2 definition af alkaliske jordmetaller er udgangspunktet, men navnet fortæller også meget om, hvordan denne gruppe opfører sig.
Hvad er de alkaliske jordmetaller i én sætning
De alkaliske jordmetaller er beryllium, magnesium, calcium, strontium, barium og radium – de seks metalliske elementer i gruppe 2, som normalt danner +2-ioner.
- Beryllium (Be)
- Magnesium (Mg)
- Kalcium (Ca)
- Strontium (Sr)
- Barium (Ba)
- Radium (Ra)
Hvorfor navnet alkaliske jordmetaller giver mening
For begyndere bliver definitionen af alkaliske jordmetaller meget nemmere, når man opdeler udtrykket i tre dele.
Alkalisk betyder, at deres oxider og hydroxider er basiske, ikke sure. Jorden er et historisk ord. Tidlige kemikere brugte det til varmebestandige, mineral-lignende stoffer, der ikke smeltede eller opløste sig let i vand, et punkt forklaret af Britannica . Metaller betyder, at elementerne selv er metalliske, typisk glinsende og gode til at afgive elektroner i reaktioner.
Det giver dig den grundlæggende betydning af alkaliske jordmetaller uden først at skulle have kendskab til avanceret kemi. Det er også en nyttig kort beskrivelse af alkaliske jordmetaller : en gruppe 2-metal-familie med fælles kemiske egenskaber, en fælles placering i det periodiske system og en betydelig rolle i den virkelige verden. Magnesium forekommer i legeringer og biologiske systemer. Calcium er afgørende for knogler, skaller og byggematerialer. Barium, strontium og radium optræder i mere specialiserede sammenhænge.
Denne artikel starter bevidst simpelt. En overskuelig liste er nem at huske, men familien bliver rigtigt tydelig, når man ser, hvor disse grundstoffer er placeret, og hvorfor netop denne placering giver dem så lignende egenskaber.
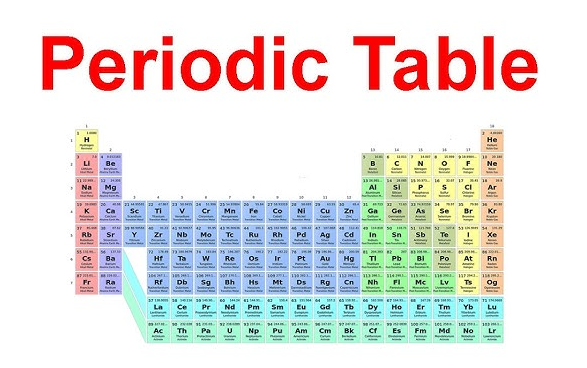
Hvor gruppe 2 ligger i det periodiske system
Familiens navn bliver meget nemmere at huske, når man faktisk kan identificere den. Hvis du undrer dig over hvor alkaliske jordmetaller findes i det periodiske system , så se på den anden lodrette kolonne fra venstre. Denne lodrette kolonne er gruppe 2 i det periodiske system , placeret lige ved siden af alkalimetallerne i gruppe 1. A gruppe 2 i det periodiske system visningen viser hver gang den samme rette linje: beryllium øverst, derefter magnesium, calcium, strontium, barium og radium nedad gennem perioderne.
I et alkalijordmetaller i det periodiske system diagrammet tilhører disse seks elementer s-blokken. Deres fælles placering er betydningsfuld, fordi den afspejler et fælles elektronmønster. Som LibreTexts forklarer, har gruppens 2-elementer en ns 2valenskonfiguration, hvilket betyder, at de har to ydre elektroner.
Hvor alkalijordmetallerne findes i det periodiske system
Visuelt er mønsteret simpelt. Den gruppe 2-elementer i det periodiske system danner én familiekolonne tværs gennem perioderne 2 til 7. Mange undervisningsdiagrammer fremhæver alkaliske jordmetaller i det periodiske system opstillinger med samme farve, fordi elementfamilier læses lodret, ikke vandret. Søgninger efter det periodiske system alkaliske jordmetaller handler faktisk om den ene søjle.
| Element | Symbol | Gruppe 2-position | Typisk ion | Kendt forbindelse |
|---|---|---|---|---|
| Beryllium | Be | Periode 2, øverst i gruppe 2 | Be2+ | BeO |
| Magnesium | Mg | Periode 3 | Mg2+ | Mgo |
| Calcium | Ca | Periode 4 | Ca2+ | Caco 3 |
| Strontium | Sr | Periode 5 | Sr2+ | SrCO 3 |
| Barium | BA | Periode 6 | BA 2+ | BaSO 4 |
| Radium | RA | Periode 7, nederst i gruppe 2 | RA 2+ | RaCl 2 |
Hvorfor grundstofferne i gruppe 2 danner +2-ioner
Disse to yderste elektroner styrer kemien. Atomerne i gruppe 2 har tendens til at miste begge elektroner, fordi det giver dem en mere stabil elektronkonfiguration. Resultatet er en +2-ion , såsom Mg 2+eller Ca 2+. Derfor danner disse metaller ofte forbindelser som oxider, chlorider, carbonater og sulfater. Mønsteret i formlerne er tydeligt: MgO, CaCl 2, CaCO 3, BaSO 4.
Hvordan man hurtigt genkender alkaliske jordmetallerne
En hurtig identifikationstrik er at lede efter tre kriterier på én gang: anden gruppe, metalliske elementer og en typisk +2-ladning. I forhold til de tilstødende alkalimetaller, som har ét valenselektron og normalt danner +1-ioner, har gruppens 2-elementer ét ekstra ydre elektron og er generelt mindre reaktive. Alligevel hører de tydeligt til samme familie. Det interessante er, at hvert medlem udtrykker dette mønster lidt forskelligt, især fra beryllium øverst til radium nederst.
De seks alkaliske jordmetaller
En liste er nyttig, men den er ikke særlig huskelsesværdig i sig selv. Gruppe 2 begynder at føles mere reel, når hvert medlem har en tydelig identitet. Nogle forekommer i knogler eller havvand. Nogle farver fyrwerkeri. Én er fortrinsvis et historisk advarselstegn. Sammen tilhører de stadig samme familie, men hver har sin egen personlighed.
| Element | Symbol | Almindelig forekomst | Udpræget egenskab | Relevans i det virkelige liv |
|---|---|---|---|---|
| Beryllium | Be | Forekommer i mineraler såsom beryl | Meget let og stiv for en metal | Anvendes i specialiserede luft- og rumfarts- samt røntgenanvendelser; støv er farligt, hvis det indåndes |
| Magnesium | Mg | Forekommer i havvand og mineraler | Lav densitet og kraftigt hvid flamme ved forbrænding | Vigtig i lette legeringer, kosttilskud og biologi |
| Calcium | Ca | Almindelig i kalksten, knogler, skaller og kridt | Biologisk velkendt ion fra gruppe 2 | Nøgleelement i skeletter, cement, gips og mange naturlige mineraler |
| Strontium | Sr | Forekommer hovedsageligt i celestinit og strontianit | Salte frembringer en levende rød farve i flammer | Anvendes i fyrværkeri, signalraketter, lysstofmaterialer og nogle tandplejeprodukter |
| Barium | BA | Forekommer normalt sammen med baryt | Tung, tæt alkalisk jordmetalkation | Bariumsulfat er vigtigt inden for boring og medicinsk billeddannelse; opløselige bariumforbindelser kræver forsigtighed |
| Radium | RA | Forekommer i spormængder i uranmalm | Kraftig radioaktivitet dominerer dens kemiske historie | Mest historisk eller strengt kontrolleret videnskabelig relevans i dag |
Beryllium og magnesium øverst i gruppe 2
Den grundstoffet beryllium står øverst i familien og antyder allerede, at gruppe 2 ikke er fuldstændig ensartet. Det er almindeligt forbundet med mineralet beryl, den samme mineralfamilie, der omfatter smaragd og aquamarin. Beryllium skiller sig ud, fordi det er usædvanligt let og stift. Det gør det nyttigt i højtydende komponenter, hvor lav masse er afgørende. Samtidig er beryllium et materiale, der kræver særlig forsigtighed i industrielle miljøer, da fin støv kan være skadeligt, hvis det indåndes. Det huskes derfor både for sin ydeevne og for den forsigtighed, der kræves ved håndtering.
Magnesium føles langt mere velkendt. magnesiums kemiske symbol er Mg, og det er et af de mest kendte metaller i denne gruppe, fordi det forekommer i havvand, almindelige mineraler og levende systemer. Det er et meget let metal, og når det brænder, frembringer det et intensivt hvidt lys. Derfor er magnesium længe blevet associeret med fakler og stoffer, der brænder kraftigt. I dagligdagen møder de fleste mennesker det dog i mildere former, såsom kosttilskud, mavevægsneutraliserende forbindelser eller lette legeringer, der anvendes, hvor reduktion af masse er afgørende.
Calcium og strontium i dagligdags materialer
Calcium er det mest genkendelige medlem af gruppe 2 for mange læsere. Det forekommer i kalksten, kridt, skaller og knogler, så det forbinder kemi med både geologi og biologi næsten øjeblikkeligt. Calciumcarbonat er den velkendte forbindelse her. Den hjælper med at forklare, hvorfor samme grundstofgruppe spiller en rolle ved huleformationer, byggematerialer og skeletter. Selv om calciummetallet i sig selv er reaktivt, er calciumforbindelser overalt, hvilket er grunden til, at dette grundstof ofte føles mere velkendt end eksotisk.
Strontium er nemmere at huske, når man forbinder det med farve. Det symbol for strontium er Sr, og strontium findes hovedsageligt i mineralerne celestinit og strontianit. Den Kongelige Kemiselskab beskriver det som et blødt, sølvfarvet metal, der brænder i luften og reagerer med vand. Dets salte er berømte for at frembringe glimrende røde farver i fyrværkeri og signalraketter. Samme kilde nævner også anvendelsen i mørkeglødende materialer samt strontiumchlorid-hexahydrat i tandpasta til følsomme tænder. Det gør strontium til et fremragende eksempel på, hvordan et grundstof kan være kemisk reaktivt, men alligevel primært opleves gennem dets forbindelser.
Barium og radium i avancerede eller specialiserede sammenhænge
Den barium-grundstoffet bliver ofte husket gennem sin vægt. Det er almindeligt forbundet med baryt, og en af dets mest kendte forbindelser er bariumsulfat. Denne forbindelse er betydningsfuld, fordi den er meget usolubel, hvilket hjælper med at forklare, hvorfor barium kan forekomme i praktiske sammenhænge såsom boringvæsker og medicinsk billeddannelse, mens andre opløselige bariumforbindelser behandles mere forsigtigt på grund af toksicitetsbekymringer. Barium minder læserne om, at den nyttige form af et gruppe-2-element ofte er en forbindelse, ikke det glinsende metal selv.
Radium sidder nederst i familien, men det blander sig ikke stille ind. På en radium-periodisk tabel syn, Ra markerer det punkt, hvor radioaktivitet bliver den afgørende egenskab. Radium forekommer naturligt kun i små mængder og er typisk forbundet med uranmalm. Historisk set blev det berømt for lysgivende farver og tidlige medicinske eksperimenter. I dag skyldes dets fare radioaktiviteten snarere end dens almindelige metaladfærd, så det håndteres under strenge kontrolforanstaltninger. I enkle ord tilhører radium stadig gruppe 2, men det behandles lige så meget med kernefysisk sikkerhed som med kemi i tankerne.
Placer disse seks side om side, og familien ser ikke længere ud som en tom liste over navne. Størrelse, reaktivitet, almindelige forbindelser og endda den måde, hvorpå hvert grundstof optræder i hverdagen, ændrer sig, når man bevæger sig nedad i gruppen. Dette skiftende mønster er netop, hvor gruppe 2 bliver særligt nyttig, fordi rækkefølgen fra beryllium til radium begynder at afsløre tendenser i stedet for uvæsentlige detaljer.
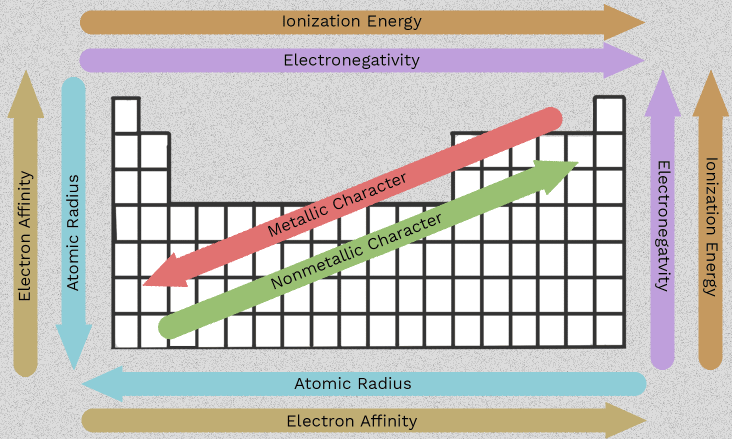
Egenskaber ved alkaliske jordmetaller og tendenser i gruppe 2
Denne ændring i rækkefølge fra beryllium til radium er, hvad der gør gruppe 2 nyttig. I stedet for at huske seks isolerede fakta kan du følge et par mønstre, der gentager sig ned ad kolonnen. Det vigtigste egenskaber for alkaliske jordmetaller udgår alle fra én fælles egenskab: Hvert atom har to yderste elektroner, som det typisk taber.
Når du forstår, hvordan størrelse, elektronbeskyttelse og ioniseringsenergi ændrer sig ned ad gruppen, bliver familien meget nemmere at forudsige. Disse karakteristika for alkaliske jordmetaller er ikke blot eksamensfakta. De forklarer, hvorfor nogle medlemmer reagerer hurtigere, hvorfor nogle forbindelser opløses bedre end andre og hvorfor nogle tendenser kræver omhyggelig formulering i stedet for simple pile.
Fælles egenskaber for alkaliske jordmetaller
De fleste medlemmer af gruppe 2 er silberfarvede metaller, der normalt danner M 2+ioner og danner fortrinsvis ioniske forbindelser. De opfører sig som reduktionsmidler, fordi de afgiver elektroner. I forhold til metallene i gruppe 1 er de generelt mindre reaktive, men de er stadig kemisk aktive nok til at danne mange almindelige oxider, chlorider, carbonater og sulfater.
En simpel måde at organisere de kemiske egenskaber ved alkaliske jordmetaller er at adskille det, der forbliver konstant, fra det, der ændrer sig. Det, der forbliver konstant, er den sædvanlige +2 oxidationstilstand. Det, der ændrer sig, er, hvor nemt hvert enkelt element afgiver disse to elektroner. Det er her, at tendenserne begynder at blive relevante.
Tendenser nedad i gruppe 2 og hvad de betyder
Data indsamlet af LibreTexts og tendensforklaringer fra Save My Exams viser samme overordnede mønster. Atomradius stiger fra 112 pm for Be til 253 pm for Ba, mens den første ioniseringsenergi falder fra 900 til 503 kJ/mol. I almindeligt sprog betyder det, at de yderste elektroner befinder sig længere fra kernen og er afskærmet af flere indre skaller, så de er nemmere at fjerne.
| Trend | Retning nedad i gruppe 2 | Kemisk årsag | Hvad dette betyder i praksis |
|---|---|---|---|
| Atomradius | Øger | Hvert element har en ekstra elektronskal og mere afskærmning | Større atomer holder ydre elektroner mindre fast |
| Første og anden ioniseringsenergi | Fald samlet set | Ydre elektroner er længere fra kernen, så tiltrækningen er svagere | Dannelse af M 2+ioner bliver nemmere |
| Reaktivitet | Stiger samlet set | Lavere ioniseringsenergier gør det nemmere at miste elektroner | Tungere medlemmer reagerer mere voldsomt med syrer, oxygen og ofte også vand |
| Smeltpunkt | Faldende generelt, men ikke jævnt | Større metalioner svækker metalbindingen, selvom strukturen også spiller en rolle | Brug ordet "generelt" her, fordi Mg og Ca ikke følger en perfekt pæn linje |
| Tæthed | Uregelmæssig | Masse, atomstørrelse og metalpakning ændres alle sammen | Du kan ikke betragte densiteten som én simpel faldende tendens |
| Hydroxidopløselighed | Øger | Balancen mellem gitterenergi og hydrateringsenergi skifter nedad i gruppen | Tungere hydroxider danner mere alkaliske opløsninger |
| Sulfatopløselighed | Formindsker | Hydrateringsenergien falder, når kationen bliver større | Forbindelser som BaSO 4bliver meget uopløselige |
Tæthed og smelteadfærd er de to tendenser, som elever ofte forenkler for meget. Tætheden følger ikke en lige linje, fordi både masse og volumen ændrer sig, og metalatomerne pakkes ikke på samme måde i hver krystal. Smeltepunkter kræver også omhu. De falder generelt nedad, fordi større ioner svækker den metalliske gitterstruktur, men Mg har et usædvanligt lavt smeltepunkt på 650 °C, mens Ca stiger til 842 °C, inden værdierne falder igen. Så en af de sikreste karakteristika for alkaliske jordmetaller er denne: Den brede tendens er reel, men de fysiske detaljer er ikke perfekt glatte.
Opløselighed har samme advarselsetiket. Der findes ingen enkelt regel, der dækker alle salte i gruppe 2. Hydroxider bliver mere opløselige nedad i gruppen, mens sulfater bliver mindre opløselige. Hvis nogen siger «opløseligheden stiger nedad i gruppe 2», er det vigtigste spørgsmål: «Hvilke forbindelser?»
Hvorfor reagerer alkaliske jordmetaller, som de gør
Så, er alkaliske jordmetaller reaktive ? Ja, og det generelle svar er, at de bliver mere reaktive, når man bevæger sig nedad i gruppen. Årsagen er den samme elektronhistorie, der er beskrevet ovenfor. Lavere første og anden ioniseringsenergi betyder, at atomerne kan miste to elektroner nemmere og nå den almindelige M 2+-tilstand hurtigere.
Det påvirker reelle reaktioner. Nedad i gruppen bliver reaktioner med fortyndede syrer hurtigere, reaktioner med oxygen mere voldsomme, og de tungere medlemmer er nemmere at oxideres. Save My Exams bemærker, at barium er så reaktivt, at det skal opbevares under olie – hvilket er et praktisk tegn på, hvor langt reaktivitetstrenden kan gå.
- Atomradius stiger nedad i gruppe 2.
- Ioniseringsenergien falder nedad i gruppe 2.
- Reaktiviteten stiger, fordi det bliver nemmere at miste to elektroner.
- Smeltepunkter og densitet viser uregelmæssigheder, så undgå absolutte regler.
- Hydroxider og sulfater viser modsatte opløselighedstendenser.
Disse mønstre gør familien forudsigelig, men ikke fuldstændig ensartet. Lige nær toppen af gruppen begynder beryllium allerede at bøje reglerne, og magnesium tilføjer endnu en almindelig undtagelse, der er mere betydningsfuld, end mange begyndere forventer.
Alkalimetaller og jordalkalimetaller
Brede tendenser gør gruppe 2 nemmere at lære, men familien giver ikke længere mening, hvis hvert medlem behandles som identisk. Den største advarsel er beryllium. Magnesium tilføjer en mere praktisk, daglig undtagelse. Og når folk sammenligner alkalimetaller og jordalkalimetaller , kan lignende navne skjule nogle meget forskellige kemiske egenskaber.
Hvorfor beryllium ikke opfører sig som et typisk metal fra gruppe 2
BYJU'S beskriver beryllium som den tydelige outlier i gruppe 2. Dets usædvanligt lille størrelse, høje ioniseringsenergi og stærke polariserende evne giver det en adfærd, der er mindre karakteristisk for familien. I almindeligt sprog er Be 2+trækker kraftigt i nærliggende elektron skyer, så berylliumforbindelser er ofte mere kovalente end de mere ioniske forbindelser, der dannes af de tungere medlemmer. Samme kilde bemærker også, at beryllium har højere smelte- og kogepunkter end de øvrige gruppemedlemmer og ikke reagerer med vand på samme måde som dets naboer.
Magnesium er ikke så usædvanligt som beryllium, men det kan alligevel virke mindre reaktivt, end eleverne forventer. LibreTexts bemærker, at meget ren magnesium reagerer kun svagt med koldt vand, og reaktionen bremses hurtigt, fordi næsten uopløseligt magnesiumhydroxid danner en barriere på overfladen. Nederst i gruppen diskuteres radium normalt særskilt, fordi dets radioaktivitet dominerer både praktisk anvendelse og sikkerhedsdiskussioner.
Hvordan alkaliske jordmetaller adskiller sig fra alkalimetaller
I simpel alkali versus alkalisk jord betydning mister metalgruppe 1 én yderste elektron, mens metalgruppe 2 mister to. Den enkelte forskel former egenskaberne for alkalimetaller og alkaliske jordmetaller mere end næsten noget andet. mere end næsten noget andet.
| Funktion | Alkalimetaller, gruppe 1 | Alkalijordmetaller, gruppe 2 |
|---|---|---|
| Valenselektroner | 1 | 2 |
| Typisk ion | Herrer stræk jeans + | Herrer stræk jeans 2+ |
| Reaktion med koldt vand | Ofte kraftig eller endda voldelig og danner hydroxid og brint | Mindre ensartet: Be reagerer ikke med vand, Mg reagerer svagt, mens Ca, Sr og Ba reagerer med stigende kraft |
| Almindelig iltoxygen-kemi | Kan danne oxider, peroxider eller superoxider | Danner typisk monoxider; de fleste af disse oxider danner hydroxider med vand, men BeO er en undtagelse |
Vigtige undtagelser, som elever ofte overser
- Ikke alle metaller i gruppe 2 reagerer på samme måde med vand.
- Berylliumforbindelser er mere kovalente end resten af familien.
- Forveksl ikke alkalimetaller og jordalkalimetaller som samme gruppe bare fordi navnene lyder beslægtede.
- Den egenskaberne for alkalimetaller og jordalkalimetaller lærer man bedst som mønstre med undtagelser, ikke som faste slagord.
Det er også den bedste måde at forstå de kemiske egenskaber for alkalimetaller og jordalkalimetaller . Elektronmønstre giver dig reglen, men reelle stoffer tilføjer struktur. Og denne struktur bliver endnu tydeligere, når man ser på, hvor grundstofferne i gruppe 2 faktisk forekommer: sjældent som rene metaller og langt oftere inden i mineraler, klipper, havvand, knogler og industrielle forbindelser.
Hvordan jordalkalimetaller forekommer i naturen
Hvis du forestiller dig en alkalijordmetal som en lys, ren prøve, der ligger i en klippe, så fungerer naturen anderledes. Grundstofferne i gruppe 2 er reaktive nok til, at de normalt optræder som ioner i mineraler, salte, klipper, havvand, knogler og skaller frem for som frie metaller. Uanset om nogen søger efter alkalijordmetaller eller den mere almindelige betegnelse, er det naturlige mønster det samme: denne gruppe foretrækker kraftigt forbindelser.
Dette mønster stammer direkte fra de kemiske egenskaber ved alkalijordmetaller . De har tendens til at miste to ydre elektroner og danne stabile M 2+ioner. Når dette sker, binder oxygen-, carbonat-, sulfat- og halidioner dem hurtigt sammen i faste forbindelser, der kan overleve i geologi og biologi.
Hvorfor alkalijordmetaller ikke findes frit i naturen
Britannica og ThoughtCo begge beskriver gruppe 2 som reaktive, hvilket forklarer, hvorfor disse elementer sjældent findes i ubundet form. I luften danner mange hurtigt oxidlag. I naturlige miljøer stabiliseres de yderligere som carbonater, sulfater, silikater, fluorider eller chlorider. Derfor findes calcium i kalksten og skaller, magnesium i mineraler og havvand samt strontium og barium i malmforekomster. Radium er endnu sjældnere og forekommer kun i spor mængder i uranmalm.
Almindelige mineraler og forbindelser af gruppe 2
| Element | Almindelig naturlig kilde | Kendt forbindelse | Hvorfor denne forbindelse er betydningsfuld |
|---|---|---|---|
| Beryllium | Beryl | BeO | Beryl er en kommerciel kilde til elementet, mens berylliumoxid er en vigtig forbindelse i specialmaterialer |
| Magnesium | Magnesit, dolomit, havvand | MgCO₃ 3eller Mg(OH)₂ 2 | Viser, hvorfor magnesium oftere mødes i mineraler, havvand og medicin end som rent metal |
| Calcium | Kalksten, kridt, marmor, gips, knogler, skaller | Caco 3 | Forbinder geologi, byggematerialer og skeletter i én meget almindelig forbindelse |
| Strontium | Celestit, strontianit | SrSO 4eller SrCO 3 | Disse mineraler er de vigtigste naturlige kilder til strontiumforbindelser |
| Barium | Baryt, witherit | BaSO 4 | Baryt er den vigtigste malm, og bariumsulfat er en af de mest kendte bariumforbindelser |
| Radium | Spormængder i pitchblende og andre uranmalm | RaCl 2 | Dets sjældenhed og radioaktivitet gør radiumforbindelser historisk betydningsfulde, men sjældne |
EBSCO bemærker, at calcium og magnesium også forekommer i havvand i koncentrationer på ca. 0,4 g/L og 1,3 g/L henholdsvis. Det hjælper med at forklare, hvorfor denne alkaliske jordart familie ikke kun er forbundet med malm, men også med hårdt vand, marine systemer og levende væv.
Hvordan disse metaller isoleres fra deres forbindelser
Da gruppe 2-metaller normalt er indkapslet i forbindelser, starter udvindingen med malme, saltvandskoncentrater (brine) eller mineralaflejringer. En almindelig industriel fremgangsmåde er simpel: først omdannes materialet til en mere brugbar oxid- eller halogenidform, hvorefter metallet frigøres ved elektrolyse eller kemisk reduktion. Britannica beskriver tidlig isolering af magnesium, calcium, strontium og barium ved elektrolyse, mens EBSCO bemærker, at moderne produktion stadig ofte bygger på smeltede chlorider, oxidreduktion eller beslægtede ruter, afhængigt af det pågældende grundstof. Beryllium er en nyttig påmindelse om, at familien ikke er fuldstændig ensartet, da beryllium kan fremstilles ved reduktion af berylliumfluorid.
Så i det daglige liv støder folk normalt på gruppe 2 gennem kalksten, gips, magnesium fra havvand, baryt eller biologisk calcium, ikke gennem rå metalprøver. Denne detalje er vigtig, fordi de reelle anvendelsesmuligheder for disse grundstoffer i praksis er langt mere knyttet til deres forbindelser og former end til de rene metaller selv.
Eksempler på alkaliske jordmetaller i det daglige liv
Gruppe 2 bliver langt mere huskelsværdig, når man forbinder hvert grundstof med noget konkret. Knogler, mavesyretabletter, gips, fyrværkeri, boringsslam og gamle lysende urvisere er alle nyttige eksempler på alkaliske jordmetaller. eksempler på alkaliske jordmetaller . Hvis du nogensinde har undret dig over er magnesium et metal eller et ikke-metal eller er Ca et metal , er begge svar enkle: magnesium og calcium er metaller. I det daglige liv støder folk dog normalt på disse stoffer som forbindelser, ikke som rene metalprøver.
Almindelige anvendelser af magnesium- og calciumforbindelser
- Magnesium : Magnesium er ét af de biologisk mest vigtige alkaliske jordmetaller . Den NIH's faktablad om magnesium bemærker, at det er en cofaktor i mere end 300 enzymsystemer og understøtter muskel- og nervesfunktion, energiproduktion samt knogestruktur. Magnesiumforbindelser forekommer også i nogle mavesyremedicin og afføringsmidler, mens magnesiummetal værdsættes i lette legeringer, hvor reduktion af masse er afgørende.
- Calcium calciumforbindelser dominerer det daglige liv. Calcium bidrager til knoglers og tænders struktur, og forbindelser som calciumcarbonat og calciumsulfat er centrale i kridt, cement, gips og gipsplader. Det gør calcium til én af de tydeligste forbindelser mellem kemi, biologi og byggeri.
Specialiserede anvendelser af strontium og barium
- Strontium strontiumsalte er bedst kendt for at frembringe dybt røde farver i fyrværkeri og signalraketter. Endda læsere, der ikke husker hele gruppe 2-listen, husker ofte strontium, så snart farve bliver forbundet med det.
- Barium bariumforbindelser er betydningsfulde inden for industri og medicin. Den NLM's profil på barium beskriver de vigtigste anvendelser i boringsslam, maling, plastik, mursten og glas. Der nævnes også en vigtig medicinsk kontrast: stærkt usolubelt bariumsulfat bruges som et radiopaque materiale i nogle røntgenundersøgelser, fordi det generelt ikke absorberes af kroppen.
- Radium : Radium er primært et historisk eller strengt reguleret videnskabeligt tilfælde. NRC's radiumside beskriver dets tidligere anvendelse i lysgivende maling og tidlig kræftbehandling. De fleste af disse anvendelser er blevet erstattet, selvom der stadig findes nogle regulerede anvendelser, såsom bestemte industrielle radiografiapplikationer.
Hvorfor form og forbindelsestype betyder noget i praksis
I gruppe 2 er den form, man bruger, ofte forbindelsen og ikke det rene metal.
Den enkelte idé afklarer meget forvirring. Magnesium i føde eller medicin er ikke det samme som brændende magnesiumbånd. Calcium i knogler er ikke det samme som reaktivt calciummetal. Barium er det skarpeste eksempel på, hvorfor formen betyder noget: uopløseligt bariumsulfat kan være nyttigt ved billeddannelse, mens mere opløselige bariumforbindelser kræver langt større forsigtighed. Radium understreger punktet endnu mere, fordi dets radioaktivitet – og ikke kun dens placering blandt metallementerne – styrer, hvordan det håndteres.
Så værdien af gruppe 2 er slet ikke abstrakt. Disse elementer hjælper med at forklare, hvordan samme gruppe kan være relevant inden for ernæring, materialer, medicin, industrielle proceser og sikkerhedsregler. En kort liste over reelle anvendelser er ofte alt, hvad der kræves for, at det større mønster bliver vedholdende.
Vigtigste konklusioner om gruppe-2-elementer
På dette tidspunkt bør alkaliske jordmetaller-gruppen føles mindre som en liste, der skal læres udenad, og mere som et mønster, man direkte kan aflæse fra gruppe 2 i det periodiske system kolonne. Hvis nogen stadig spørger, hvad er de alkaliske jordmetaller , det korte svar forbliver enkelt: beryllium, magnesium, calcium, strontium, barium og radium. En mere udførlig definition af alkaliske jordmetaller er endnu mere nyttig: seks metalliske elementer i gruppe 2, der normalt afgiver to ydre elektroner og danner M 2+-ioner.
Vigtige konklusioner om de alkaliske jordmetaller
- Placeringen betyder noget: disse seks gruppe-2-elementer sidder i den anden kolonne fra venstre, altså i gruppe-2-området af s-blokken.
- Familieelementerne er faste: Be, Mg, Ca, Sr, Ba og Ra udgør hele gruppen.
- Fælles kemiske egenskaber forklarer familieligheden: deres ns 2valensmønster gør +2-ioner til den almindelige konsekvens, et kerneprincip, der opsummeres af LibreTexts.
- De vigtigste nedadgående tendenser er forudsigelige: atomradius stiger, ioniseringsenergien falder generelt, og reaktiviteten stiger normalt, når man bevæger sig ned ad gruppen.
- Undtagelserne er betydningsfulde: beryllium opfører sig mere kovalent end de øvrige, magnesium kan virke mindre reaktiv på grund af sin overfladelag, og radium diskuteres primært i forbindelse med radioaktivitet.
- I praksis betyder det normalt forbindelser, ikke rene metaller: folk støder på calciumcarbonat, magnesiumoxid og bariumsulfat langt oftere end på grundstofferne Ca, Mg eller Ba.
Den alkaliske jordmetaller – periodesystemet kolonne er nemmest at huske som seks metaller forbundet af én regel: de bliver normalt 2+-ioner, men hvert medlem udtrykker den regel lidt forskelligt.
Fra gruppe-2-kemi til konstruerede metaldele
Denne kemi rækker langt ud over lærebøger. LibreTexts bemærker, at grundstofmagnesium fremstilles i stor målestok og anvendes i lette legeringer til flyrammer og bilmotordelen. En mere omfattende legeringsvejledning viser, hvorfor det er vigtigt: ingeniører justerer sammensætning og bearbejdning for at opnå en balance mellem vægt, styrke, korrosionsbestandighed og bearbejdningsvenlighed i reelle komponenter.
For læserne, der bevæger sig fra gruppe 2 i det periodiske system synsvinkel til fremstilling, Shaoyi Metal Technology giver et praktisk eksempel på denne sammenhæng. Dets sider om automobilmaterialer og maskinbearbejdning beskriver fremstilling af metaldele fra prototypering til masseproduktion, hvor materialeadfærd og proceskontrol skal fungere sammen. Det gør alkaliske jordmetaller – periodesystemet mere end et tavlebillede til undervisning. Det er også en del af logikken bag valget af metaller og legeringer til tekniske dele, der skal være lette, pålidelige og fremstillelige.
Ofte stillede spørgsmål om alkaliske jordmetaller
1. Hvad er de seks alkaliske jordmetaller?
De seks alkaliske jordmetaller er beryllium, magnesium, calcium, strontium, barium og radium. De indtager gruppe 2 i det periodiske system og er samlet i denne gruppe, fordi de normalt afgiver to yderste elektroner, hvilket fører til et fælles 2+-ionmønster i mange forbindelser.
2. Hvordan adskiller alkaliske jordmetaller sig fra alkalimetaller?
Alkalimetallerne tilhører gruppe 1 og danner typisk 1+-ioner, fordi de har ét yderste elektron. Alkalijordmetallerne findes i gruppe 2, danner normalt 2+-ioner og er generelt mindre reaktive. Det ene ekstra valenselektron ændrer, hvor stærkt de binder, hvordan de reagerer med vand og hvilke typer salte og oxider de typisk danner.
3. Hvorfor findes alkalijordmetallerne ikke frit i naturen?
Disse metaller er så reaktive, at de normalt ikke forbliver i ren elementarform i længere tid i naturlige miljøer. I stedet forbinder de sig med oxygen-, carbonat-, sulfat-, chlorid- eller silikationer og bliver en del af mineraler, klipper, havvand, skaller og knogler. Derfor støder man normalt på gruppe 2 gennem forbindelser frem for rå metalprøver.
4. Reagerer alle alkalijordmetaller med vand?
Nej, og dette er en af de mest nyttige undtagelser, man bør huske. Beryllium er stort set modstandsdygtigt over for vand, magnesium reagerer langsomt i koldt vand, fordi en overfladelag begrænser reaktionen, og calcium, strontium og barium reagerer mere let. Generelt bliver reaktiviteten over for vand stærkere, jo længere ned ad gruppe 2 man bevæger sig.
5. Hvorfor er alkaliske jordmetaller vigtige inden for industri og fremstilling?
Deres betydning skyldes både deres forbindelser og deres rolle ved valg af legeringer. Magnesium er værdifuldt, hvor lavere vægt er afgørende, calciumforbindelser er centrale i cement og gips, og bariumforbindelser vælges til specialiserede industrielle og medicinske anvendelser. I praksis hjælper forståelse af metaladfærd med at styre bearbejdning, processtabilitet og delkvalitet, hvilket er grunden til, at leverandører som Shaoyi Metal Technology fremhæver certificeret automobilbearbejdning, proceskontrol samt support fra prototypedele til masseproduktion.
 Små partier, høje standarder. Vores hurtige prototyperingservice gør validering hurtigere og nemmere —
Små partier, høje standarder. Vores hurtige prototyperingservice gør validering hurtigere og nemmere —
