Alkaline Earth Metalleri Nedir? 2. Grup Sonunda Anlaşılır Hale Geliyor
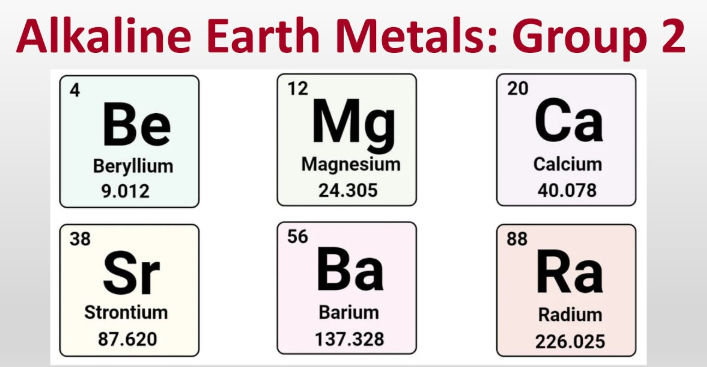
Alkaline Earth Metalleri Nedir?
Eğer aradıysanız alkaline earth metalleri nedir , işte doğrudan cevap: bunlar periyodik tablonun Grup 2 grubundaki altı elementtir. Bu hızlı alkaline earth metalleri tanımı başlangıç noktasıdır; ancak bu ailenin adı aynı zamanda davranışlarını da çok şey anlatır.
Alkaline earth metalleri tek bir cümleyle neydir?
Alkaline earth metalleri, berilyum, magnezyum, kalsiyum, stronsiyum, baryum ve radyum olmak üzere Grup 2’de yer alan ve genellikle +2 iyonları oluşturan altı metal elementidir.
- Berilyum (Be)
- Magnezyum (Mg)
- Kalsiyum (Ca)
- Stronsiyum (Sr)
- Baryum (Ba)
- Radyum (Ra)
Neden 'alkali toprak metalleri' adının mantıklı olduğu
Başlangıç seviyesi için alkali toprak tanımı ifadeyi üç parçaya ayırarak çok daha kolay anlaşılır hale gelir.
Alkalin bunun anlamı, bu elementlerin oksit ve hidroksitlerinin asidik değil, temel (bazik) özellik göstermesidir. Earth 'Toprak', tarihsel bir kelimedir. Erken dönem kimyacılar, suya kolayca çözünmeyen veya erimeyen, ısıya dayanıklı ve mineral benzeri maddeler için bu terimi kullanmışlardır; bu durum, Britannica . Metaller 'Metal' kelimesi ise bu elementlerin kendilerinin metalik olduğunu, genellikle parlak olduklarını ve kimyasal tepkimelerde elektron kaybetme eğiliminde olduklarını ifade eder.
Bu bilgiler size temel alkali toprak metalleri anlamını verir ileri kimya bilgisi gerektirmeden. Aynı zamanda toprak alkali metallerinin yararlı kısa tanımıdır : paylaşılan kimyasal özelliklere, periyodik tablodaki ortak konuma ve gerçek dünyada büyük bir role sahip olan 2. Grup metalleri ailesidir. Magnezyum, alaşımlarda ve biyolojide yer alır. Kalsiyum, kemiklerde, kabuklarda ve inşaat malzemelerinde önemlidir. Baryum, stronsiyum ve radyum daha özel bağlamlarda görünür.
Bu makale kasıtlı olarak basit başlar. Temiz bir liste ezberlemesi kolaydır; ancak bu elementlerin nerede yer aldıklarını ve neden bu konumlarının onlara benzer davranış kazandırdığını gördüğünüzde aile kavramı gerçekten netleşir.
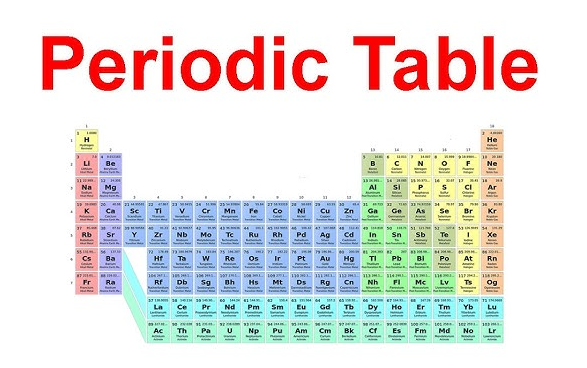
2. Grubun Periyodik Tablodaki Yeri
Aile ismi, onu gerçekten görebildiğinizde çok daha kolay akılda kalır. Eğer toprak alkali metaller periyodik tabloda nerede bulunur sorusunu soruyorsanız, soldan ikinci dikey sütuna bakın. Bu dikey sütun, periyodik tablodaki 2. gruptur , 1. Grup alkali metallerin hemen yanındadır. A 2. grup periyodik tablo görünüm, her seferinde aynı düz çizgiyi gösterir: en üstte berilyum, ardından aşağı doğru periyotlar boyunca magnezyum, kalsiyum, stronsiyum, baryum ve radyum.
Bir alkalin toprak metalleri periyodik tablosu grafikte bu altı element s-blok’a aittir. Ortak konumları önemli olur çünkü ortak bir elektron düzenini yansıtır. Çünkü LibreTexts açıklar, 2. gruptaki elementlerin ns 2değerlik konfigürasyonu vardır; bu da dış kabuklarında iki elektron taşıdıklarını gösterir.
Alkalin toprak metallerinin periyodik tabloda nerede bulunduğu
Görsel olarak desen basittir. periyodik tablonun 2. grubu elementleri 2. ile 7. periyotlar arasında tek bir aile sütunu oluşturur. Birçok sınıf diyagramı bunu vurgular. periyodik tablodaki toprak alkali metaller aynı renge sahip düzenler, çünkü element aileleri yatay değil, dikey olarak okunur. Aramalar: periyodik tablo toprak alkali metaller aslında o tek sütunu arar.
| Eleman | Sembolik | 2. Grup konumu | Tipik iyon | Tanıdık bileşik |
|---|---|---|---|---|
| Berilyum | Be | 2. Periyot, 2. Grubun tepesi | Be2+ | BeO |
| Magnesium | Mg | 3. Periyot | Mg2+ | MgO |
| Kalsiyum | Ca | Dönem 4 | Ca2+ | Cako 3 |
| Strontiyum | Sr | Dönem 5 | Sr2+ | SrCO 3 |
| Baryum | BA | Dönem 6 | BA 2+ | BaSO 4 |
| Radyum | RA | 2. Grup’un alt kısmı, 7. Dönem | RA 2+ | RaCl 2 |
2. Grup elementlerinin neden +2 iyon oluşturduğu
Bu iki dış elektron kimyasal davranışları belirler. 2. Grup atomları, daha kararlı bir elektron düzeni elde etmek için genellikle her iki elektronu da kaybeder. Sonuç olarak bir +2 iyon , örneğin Mg 2+veya Ca 2+. Bu nedenle bu metaller, oksitler, klorürler, karbonatlar ve sülfatlar gibi bileşikler oluşturur. Formüllerdeki deseni hemen fark edersiniz: MgO, CaCl 2, CaCO 3, BaSO 4.
Alkaline earth metalleri ailesini hızlıca tanıma yöntemi
Hızlı tanıma yöntemi olarak üç ipucunu aynı anda kontrol etmek yeterlidir: ikinci sütun, metal elementler ve genellikle +2 yük. Komşu alkali metallerle karşılaştırıldığında, alkali metallerin birer değerlik elektronu vardır ve genellikle +1 iyonlar oluştururken, 2. Grup elementleri bir ek dış elektrona sahiptir ve genellikle daha az reaktiftir. Yine de açıkça ortak bir aileye aittirler. İlginç olan kısım, her bir üyenin bu deseni biraz farklı şekilde sergilemesidir; özellikle en üstteki berilyumdan en alttaki radyuma kadar.
Altı Alkaline Earth Metal ile Tanışın
Bir liste yararlıdır, ancak yalnız başına çok akılda kalıcı değildir. Grup 2, her üyesi net bir kimliğe sahip olduğunda daha gerçekçi hale gelmeye başlar. Bazıları kemiklerde veya deniz suyunda bulunur. Bazıları havai fişekleri renklendirir. Bir tanesi çoğunlukla tarihsel bir uyarı işareti olarak geçer. Bir araya geldiklerinde hâlâ aynı aileye ait olsalar da her birinin kendi kişiliği vardır.
| Eleman | Sembolik | Yaygın oluşum | Dikkat çekici özellik | Gerçek Dünyadaki Geçerlilik |
|---|---|---|---|---|
| Berilyum | Be | Beril gibi minerallerde bulunur | Bir metal olarak çok hafif ve serttir | Uzay teknolojisi ve X-ışını uygulamalarında özel amaçlarla kullanılır; tozu solunursa tehlikelidir |
| Magnesium | Mg | Deniz suyunda ve minerallerde bulunur | Düşük yoğunluğa sahiptir ve yanarken parlak beyaz alev üretir | Hafif alaşımlarda, takviyelerde ve biyolojide önemlidir |
| Kalsiyum | Ca | Kireçtaşı, kemikler, kabuklar ve tebeşirde yaygındır | Biyolojik olarak tanıdık Grup 2 iyonu | İskeletlerde, çimentoda, alçıda ve birçok doğal minerallerde anahtar rol oynar |
| Strontiyum | Sr | Ana olarak selesit ve stronsiyanit içinde bulunur | Tuzları alevlerde canlı kırmızı renk üretir | Havanlar, işaret fişekleri, parlayan malzemeler ve bazı diş ürünleri için kullanılır |
| Baryum | BA | Genellikle baritin yanında bulunur | Yoğun, ağır bir toprak alkali metalidir | Baryum sülfat, sondaj ve tıbbi görüntülemede önemlidir; çözünebilir baryum bileşikleri dikkatli kullanılmalıdır |
| Radyum | RA | Uranyum cevherlerinde iz miktarlarda bulunur | Güçlü radyoaktivite, kimyasal davranışını belirler | Bugün çoğunlukla tarihsel ya da sıkı şekilde kontrol edilen bilimsel bir öneme sahiptir |
2. Grup’un başında berilyum ve magnezyum bulunur
The berilyum elementi bu ailenin en üstünde yer alır ve zaten 2. Grup’un tam olarak homojen olmadığını gösterir. Genellikle beril mineraliyle ilişkilendirilir; bu, aynı zamanda zümrüt ve akvamarin minerallerini de içeren bir mineral ailesidir. Berilyum, olağanüstü hafif ve rijit olması nedeniyle dikkat çeker. Bu özelliği, düşük kütle önemli olduğu yüksek performanslı parçalarda kullanılmasını sağlar. Aynı zamanda berilyum, endüstriyel ortamlarda dikkatli işlenmesi gereken bir maddedir; çünkü ince tozu solunduğunda zararlı olabilir. Dolayısıyla hem yüksek performansı hem de dikkatli işlemesi gerektirmesiyle hatırlanır.
Magnezyum çok daha tanıdık bir his verir. magnezyumun kimyasal sembolü mg'dir ve bu gruptaki en iyi bilinen metallerden biridir çünkü deniz suyunda, yaygın minerallerde ve canlı sistemlerde bulunur. Çok hafif bir metaldir ve yanarken yoğun bir beyaz ışık yayar. Bu nedenle magnezyum, uzun süredir işaret fişekleri ve parlak yanan malzemelerle ilişkilendirilmiştir. Ancak günlük yaşamda çoğu kişi onu daha yumuşak formlarda, örneğin beslenme açısından rolleri, antiasit bileşikleri veya kütle azaltılmasının önemli olduğu yerlerde kullanılan hafif alaşımlar şeklinde karşılar.
Günlük malzemelerde kalsiyum ve stronsiyum
Kalsiyum, birçok okuyucu için Grup 2'nin en tanınabilir üyesidir. Kireçtaşı, tebeşir, kabuklar ve kemiklerde bulunduğu için kimyayı hemen hem jeolojiye hem de biyolojiye bağlar. Burada tanıdık bileşik kalsiyum karbonattır. Aynı ailenin mağara oluşumlarında, yapı taşlarında ve iskeletlerde önem taşıyabileceğini açıklamaya yardımcı olur. Kalsiyum metalinin kendisi reaktiftir; ancak kalsiyum bileşikleri her yerdedir ve bu yüzden bu element genellikle egzotikten ziyade daha tanıdık hissedilir.
Stronsiyum, bir rengiyle ilişkilendirildiğinde hatırlaması daha kolay hale gelir. stronsiyumun sembolü sr'dir ve strontiyum ana olarak selestin ve stronsiyanit minerallerinde bulunur. Royal Society of Chemistry, stronsiyumu, havada yanabilen ve suyla tepkimeye giren yumuşak, gümüşümsü bir metal olarak tanımlar. Tuzları, havai fişeklerde ve işaret fişeklerinde parlak kırmızı renkler üretmesiyle ünlüdür. Aynı kaynak, stronsiyumun karanlıkta parlayan malzemelerde ve hassas dişler için diş macunu içindeki stronsiyum klorür heksahidratında da kullanıldığını belirtir. Bu da stronsiyumu, kimyasal olarak reaktif olmasına rağmen çoğunlukla bileşikleri aracılığıyla karşılaşılan bir element örneği haline getirir.
İleri düzey veya özel bağlamlarda barium ve radyum
The baryum elementi genellikle ağırlığıyla hatırlanır. Genellikle barit ile ilişkilendirilir ve en tanıdık bileşiklerinden biri de baryum sülfattır. Bu bileşik önemlidir çünkü çok az çözünürdür; bu da baryumun sondaj sıvıları ve tıbbi görüntüleme gibi pratik uygulamalarda görünmesini açıklar, oysa diğer çözünebilir baryum bileşikleri toksisite endişeleri nedeniyle daha dikkatli şekilde ele alınır. Baryum, Grup 2 elementlerinin yararlı biçiminin genellikle parlak metal değil, bir bileşik olduğunu okuyuculara hatırlatır.
Radyum ailemin dibinde yer alır, ancak sessizce kaynaşmaz. Bir radyum periyodik tablosu görünüm, Ra işareti radyoaktivitenin tanımlayıcı özellik haline geldiği noktayı gösterir. Radyum yalnızca çok küçük miktarlarda doğal olarak bulunur ve genellikle uranyum cevherleriyle ilişkilidir. Tarihsel olarak, parlak boyalar ve erken tıbbi deneyler ile ün kazanmıştır. Bugün tehlikesi, sıradan bir metal davranışı yerine radyoaktivitesinden kaynaklanır; bu nedenle katı kontroller altında tutulur. Basit bir ifadeyle, radyum hâlâ 2. Grup’a aittir ancak kimya kadar nükleer güvenlik açısından da ele alınır.
Bu altı elementi yan yana koyarsanız, aile artık sadece isimlerden oluşan soyut bir liste gibi görünmez. Boyut, reaktivite, yaygın bileşikler ve her bir elementin yaşamda nasıl ortaya çıktığı aşağı doğru ilerledikçe değişir. Bu değişen örüntü, 2. Grubun özellikle faydalı hale geldiği noktadır; çünkü berilyumdan radyuma kadar olan sıralama, gereksiz bilgiler yerine eğilimleri ortaya çıkarır.
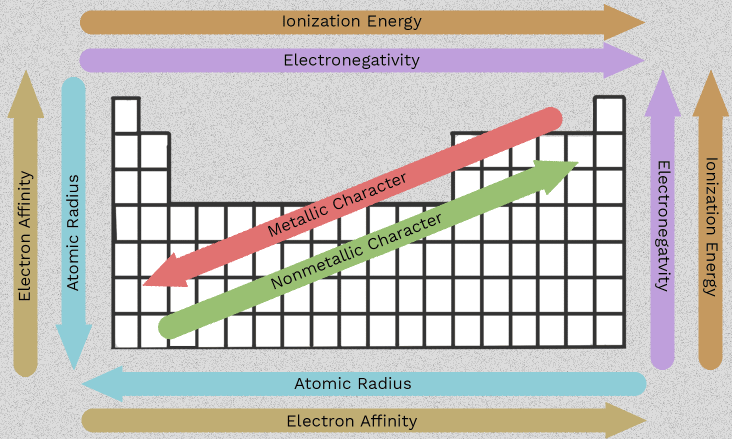
Alkaline Toprak Metalleri Özellikleri ve 2. Grup Eğilimleri
Berilyumdan radyuma doğru değişen bu sıralama, 2. Grubu yararlı kılan şeydir. Altı ayrılmış gerçeği ezberlemek yerine, sütun boyunca tekrarlayan birkaç kalıbı takip edebilirsiniz. En önemli alkalin toprak metalleri özellikleri tümü, her bir atomun kaybetmeye eğilimli iki dış elektronu olması gibi ortak bir özelliktendir.
Bir kez boyutun, elektron perdelemenin ve iyonlaşma enerjisinin grubun aşağısına doğru nasıl değiştiğini anladığınızda, bu element ailesini tahmin etmek çok daha kolay hale gelir. Bu alkalin toprak metalleri karakteristik özellikleri sadece sınav bilgileri değildir. Bunlar, bazı üyelerin neden daha hızlı tepkime verdiğini, bazı bileşiklerin neden diğerlerinden daha iyi çözündüğünü ve neden bazı trendlerin basit oklarla değil, dikkatli bir ifadeyle açıklanması gerektiğini açıklar.
Alkalin toprak metallerinin ortak özellikleri
Çoğu 2. Grup üyesi, genellikle M 2+iyonlar oluşturur ve çoğunlukla iyonik bileşikler meydana getirirler. Elektron kaybettikleri için indirgen ajanlar gibi davranırlar. Grup 1 metalleriyle karşılaştırıldığında genellikle daha az reaktiftirler; ancak yine de birçok yaygın oksit, klorür, karbonat ve sülfat oluşturacak kadar kimyasal olarak aktiftirler.
Bir organizasyon yöntemi olarak alkalin toprak metallerinin kimyasal özelliklerini sabit kalanları değişenlerden ayırmak suretiyle düzenlemek mümkündür. Sabit kalan şey, genellikle +2 yükseltgenme durumudur. Değişen şey ise her bir elementin bu iki elektronu ne kadar kolay verdiğidir. İşte burada trendler önem kazanmaya başlar.
Grup 2’de aşağı doğru olan trendler ve bunların anlamı
LibreTexts tarafından toplanan veriler ile Save My Exams tarafından sunulan trend açıklamaları aynı genel deseni göstermektedir. Atom yarıçapı Be için 112 pm’den Ba için 253 pm’ye kadar artarken, birinci iyonlaşma enerjisi 900 kJ/mol’dan 503 kJ/mol’e kadar düşer. Basit bir dille ifade edilirse, dış elektronlar çekirdekten daha uzakta yer alır ve daha fazla iç kabuk tarafından perdelendiğinden, bu elektronlar daha kolay uzaklaştırılabilir.
| Eğilim | Grup 2’de aşağı doğru yön | Kimyasal neden | Bunun Pratikte Anlamı |
|---|---|---|---|
| Atom yarıçapı | Artırır | Her elementin bir ek elektron kabuğu ve daha fazla perdeleme vardır | Daha büyük atomlar dış elektronları daha zayıf tutar |
| Birinci ve ikinci iyonlaşma enerjisi | Genel olarak azalır | Dış elektronlar çekirdekten daha uzakta olduğundan çekim daha zayıftır | M 2+iyonlarının oluşması kolaylaşır |
| Reaktivite | Genel olarak artar | Daha düşük iyonlaşma enerjileri elektron kaybını kolaylaştırır | Daha ağır elementler asitler, oksijen ve genellikle su ile daha şiddetli tepkime verir |
| Erime noktası | Genellikle azalır, ancak düzgün bir şekilde değil | Daha büyük metal iyonları metalik bağlamayı zayıflatır; ancak yapı da önemlidir | Burada "genel" kelimesini kullanın, çünkü Mg ve Ca tam olarak düzgün bir çizgiye uymaz |
| Yoğunluk | Düzensiz | Kütle, atom boyutu ve metal paketlenmesi birlikte değişir | Yoğunluğu tek bir aşağı yönlü eğilim olarak değerlendiremezsiniz |
| Hidroksit çözünürlüğü | Artırır | Kafes enerjisi ile hidrasyon enerjisi arasındaki denge grubun aşağısına doğru kayar | Daha ağır hidroksitler daha kuvvetli alkali çözeltiler oluşturur |
| Sülfat çözünürlüğü | Azalır | Katyondaki iyon büyüklüğü arttıkça hidrasyon enerjisi düşer | BaSO gibi bileşikler 4çok az çözünür hâle gelir |
Yoğunluk ve erime davranışı, öğrencilerin genellikle aşırı basitleştirdiği iki eğilimdir. Yoğunluk düz bir çizgide değişmez çünkü hem kütle hem de hacim değişmektedir ve metal atomları her kristalde aynı şekilde paketlenmez. Erime noktaları da dikkatli ele alınmalıdır. Genel olarak aşağı doğru bir eğilim gösterirler çünkü daha büyük iyonlar metalik örgüyü zayıflatır; ancak Mg’nin erime noktası olağanüstü düşük olan 650 °C’dir, Ca ise değerler tekrar düşmeden önce 842 °C’ye yükselir. Dolayısıyla en güvenilir alkalin toprak metallerinin özellikleri şudur: Genel eğilim gerçektir ama fiziksel ayrıntılar tam anlamıyla düzgün değildir.
Çözünürlük de aynı uyarı etiketine sahiptir. Grup 2 tuzlarının tamamını kapsayan tek bir kural yoktur. Hidroksitler grubun aşağısına doğru gidildikçe daha çok çözünür hâle gelirken sülfatlar daha az çözünür hâle gelir. Eğer biri "Grup 2’de çözünürlük aşağı doğru artar" derse, önemli soru şudur: "Hangi bileşiklerden bahsediliyor?"
Alkaline toprak metallerinin neden bu şekilde tepkime verdiğinin açıklaması
O halde, alkaline toprak metalleri reaktif midir ? Evet, genel cevap aşağı doğru ilerledikçe daha reaktif hâle geldikleridir. Bunun nedeni yukarıda bahsedilen aynı elektron öyküsüdür. Daha düşük birinci ve ikinci iyonlaşma enerjileri, atomların iki elektronu daha kolay kaybedebilmesini ve yaygın M 2+ durumuna daha hızlı ulaşmasını sağlar.
Bu durum gerçek tepkimeleri etkiler. Grup boyunca aşağı doğru inildikçe seyreltik asitlerle tepkimeler hızlanır, oksijenle tepkimeler daha şiddetli hâle gelir ve daha ağır üyelerin yükseltgenmesi daha kolaylaşır. Save My Exams, bariumun reaktivitesinin yeterince yüksek olduğunu ve bu yüzden yağ altında saklanması gerektiğini belirtir; bu da reaktivite eğiliminin ne kadar ileriye gidebileceğinin pratik bir göstergesidir.
- Atom yarıçapı 2. Grup boyunca aşağı doğru artar.
- İyonlaşma enerjisi 2. Grup boyunca aşağı doğru azalır.
- İki elektronun kaybedilmesinin kolaylaşması nedeniyle reaktivite artar.
- Erime noktası ve yoğunlukta düzensizlikler gözlenir; bu nedenle kesin kurallardan kaçınmalısınız.
- Hidroksitler ve sülfatlar zıt çözünürlük eğilimleri gösterir.
Bu desenler aileyi tahmin edilebilir kılar, ancak tamamen homojen hale getirmez. Grubun hemen en üst kısmında, berilyum zaten kuralları bükme eğilimine girer ve magnezyum, birçok başlangıç seviyesi öğrencinin beklediğinden daha fazla önem taşıyan, günlük yaşamda karşılaşılan başka bir istisnayı da ekler.
Alkali ve toprak alkali metalleri
Genel eğilimler, 2. Grubu öğrenmeyi kolaylaştırır; ancak her üyeyi özdeşmiş gibi ele alırsanız aile yapısı anlamsız hâle gelir. En büyük uyarı işareti berilyumdur. Magnezyum ise daha pratik, günlük yaşamda karşılaşılan bir istisna sunar. Ve insanlar alkali ve toprak alkali metalleri karşılaştırdığında, benzer isimler bazı çok farklı kimyasal davranışları gizleyebilir.
Neden berilyum tipik bir 2. Grup metali gibi davranmaz
BYJU'S berilyumu, 2. Grup içinde açıkça dikkat çekici bir dışlı olarak tanımlar. Olağanüstü küçük boyutu, yüksek iyonlaşma enerjisi ve güçlü kutuplaştırıcı gücü, ona ailenin diğer üyelerine göre daha az tipik davranışlar kazandırır. Basit bir dille ifade edersek, Be 2+yakındaki elektron bulutlarına güçlü bir şekilde çeker, bu nedenle berilyum bileşikleri, daha ağır üyeler tarafından oluşturulan daha iyonik bileşiklere kıyasla genellikle daha kovalenttir. Aynı kaynak, berilyumun grubun geri kalanına göre daha yüksek erime ve kaynama noktalarına sahip olduğunu ve diğer üyelerinin aksine suyla tepkime vermediğini de belirtir.
Magnezyum, berilyum kadar olağandışı değildir; ancak yine de öğrencilerin beklediğinden daha az reaktif görünebilir. LibreTexts, çok temiz magnezyumun soğuk su ile yalnızca hafifçe tepkime verdiğini ve reaksiyonun, neredeyse çözünmez magnezyum hidroksitin yüzeyde bir bariyer oluşturması nedeniyle hızla yavaşladığını belirtir. Ailenin en alt kısmında yer alan radyum, radyoaktivitesinin pratik kullanım ve güvenlik tartışmalarını domine etmesi nedeniyle genellikle ayrı olarak ele alınır.
Alkaline toprak metallerinin alkali metallerden farkı
Basit alkali ile alkaline terimlerle ifade edersek, 1. Grup metalleri bir dış elektron kaybederken, 2. Grup metalleri iki dış elektron kaybeder. Bu tek fark, alkali ve alkaline toprak metallerinin özelliklerini neredeyse her şeyden daha fazla şekillendirir. alkali ve alkaline toprak metallerinin özellikleri neredeyse her şeyden daha fazla.
| Özellik | Alkali metaller, 1. Grup | Toprak alkali metaller, 2. Grup |
|---|---|---|
| Değerlik elektronlarını | 1 | 2 |
| Tipik iyon | M + | M 2+ |
| Soğuk su ile tepkime | Genellikle şiddetli veya hatta patlayıcı olabilir; hidroksit ve hidrojen oluşturur | Daha az düzenli: Be su ile tepkime vermez, Mg hafifçe tepkime verir, Ca, Sr ve Ba ise artan şiddette tepkime verir |
| Yaygın oksijen kimyası | Oksitler, peroksitler veya süperoksitler oluşturabilir | Genellikle monoksitler oluşturur; bu oksitlerin çoğu su ile hidroksit verir, ancak BeO bir istisnadır |
Öğrencilerin sıklıkla kaçırığı önemli istisnalar
- 2. Grup’taki her metal su ile aynı şekilde tepkime vermez.
- Berilyum bileşikleri, ailenin geri kalanına göre daha kovalenttir.
- Karıştırmayın alkali ve toprak alkali isimlerinin benzer sounding olması nedeniyle aynı grup gibi düşünmeyin.
- The alkali metallerin ve toprak alkali metallerin özellikleri katı sloganlar yerine, istisnaları olan kalıplar olarak öğrenilmelidir.
Bu aynı zamanda alkali metallerin ve toprak alkali metallerin kimyasal özelliklerini anlamanın en iyi yoludur . Elektron düzenleri size kuralı verir, ancak gerçek maddeler dokuyu kazandırır. Ve bu doku, Grup 2 elementlerinin aslında nerede bulunduğuna baktığınızda daha da netleşir: saf metaller olarak nadiren, ancak çok daha sık minerallerin içinde, kayalarda, deniz suyunda, kemiklerde ve endüstriyel bileşiklerde.
Toprak Alkali Metallerin Doğada Bulunuş Şekli
Eğer bir alkali toprak metali gibi parlak, saf bir örneği bir kayanın içinde otururken hayal ederseniz, doğa farklı bir şekilde çalışır. 2. Grup elementleri, genellikle serbest metaller olarak değil, minerallerin, tuzların, kayaların, deniz suyunun, kemiklerin ve kabukların içinde iyonlar halinde bulunacak kadar reaktiftir. Birisi alkali toprak metalleri ya da daha yaygın kullanılan terimi arar mı, doğal desen aynıdır: bu element ailesi güçlü bir şekilde bileşikleri tercih eder.
Bu desen doğrudan alkali toprak metallerinin kimyasal özellikleri kaynaklanır. Bunlar genellikle iki dış elektron kaybederek kararlı M 2+iyonları oluştururlar. Bu gerçekleştiğinde, oksijen, karbonat, sülfat ve halojenür iyonları onları jeoloji ve biyolojide kalıcı olabilen katı bileşiklere kolayca bağlar.
Alkali toprak metallerinin doğada serbest halde bulunmamasının nedeni
Britannica ve ThoughtCo her ikisi de Grup 2'yi reaktif olarak tanımlar; bu nedenle bu elementler nadiren birleşmemiş halde bulunur. Havada birçok element hızla oksit kaplamaları oluşturur. Doğal ortamlarda ise karbonatlar, sülfatlar, silikatlar, florürler veya klorürler şeklinde daha da stabilize olurlar. Bu yüzden kalsiyum kireçtaşı ve kabuklarda, magnezyum minerallerde ve deniz suyunda, stronsiyum veya baryum ise cevher yataklarında bulunur. Radyum ise daha da nadir olup yalnızca uranyum cevherlerinde iz miktarlarda bulunur.
Grup 2'nin yaygın mineralleri ve bileşikleri
| Eleman | Yaygın doğal kaynak | Tanıdık bileşik | Bu bileşiğin önemi |
|---|---|---|---|
| Berilyum | Beryl | BeO | Beril, bu elementin ticari kaynağıdır; berilyum oksit ise özel malzemelerde önemli bir bileşiktir |
| Magnesium | Magnezit, dolomit, deniz suyu | MgCO₃ 3veya Mg(OH)₂ 2 | Magnezyumun saf metal olarak değil, minerallerde, deniz suyunda ve ilaçlarda daha sık karşılaşıldığını gösterir |
| Kalsiyum | Kireçtaşı, tebeşir, mermer, alçı taşı, kemikler, kabuklar | Cako 3 | Jeolojiyi, inşaat malzemelerini ve iskeletleri tek bir çok yaygın bileşikte birleştirir |
| Strontiyum | Celestit, stronsiyant | SrSO 4veya SrCO 3 | Bu mineraller, stronsiyum bileşiklerinin başlıca doğal kaynaklarıdır |
| Baryum | Barit, witherit | BaSO 4 | Barit ana cevherdir ve baryum sülfat, en bilinen baryum bileşiklerinden biridir |
| Radyum | Pitchblende ve diğer uranyum cevherlerinde iz miktarlarda | RaCl 2 | Nadir oluşu ve radyoaktivitesi, radyum bileşiklerini tarihsel olarak önemli ancak nadir kılacaktır |
EBSCO kalsiyum ve magnezyumun sırasıyla yaklaşık 0,4 g/L ve 1,3 g/L oranlarında deniz suyunda da bulunduğunu belirtir. Bu durum, bunun alkali toprak grubunun yalnızca cevherlere değil, aynı zamanda sert suya, deniz sistemlerine ve canlı dokulara da bağlanmasını açıklar.
Bu metallerin bileşiklerinden nasıl izole edildiği
Grup 2 metalleri genellikle bileşiklerin içinde hapsedildiği için, ekstraksiyon işlemi cevherlerden, tuzlu sulardan veya mineral yataklarından başlar. Yaygın bir endüstriyel yaklaşım oldukça basittir: öncelikle maddeyi daha işlenebilir bir oksit veya halojenür haline dönüştürmek, ardından metalin serbest bırakılması için elektroliz veya kimyasal indirgemeyi kullanmak. Britannica, magnezyum, kalsiyum, stronsiyum ve baryumun erken dönem izolasyonlarının elektroliz yoluyla yapıldığını açıklar; EBSCO ise günümüzde üretim süreçlerinin hâlâ çoğunlukla erimiş klorürler, oksit indirgemesi veya ilgili yöntemlere dayandığını belirtir; bu yöntemler kullanılan elemente göre değişiklik gösterir. Berilyum, bu grubun tam olarak homojen olmadığını hatırlatan faydalı bir örnektir çünkü berilyum florürün indirgenmesiyle üretilebilir.
Dolayısıyla günlük hayatta insanlar, bu elementleri genellikle kireçtaşı, alçı, deniz suyu magnezyumu, barit veya biyolojik kalsiyum yoluyla, ham metal örnekleriyle değil, Grup 2 ile tanışır. Bu ayrıntı önemlidir çünkü bu elementlerin gerçek dünyadaki önemi, saf metallerine göre çok daha fazla bileşikleri ve formlarıyla ilişkilidir.
Günlük Hayatta Alkaline Toprak Metalleri Örnekleri
Grup 2, her bir elementi somut bir şeyle ilişkilendirdiğinizde çok daha akılda kalıcı hale gelir. Kemikler, antasitler, alçı, havai fişekler, sondaj sıvıları ve eski parlak saat kadranları hepsi yararlı örneklerdir. alkaline toprak metalleri örnekleri eğer hiç merak ettiyseniz magnezyum bir metal mi yoksa ametal mi veya ca bir metal midir , her iki sorunun cevabı da basittir: magnezyum ve kalsiyum metallerdir. Ancak günlük hayatta insanlar bu maddelerle genellikle saf metal örnekleri olarak değil, bileşikleri olarak tanışır.
Magnezyum ve kalsiyum bileşiklerinin günlük kullanım alanları
- Magnesium : Magnezyum, biyolojik olarak en önemli elementlerden biridir. alkalin toprak elementleri . NIH magnezyum bilgi sayfası magnezyumun, 300’den fazla enzim sisteminde kofaktör olarak görev aldığını ve kas ile sinir fonksiyonlarını, enerji üretimini ve kemik yapısını desteklediğini belirtir. Magnezyum bileşikleri ayrıca bazı antiasitlerde ve müshillerde yer alırken, magnezyum metali, kütle azaltmanın önemli olduğu hafif ağırlıklı alaşımlarda değerlidir.
- Kalsiyum kalsiyum bileşikleri günlük yaşamda baskın rol oynar. Kalsiyum, kemiklerin ve dişlerin yapısını oluşturmasına yardımcı olur; kalsiyum karbonatı ve kalsiyum sülfatı gibi bileşikler ise kireçtaşı, çimento, alçı ve alçıpan üretiminde merkezî öneme sahiptir. Bu da kalsiyumu, kimya, biyoloji ve inşaat arasındaki en açık bağlantılar arasında yer almasına neden olur.
Stronsiyum ve baryum’un özel uygulamaları
- Strontiyum stronsiyum tuzları, havai fişeklerde ve işaret fişeklerinde derin kırmızı renkler üretmesiyle en çok bilinir. Tam Grup 2 listesini hatırlamayan okuyucular bile, stronsiyumun rengiyle ilişkilendirilmesi durumunda genellikle onu hatırlar.
- Baryum baryum bileşikleri, sanayide ve tıpta önem taşır. NLM baryum profili kazma çamurlarında, boyalarda, plastiklerde, tuğlalarda ve camda önemli kullanım alanlarını tanımlar. Ayrıca önemli bir tıbbi karşıtlık da belirtir: yüksek derecede çözünmeyen baryum sülfat, genellikle vücut tarafından emilmediği için bazı röntgen muayenelerinde radyo-opak madde olarak kullanılır.
- Radyum : Radyum çoğunlukla tarihsel veya sıkı denetim altındaki bilimsel bir durumdur. NRC radyum sayfası radyumun geçmişte luminözes boya ve erken dönem kanser tedavisindeki kullanımını açıklar. Bu kullanımların çoğu günümüzde yerini değiştirmiştir; ancak bazı düzenlenmiş kullanımlar hâlâ devam etmektedir, örneğin belirli endüstriyel radyografya uygulamaları gibi.
Gerçek hayatta kullanım açısından formun ve bileşik türünün neden önemli olduğu
2. Grup elementleriyle ilgili olarak insanların kullandığı form genellikle saf metal değil, bileşiktir.
Bu tek fikir, birçok karışıklığı giderir. Gıdalarda veya ilaçlarda bulunan magnezyum, yanıcı magnezyum şeridiyle aynı şey değildir. Kemikteki kalsiyum, reaktif kalsiyum metalıyla aynı şey değildir. Formun neden önemli olduğunu gösteren en net örnek baryumdur: çözünmeyen baryum sülfat, görüntüleme amacıyla yararlı olabilirken, daha çözünebilir baryum bileşikleri çok daha dikkatli bir şekilde ele alınmalıdır. Radyum bu durumu daha da ileriye taşır çünkü onunla başa çıkma şekli, yalnızca metaller grubundaki yerine değil, aynı zamanda radyoaktivitesine bağlıdır.
Dolayısıyla 2. Grup’un değeri hiç de soyut değildir. Bu elementler, aynı ailenin beslenme, malzemeler, tıp, endüstriyel işlem ve güvenlik kuralları gibi farklı alanlarda nasıl önemli olabileceğini açıklamaya yardımcı olur. Gerçek hayattaki kullanım örneklerinden oluşan kısa bir liste, genel deseni akılda tutmak için çoğu zaman yeterlidir.
2. Grup Elementleriyle İlgili Temel Çıkarımlar
Bu noktaya gelindiğinde, alkali toprak metalleri grubu ezberlemek için bir liste gibi değil, doğrudan periyodik tablonun 2. grup sütunu üzerinden okuyabileceğiniz bir desen gibi hissedilmelidir. Eğer hâlâ birisi sorarsa, alkali toprak metalleri nelerdir , kısa cevap basit kalır: berilyum, magnezyum, kalsiyum, stronsiyum, baryum ve radyum. Daha kapsamlı bir alkali toprak metalleri tanımı daha da yararlıdır: genellikle iki dış elektron kaybeden ve M 2+iyonları oluşturan, 2. grupta yer alan altı metal element.
Alkali toprak metalleriyle ilgili temel bilgiler
- Konum önemlidir: bu altı 2. grup elementi soldan ikinci sütunda, s-blokun 2. grubu bölümünde yer alır.
- Aile üyeleri sabittir: Be, Mg, Ca, Sr, Ba ve Ra tam seti oluşturur.
- Ortak kimya, aile benzerliğini açıklar: ns 2değerlik düzeni, +2 iyonlarının yaygın sonuç olmasını sağlar; bu temel nokta LibreTexts tarafından özetlenmiştir.
- Ana aşağı yönlü eğilimler tahmin edilebilirdir: atom yarıçapı artar, iyonlaşma enerjisi genellikle azalır ve grubun aşağısına doğru ilerledikçe reaktivite genellikle artar.
- İstisnalar önemlidir: berilyum diğerlerine kıyasla daha kovalent davranış gösterir, magnezyum yüzey katmanı nedeniyle daha az reaktif gibi görünebilir ve radyum çoğunlukla radyoaktivitesi üzerinden ele alınır.
- Gerçek yaşam genellikle saf metallerden ziyade bileşikler anlamına gelir: i̇nsanlar, elementel Ca, Mg veya Ba’ya kıyasla kalsiyum karbonat, magnezyum oksit ve baryum sülfat ile çok daha sık karşılaşır.
The alkaline toprak metalleri periyodik tablosu sütun, altı metalin tek bir kurala göre bağlantılı olduğu şekilde en kolay hatırlanır: genellikle 2+ iyon oluştururlar; ancak her üye bu kuralı biraz farklı şekilde gösterir.
Grup 2 kimyasından mühendislikle üretilen metal parçalara kadar
Bu kimya, ders kitaplarının ötesine de uzanır. LibreTexts, elementel magnezyumun büyük ölçekte üretildiğini ve uçak gövdesi ile otomobil motor parçaları için hafif alaşımlarda kullanıldığını belirtir. Daha kapsamlı bir alaşım kılavuzu, bunun neden önemli olduğunu gösterir: mühendisler, gerçek bileşenlerde ağırlık, dayanıklılık, korozyon direnci ve işlenebilirlik arasında denge kurmak amacıyla bileşim ve işlem yöntemlerini ayarlar.
Okuyucuların 2. grup sütunu görüşünden üretim sürecine geçiş yaparken, Shaoyi Metal Technology bu bağlantının pratik bir örneğini sunar. Otomotiv malzemeleri ve işlenmesi sayfaları, prototiplemeden seri üretime kadar metal parça üretimi hakkında bilgi verir; burada malzeme davranışı ve süreç kontrolü birlikte çalışmak zorundadır. Bu da alkaline toprak metalleri periyodik tablosu öğrenciler için yalnızca bir sınıf tablosundan daha fazlasıdır. Aynı zamanda, hafif, güvenilir ve üretilebilir olması gereken mühendislik parçaları için metallerin ve alaşımların seçilmesinin arkasındaki mantığın bir parçasıdır.
Alkaline Toprak Metalleri Hakkında SSS
1. Altı alkaline toprak metali hangileridir?
Altı alkaline toprak metali berilyum, magnezyum, kalsiyum, stronsiyum, baryum ve radyumdur. Periyodik tabloda 2. Grup’u oluştururlar ve genellikle iki dış elektron kaybettikleri için çoğu bileşikte ortak bir 2+ iyon yapısı gösterdikleri için bir araya gruplandırılmışlardır.
2. Alkaline toprak metalleri alkali metallerden nasıl farklıdır?
Alkali metaller, 1. Gruba ait olup genellikle bir dış elektronları olduğu için 1+ iyonlar oluştururlar. Alkaline toprak metalleri 2. Grupta yer alır, genellikle 2+ iyonlar oluşturur ve genel olarak daha az reaktiftirler. O ekstra değerlik elektronu, bağ kuvvetlerini, su ile tepkimelerini ve yaygın olarak oluşturdukları tuzlar ile oksitleri değiştirir.
3. Neden alkaline toprak metalleri doğada serbest halde bulunmaz?
Bu metaller, doğal ortamlarda uzun süre saf elementel formda kalmayacak kadar reaktiftirler. Bunun yerine oksijen, karbonat, sülfat, klorür veya silikat iyonlarıyla birleşerek minerallerin, kayaların, deniz suyunun, kabukların ve kemiklerin bir parçası haline gelirler. Bu nedenle insanlar genellikle Grup 2 elementlerini ham metal örnekleri yerine bileşikleri aracılığıyla karşılarlar.
4. Tüm alkaline toprak metalleri su ile tepkimeye girer mi?
Hayır, ve bu hatırlanması gereken en yararlı istisnalardan biridir. Berilyum, suya karşı büyük ölçüde dirençlidir; magnezyum, soğuk suda yüzey tabakası reaksiyonu sınırladığı için yavaşça tepkime verir; kalsiyum, stronsiyum ve baryum ise daha kolay tepkime verir. Genel olarak, 2. Grup’ta aşağı doğru ilerledikçe su ile reaktivite artar.
5. Alkaline toprak metalleri neden sanayi ve üretimde önemlidir?
Bunların önemi hem bileşiklerinden hem de alaşım seçimi açısından kaynaklanır. Daha düşük ağırlık önemliyse magnezyum değerlidir; kalsiyum bileşikleri çimento ve alçı üretiminde merkezdedir; baryum bileşikleri ise özel endüstriyel ve tıbbi uygulamalar için tercih edilir. Gerçek üretim süreçlerinde metal davranışını anlama, işlenebilirlik, proses kararlılığı ve parça kalitesi açısından rehberlik eder; bu nedenle Shaoyi Metal Technology gibi tedarikçiler, otomotiv sektörüne yönelik sertifikalı tornalama hizmetleri, proses kontrolü ve prototip parçalardan seri üretime kadar destek sunmayı vurgular.
 Küçük partiler, yüksek standartlar. Hızlı prototip hizmetimiz doğrulamayı daha hızlı ve kolay hale getirir —
Küçük partiler, yüksek standartlar. Hızlı prototip hizmetimiz doğrulamayı daha hızlı ve kolay hale getirir —
