Wat zijn de aardalkalimetalen? Groep 2 wordt eindelijk duidelijk
Wat zijn alkalische aardmetalen?
Als u heeft gezocht naar wat zijn alkalische aardmetalen , dan is hier het directe antwoord: het zijn de zes elementen in Groep 2 van het periodiek systeem. Deze snelle definitie van alkalische aardmetalen is het uitgangspunt, maar de naam vertelt u ook veel over het gedrag van deze elementenfamilie.
Wat zijn de alkalische aardmetalen in één zin?
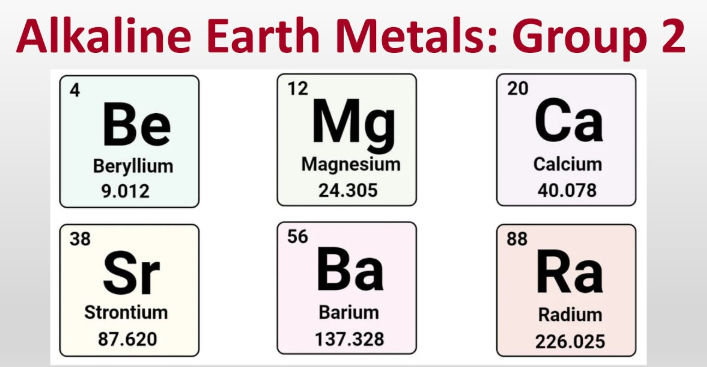
De alkalische aardmetalen zijn beryllium, magnesium, calcium, strontium, barium en radium, de zes metalen in groep 2 die meestal +2-ionen vormen.
- Berillium (Be)
- Magnesium (Mg)
- Calcium (Ca)
- Strontium (Sr)
- Barium (Ba)
- Radium (Ra)
Waarom de naam alkalische aardmetalen logisch is
Voor beginners is de definitie van alkalische aardmetalen veel eenvoudiger wanneer je de term in drie delen verdeelt.
Alkalisch betekent dat hun oxiden en hydroxiden basisch zijn, niet zuur. Aarde is een historisch woord. Vroege chemici gebruikten het voor hittebestendige, mineraalachtige stoffen die niet smolten of gemakkelijk oplosten in water, een punt dat wordt uitgelegd door Britannica . Metalen betekent dat de elementen zelf metaalachtig zijn, meestal glanzend en goed in staat om elektronen te verliezen tijdens reacties.
Dat geeft je de basisdefinitie van alkalische aardmetalen zonder eerst geavanceerde chemie te hoeven kennen. Het is ook een nuttige korte beschrijving van aardalkalimetalen : een metaalgroep 2 met gedeelde chemie, een gedeelde positie in het periodiek systeem en een belangrijke rol in de werkelijkheid. Magnesium komt voor in legeringen en biologie. Calcium is van belang voor botten, schelpen en bouwmaterialen. Barium, strontium en radium komen voor in meer gespecialiseerde toepassingen.
Dit artikel begint expres eenvoudig. Een duidelijke lijst is gemakkelijk uit het hoofd te leren, maar de familie wordt pas echt duidelijk als je ziet waar deze elementen zich bevinden en waarom die plek hen zo vergelijkbaar gedrag geeft.
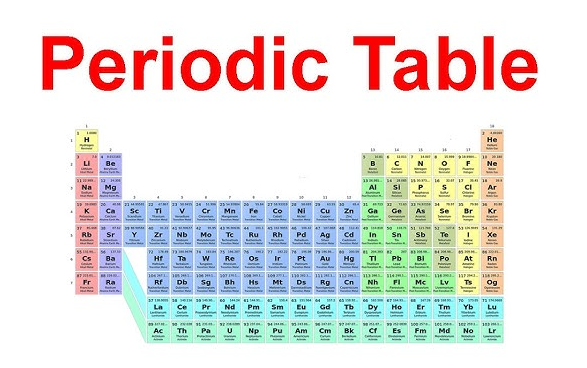
Waar groep 2 zich in het periodiek systeem bevindt
De familienaam wordt veel makkelijker om te onthouden als je hem daadwerkelijk kunt vinden. Als je je afvraagt waar aardalkalimetalen zich in het periodiek systeem bevinden , kijk dan naar de tweede kolom van links. Die verticale kolom is groep 2 in het periodiek systeem , direct naast de alkalimetalen in groep 1. Een groep 2 van het periodiek systeem de weergave toont telkens dezelfde rechte lijn: beryllium bovenaan, gevolgd door magnesium, calcium, strontium, barium en radium die omlaag bewegen door de perioden.
In een alkalische aardmetalen in het periodiek systeem grafiek behoren deze zes elementen tot het s-blok. Hun gezamenlijke locatie is belangrijk omdat deze een gezamenlijk elektronenpatroon weerspiegelt. Zoals LibreTexts uitlegt, hebben groep-2-elementen een ns 2waarde-elektronconfiguratie, wat betekent dat ze twee elektronen in de buitenste schil bezitten.
Waar alkalische aardmetalen zich op het periodiek systeem bevinden
Visueel is het patroon eenvoudig. De groep-2-elementen van het periodiek systeem vormen één familiekolom over de perioden 2 tot en met 7. Veel lesmateriaal in het klaslokaal benadrukt de aardalkalimetalen in het periodiek systeem indelingen met dezelfde kleur, omdat elementfamilies verticaal, niet horizontaal, worden gelezen. Zoekopdrachten voor periodiek systeem aardalkalimetalen vragen eigenlijk om die ene kolom.
| Elementen | Symbool | Groep 2-positie | Typisch ion | Bekende verbinding |
|---|---|---|---|---|
| Beryllium | Be | Periode 2, bovenaan Groep 2 | Be2+ | BeO |
| Magnesium | Mg | Periode 3 | Mg2+ | MgO |
| Calcium | Ca | Periode 4 | Ca2+ | Caco 3 |
| Strontium | Sr | Periode 5 | Sr2+ | SrCO 3 |
| Barium | BA | Periode 6 | BA 2+ | BaSO 4 |
| Radium | RA | Periode 7, onderaan Groep 2 | RA 2+ | RaCl 2 |
Waarom elementen uit groep 2 tweeplus-ionen vormen
Die twee buitenste elektronen bepalen de chemie. Atomen van groep 2 verliezen doorgaans beide elektronen, omdat dat een stabielere elektronenconfiguratie oplevert. Het resultaat is een +2-ion , zoals Mg 2+ of Ca 2+. Daarom vormen deze metalen vaak verbindingen zoals oxiden, chloriden, carbonaten en sulfaten. Het patroon in de formules is direct herkenbaar: MgO, CaCl 2, CaCO 3, BaSO 4.
Hoe u de groep alkalische aardmetalen snel kunt herkennen
Een snelle herkenningstruc is om tegelijkertijd naar drie kenmerken te kijken: de tweede kolom van het periodiek systeem, metalen elementen en een gebruikelijke lading van +2. In vergelijking met de aangrenzende alkali-metalen, die één valentie-elektron hebben en meestal +1-ionen vormen, bezitten de elementen uit groep 2 één extra buitenste elektron en zijn over het algemeen minder reactief. Toch behoren ze duidelijk tot dezelfde familie. Het interessante is dat elk lid dit patroon op een iets andere manier uitdrukt, vooral van beryllium bovenaan tot radium onderaan.
De zes alkalische aardmetalen
Een lijst is handig, maar is op zichzelf niet erg onthoudbaar. Groep 2 begint meer levensecht te voelen wanneer elk lid een duidelijke identiteit heeft. Sommigen komen voor in botten of zeewater. Sommigen geven vuurwerk zijn kleur. Eén is voornamelijk een historisch waarschuwingssignaal. Samen behoren ze nog steeds tot dezelfde familie, maar elk heeft zijn eigen persoonlijkheid.
| Elementen | Symbool | Veelvoorkomend verschijnsel | Opvallende eigenschap | Relevantie in de praktijk |
|---|---|---|---|---|
| Beryllium | Be | Komt voor in mineralen zoals beryl | Zeer licht en stijf voor een metaal | Wordt gebruikt in gespecialiseerde aerospace- en röntgentoepassingen; stof is gevaarlijk bij inademing |
| Magnesium | Mg | Komt voor in zeewater en mineralen | Lage dichtheid en fel witte vlam bij verbranding | Belangrijk in lichtgewicht legeringen, supplementen en biologie |
| Calcium | Ca | Veelvoorkomend in kalksteen, botten, schelpen en krijt | Biologisch vertrouwde ion van groep 2 | Belangrijk in skeletten, cement, gips en vele natuurlijke mineralen |
| Strontium | Sr | Komt voornamelijk voor in celestien en strontianiet | Zouten geven een levendige rode kleur in vlammen | Wordt gebruikt in vuurwerk, signaallichten, gloeiende materialen en sommige tandheelkundige producten |
| Barium | BA | Komt meestal voor samen met barit | Dich, zwaar aardalkalimetaal | Bariumsulfaat is belangrijk bij boren en medische beeldvorming; oplosbare bariumverbindingen vereisen voorzichtigheid |
| Radium | RA | Komt in sporen voor in uraniumerts | Sterke radioactiviteit domineert zijn chemische geschiedenis | Vandaag voornamelijk van historisch of streng gecontroleerd wetenschappelijk belang |
Beryllium en magnesium bovenaan Groep 2
De element beryllium staat bovenaan de groep en geeft al aan dat Groep 2 niet volkomen uniform is. Het wordt vaak geassocieerd met het mineraal beryl, dezelfde mineraalfamilie waartoe ook smaragd en aquamarijn behoren. Beryllium onderscheidt zich doordat het ongewoon licht en stijf is. Dat maakt het geschikt voor hoogwaardige onderdelen waar een lage massa van belang is. Tegelijkertijd is beryllium een materiaal waarbij in industriële omgevingen voorzichtigheid vereist is, omdat fijn stof schadelijk kan zijn bij inademing. Het wordt daarom zowel herinnerd om zijn prestaties als om de voorzorgsmaatregelen die bij de verwerking nodig zijn.
Magnesium voelt veel vertrouwder aan. De chemische symbool van magnesium is Mg en is een van de meest bekende metalen in deze groep, omdat het voorkomt in zeewater, gewone mineralen en levende systemen. Het is een zeer licht metaal en produceert bij verbranding een intense witte gloed. Daarom is magnesium al lang geassocieerd met signaalpijlen en stoffen die fel branden. In het dagelijks leven komt men het echter meestal tegen in zachtere vormen, zoals in voeding, als bestanddeel van zuurremmers of in lichtgewicht legeringen die worden gebruikt waar massa-reductie belangrijk is.
Calcium en strontium in alledaagse materialen
Calcium is voor veel lezers het meest herkenbare lid van groep 2. Het komt voor in kalksteen, krijt, schelpen en botten, waardoor het de chemie bijna onmiddellijk verbindt met zowel de geologie als de biologie. Calciumcarbonaat is de bekende verbinding in dit verband. Het helpt uitleggen waarom dezelfde elementenfamilie van belang is voor grotvorming, bouwsteen en skeletten. Het calciummetaal zelf is reaktief, maar calciumverbindingen zijn overal aanwezig, wat verklaart waarom dit element vaak vertrouwder aanvoelt dan exotisch.
Strontium is gemakkelijker te onthouden zodra je het aan een kleur koppelt. De symbool voor strontium is Sr en strontium komt voornamelijk voor in de mineralen celestiet en strontianiet. De Royal Society of Chemistry beschrijft het als een zacht, zilverachtig metaal dat brandt in lucht en reageert met water. Zijn zouten staan bekend om het produceren van felrode kleuren in vuurwerk en signaalvuurpijlen. Dezelfde bron vermeldt ook toepassingen in nachtverlichtende materialen en strontiumchloridehexahydraat in tandpasta voor gevoelige tanden. Dat maakt strontium een uitstekend voorbeeld van hoe een element chemisch reactief kan zijn, maar meestal via verbindingen wordt aangetroffen.
Barium en radium in geavanceerde of gespecialiseerde contexten
De barium-element wordt vaak herinnerd door zijn zwaarte. Het wordt veelal geassocieerd met bariet, en een van zijn meest bekende verbindingen is bariumsulfaat. Deze verbinding is belangrijk omdat deze zeer onoplosbaar is, wat helpt verklaren waarom barium voorkomt in praktische toepassingen zoals boorvloeistoffen en medische beeldvorming, terwijl andere oplosbare bariumverbindingen voorzichtiger worden behandeld vanwege toxiciteitsbezorgdheden. Barium herinnert lezers eraan dat de nuttige vorm van een element uit groep 2 vaak een verbinding is, niet het glanzende metaal zelf.
Radium staat onderaan de familie, maar het mengt zich niet stilletjes in. Op een radium-periodieke tabel bekijk het, Ra markeert het punt waar radioactiviteit het bepalende kenmerk wordt. Radium komt van nature slechts in zeer kleine hoeveelheden voor, meestal geassocieerd met uraniumerts. Historisch gezien werd het beroemd door lichtgevende verf en vroege medische experimenten. Tegenwoordig is het gevaar voornamelijk afkomstig van de radioactiviteit, niet van het gewone gedrag van een metaal, waardoor het onder strikte controle wordt gehandhaafd. In eenvoudige bewoordingen behoort radium nog steeds tot Groep 2, maar het wordt evenzeer besproken vanuit het oogpunt van nucleaire veiligheid als vanuit dat van de chemie.
Plaats deze zes naast elkaar en de familie lijkt niet langer op een kale lijst met namen. Grootte, reactiviteit, veelvoorkomende verbindingen en zelfs de manier waarop elk element in het dagelijks leven optreedt, veranderen bij neergaan in de groep. Dit veranderende patroon maakt Groep 2 bijzonder nuttig, omdat de volgorde van beryllium tot radium trends onthult in plaats van willekeurige feiten.
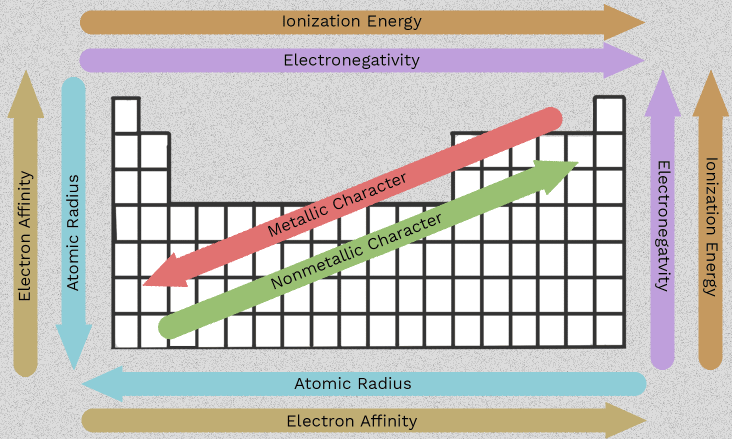
Eigenschappen van alkalische aardmetalen en trends binnen Groep 2
Die verandering in volgorde van beryllium naar radium maakt Groep 2 nuttig. In plaats van zes geïsoleerde feiten uit je hoofd te leren, kun je een handvol patronen volgen die zich herhalen langs de kolom. Het belangrijkste eigenschappen van aardalkalimetalen vloeien allemaal voort uit één gemeenschappelijke kenmerk: elk atoom heeft twee buitenste elektronen die het geneigd is kwijt te raken.
Zodra je ziet hoe grootte, elektronenschermming en ionisatie-energie naar beneden in de groep veranderen, wordt de familie veel makkelijker voorspelbaar. Deze kenmerken van aardalkalimetalen zijn niet alleen examenfeiten. Ze verklaren waarom sommige leden sneller reageren, waarom sommige verbindingen beter oplossen dan andere, en waarom een paar trends voorzichtig geformuleerd moeten worden in plaats van met eenvoudige pijlen.
Gedeelde eigenschappen van aardalkalimetalen
De meeste leden van Groep 2 zijn zilverachtige metalen die meestal M 2+ionen en vormen voornamelijk ionische verbindingen. Ze gedragen zich als reductiemiddelen omdat ze elektronen afstaan. In vergelijking met de metalen uit groep 1 zijn ze over het algemeen minder reactief, maar ze zijn nog steeds chemisch actief genoeg om veel voorkomende oxiden, chloriden, carbonaten en sulfaten te vormen.
Een eenvoudige manier om de chemische eigenschappen van aardalkalimetalen te ordenen is om te onderscheiden wat constant blijft van wat verandert. Wat constant blijft, is de gebruikelijke oxidatietoestand van +2. Wat verandert, is hoe gemakkelijk elk element die twee elektronen afstaat. Daar komen de trends om de hoek kijken.
Trends naar beneden in groep 2 en wat ze betekenen
Gegevens verzameld door LibreTexts en uitleg van de trends door Save My Exams tonen hetzelfde algemene patroon. De atoomstraal neemt toe van 112 pm voor Be tot 253 pm voor Ba, terwijl de eerste ionisatie-energie daalt van 900 naar 503 kJ/mol. In gewoon Nederlands: de buitenste elektronen bevinden zich verder van de kern en worden afgeschermd door meer binnenste schillen, waardoor ze gemakkelijker te verwijderen zijn.
| De trend | Richting beneden in groep 2 | Chemische oorzaak | Wat dit in de praktijk betekent |
|---|---|---|---|
| Atoomstraal | Verhoogt | Elk element heeft een extra elektronenschil en meer afscherming | Grotere atomen houden buitenste elektronen minder stevig vast |
| Eerste en tweede ionisatie-energie | Neemt in het algemeen af | Buitenste elektronen bevinden zich verder van de kern, dus de aantrekking is zwakker | Vorming van M 2+ionen wordt gemakkelijker |
| Reactiviteit | Neemt in het algemeen toe | Lagere ionisatie-energieën maken het verliezen van elektronen gemakkelijker | Zwaardere elementen reageren heftiger met zuren, zuurstof en vaak ook met water |
| Smeltpunt | Neemt over het algemeen af, maar niet gelijkmatig | Grotere metaalionen verzwakken de metaalbinding, hoewel de structuur ook van belang is | Gebruik hier het woord "algemeen", omdat Mg en Ca niet precies op een nette lijn passen |
| Dichtheid | Onregelmatig | Massa, atoomgrootte en metaalverpakking veranderen allemaal samen | Je kunt dichtheid niet beschouwen als één eenvoudige dalende trend |
| Oplosbaarheid van hydroxiden | Verhoogt | De balans tussen roosterenergie en hydratie-energie verschuift naar beneden in de groep | Zwaardere hydroxiden vormen meer alkalische oplossingen |
| Oplosbaarheid van sulfaten | Vermindert | Hydratie-energie daalt naarmate de kation groter wordt | Verbindingen zoals BaSO 4worden zeer onoplosbaar |
Dichtheid en smelgedrag zijn de twee trends die studenten vaak te sterk vereenvoudigen. Dichtheid verloopt niet in een rechte lijn, omdat zowel massa als volume veranderen en de metaalatomen niet op dezelfde manier in elk kristal worden verpakt. Ook smeltpunten vereisen voorzichtigheid. Deze dalen over het algemeen, omdat grotere ionen het metalen rooster verzwakken, maar Mg heeft een ongewoon laag smeltpunt van 650 °C, terwijl Ca stijgt naar 842 °C voordat de waarden weer dalen. Een van de veiligste kenmerken van aardalkalimetalen is dan ook het volgende: het brede patroon is reëel, maar de fysieke details verlopen niet perfect soepel.
Oplosbaarheid draagt hetzelfde waarschuwingslabel. Er bestaat geen enkele regel die op alle groep-2-zouten van toepassing is. Hydroxiden worden oplosbaarder naar beneden in de groep, terwijl sulfaten minder oplosbaar worden. Als iemand zegt: "oplosbaarheid neemt toe naar beneden in groep 2", dan is de belangrijke vraag: "Welke verbindingen?"
Waarom alkalische aardmetalen op de manier reageren waarop ze dat doen
Dus, zijn alkalische aardmetalen reactief ? Ja, en het algemene antwoord is dat ze reacteren naarmate u naar beneden gaat in de groep. De reden is hetzelfde elektronverhaal als hierboven beschreven. Lagere eerste en tweede ionisatie-energie betekent dat de atomen twee elektronen gemakkelijker kunnen verliezen en sneller de gangbare M 2+-toestand bereiken.
Dat heeft gevolgen voor werkelijke reacties. Naar beneden in de groep worden reacties met verdunde zuren sneller, worden reacties met zuurstof heftiger en zijn de zwaardere leden gemakkelijker te oxideren. Save My Exams merkt op dat barium zo reactief is dat het onder olie moet worden bewaard, wat een praktisch teken is van hoe ver de reactiviteitstrend kan gaan.
- De atoomstraal neemt toe naar beneden in groep 2.
- De ionisatie-energie neemt af naar beneden in groep 2.
- De reactiviteit neemt toe omdat het verliezen van twee elektronen gemakkelijker wordt.
- Smeltpunt en dichtheid vertonen onregelmatigheden, dus vermijd absolute regels.
- Hydroxiden en sulfaten tonen tegengestelde oplosbaarheidstrends.
Die patronen maken de familie voorspelbaar, maar niet volkomen uniform. Vlak bij de top van de groep begint beryllium al met het verbuigen van de regels, en magnesium voegt een andere alledaagse uitzondering toe die belangrijker is dan veel beginners verwachten.
Alkalimetalen en aardalkalimetalen
Algemene trends maken Groep 2 gemakkelijker te leren, maar de familie verliest haar zin als elk lid wordt behandeld alsof het identiek is. Het grootste waarschuwingsteken is beryllium. Magnesium voegt een meer praktische, alledaagse uitzondering toe. En wanneer mensen alkalimetalen en aardalkalimetalen vergelijken, kunnen vergelijkbare namen soms zeer verschillende chemie verbergen.
Waarom beryllium zich niet gedraagt als een typisch metaal uit Groep 2
BYJU'S beschrijft beryllium als de duidelijke uitschieter in Groep 2. Zijn ongewoon kleine grootte, hoge ionisatie-energie en sterke polariserende kracht geven het een gedrag dat minder typerend is voor de familie. In gewone taal: Be 2+trekt sterk aan nabijgelegen elektronenwolken, waardoor berylliumverbindingen vaak meer covalent zijn dan de meer ionische verbindingen die worden gevormd door de zwaardere leden van de groep. Dezelfde bron merkt ook op dat beryllium hogere smelt- en kookpunten heeft dan de overige leden van de groep en niet met water reageert zoals zijn groepsleden.
Magnesium is minder ongebruikelijk dan beryllium, maar kan toch minder reactief lijken dan leerlingen verwachten. LibreTexts wijst erop dat zeer schone magnesium slechts matig reageert met koud water, en dat de reactie spoedig vertraagt omdat bijna onoplosbaar magnesiumhydroxide een barrière vormt op het oppervlak. Onderaan de groep wordt radium meestal afzonderlijk besproken, omdat zijn radioactiviteit overheerst in praktische toepassingen en veiligheidsbesprekingen.
Hoe aardalkalimetalen verschillen van alkaliemetalen
In eenvoudige alkali versus aardalkali termen verliezen metaalgroep 1 één buitenste elektron, terwijl metaalgroep 2 twee elektronen verliest. Dat enkele verschil bepaalt de eigenschappen van alkali- en aardalkalimetalen meer dan bijna elk ander kenmerk.
| Kenmerk | Alkalimetalen, groep 1 | Aardalkalimetalen, groep 2 |
|---|---|---|
| Valentie-elektronen | 1 | 2 |
| Typisch ion | M + | M 2+ |
| Reactie met koud water | Vaak heftig of zelfs gewelddadig, waarbij een hydroxide en waterstof ontstaan | Minder eenvormig: Be reageert niet met water, Mg reageert matig, Ca, Sr en Ba reageren met toenemende hevigheid |
| Gemeenschappelijke zuurstofchemie | Kunnen oxiden, peroxiden of superoxiden vormen | Vormen meestal monoxiden; de meeste van deze oxiden vormen hydroxiden met water, maar BeO is een uitzondering |
Belangrijke uitzonderingen die leerlingen vaak over het hoofd zien
- Niet elk metaal uit groep 2 reageert op dezelfde manier met water.
- Berylliumverbindingen zijn meer covalent dan de rest van de groep.
- Verwar niet alkalimetalen en aardalkalimetalen met dezelfde groep alleen omdat de namen op elkaar lijken.
- De eigenschappen van alkalimetalen en aardalkalimetalen worden het beste geleerd als patronen met uitzonderingen, niet als starre slogans.
Dat is ook de beste manier om de chemische eigenschappen van alkalimetalen en aardalkalimetalen te begrijpen. Elektronenpatronen geven u de regel, maar reële stoffen voegen textuur toe. En die textuur wordt nog duidelijker wanneer u bekijkt waar elementen uit groep 2 daadwerkelijk voorkomen: zelden als zuivere metalen, en veel vaker in mineralen, gesteenten, zeewater, botten en industriële verbindingen.
Hoe aardalkalimetalen in de natuur voorkomen
Als u zich een aardalkalimetaal voorstelt als een heldere, zuivere staal dat in een steen ligt, werkt de natuur op een andere manier. Elementen uit groep 2 zijn reactief genoeg om meestal als ionen in mineralen, zouten, gesteenten, zeewater, botten en schelpen te voorkomen, in plaats van als vrije metalen. Of iemand nu zoekt naar aardalkalimetalen of naar de meer gebruikelijke term: het natuurlijke patroon is hetzelfde — deze elementenfamilie heeft een sterke voorkeur voor verbindingen.
Dat patroon volgt direct uit de chemische eigenschappen van aardalkalimetalen . Ze verliezen doorgaans twee buitenste elektronen en vormen stabiele M 2+²⁺-ionen. Zodra dat gebeurt, binden zuurstof-, carbonaat-, sulfaat- en halide-ionen ze gemakkelijk in vaste verbindingen die kunnen blijven bestaan in de geologie en biologie.
Waarom aardalkalimetalen niet vrij in de natuur voorkomen
Britannica en ThoughtCo beiden beschrijven Groep 2 als reactief, wat verklaart waarom deze elementen zelden ongebonden voorkomen. In lucht vormen veel ervan snel oxidecoatings. In natuurlijke omgevingen worden ze nog verder gestabiliseerd als carbonaten, sulfaten, silicaten, fluoriden of chloriden. Daarom komt calcium voor in kalksteen en schelpen, magnesium in mineralen en zeewater, en strontium of barium in ertsafzettingen. Radium is nog zeldzamer en komt uitsluitend in sporen aanwezig voor in uraniumerts.
Veelvoorkomende mineralen en verbindingen van Groep 2
| Elementen | Veelvoorkomende natuurlijke bron | Bekende verbinding | Waarom die verbinding belangrijk is |
|---|---|---|---|
| Beryllium | Beryl | BeO | Beryl is een commerciële bron van het element, terwijl berylliumoxide een belangrijke verbinding is in gespecialiseerde materialen |
| Magnesium | Magnesiet, dolomiet, zeewater | MgCO₃ 3of Mg(OH)₂ 2 | Toont aan waarom magnesium vaker wordt aangetroffen in mineralen, zeewater en geneeskunde dan als zuiver metaal |
| Calcium | Kalksteen, krijt, marmer, gips, botten, schelpen | Caco 3 | Verbindt geologie, bouwmaterialen en skeletten in één zeer gebruikelijke verbinding |
| Strontium | Celestiet, strontianiet | SrSO 4of SrCO 3 | Deze mineralen zijn de belangrijkste natuurlijke bronnen van strontiumverbindingen |
| Barium | Bariet, witheriet | BaSO 4 | Bariet is het belangrijkste erts, en bariumsulfaat is een van de meest bekende bariumverbindingen |
| Radium | Sporen in pechblende en andere uraniumertsen | RaCl 2 | Zijn zeldzaamheid en radioactiviteit maken radiumverbindingen historisch belangrijk, maar zeldzaam |
EBSCO merkt op dat calcium en magnesium ook voorkomen in zeewater, respectievelijk in een concentratie van ongeveer 0,4 g/L en 1,3 g/L. Dat helpt verklaren waarom deze aardalkalimetalen familie niet alleen verbonden is met ertsen, maar ook met hard water, mariene systemen en levend weefsel.
Hoe deze metalen uit hun verbindingen worden geïsoleerd
Aangezien groep-2-metalen meestal gebonden zijn in verbindingen, begint de winning met ertsen, pekel of minerale afzettingen. Een veelgebruikt industrieel principe is eenvoudig: converteer het materiaal eerst naar een beter verwerkbaar oxide of halide, en gebruik vervolgens elektrolyse of chemische reductie om het metaal vrij te maken. Volgens Britannica vond de eerste isolatie van magnesium, calcium, strontium en barium plaats via elektrolyse, terwijl EBSCO opmerkt dat moderne productie nog steeds vaak berust op gesmolten chloriden, oxide-reductie of verwante methoden, afhankelijk van het betreffende element. Beryllium is een nuttige herinnering aan het feit dat de familie niet volkomen uniform is, aangezien berylliumfluoride kan worden gebruikt voor de reductie tot beryllium.
Dus in het dagelijks leven komen mensen meestal Group 2 tegen via kalksteen, gips, magnesium uit zeewater, bariumsulfaat of biologische calcium, niet via zuivere metaalmonsters. Dat detail is belangrijk, omdat het praktische belang van deze elementen veel meer verband houdt met hun verbindingen en vormen dan met de zuivere metalen zelf.
Voorbeelden van aardalkalimetalen in het dagelijks leven
Group 2 wordt veel onvergetelijker wanneer u elk element verbindt met iets concreets. Botten, maagzuurremmers, gips, vuurwerk, boorvloeistoffen en oude lichtgevende wijzerplaten zijn allemaal nuttige voorbeelden van aardalkalimetalen . Als u zich ooit heeft afgevraagd is magnesium een metaal of een niet-metaal of is Ca een metaal , zijn beide antwoorden eenvoudig: magnesium en calcium zijn metalen. In het gewone leven komen mensen deze stoffen echter meestal tegen als verbindingen, niet als zuivere metaalmonsters.
Alledaagse toepassingen van magnesium- en calciumverbindingen
- Magnesium : Magnesium is een van de biologisch belangrijkste alkalische aardalkalimetalen gelanceerd. De NIH-magnesiuminformatieblad vermeldt dat het een cofactor is in meer dan 300 enzymstelsels en ondersteunt de spier- en zenuwfunctie, energieproductie en botstructuur. Magnesiumverbindingen komen ook voor in sommige maagzuurremmers en laxeermiddelen, terwijl magnesiummetaal gewaardeerd wordt in lichtgewicht legeringen waarbij massa-reductie van belang is.
- Calcium : Calciumverbindingen domineren het dagelijks leven. Calcium draagt bij aan de structuur van botten en tanden, en verbindingen zoals calciumcarbonaat en calciumsulfaat zijn centraal in kalksteen, cement, gips en gipsplaten. Dat maakt calcium één van de duidelijkste koppelingen tussen chemie, biologie en bouw.
Gespecialiseerde toepassingen van strontium en barium
- Strontium : Strontiumzouten staan vooral bekend om het veroorzaken van dieprode kleuren in vuurwerk en signaalvlammen. Zelfs lezers die zich de volledige lijst van groep 2-elementen niet herinneren, herinneren zich vaak strontium zodra er een kleur aan wordt gekoppeld.
- Barium : Bariumverbindingen zijn van belang in de industrie en geneeskunde. De NLM-bariumprofiel beschrijft de belangrijkste toepassingen in boorslibben, verf, kunststoffen, bakstenen en glas. Het noemt ook een belangrijk medisch contrast: zeer onoplosbaar bariumsulfaat wordt gebruikt als radio-opaque materiaal bij bepaalde röntgenonderzoeken, omdat het over het algemeen niet door het lichaam wordt opgenomen.
- Radium : Radium is voornamelijk een historisch of streng gereguleerd wetenschappelijk geval. De NRC-radiumpagina beschrijft het vroegere gebruik van radium in lichtgevende verf en bij vroege kankertherapie. De meeste van die toepassingen zijn inmiddels vervangen, hoewel nog steeds enkele gereguleerde toepassingen bestaan, zoals bepaalde industriële radiografietoepassingen.
Waarom vorm en verbindingstype van belang zijn in praktisch gebruik
Bij groep 2 is de vorm die mensen vaak gebruiken meestal de verbinding, niet het zuivere metaal.
Dat ene idee verduidelijkt veel verwarring. Magnesium in voedsel of medicijnen is niet hetzelfde als brandend magnesiumlint. Calcium in bot is niet hetzelfde als reactief calciummetaal. Barium is het meest duidelijke voorbeeld van waarom de vorm van een stof zo belangrijk is: onoplosbaar bariumsulfaat kan nuttig zijn bij medische beeldvorming, terwijl meer oplosbare bariumverbindingen veel grotere voorzichtigheid vereisen. Radium onderstreept dit nog sterker, omdat de radioactiviteit ervan — en niet alleen zijn plaats onder de metalen — bepaalt hoe ermee omgegaan moet worden.
De waarde van groep 2 is dus helemaal niet abstract. Deze elementen helpen uitleggen hoe dezelfde elementenfamilie relevant kan zijn voor voeding, materialen, geneeskunde, industriële verwerking en veiligheidsvoorschriften. Een korte lijst met concrete toepassingen is vaak al voldoende om het bredere patroon te onthouden.
Belangrijkste conclusies over groep 2-elementen
Op dit moment zou de alkalische aardmetalen-groep minder moeten aanvoelen als een lijst die uit het hoofd geleerd moet worden en meer als een patroon dat u direct kunt aflezen uit de groep 2 in het periodiek systeem kolom. Als iemand nog steeds vraagt, wat zijn de aardalkalimetalen? , het korte antwoord blijft eenvoudig: beryllium, magnesium, calcium, strontium, barium en radium. Een uitgebreidere definitie van aardalkalimetalen is nog nuttiger: zes metalen in groep 2 die meestal twee buitenste elektronen verliezen en M 2+-ionen vormen.
Belangrijkste conclusies over de aardalkalimetalen
- Locatie is belangrijk: deze zes groep-2-elementen staan in de tweede kolom van links, in het groep-2-gedeelte van het s-blok.
- De familieleden zijn vastgesteld: Be, Mg, Ca, Sr, Ba en Ra vormen de gehele reeks.
- Gedeelde chemie verklaart de familiegelijkenis: hun ns 2waardheidspatroon maakt +2-ionen het meest voorkomende resultaat, een kernpunt samengevat door LibreTexts.
- De belangrijkste neerwaartse trends zijn voorspelbaar: de atoomstraal neemt toe, de ionisatie-energie neemt over het algemeen af en de reactiviteit stijgt meestal naarmate u naar beneden in de groep gaat.
- De uitzonderingen zijn van belang: beryllium gedraagt zich meer covalent dan de andere elementen, magnesium kan minder reactief lijken vanwege zijn oppervlaktelaag, en radium wordt voornamelijk besproken in verband met zijn radioactiviteit.
- In het dagelijks leven betekent dit meestal verbindingen, niet zuivere metalen: mensen komen calciumcarbonaat, magnesiumoxide en bariumsulfaat veel vaker tegen dan elementair Ca, Mg of Ba.
De alkalische aardmetalen in het periodiek systeem kolom is het makkelijkst te onthouden als zes metalen die door één regel worden verbonden: ze vormen meestal 2+-ionen, maar elk lid toont die regel op een iets andere manier.
Van chemie van groep 2 tot geconstrueerde metalen onderdelen
Deze chemie reikt ver buiten leerboeken. LibreTexts merkt op dat elementair magnesium op grote schaal wordt geproduceerd en wordt gebruikt in lichtgewicht legeringen voor vliegtuigrompen en auto-motoronderdelen. Een uitgebreidere legeringsgids laat zien waarom dat belangrijk is: ingenieurs passen de samenstelling en bewerking aan om gewicht, sterkte, corrosieweerstand en bewerkbaarheid in werkelijke onderdelen in evenwicht te brengen.
Van de groep 2 in het periodiek systeem naar de productie, Shaoyi Metal Technology geeft een praktisch voorbeeld van die verbinding. De pagina's over automotive materialen en bewerking beschrijven de productie van metalen onderdelen, van prototyping tot massaproductie, waarbij het materiaalgedrag en de procescontrole samen moeten werken. Dat maakt de alkalische aardmetalen in het periodiek systeem meer dan een leskamergrafiek. Het vormt ook de logica achter de keuze van metalen en legeringen voor technische onderdelen die licht, betrouwbaar en vervaardigbaar moeten zijn.
Veelgestelde vragen over aardalkalimetalen
1. Wat zijn de zes aardalkalimetalen?
De zes aardalkalimetalen zijn beryllium, magnesium, calcium, strontium, barium en radium. Ze staan in groep 2 van het periodiek systeem en zijn gegroepeerd omdat ze meestal twee buitenste elektronen verliezen, wat leidt tot een gemeenschappelijk 2+-ionpatroon in veel verbindingen.
2. Hoe verschillen aardalkalimetalen van alkali-metalen?
Alkalimetalen behoren tot groep 1 en vormen doorgaans 1+-ionen, omdat ze één buitenste elektron hebben. Aardalkalimetalen bevinden zich in groep 2, vormen meestal 2+-ionen en zijn over het algemeen minder reactief. Dat ene extra valentie-elektron beïnvloedt de sterkte van hun bindingen, hun reactie met water en de soorten zouten en oxiden die ze gewoonlijk vormen.
3. Waarom komen aardalkalimetalen niet vrij in de natuur voor?
Deze metalen zijn reëeractief genoeg om in natuurlijke omgevingen meestal niet lang in zuivere elementaire vorm te blijven bestaan. In plaats daarvan binden ze zich met zuurstof-, carbonaat-, sulfaat-, chloride- of silicaationen en worden onderdeel van mineralen, gesteenten, zeewater, schelpen en botten. Daarom komt men groep 2 meestal tegen in de vorm van verbindingen, en niet als onbewerkte metaalmonsters.
4. Reageren alle aardalkalimetalen met water?
Nee, en dit is een van de meest nuttige uitzonderingen om te onthouden. Beryllium is grotendeels bestand tegen water, magnesium reageert langzaam met koud water omdat een oppervlaktelaag de reactie beperkt, en calcium, strontium en barium reageren gemakkelijker. Over het algemeen neemt de reactiviteit met water toe naarmate u zich naar beneden in groep 2 beweegt.
5. Waarom zijn aardalkalimetalen belangrijk in de industrie en productie?
Hun belang is gebaseerd op zowel hun verbindingen als hun rol bij de keuze van legeringen. Magnesium is waardevol wanneer een lager gewicht van belang is, calciumverbindingen zijn essentieel voor cement en pleister, en bariumverbindingen worden gekozen voor gespecialiseerde industriële en medische toepassingen. In de praktijk helpt het begrijpen van het gedrag van metalen bij het bepalen van bewerkingsmethoden, processtabiliteit en onderdeelkwaliteit. Daarom benadrukken leveranciers zoals Shaoyi Metal Technology gecertificeerde automobielbewerking, procescontrole en ondersteuning van prototype-onderdelen tot massaproductie.
 Kleine series, hoge eisen. Onze snelprototyperingservice maakt validatie sneller en eenvoudiger —
Kleine series, hoge eisen. Onze snelprototyperingservice maakt validatie sneller en eenvoudiger —
