Apakah Logam Tanah Alkali? Kumpulan 2 Akhirnya Menjadi Jelas
Apakah Logam Alkalina Tanah?
Jika anda mencari apakah logam alkalina tanah , berikut adalah jawapan langsung: ianya adalah enam unsur dalam Kumpulan 2 kumpulan 2 takrifan ringkas logam alkalina tanah ialah titik permulaan, tetapi nama tersebut juga memberitahu banyak mengenai cara keluarga unsur ini bertindak.
Apakah logam alkalina tanah dalam satu ayat
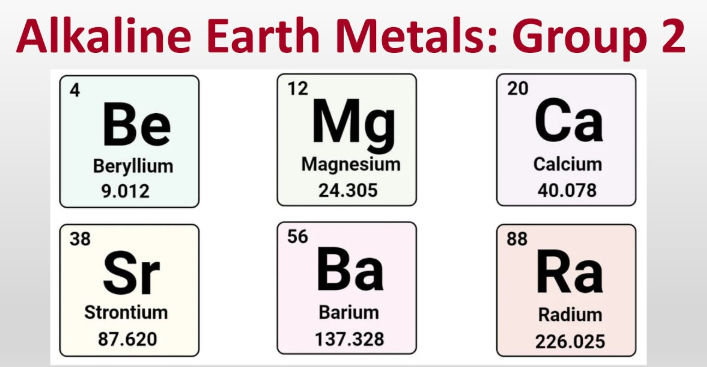
Logam alkalina tanah ialah berilium, magnesium, kalsium, stronsium, barium dan radium, iaitu enam unsur logam dalam Kumpulan 2 yang biasanya membentuk ion +2.
- Berilium (Be)
- Magnesium (Mg)
- Kalsium (Ca)
- Strontium (Sr)
- Barium (Ba)
- Radium (Ra)
Mengapa nama logam alkali tanah masuk akal
Untuk pemula, takrif logam alkali tanah menjadi jauh lebih mudah apabila anda membahagikan frasa tersebut kepada tiga bahagian.
Alkalin bermaksud oksida dan hidroksida mereka bersifat bes (alkali), bukan berasid. Bumi ialah perkataan bersejarah. Ahli kimia awal menggunakannya untuk bahan-bahan mineral seperti haba-stabil yang tidak melebur atau larut dengan mudah dalam air, suatu aspek yang dijelaskan oleh Britannica . Logam bermaksud unsur-unsur itu sendiri bersifat logam, biasanya berkilat dan cenderung kehilangan elektron dalam tindak balas.
Itu memberikan anda takrif asas logam alkali tanah tanpa perlu mempelajari kimia lanjutan terlebih dahulu. Ia juga merupakan huraian ringkas yang berguna mengenai logam alkali tanah : sebuah keluarga logam Kumpulan 2 dengan sifat kimia yang sama, kedudukan bersama dalam jadual berkala, dan peranan besar dalam dunia sebenar. Magnesium wujud dalam aloi dan biologi. Kalsium penting dalam tulang, cangkerang, dan bahan binaan. Barium, stronsium, dan radium muncul dalam konteks yang lebih khusus.
Artikel ini bermula secara ringkas secara sengaja. Senarai yang jelas mudah dihafal, tetapi kefahaman sebenar mengenai keluarga ini hanya tercapai apabila anda melihat di mana unsur-unsur ini berada dan mengapa kedudukan tersebut memberikan sifat yang begitu serupa.
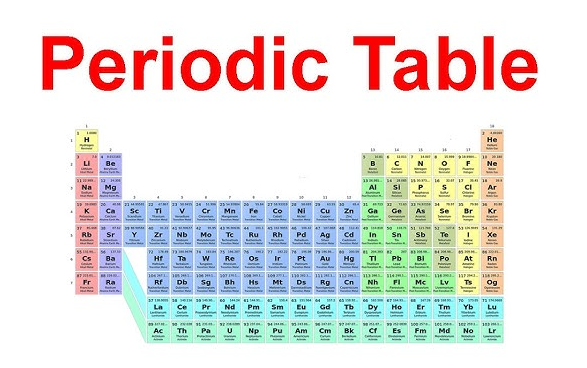
Kedudukan Kumpulan 2 dalam Jadual Berkala
Nama keluarga ini menjadi jauh lebih mudah diingati apabila anda benar-benar dapat mengenal pastinya. Jika anda bertanya-tanya di manakah logam alkali tanah terdapat dalam jadual berkala , lihat lajur kedua dari kiri. Lajur menegak ini ialah kumpulan 2 dalam jadual berkala , yang terletak tepat di sebelah logam alkali dalam Kumpulan 1. A kumpulan 2 jadual berkala gambar menunjukkan garis lurus yang sama setiap kali: berilium di bahagian atas, kemudian magnesium, kalsium, stronsium, barium, dan radium bergerak ke bawah melalui tempoh-tempoh tersebut.
Dalam sebuah jadual berkala logam alkali tanah carta, keenam-enam unsur ini termasuk dalam blok-s. Lokasi bersama mereka penting kerana ia mencerminkan corak elektron yang sama. Seperti LibreTexts menjelaskan, unsur-unsur Kumpulan 2 mempunyai konfigurasi valens ns 2, yang bermaksud mereka mempunyai dua elektron di petala luar.
Di manakah logam alkali tanah terletak dalam jadual berkala
Secara visual, coraknya mudah. unsur-unsur kumpulan 2 jadual berkala membentuk satu lajur keluarga merentasi tempoh 2 hingga 7. Ramai rajah bilik darjah menonjolkan logam alkali tanah dalam jadual berkala susun atur dengan warna yang sama kerana keluarga unsur dibaca secara menegak, bukan mengufuk. Carian untuk jadual berkala logam alkali tanah benar-benar meminta lajur tersebut.
| Unsur | Simbol | Kedudukan Kumpulan 2 | Ion lazim | Sebatian biasa |
|---|---|---|---|---|
| Berilium | Be | Tempoh 2, bahagian atas Kumpulan 2 | Be2+ | BeO |
| Magnesium | Mg | Tempoh 3 | Mg2+ | MgO |
| Kalsium | Ca | Tempoh 4 | Ca2+ | CaCO 3 |
| Strontium | Sr | Tempoh 5 | Sr2+ | SrCO 3 |
| Barium | BA | Tempoh 6 | BA 2+ | BaSO 4 |
| Radium | Ra | Tempoh 7, bahagian bawah Kumpulan 2 | Ra 2+ | RaCl 2 |
Mengapa unsur-unsur Kumpulan 2 membentuk ion positif dua
Dua elektron luaran itu menggerakkan kimia. Atom-atom Kumpulan 2 cenderung kehilangan kedua-dua elektron tersebut kerana tindakan ini memberikan susunan elektron yang lebih stabil. Hasilnya ialah ion +2 , seperti Mg 2+atau Ca 2+. Itulah sebabnya logam-logam ini biasanya membentuk sebatian seperti oksida, klorida, karbonat, dan sulfat. Anda dapat melihat corak tersebut dalam formula-formula dengan serta-merta: MgO, CaCl 2, CaCO 3, BaSO 4.
Cara Mengenali Keluarga Logam Alkali Tanah Secara Pantas
Suatu tip pengenalan pantas ialah mencari tiga petunjuk secara serentak: lajur kedua, unsur-unsur logam, dan cas biasa +2. Berbanding dengan logam alkali bersebelahan, yang mempunyai satu elektron valens dan biasanya membentuk ion +1, unsur-unsur Kumpulan 2 mempunyai satu elektron luaran tambahan dan secara umumnya kurang reaktif. Walaupun begitu, jelas bahawa unsur-unsur ini termasuk dalam keluarga yang sama. Bahagian yang menarik ialah setiap ahli menzahirkan corak tersebut dengan cara yang sedikit berbeza, terutamanya dari berilium di bahagian atas hingga radium di bahagian bawah.
Kenali Enam Logam Alkali Tanah
Senarai adalah berguna, tetapi ia tidak begitu mudah diingati secara tersendiri. Kumpulan 2 mula terasa lebih nyata apabila setiap ahlinya mempunyai identiti yang jelas. Sebilangan daripadanya wujud dalam tulang atau air laut. Sebilangan lagi memberi warna kepada bunga api. Salah satunya kebanyakannya merupakan tanda amaran sejarah. Secara bersama-sama, mereka masih termasuk dalam keluarga yang sama, tetapi setiap satu mempunyai personalitinya sendiri.
| Unsur | Simbol | Kemunculan biasa | Sifat menonjol | Kerelevanan Dalam Dunia Sebenar |
|---|---|---|---|---|
| Berilium | Be | Dijumpai dalam mineral seperti beril | Sangat ringan dan kaku untuk suatu logam | Digunakan dalam aplikasi penerbangan angkasa lepas dan sinar-X khusus; habuknya berbahaya jika dihirup |
| Magnesium | Mg | Wujud dalam air laut dan mineral | Ketumpatan rendah dan nyalaan putih terang semasa terbakar | Penting dalam aloi ringan, suplemen, dan biologi |
| Kalsium | Ca | Biasa dijumpai dalam batu kapur, tulang, cengkerang, dan kapur | Ion kumpulan 2 secara biologi akrab | Komponen utama dalam rangka, simen, plaster, dan banyak mineral semula jadi |
| Strontium | Sr | Wujud terutamanya dalam celestite dan strontianite | Garam-garamnya menghasilkan warna merah terang dalam nyalaan | Digunakan dalam bunga api, lampu isyarat, bahan bercahaya, dan beberapa produk pergigian |
| Barium | BA | Biasanya berkaitan dengan barit | Logam alkali tanah yang tumpat dan berat | Barium sulfat penting dalam pengeboran dan imej perubatan; sebatian barium larut memerlukan keberhatian |
| Radium | Ra | Wujud dalam jumlah surih dalam bijih uranium | Keradioaktifan yang kuat mendominasi kisah kimianya | Kebanyakan mempunyai relevansi sejarah atau saintifik yang ketat pada hari ini |
Berilium dan magnesium di bahagian atas Kumpulan 2
Yang unsur berilium terletak di bahagian atas keluarga tersebut dan sudah menunjukkan bahawa Kumpulan 2 tidak sepenuhnya seragam. Ia biasanya dikaitkan dengan mineral beril, iaitu keluarga mineral yang sama yang termasuk zamrud dan akuarin. Berilium menonjol kerana ia luar biasa ringan dan kaku. Sifat ini menjadikannya berguna dalam komponen berprestasi tinggi di mana jisim rendah menjadi penting. Pada masa yang sama, berilium merupakan bahan yang memerlukan penjagaan khusus dalam persekitaran industri, kerana habuk halusnya boleh membahayakan jika dihirup. Oleh itu, berilium diingati baik kerana prestasinya mahupun kerana keperluan keberhati-hatian dalam pengendaliannya.
Magnesium terasa jauh lebih akrab. simbol kimia magnesium ialah Mg, dan ia merupakan salah satu logam paling terkenal dalam kumpulan ini kerana wujud dalam air laut, mineral biasa, dan sistem hidup. Ia merupakan logam yang sangat ringan, dan apabila terbakar, ia menghasilkan cahaya putih yang terang. Oleh sebab itu, magnesium telah lama dikaitkan dengan peluru berpandu dan bahan yang terbakar dengan terang. Namun, dalam kehidupan harian, kebanyakan orang menjumpainya dalam bentuk yang lebih lembut seperti peranan dalam diet, sebatian antasid, atau aloi ringan yang digunakan di tempat di mana pengurangan jisim menjadi penting.
Kalsium dan stronsium dalam bahan harian
Kalsium merupakan ahli Kumpulan 2 yang paling dikenali oleh ramai pembaca. Ia wujud dalam batu kapur, kapur, cengkerang, dan tulang, sehingga menghubungkan kimia dengan geologi dan biologi secara langsung. Kalsium karbonat ialah sebatian yang dikenali di sini. Ia membantu menerangkan mengapa keluarga unsur yang sama boleh memainkan peranan dalam pembentukan gua, batu bangunan, dan rangka. Logam kalsium sendiri bersifat reaktif, tetapi sebatian kalsium wujud di mana-mana, justeru unsur ini sering dirasai lebih akrab berbanding eksotik.
Stronsium lebih mudah diingat apabila dikaitkan dengan warna. simbol bagi stronsium ialah Sr, dan strontium dijumpai terutamanya dalam mineral celestite dan strontianite. Royal Society of Chemistry menghuraikannya sebagai logam lembut berwarna keperakan yang terbakar di udara dan bertindak balas dengan air. Garam-garamnya terkenal kerana menghasilkan warna merah terang dalam bunga api dan lampu isyarat. Sumber yang sama juga mencatatkan kegunaannya dalam bahan bercahaya dalam gelap dan stronsium klorida heksahidrat dalam ubat gigi untuk gigi sensitif. Ini menjadikan stronsium contoh yang baik tentang bagaimana suatu unsur boleh bersifat reaktif secara kimia namun kebanyakannya dijumpai melalui sebatian.
Barium dan radium dalam konteks lanjutan atau khusus
Yang unsur barium sering diingati melalui beratnya. Ia biasanya dikaitkan dengan barit, dan salah satu sebatian paling dikenali ialah barium sulfat. Sebatian ini penting kerana ia sangat tidak larut, yang membantu menerangkan mengapa barium boleh wujud dalam konteks praktikal seperti cecair pengeboran dan imej perubatan, manakala sebatian barium lain yang larut ditangani dengan lebih berhati-hati disebabkan kebimbangan toksisiti. Barium mengingatkan pembaca bahawa bentuk berguna unsur Kumpulan 2 sering kali adalah sebatian, bukan logam berkilat itu sendiri.
Radium terletak di bahagian bawah keluarga ini, tetapi ia tidak menyatu secara senyap. jadual berkala radium lihat, Ra menandakan titik di mana radioaktiviti menjadi ciri utama. Radium wujud secara semula jadi hanya dalam jumlah yang sangat kecil, biasanya berkaitan dengan bijih uranium. Secara sejarah, radium menjadi terkenal kerana cat bercahaya dan eksperimen perubatan awal. Hari ini, bahayanya berasal daripada radioaktivitinya, bukan daripada sifat logam biasa, maka ia dikendalikan di bawah kawalan ketat. Secara ringkasnya, radium masih termasuk dalam Kumpulan 2, tetapi dibincangkan dengan mempertimbangkan keselamatan nuklear sama pentingnya dengan kimia.
Susun keenam-enam unsur ini secara bersebelahan, dan keluarga tersebut tidak lagi kelihatan seperti senarai nama kosong. Saiz, kereaktifan, sebatian lazim, dan malah cara setiap unsur muncul dalam kehidupan berubah apabila anda bergerak ke bawah. Corak perubahan inilah yang menjadikan Kumpulan 2 terutamanya berguna, kerana susunan dari berilium hingga radium mula menyingkap corak (trend) bukannya fakta-fakta remeh.
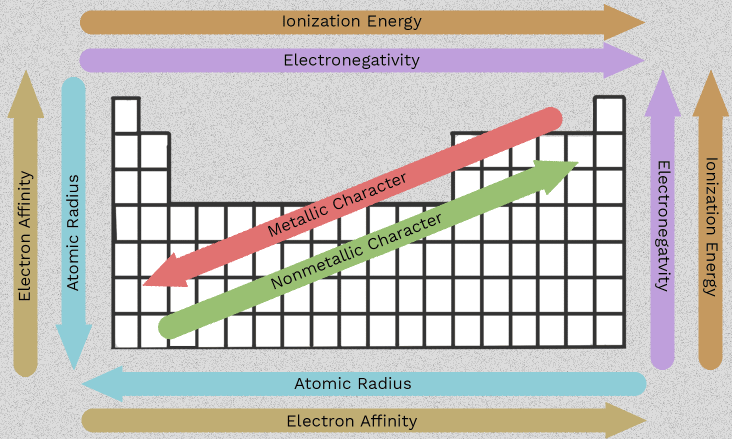
Sifat Logam Alkalina Tanah dan Corak Kumpulan 2
Urutan perubahan dari berilium hingga radium itulah yang menjadikan Kumpulan 2 berguna. Alih-alih menghafal enam fakta terpisah, anda boleh mengikuti beberapa corak yang berulang sepanjang lajur tersebut. Corak yang paling penting sifat logam alkali tanah semuanya berasal daripada satu ciri bersama: setiap atom mempunyai dua elektron luaran yang cenderung hilang.
Apabila anda memahami bagaimana saiz atom, perlindungan elektron, dan tenaga pengionan berubah ke bawah kumpulan tersebut, keluarga unsur ini menjadi jauh lebih mudah diramalkan. Sifat-sifat ini ciri logam alkali tanah bukan sekadar fakta untuk peperiksaan. Sebaliknya, sifat-sifat ini menerangkan mengapa sesetengah ahli bertindak balas lebih cepat, mengapa sesetengah sebatian lebih larut berbanding yang lain, dan mengapa beberapa tren memerlukan pernyataan yang teliti bukan sekadar anak panah ringkas.
Sifat bersama logam alkali tanah
Kebanyakan ahli Kumpulan 2 adalah logam berkilau perak yang biasanya membentuk M 2+ion dan membentuk sebahagian besar sebatian ionik. Mereka bertindak sebagai agen penurun kerana mereka kehilangan elektron. Berbanding dengan logam Kumpulan 1, logam ini secara umumnya kurang reaktif, tetapi masih cukup aktif secara kimia untuk membentuk banyak oksida, klorida, karbonat, dan sulfat biasa.
Cara mudah untuk mengatur sifat-sifat kimia logam alkali tanah ialah dengan memisahkan apa yang kekal tetap daripada apa yang berubah. Apa yang kekal tetap ialah keadaan pengoksidaan +2 yang biasa. Apa yang berubah ialah seberapa mudah setiap unsur melepaskan dua elektron tersebut. Di situlah tren mulai menjadi penting.
Tren menuruni Kumpulan 2 dan maksudnya
Data yang dikumpulkan oleh LibreTexts dan penjelasan tren daripada Save My Exams menunjukkan corak keseluruhan yang sama. Jejari atom meningkat daripada 112 pm bagi Be hingga 253 pm bagi Ba, manakala tenaga pengionan pertama menurun daripada 900 hingga 503 kJ/mol. Dalam bahasa mudah, elektron luar terletak semakin jauh daripada nukleus dan dilindungi oleh lebih banyak petala dalaman, maka lebih mudah untuk dikeluarkan.
| Trend | Arah menuruni Kumpulan 2 | Sebab kimia | Maksudnya Dalam Amalan |
|---|---|---|---|
| Jejari atom | Meningkatkan | Setiap unsur mempunyai satu cengkerang elektron tambahan dan lebih banyak pelindungan | Atom yang lebih besar mengikat elektron luar dengan kurang ketat |
| Tenaga pengionan pertama dan kedua | Menurun secara keseluruhan | Elektron luar berada lebih jauh dari nukleus, maka daya tarikan menjadi lebih lemah | Pembentukan M 2+ion menjadi lebih mudah |
| Tindak Balas | Meningkat secara keseluruhan | Tenaga pengionan yang lebih rendah menjadikan kehilangan elektron lebih mudah | Ahli yang lebih berat bertindak balas lebih cergas dengan asid, oksigen, dan sering kali air |
| Titik lebur | Secara umum menurun, tetapi tidak secara licin | Ion logam yang lebih besar melemahkan ikatan logam, walaupun struktur juga memainkan peranan | Gunakan perkataan "umum" di sini, kerana Mg dan Ca tidak mengikuti garis yang sempurna |
| Ketumpatan | Tidak teratur | Jisim, saiz atom, dan pengepakan logam semua berubah secara serentak | Anda tidak boleh menganggap ketumpatan sebagai satu kecenderungan menurun yang mudah |
| Keterlarutan hidroksida | Meningkatkan | Keseimbangan tenaga kisi dan tenaga hidrasi berubah ke bawah kumpulan | Hidroksida yang lebih berat menghasilkan larutan yang lebih beralkali |
| Keterlarutan sulfat | Berkurang | Tenaga penghidratan menurun apabila kation menjadi lebih besar | Sebatian seperti BaSO 4menjadi sangat tidak larut |
Ketumpatan dan tingkah laku peleburan merupakan dua kecenderungan yang sering disederhanakan secara berlebihan oleh pelajar. Ketumpatan tidak berubah secara linear kerana kedua-dua jisim dan isipadu berubah, dan atom logam tidak tersusun dengan cara yang sama dalam setiap hablur. Titik lebur juga memerlukan perhatian khusus. Secara umumnya, titik lebur cenderung menurun kerana ion yang lebih besar melemahkan kekisi logam, tetapi Mg mempunyai titik lebur yang tidak biasa rendah iaitu 650 °C, manakala Ca meningkat kepada 842 °C sebelum nilai-nilai tersebut turun semula. Oleh itu, salah satu ciri paling selamat logam alkali tanah ialah ini: corak umum adalah benar, tetapi butiran fizikalnya tidak sepenuhnya licin.
Keterlarutan mempunyai amaran yang sama. Tiada satu peraturan tunggal yang merangkumi semua garam Kumpulan 2. Hidroksida menjadi lebih larut ke bawah kumpulan, manakala sulfat menjadi kurang larut. Jika seseorang berkata "keterlarutan meningkat ke bawah Kumpulan 2", soalan penting yang perlu ditanya ialah, "Sebatian yang mana?"
Mengapa logam alkali tanah bertindak balas dengan cara yang demikian
Jadi, adakah logam alkali tanah reaktif ? Ya, dan jawapan umumnya ialah reaktivitas meningkat apabila bergerak ke bawah. Sebabnya adalah cerita elektron yang sama seperti yang dinyatakan di atas. Tenaga pengionan pertama dan kedua yang lebih rendah bermaksud atom-atom tersebut dapat kehilangan dua elektron dengan lebih mudah dan mencapai keadaan M 2+dengan lebih cepat.
Ini mempengaruhi tindak balas sebenar. Sepanjang kumpulan, tindak balas dengan asid cair menjadi lebih cepat, tindak balas dengan oksigen menjadi lebih cergas, dan ahli-ahli yang lebih berat lebih mudah dioksidakan. Nota Save My Exams menyatakan bahawa barium cukup reaktif untuk disimpan di bawah minyak, iaitu tanda praktikal sejauh mana trend reaktivitas ini boleh berlaku.
- Jejari atom meningkat ke bawah Kumpulan 2.
- Tenaga pengionan menurun ke bawah Kumpulan 2.
- Reaktivitas meningkat kerana kehilangan dua elektron menjadi lebih mudah.
- Takat lebur dan ketumpatan menunjukkan ketidaksekataan, jadi elakkan peraturan mutlak.
- Hidroksida dan sulfat menunjukkan trend kelarutan yang bertentangan.
Corak-corak tersebut menjadikan keluarga ini boleh diramalkan, tetapi tidak sepenuhnya seragam. Betul-betul di bahagian atas kumpulan ini, berilium sudah mula melanggar peraturan, manakala magnesium menambah satu pengecualian harian lain yang lebih penting daripada yang dijangkakan oleh ramai pemula.
Logam alkali dan logam alkalina tanah
Kecenderungan umum menjadikan Kumpulan 2 lebih mudah dipelajari, tetapi keluarga ini berhenti masuk akal jika setiap ahlinya dikendalikan sebagai identik. Tanda amaran terbesar ialah berilium. Magnesium menambah satu pengecualian harian yang lebih praktikal. Dan apabila orang membandingkan logam alkali dan logam alkalina tanah , nama-nama yang serupa boleh menyembunyikan beberapa kimia yang sangat berbeza.
Mengapa berilium tidak bertindak seperti logam Kumpulan 2 yang lazim
BYJU'S menggambarkan berilium sebagai peserta luar biasa yang jelas dalam Kumpulan 2. Saiznya yang tidak biasa kecil, tenaga pengionannya yang tinggi, dan kuasa pengutubannya yang kuat memberikannya sifat-sifat yang kurang mencerminkan ciri keluarga ini. Dalam bahasa biasa, Be 2+menarik dengan kuat pada awan elektron berdekatan, jadi sebatian berilium sering lebih kovalen berbanding sebatian yang lebih ionik yang dibentuk oleh ahli-ahli kelompok yang lebih berat. Sumber yang sama juga mencatat bahawa berilium mempunyai takat lebur dan takat didih yang lebih tinggi berbanding ahli-ahli kelompok lain dan tidak bertindak balas dengan air seperti rakan-rakannya.
Magnesium tidak seaneh berilium, tetapi ia masih boleh kelihatan kurang reaktif daripada yang dijangkakan pelajar. LibreTexts mencatat bahawa magnesium yang sangat bersih hanya bertindak balas secara ringan dengan air sejuk, dan tindak balas tersebut cepat melambat kerana magnesium hidroksida yang hampir tidak larut membentuk halangan pada permukaan. Di bahagian bawah keluarga ini, radium biasanya dibincangkan secara berasingan kerana sifat radioaktifnya mendominasi perbincangan mengenai kegunaan praktikal dan keselamatan.
Bagaimana logam alkali tanah berbeza daripada logam alkali
Secara ringkas alkali berbanding alkali tanah secara istilah, logam Kumpulan 1 kehilangan satu elektron luaran, manakala logam Kumpulan 2 kehilangan dua elektron. Perbezaan tunggal ini membentuk sifat-sifat logam alkali dan logam alkali tanah lebih daripada hampir apa-apa perkara lain.
| Ciri | Logam alkali, Kumpulan 1 | Logam alkali tanah, Kumpulan 2 |
|---|---|---|
| Valens aluminium | 1 | 2 |
| Ion lazim | M + | M 2+ |
| Tindak balas dengan air sejuk | Kebanyakan bersifat cergas atau bahkan ganas, membentuk hidroksida dan hidrogen | Kurang seragam: Be tidak bertindak balas dengan air, Mg bertindak balas secara ringan, manakala Ca, Sr, dan Ba bertindak balas dengan kecergasan yang meningkat |
| Kimia oksigen biasa | Boleh membentuk oksida, peroksida, atau superoksida | Kebanyakan membentuk monoksida; kebanyakan oksida ini menghasilkan hidroksida apabila bertindak balas dengan air, tetapi BeO merupakan pengecualian |
Pengecualian penting yang sering diabaikan pelajar
- Tidak semua logam Kumpulan 2 bertindak balas dengan air dengan cara yang sama.
- Sebatian berilium lebih kovalen berbanding unsur-unsur lain dalam keluarga ini.
- Jangan kelirukan logam alkali dan logam alkali tanah sebagai kumpulan yang sama hanya kerana nama-nama tersebut kedengaran berkaitan.
- Yang sifat-sifat logam alkali dan logam alkali tanah paling baik dipelajari sebagai corak-corak dengan pengecualian, bukan sebagai jata-jata yang kaku.
Itulah juga cara terbaik untuk memahami sifat-sifat kimia logam alkali dan logam alkali tanah . Corak elektron memberikan anda peraturan, tetapi bahan-bahan sebenar menambah dimensi. Dan dimensi ini menjadi lebih jelas apabila anda melihat di mana unsur-unsur Kumpulan 2 benar-benar wujud: jarang sebagai logam tulen, dan jauh lebih kerap di dalam mineral, batuan, air laut, tulang, dan sebatian industri.
Bagaimana Logam Alkali Tanah Wujud di Alam Semula Jadi
Jika anda membayangkan suatu logam alkali tanah sebagai contoh yang terang dan tulen yang terletak di dalam batu, alam beroperasi dengan cara yang berbeza. Unsur-unsur Kumpulan 2 cukup reaktif sehingga biasanya wujud sebagai ion di dalam mineral, garam, batu, air laut, tulang, dan cangkerang, bukan sebagai logam bebas. Sama ada seseorang mencari logam alkali tanah atau istilah yang lebih standard, corak semula jadi tetap sama: keluarga ini sangat mengutamakan sebatian.
Corak ini timbul secara langsung daripada sifat kimia logam alkali tanah . Mereka cenderung kehilangan dua elektron luaran dan membentuk ion M 2+yang stabil. Setelah ini berlaku, ion oksigen, karbonat, sulfat, dan halida dengan mudah mengikatnya ke dalam sebatian pepejal yang mampu bertahan dalam geologi dan biologi.
Mengapa logam alkali tanah tidak dijumpai dalam bentuk bebas di alam
Britannica dan ThoughtCo keduanya menggambarkan Kumpulan 2 sebagai reaktif, yang menjelaskan mengapa unsur-unsur ini jarang ditemukan dalam bentuk tidak terkombinasi. Di udara, banyak unsur ini dengan cepat membentuk lapisan oksida. Dalam lingkungan alami, stabilitasnya meningkat lebih lanjut sebagai karbonat, sulfat, silikat, fluorida, atau klorida. Oleh sebab itu, kalsium ditemukan dalam batu kapur dan cangkang, magnesium dalam mineral dan air laut, serta stronsium atau barium dalam endapan bijih. Radium jauh lebih jarang lagi, hanya terdapat dalam jumlah jejak di bijih uranium.
Mineral dan sebatian biasa bagi Kumpulan 2
| Unsur | Sumber semula jadi biasa | Sebatian biasa | Mengapa sebatian tersebut penting |
|---|---|---|---|
| Berilium | Beryl | BeO | Beryl merupakan sumber komersial unsur ini, manakala oksida berilium merupakan sebatian penting dalam bahan khusus |
| Magnesium | Magnesit, dolomit, air laut | MgCO₃ 3atau Mg(OH)₂ 2 | Menunjukkan mengapa magnesium lebih sering dijumpai dalam mineral, air laut, dan perubatan berbanding dalam bentuk logam tulen |
| Kalsium | Batu kapur, kapur, marmar, gips, tulang, cangkang | CaCO 3 | Menghubungkan geologi, bahan-bahan binaan, dan rangka dalam satu sebatian yang sangat biasa |
| Strontium | Celestit, stronsianit | SrSO 4atau SrCO 3 | Mineral-mineral ini merupakan sumber semula jadi utama sebatian stronsium |
| Barium | Barit, witerit | BaSO 4 | Barit merupakan bijih utama, dan barium sulfat merupakan salah satu sebatian barium yang paling dikenali |
| Radium | Jumlah jejak dalam pitchblende dan bijih uranium lain | RaCl 2 | Kelangkaan dan sifat radioaktifnya menjadikan sebatian radium penting secara sejarah tetapi jarang dijumpai |
EBSCO menyatakan bahawa kalsium dan magnesium juga wujud dalam air laut pada kepekatan sekitar 0.4 g/L dan 1.3 g/L, masing-masing. Ini membantu menjelaskan mengapa logam alkali tanah keluarga ini tidak hanya berkaitan dengan bijih, tetapi juga dengan air liat, sistem marin, dan tisu hidup.
Cara logam-logam ini diasingkan daripada sebatian mereka
Memandangkan logam Kumpulan 2 biasanya terperangkap di dalam sebatian, proses pengekstrakan bermula dengan bijih, air masin (brine), atau deposit mineral. Prinsip industri umum yang digunakan adalah mudah: pertama-tama menukar bahan tersebut kepada oksida atau halida yang lebih mudah diproses, kemudian menggunakan elektrolisis atau penurunan kimia untuk membebaskan logam tersebut. Britannica menerangkan pengekstrakan awal magnesium, kalsium, stronsium, dan barium melalui elektrolisis, manakala EBSCO mencatat bahawa pengeluaran moden masih biasanya bergantung pada klorida lebur, penurunan oksida, atau kaedah berkaitan lain bergantung kepada unsur yang dimaksudkan. Berilium merupakan pengingat berguna bahawa keluarga ini tidak sepenuhnya seragam, kerana berilium boleh dihasilkan melalui penurunan fluorida berilium.
Jadi dalam kehidupan seharian, orang biasanya menjumpai Kumpulan 2 melalui batu kapur, plaster, magnesium air laut, barit, atau kalsium biologi, bukan melalui sampel logam mentah. Butiran ini penting, kerana kepentingan unsur-unsur ini dalam dunia sebenar lebih berkaitan dengan sebatian dan bentuknya berbanding dengan logam tulen itu sendiri.
Contoh Logam Alkalina Tanah dalam Kehidupan Seharian
Kumpulan 2 menjadi jauh lebih mudah diingati apabila setiap unsur dikaitkan dengan sesuatu yang nyata. Tulang, ubat penawar asid (antacid), plaster, bunga api, cecair pemboran, dan penunjuk bercahaya lama semuanya berguna contoh logam alkalina tanah . Jika anda pernah bertanya-tanya adakah magnesium logam atau bukan logam aTAU adakah Ca logam , kedua-dua jawapan adalah mudah: magnesium dan kalsium adalah logam. Namun, dalam kehidupan biasa, orang biasanya menjumpai bahan-bahan ini dalam bentuk sebatian, bukan sebagai sampel logam tulen.
Kegunaan harian sebatian magnesium dan kalsium
- Magnesium : Magnesium merupakan salah satu unsur yang paling penting secara biologi unsur-unsur alkali tanah . Siri Lembar Fakta Magnesium NIH menyatakan bahawa ia merupakan kofaktor dalam lebih daripada 300 sistem enzim dan menyokong fungsi otot dan saraf, penghasilan tenaga, serta struktur tulang. Sebatian magnesium juga terdapat dalam beberapa antasid dan laksatif, manakala logam magnesium dihargai dalam aloi ringan di mana pengurangan jisim menjadi penting.
- Kalsium sebatian kalsium mendominasi kehidupan harian. Kalsium membantu memberikan struktur kepada tulang dan gigi, dan sebatian seperti kalsium karbonat dan kalsium sulfat memainkan peranan utama dalam batu kapur, simen, plester, dan papan gips. Ini menjadikan kalsium salah satu hubungan paling jelas antara kimia, biologi, dan pembinaan.
Aplikasi khusus stronsium dan barium
- Strontium garam stronsium paling dikenali kerana menghasilkan warna merah tua dalam bunga api dan peluru isyarat. Malah pembaca yang tidak mengingati senarai penuh Kumpulan 2 sering kali masih mengingati stronsium apabila warna dikaitkan dengannya.
- Barium sebatian barium penting dalam industri dan perubatan. Profil Barium NLM menerangkan kegunaan utama dalam lumpur pengeboran, cat, plastik, batu bata, dan kaca. Ia juga mencatat kontras perubatan penting: barium sulfat yang sangat tidak larut digunakan sebagai bahan radio-opak dalam sesetengah pemeriksaan sinar-X kerana ia secara amnya tidak diserap oleh badan.
- Radium : Radium kebanyakannya merupakan kes sejarah atau kes saintifik yang dikawal ketat. Halaman radium NRC menerangkan penggunaannya pada masa lalu dalam cat bercahaya dan terapi kanser awal. Kebanyakan penggunaan tersebut telah digantikan, walaupun beberapa penggunaan yang dikawal masih wujud, seperti aplikasi radiografi industri tertentu.
Mengapa bentuk dan jenis sebatian penting dalam penggunaan sebenar
Dalam Kumpulan 2, bentuk yang digunakan orang kebanyakannya adalah sebatian, bukan logam tulen.
Idea tunggal itu menghilangkan banyak kekeliruan. Magnesium dalam makanan atau ubat bukanlah perkara yang sama dengan pembakaran pita magnesium. Kalsium dalam tulang bukanlah perkara yang sama dengan logam kalsium yang reaktif. Barium merupakan contoh paling jelas mengapa bentuk suatu unsur penting: barium sulfat yang tidak larut boleh digunakan secara berguna dalam imej perubatan, manakala sebatian barium yang lebih larut memerlukan tahap kewaspadaan yang jauh lebih tinggi. Radium membawa hujah ini lebih jauh lagi, kerana sifat radioaktifnya—bukan sekadar kedudukannya dalam kelompok logam—yang menentukan cara penanganannya.
Jadi, nilai Kelompok 2 sama sekali tidak abstrak. Unsur-unsur ini membantu menjelaskan bagaimana satu keluarga unsur yang sama boleh memainkan peranan penting dalam nutrisi, bahan, perubatan, pemprosesan industri, dan peraturan keselamatan. Senarai ringkas kegunaan sebenar sering kali sudah cukup untuk membuat corak besar ini melekat dalam ingatan.
Rumusan Utama Mengenai Unsur-unsur Kelompok 2
Pada tahap ini, logam alkali tanah sepatutnya terasa kurang seperti senarai yang perlu dihafal dan lebih seperti corak yang boleh dibaca secara langsung daripada kelompok 2 dalam jadual berkala lajur. apakah logam alkali tanah itu , jawapan ringkasnya tetap mudah: berilium, magnesium, kalsium, stronium, barium, dan radium. Definisi yang lebih lengkap logam alkali tanah malah lebih berguna: enam unsur logam dalam Kumpulan 2 yang biasanya kehilangan dua elektron luar dan membentuk ion M 2+.
Rumusan utama mengenai logam alkali tanah
- Lokasi penting: keenam-enam unsur Kumpulan 2 terletak dalam lajur kedua dari kiri, iaitu bahagian Kumpulan 2 dalam blok-s.
- Ahli keluarga adalah tetap: Be, Mg, Ca, Sr, Ba, dan Ra membentuk keseluruhan set tersebut.
- Kimia bersama menerangkan persamaan keluarga: ns mereka 2corak valensi menjadikan ion +2 sebagai hasil yang biasa, suatu titik utama yang diringkaskan oleh LibreTexts.
- Kecenderungan utama ke bawah adalah boleh diramalkan: jejari atom meningkat, tenaga pengionan secara amnya menurun, dan kereaktifan biasanya meningkat apabila bergerak ke bawah kumpulan.
- Pengecualian adalah penting: berilium bertindak lebih kovalen berbanding unsur lain, magnesium boleh kelihatan kurang reaktif disebabkan lapisan permukaannya, dan radium dibincangkan terutamanya dari segi keradioaktifannya.
- Dalam kehidupan sebenar, maksudnya biasanya sebatian, bukan logam tulen: orang ramai lebih kerap berjumpa dengan kalsium karbonat, magnesium oksida, dan barium sulfat berbanding dengan unsur Ca, Mg, atau Ba secara langsung.
Yang jadual berkala logam alkali tanah lajur ini paling mudah diingati sebagai enam logam yang dikaitkan oleh satu peraturan: logam-logam ini biasanya membentuk ion 2+, tetapi setiap ahli menzahirkan peraturan tersebut dengan cara yang sedikit berbeza.
Daripada kimia Kumpulan 2 kepada komponen logam yang direkabentuk
Kimia ini meluas jauh ke luar daripada buku teks. LibreTexts mencatat bahawa magnesium unsur dihasilkan dalam skala besar dan digunakan dalam aloi ringan untuk rangka pesawat dan komponen enjin kereta. Panduan aloi yang lebih luas menunjukkan mengapa perkara ini penting: jurutera menyesuaikan komposisi dan proses pengeluaran untuk menyeimbangkan faktor-faktor seperti berat, kekuatan, rintangan kakisan, dan kemudahan pemesinan dalam komponen sebenar.
Untuk pembaca yang berpindah daripada pandangan kelompok 2 dalam jadual berkala ke pembuatan, Shaoyi Metal Technology menawarkan contoh praktikal hubungan tersebut. Halaman bahan automotif dan pemesinan menyatakan pengeluaran komponen logam dari peringkat prototaip hingga pengeluaran berkelompok, di mana kelakuan bahan dan kawalan proses perlu berfungsi secara serentak. Ini menjadikan jadual berkala logam alkali tanah lebih daripada sekadar carta bilik darjah. Ia juga merupakan sebahagian daripada logik dalam memilih logam dan aloi untuk komponen kejuruteraan yang perlu ringan, boleh dipercayai, dan mudah dikeluarkan.
Soalan Lazim Mengenai Logam Alkalina Tanah
1. Apakah enam logam alkalina tanah?
Enam logam alkalina tanah ialah berilium, magnesium, kalsium, stronsium, barium, dan radium. Logam-logam ini terletak dalam Kumpulan 2 jadual berkala dan dikumpulkan bersama kerana biasanya kehilangan dua elektron luaran, menghasilkan corak ion 2+ yang umum dalam banyak sebatian.
2. Bagaimanakah logam alkalina tanah berbeza daripada logam alkali?
Logam alkali termasuk dalam Kumpulan 1 dan biasanya membentuk ion 1+ kerana mempunyai satu elektron luaran. Logam alkali tanah berada dalam Kumpulan 2, biasanya membentuk ion 2+, dan cenderung kurang reaktif secara keseluruhan. Satu elektron valensi tambahan itu mengubah kekuatan ikatan mereka, cara tindak balas mereka dengan air, serta jenis garam dan oksida yang biasa terbentuk.
3. Mengapa logam alkali tanah tidak dijumpai dalam bentuk bebas di alam?
Logam-logam ini cukup reaktif sehingga biasanya tidak kekal dalam bentuk unsur tulen untuk jangka masa yang lama dalam persekitaran semula jadi. Sebaliknya, mereka bergabung dengan ion oksigen, karbonat, sulfat, klorida, atau silikat dan menjadi sebahagian daripada mineral, batuan, air laut, cangkerang, dan tulang. Oleh sebab itu, orang ramai biasanya menjumpai Kumpulan 2 melalui sebatian-sebatian, bukan dalam bentuk logam mentah.
4. Adakah semua logam alkali tanah bertindak balas dengan air?
Tidak, dan ini merupakan salah satu pengecualian yang paling berguna untuk diingat. Berilium secara umum tahan terhadap air, magnesium bereaksi perlahan dalam air sejuk kerana lapisan permukaan menghadkan tindak balas tersebut, manakala kalsium, stronsium, dan barium bereaksi lebih mudah. Secara umum, kereaktifan terhadap air menjadi lebih kuat apabila bergerak ke bawah Kumpulan 2.
5. Mengapa logam alkali tanah penting dalam industri dan pembuatan?
Kepentingan mereka timbul daripada sebahagian besar sebatian mereka serta peranan mereka dalam pemilihan aloi. Magnesium bernilai tinggi di mana pengurangan berat menjadi faktor utama, sebatian kalsium memainkan peranan pusat dalam simen dan plester, manakala sebatian barium dipilih untuk kegunaan industri dan perubatan khusus. Dalam pengeluaran sebenar, pemahaman tentang kelakuan logam membantu membimbing proses pemesinan, kestabilan proses, dan kualiti komponen; oleh itu, pembekal seperti Shaoyi Metal Technology menonjolkan pemesinan automotif bersertifikat, kawalan proses, serta sokongan dari bahagian prototaip hingga pengeluaran pukal.
 Jumlah kecil, piawai tinggi. Perkhidmatan prototaip pantas kami membuat pengesahan lebih cepat dan mudah —
Jumlah kecil, piawai tinggi. Perkhidmatan prototaip pantas kami membuat pengesahan lebih cepat dan mudah —
