Quels sont les métaux alcalino-terreux ? Le groupe 2 enfin expliqué
Quels sont les métaux alcalino-terreux ?
Si vous avez cherché quels sont les métaux alcalino-terreux , voici la réponse directe : ce sont les six éléments du Groupe 2 groupe 2 définition des métaux alcalino-terreux constitue le point de départ, mais le nom lui-même révèle également beaucoup sur le comportement de cette famille d’éléments.
Quels sont les métaux alcalino-terreux en une phrase
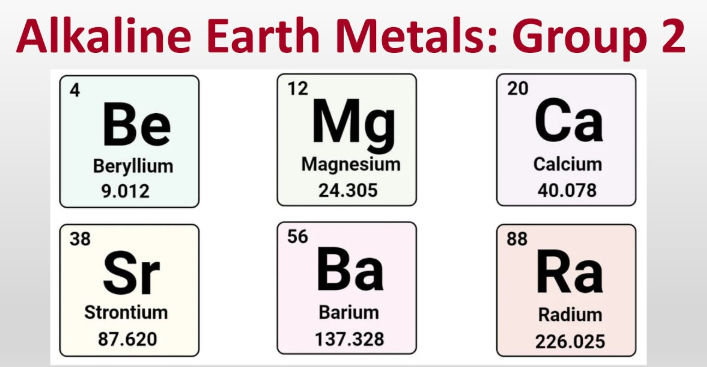
Les métaux alcalino-terreux sont le béryllium, le magnésium, le calcium, le strontium, le baryum et le radium, soit les six éléments métalliques du groupe 2, qui forment généralement des ions +2.
- Béryllium (Be)
- Magnésium (Mg)
- Calcium (Ca)
- Strontium (Sr)
- Baryum (Ba)
- Radium (Ra)
Pourquoi le nom de métaux alcalino-terreux est pertinent
Pour les débutants, la définition des métaux alcalino-terreux devient beaucoup plus facile lorsqu’on décompose l’expression en trois parties.
Alcalin signifie que leurs oxydes et leurs hydroxydes sont basiques, et non acides. Terre est un terme historique. Autrefois, les chimistes l’utilisaient pour désigner des substances minérales stables à la chaleur, qui ne fondent pas facilement ni ne se dissolvent aisément dans l’eau, un point expliqué par Britannica . Les métaux signifie que les éléments eux-mêmes sont métalliques, généralement brillants et aptes à perdre des électrons facilement au cours des réactions.
Cela vous donne la définition fondamentale de métaux alcalino-terreux sans avoir besoin d'une chimie avancée. C'est aussi un court métrage utile description des métaux des terres alcalines : une famille de métaux du groupe 2 avec une chimie commune, une position commune sur le tableau périodique, et un grand rôle dans le monde réel. Le magnésium apparaît dans les alliages et la biologie. Le calcium est important dans les os, les coquilles et les matériaux de construction. Le baryum, le strontium et le radium apparaissent dans des contextes plus spécialisés.
Cet article commence simplement. Une liste propre est facile à mémoriser, mais la famille clique vraiment quand vous voyez où ces éléments se trouvent et pourquoi cet endroit leur donne un comportement si similaire.
Où le groupe 2 siège sur le tableau périodique
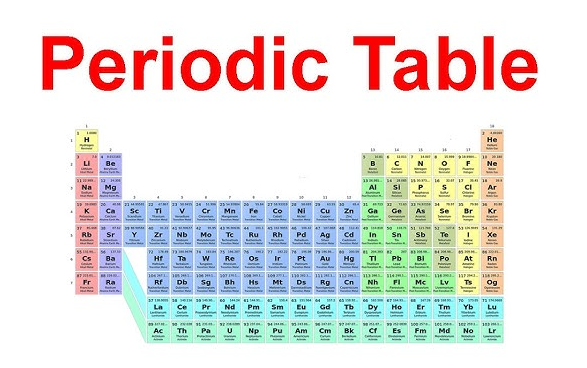
Le nom de famille devient beaucoup plus facile à retenir quand on peut le repérer. Si vous vous demandez où se trouvent les métaux alcalins de la terre dans le tableau périodique , regardez la deuxième colonne de gauche. Cette colonne verticale est groupe 2 du tableau périodique , situé immédiatement à côté des métaux alcalins du groupe 1. Une groupe 2 du tableau périodique la vue montre chaque fois la même ligne droite : béryllium en haut, puis magnésium, calcium, strontium, baryum et radium descendant progressivement à travers les périodes.
Dans un tableau périodique des métaux alcalino-terreux sur ce graphique, ces six éléments appartiennent au bloc s. Leur emplacement commun est significatif, car il reflète une configuration électronique commune. Comme LibreTexts l’explique, les éléments du groupe 2 possèdent une configuration de valence ns 2, ce qui signifie qu’ils possèdent deux électrons sur leur couche externe.
Où se trouvent les métaux alcalino-terreux sur le tableau périodique
Visuellement, le schéma est simple. Le groupe 2 du tableau périodique forme une colonne familiale unique couvrant les périodes 2 à 7. De nombreux diagrammes pédagogiques mettent en évidence les métaux alcalino-terreux dans le tableau périodique dispositions avec la même couleur, car les familles d'éléments se lisent verticalement, et non horizontalement. Les recherches portant sur tableau périodique des métaux alcalino-terreux visent en réalité cette colonne précise.
| Élément | Le symbole | Position du groupe 2 | Ion typique | Composé familier |
|---|---|---|---|---|
| Béryllium | Be | Période 2, sommet du groupe 2 | Be2+ | BeO |
| Magnésium | Mg | Période 3 | Mg2+ | MgO |
| Calcium | Ca | Période 4 | Ca2+ | CaCO 3 |
| Strontium | Sr | Période 5 | Sr2+ | SrCO 3 |
| Baryum | BA | Période 6 | BA 2+ | BaSO 4 |
| Radium | RA | Période 7, en bas du groupe 2 | RA 2+ | RaCl 2 |
Pourquoi les éléments du groupe 2 forment-ils des ions +2
Ces deux électrons externes déterminent la réactivité chimique. Les atomes du groupe 2 ont tendance à perdre ces deux électrons, car cela leur confère une configuration électronique plus stable. Le résultat est un +2 ion , tels que Mg 2+ ou Ca 2+. C’est pourquoi ces métaux forment couramment des composés tels que des oxydes, des chlorures, des carbonates et des sulfates. On remarque immédiatement le schéma dans les formules : MgO, CaCl 2, CaCO 3, BaSO 4.
Comment reconnaître rapidement la famille des métaux alcalino-terreux
Un truc rapide d’identification consiste à rechercher simultanément trois indices : colonne 2 du tableau périodique, éléments métalliques et charge usuelle de +2. Comparés aux métaux alcalins voisins, qui possèdent un électron de valence et forment généralement des ions +1, les éléments du groupe 2 possèdent un électron de valence supplémentaire en couche externe et sont globalement moins réactifs. Néanmoins, ils appartiennent clairement à une même famille. Ce qui est intéressant, c’est que chaque membre exprime ce schéma de manière légèrement différente, notamment du béryllium en haut jusqu’au radium en bas.
Découvrez les six métaux alcalino-terreux
Une liste est utile, mais elle n’est pas très mémorable en soi. Le groupe 2 commence à paraître plus concret lorsque chaque membre possède une identité claire. Certains apparaissent dans les os ou dans l’eau de mer. D’autres colorent les feux d’artifice. L’un d’eux constitue surtout un signe d’alerte historique. Ensemble, ils appartiennent encore à la même famille, mais chacun possède sa propre personnalité.
| Élément | Le symbole | Apparition courante | Propriété distinctive | Pertinence en conditions réelles |
|---|---|---|---|---|
| Béryllium | Be | Présent dans des minéraux tels que le béryl | Très léger et rigide pour un métal | Utilisé dans des applications spécialisées aérospatiales et radiographiques ; la poussière est nocive si inhalée |
| Magnésium | Mg | Présent dans l’eau de mer et dans les minéraux | Faible densité et flamme blanche éclatante lors de la combustion | Important dans les alliages légers, les compléments alimentaires et la biologie |
| Calcium | Ca | Courant dans le calcaire, les os, les coquillages et la craie | Ion du groupe 2 biologiquement familier | Présent dans les squelettes, le ciment, le plâtre et de nombreux minéraux naturels |
| Strontium | Sr | Présent principalement dans la célestine et la strontianite | Les sels produisent une couleur rouge vive dans les flammes | Utilisé dans les feux d'artifice, les fusées éclairantes, les matériaux luminescents et certains produits dentaires |
| Baryum | BA | Généralement associé au baryte | Métal alcalino-terreux dense et lourd | Le sulfate de baryum est utilisé dans le forage et l’imagerie médicale ; les composés solubles de baryum nécessitent une grande prudence |
| Radium | RA | Présent en traces dans les minerais d’uranium | Une forte radioactivité domine son histoire chimique | Principalement d’intérêt historique ou scientifique strictement contrôlé aujourd’hui |
Béryllium et magnésium en tête du groupe 2
Le élément béryllium se situe en haut de la famille et suggère déjà que le groupe 2 n’est pas parfaitement uniforme. Il est couramment associé au minéral béryl, la même famille minérale qui comprend l’émeraude et l’aigue-marine. Le béryllium se distingue par son poids inhabituellement faible et sa rigidité élevée. Cela le rend utile dans des composants haute performance où la faible masse est un critère essentiel. En même temps, le béryllium est un matériau exigeant une grande prudence dans les environnements industriels, car ses poussières fines peuvent être nocives si inhalées. Il est donc à la fois reconnu pour ses performances et pour les précautions requises lors de sa manipulation.
Magnésium paraît beaucoup plus familier. Le symbole chimique du magnésium est le Mg, et il est l’un des métaux les plus connus de ce groupe, car il est présent dans l’eau de mer, dans des minéraux courants et dans les systèmes vivants. C’est un métal très léger, et lorsqu’il brûle, il produit une lumière blanche intense. C’est pourquoi le magnésium est depuis longtemps associé aux fusées éclairantes et aux matériaux à combustion vive. Dans la vie quotidienne, toutefois, la plupart des gens le rencontrent sous des formes plus douces, telles que son rôle dans l’alimentation, ses composés antacides ou encore ses alliages légers utilisés là où la réduction de la masse est essentielle.
Calcium et strontium dans les matériaux courants
Le calcium est le membre du groupe 2 le plus reconnaissable pour de nombreux lecteurs. Il apparaît dans la pierre calcaire, la craie, les coquillages et les os, ce qui relie immédiatement la chimie à la fois à la géologie et à la biologie. Le carbonate de calcium est le composé familier en question. Il permet d’expliquer pourquoi la même famille d’éléments joue un rôle aussi important dans la formation des grottes, les pierres de construction et les squelettes. Le calcium métallique lui-même est réactif, mais les composés du calcium sont omniprésents, ce qui explique pourquoi cet élément semble souvent plus familier qu’exotique.
Le strontium est plus facile à retenir une fois associé à une couleur. Le symbole du strontium est Sr, et strontium il se trouve principalement dans les minéraux céléstine et strontianite. La Royal Society of Chemistry le décrit comme un métal mou et argenté qui brûle dans l’air et réagit avec l’eau. Ses sels sont célèbres pour produire des teintes rouges éclatantes dans les feux d’artifice et les fusées éclairantes. La même source mentionne également ses utilisations dans les matériaux phosphorescents et dans le chlorure de strontium hexahydraté présent dans les dentifrices destinés aux dents sensibles. Cela fait du strontium un excellent exemple d’un élément chimiquement réactif, mais que l’on rencontre le plus souvent sous forme de composés.
Baryum et radium dans des contextes avancés ou spécialisés
Le élément baryum est souvent associé à une sensation de lourdeur. Il est couramment lié au barytine, et l’un de ses composés les plus connus est le sulfate de baryum. Ce composé revêt une importance particulière car il est très peu soluble, ce qui explique pourquoi le baryum peut être utilisé dans des applications pratiques telles que les fluides de forage et l’imagerie médicale, tandis que d’autres composés solubles du baryum sont manipulés avec plus de précaution en raison de leurs propriétés toxiques. Le baryum rappelle aux lecteurs que la forme utile d’un élément du groupe 2 est souvent un composé, et non le métal brillant lui-même.
Radium se trouve au bas de la famille, mais il ne s’intègre pas discrètement. Sur une tableau périodique du radium la vue, Ra marque le point où la radioactivité devient la caractéristique déterminante. Le radium n’existe naturellement que en quantités infimes, généralement associé aux minerais d’uranium. Historiquement, il est devenu célèbre pour ses peintures luminescentes et ses premières expériences médicales. Aujourd’hui, son danger provient de sa radioactivité plutôt que de son comportement métallique ordinaire, aussi est-il manipulé sous des contrôles stricts. En termes simples, le radium appartient toujours au groupe 2, mais il est abordé autant dans une perspective de sécurité nucléaire que de chimie.
Placez ces six éléments côte à côte et la famille cesse de ressembler à une simple liste de noms. La taille, la réactivité, les composés courants, et même la manière dont chaque élément apparaît dans la vie quotidienne évoluent à mesure que l’on descend dans le groupe. Ce changement progressif est précisément ce qui rend le groupe 2 particulièrement utile, car l’ordre allant du béryllium au radium commence à révéler des tendances plutôt que de simples faits anecdotiques.
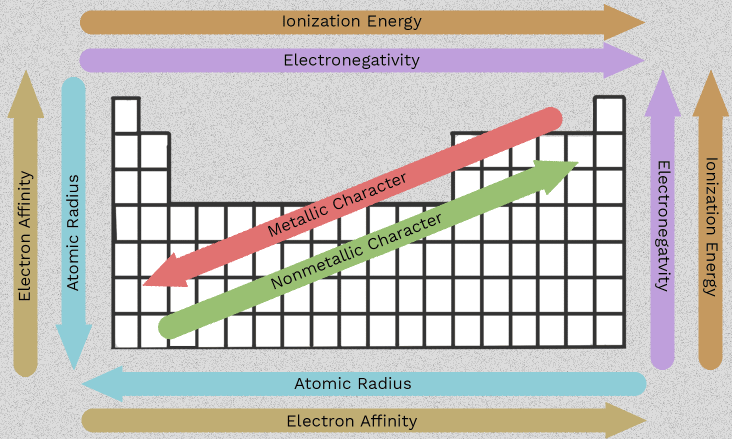
Propriétés des métaux alcalino-terreux et tendances du groupe 2
Ce changement d’ordre, du béryllium au radium, est ce qui rend le groupe 2 utile. Plutôt que de mémoriser six faits isolés, vous pouvez suivre quelques schémas qui se répètent dans toute la colonne. Le plus important propriétés des métaux alcalino-terreux découlent toutes d’une caractéristique commune : chaque atome possède deux électrons externes qu’il a tendance à perdre.
Dès que vous comprenez comment la taille atomique, le blindage électronique et l’énergie d’ionisation évoluent en descendant dans le groupe, la famille devient beaucoup plus facile à prévoir. Ces caractéristiques des métaux alcalino-terreux ne sont pas seulement des faits à retenir pour les examens. Elles expliquent pourquoi certains éléments réagissent plus rapidement, pourquoi certains composés se dissolvent mieux que d’autres, et pourquoi certaines tendances nécessitent une formulation précise plutôt que de simples flèches.
Propriétés communes aux métaux alcalino-terreux
La plupart des éléments du groupe 2 sont des métaux argentés qui forment généralement des cations M 2+ions et forment principalement des composés ioniques. Ils se comportent comme des agents réducteurs parce qu'ils perdent des électrons. Comparés aux métaux du groupe 1, ils sont généralement moins réactifs, mais restent néanmoins suffisamment actifs sur le plan chimique pour former de nombreux oxydes, chlorures, carbonates et sulfates courants.
Un moyen simple d'organiser les propriétés chimiques des métaux alcalino-terreux consiste à distinguer ce qui reste constant de ce qui varie. Ce qui reste constant est l’état d’oxydation habituel +2. Ce qui varie, c’est la facilité avec laquelle chaque élément cède ces deux électrons. C’est là que les tendances commencent à jouer un rôle.
Tendances observées vers le bas du groupe 2 et leur signification
Données recueillies par LibreTexts et explications des tendances provenant de Save My Exams montrent le même schéma général. Le rayon atomique augmente de 112 pm pour Be à 253 pm pour Ba, tandis que l’énergie de première ionisation diminue de 900 à 503 kJ/mol. En termes simples, les électrons externes se trouvent plus loin du noyau et sont protégés par davantage de couches internes, ce qui les rend plus faciles à arracher.
| Tendance | Sens descendant dans le groupe 2 | Raison chimique | Ce que cela signifie en pratique |
|---|---|---|---|
| Rayon atomique | Augmente | Chaque élément possède une couche électronique supplémentaire et une plus forte protection | Les atomes plus volumineux retiennent moins fermement leurs électrons externes |
| Première et deuxième énergie de ionisation | Diminution globale | Les électrons externes sont plus éloignés du noyau, donc l’attraction est plus faible | Formation de M 2+la formation d’ions devient plus facile |
| Réactivité | Augmentation globale | Des énergies de ionisation plus faibles rendent la perte d’électrons plus facile | Les éléments plus lourds réagissent plus vigoureusement avec les acides, l’oxygène et souvent l’eau |
| Point de fusion | Diminue généralement, mais pas de façon régulière | Les ions métalliques plus volumineux affaiblissent la liaison métallique, bien que la structure joue également un rôle | Utilisez le mot « général » ici, car Mg et Ca ne s’inscrivent pas parfaitement dans une tendance linéaire |
| Densité | Irregulier | La masse, la taille atomique et le compactage des métaux évoluent simultanément | Vous ne pouvez pas considérer la densité comme une simple tendance décroissante |
| Solubilité des hydroxydes | Augmente | L’équilibre entre l’énergie réticulaire et l’énergie d’hydratation évolue vers le bas du groupe | Les hydroxydes plus lourds produisent des solutions plus alcalines |
| Solubilité des sulfates | Diminue | L'énergie d'hydratation diminue à mesure que le cation augmente de taille | Des composés tels que BaSO 4deviennent très peu solubles |
La densité et le comportement de fusion sont les deux tendances que les étudiants simplifient souvent excessivement. La densité ne varie pas de façon linéaire, car la masse et le volume changent tous deux, et les atomes métalliques ne s’empilent pas de la même manière dans chaque réseau cristallin. Les points de fusion exigent également une attention particulière. Ils diminuent généralement vers le bas du groupe, car des ions plus volumineux affaiblissent le réseau métallique, mais le magnésium présente un point de fusion inhabituellement bas de 650 °C, tandis que celui du calcium s’élève à 842 °C avant de diminuer à nouveau. Ainsi, l’un des critères les plus fiables des métaux alcalino-terreux est le suivant : la tendance générale est réelle, mais les détails physiques ne sont pas parfaitement réguliers.
La solubilité porte la même mise en garde. Aucune règle unique ne s’applique à tous les sels du groupe 2. Les hydroxydes deviennent plus solubles en descendant dans le groupe, tandis que les sulfates deviennent moins solubles. Si quelqu’un affirme que « la solubilité augmente en descendant dans le groupe 2 », la question essentielle est la suivante : « De quels composés parle-t-on ? »
Pourquoi les métaux alcalino-terreux réagissent-ils de la manière dont ils le font
Donc, les métaux alcalino-terreux sont-ils réactifs ? Oui, et la réponse générale est qu’ils deviennent plus réactifs en descendant dans le groupe. La raison est la même histoire électronique décrite ci-dessus. Des énergies de première et de deuxième ionisation plus faibles signifient que les atomes peuvent perdre deux électrons plus facilement et atteindre l’état courant M 2+ plus rapidement.
Cela influe sur les réactions réelles. En descendant dans le groupe, les réactions avec des acides dilués s’accélèrent, les réactions avec l’oxygène deviennent plus vigoureuses, et les éléments les plus lourds sont plus faciles à oxyder. Selon les notes de Save My Exams, le baryum est suffisamment réactif pour être conservé sous huile, ce qui constitue un signe pratique de l’ampleur de cette tendance à la réactivité.
- Le rayon atomique augmente en descendant du groupe 2.
- L’énergie d’ionisation diminue en descendant du groupe 2.
- La réactivité augmente parce que la perte de deux électrons devient plus facile.
- Les points de fusion et la densité présentent des irrégularités, aussi évitez les règles absolues.
- Les hydroxydes et les sulfates présentent des tendances opposées de solubilité.
Ces particularités rendent la famille prévisible, mais pas parfaitement uniforme. Juste au sommet du groupe, le béryllium commence déjà à enfreindre les règles, et le magnésium ajoute une autre exception courante qui revêt une importance supérieure à ce que beaucoup de débutants ne s’attendent.
Métaux alcalins et métaux alcalino-terreux
Des tendances générales facilitent l’apprentissage du groupe 2, mais la famille cesse d’avoir un sens si chaque membre est considéré comme identique. Le principal signe d’alerte est le béryllium. Le magnésium ajoute une exception pratique plus courante. Et lorsque les gens comparent métaux alcalins et métaux alcalino-terreux , des dénominations similaires peuvent masquer des chimies très différentes.
Pourquoi le béryllium ne se comporte pas comme un métal typique du groupe 2
BYJU'S décrit le béryllium comme l’élément nettement atypique du groupe 2. Sa taille inhabituellement réduite, son énergie de première ionisation élevée et son fort pouvoir polarisant confèrent un comportement moins représentatif de celui de la famille. En langage simple, Be 2+attire fortement les nuages électroniques voisins, de sorte que les composés du béryllium sont souvent plus covalents que les composés plus ioniques formés par les éléments plus lourds du groupe. La même source signale également que le béryllium possède des points de fusion et d’ébullition plus élevés que les autres éléments du groupe et qu’il ne réagit pas avec l’eau comme ses homologues.
Le magnésium n’est pas aussi inhabituel que le béryllium, mais il peut toutefois sembler moins réactif que ce à quoi s’attendent les étudiants. LibreTexts indique que le magnésium très pur réagit seulement faiblement avec l’eau froide, et que la réaction ralentit rapidement, car l’hydroxyde de magnésium, presque insoluble, forme une barrière à la surface. En bas de la famille, le radium est généralement traité séparément, car sa radioactivité domine les discussions relatives à son utilisation pratique et à la sécurité.
Comment les métaux alcalino-terreux se distinguent-ils des métaux alcalins
En termes simples alcalins contre alcalino-terreux , les métaux du groupe 1 perdent un électron externe, tandis que les métaux du groupe 2 en perdent deux. Cette simple différence façonne les propriétés des métaux alcalins et des métaux alcalino-terreux davantage que presque tout autre facteur.
| Caractéristique | Métaux alcalins, groupe 1 | Métaux alcalino-terreux, groupe 2 |
|---|---|---|
| Électrons de valence | 1 | 2 |
| Ion typique | M + | M 2+ |
| Réaction avec l’eau froide | Souvent vive ou même violente, formant un hydroxyde et du dihydrogène | Moins uniforme : le béryllium ne réagit pas avec l’eau, le magnésium réagit modérément, tandis que le calcium, le strontium et le baryum réagissent avec une vigueur croissante |
| Chimie courante de l’oxygène | Peuvent former des oxydes, des peroxydes ou des superoxydes | Forment couramment des monoxydes ; la plupart de ces oxydes donnent des hydroxydes en présence d’eau, mais BeO constitue une exception |
Exceptions importantes que les étudiants omettent souvent
- Tous les métaux du groupe 2 ne réagissent pas avec l’eau de la même manière.
- Les composés du béryllium sont plus covalents que les autres éléments de cette famille.
- Ne pas confondre métaux alcalins et métaux alcalino-terreux comme appartenant au même groupe simplement parce que leurs noms semblent apparentés.
- Le les propriétés des métaux alcalins et des métaux alcalino-terreux s’apprennent mieux sous forme de schémas comportant des exceptions, plutôt que sous forme de slogans rigides.
C’est aussi la meilleure façon de comprendre les propriétés chimiques des métaux alcalins et des métaux alcalino-terreux . Les configurations électroniques vous donnent la règle, mais les substances réelles ajoutent de la richesse. Et cette richesse devient encore plus évidente lorsque l’on examine où se trouvent effectivement les éléments du groupe 2 dans la nature : rarement sous forme de métaux purs, et bien plus fréquemment à l’intérieur de minéraux, de roches, d’eau de mer, d’os et de composés industriels.
Présence des métaux alcalino-terreux dans la nature
Si vous imaginez un métal alcalino-terreux sous la forme d’un échantillon brillant et pur posé sur une roche, la nature fonctionne différemment. Les éléments du groupe 2 sont suffisamment réactifs pour apparaître généralement sous forme d’ions à l’intérieur de minéraux, de sels, de roches, d’eau de mer, d’os et de coquilles, plutôt que sous forme de métaux libres. Que quelqu’un recherche les métaux alcalino-terreux ou le terme plus courant, le schéma naturel reste le même : cette famille préfère fortement les composés.
Ce schéma découle directement des propriétés chimiques des métaux alcalino-terreux ils ont tendance à perdre deux électrons externes et à former des ions M 2+²⁺ stables. Une fois cela réalisé, les ions oxygène, carbonate, sulfate et halogénure les fixent facilement dans des composés solides capables de persister dans les domaines géologique et biologique.
Pourquoi les métaux alcalino-terreux ne se trouvent pas à l’état libre dans la nature
Britannica et ThoughtCo les deux décrivent le groupe 2 comme réactif, ce qui explique pourquoi ces éléments sont rarement trouvés à l’état libre. Dans l’air, beaucoup forment rapidement des couches d’oxydes. Dans les environnements naturels, ils sont encore davantage stabilisés sous forme de carbonates, de sulfates, de silicates, de fluorures ou de chlorures. C’est pourquoi le calcium apparaît dans le calcaire et les coquilles, le magnésium dans les minéraux et l’eau de mer, et le strontium ou le baryum dans les gisements de minerai. Le radium est encore plus rare, ne se trouvant que sous forme de traces dans les minerais d’uranium.
Minéraux et composés courants du groupe 2
| Élément | Source naturelle courante | Composé familier | Pourquoi ce composé est important |
|---|---|---|---|
| Béryllium | Béryl | BeO | La bérylline est une source commerciale de cet élément, tandis que l’oxyde de béryllium est un composé important dans des matériaux spécialisés |
| Magnésium | Magnésite, dolomie, eau de mer | MgCO₃ 3ou Mg(OH)₂ 2 | Montre pourquoi le magnésium est rencontré plus fréquemment dans les minéraux, l’eau de mer et la médecine qu’à l’état de métal pur |
| Calcium | Calcaire, craie, marbre, gypse, os, coquilles | CaCO 3 | Relie la géologie, les matériaux de construction et les squelettes dans un composé très courant |
| Strontium | Célestine, strontianite | SrSO 4ou SrCO 3 | Ces minéraux constituent les principales sources naturelles de composés de strontium |
| Baryum | Barytine, withérite | BaSO 4 | La barytine est le minerai clé, et le sulfate de baryum est l’un des composés de baryum les plus connus |
| Radium | Traces dans la pechblende et d’autres minerais d’uranium | RaCl 2 | Sa rareté et sa radioactivité rendent les composés de radium historiquement importants, mais peu courants |
EBSCO note que le calcium et le magnésium sont également présents dans l’eau de mer à hauteur d’environ 0,4 g/L et 1,3 g/L, respectivement. Cela aide à expliquer pourquoi ce groupe des métaux alcalino-terreux famille est liée non seulement aux minerais, mais aussi à l’eau dure, aux systèmes marins et aux tissus vivants.
Comment ces métaux sont extraits de leurs composés
Comme les métaux du groupe 2 sont généralement piégés dans des composés, leur extraction commence à partir de minerais, de saumures ou de gisements minéraux. Une idée industrielle courante est simple : transformer d’abord la matière en un oxyde ou un halogénure plus facile à manipuler, puis utiliser l’électrolyse ou une réduction chimique pour libérer le métal. Britannica décrit l’isolement précoce du magnésium, du calcium, du strontium et du baryum par électrolyse, tandis qu’EBSCO indique que la production moderne repose encore fréquemment sur l’électrolyse de chlorures fondus, la réduction des oxydes ou des voies apparentées, selon l’élément concerné. Le béryllium constitue un rappel utile du fait que cette famille n’est pas parfaitement uniforme, puisqu’il peut être produit par réduction du fluorure de béryllium.
Ainsi, dans la vie quotidienne, les gens rencontrent généralement le groupe 2 sous forme de calcaire, de plâtre, de magnésium extrait de l’eau de mer, de barytine ou de calcium biologique, et non sous forme d’échantillons de métal brut. Ce détail est important, car l’importance réelle de ces éléments dépend bien davantage de leurs composés et de leurs formes que du métal pur lui-même.
Exemples de métaux alcalino-terreux dans la vie quotidienne
Le groupe 2 devient beaucoup plus mémorable lorsqu’on associe chaque élément à quelque chose de concret : os, antiacides, plâtre, feux d’artifice, fluides de forage et anciens cadrans luminescents sont tous des exemples utiles exemples de métaux alcalino-terreux . Si vous vous êtes déjà demandé(e) le magnésium est-il un métal ou un non-métal ou ca est-il un métal , les deux réponses sont simples : le magnésium et le calcium sont des métaux. Dans la vie courante, toutefois, les gens rencontrent généralement ces substances sous forme de composés, et non sous forme d’échantillons de métal pur.
Utilisations courantes des composés de magnésium et de calcium
- Magnésium : Le magnésium est l’un des éléments les plus importants sur le plan biologique éléments alcalino-terreux . Le Fiche d'information sur le magnésium des NIH note qu’il est un cofacteur de plus de 300 systèmes enzymatiques et qu’il soutient la fonction musculaire et nerveuse, la production d’énergie et la structure osseuse. Des composés de magnésium apparaissent également dans certains antiacides et laxatifs, tandis que le magnésium métallique est valorisé dans les alliages légers où la réduction de la masse est essentielle.
- Calcium les composés du calcium dominent la vie quotidienne. Le calcium contribue à la structure des os et des dents, et des composés tels que le carbonate de calcium et le sulfate de calcium sont au cœur de la pierre calcaire, du ciment, du plâtre et des plaques de plâtre. Cela fait du calcium l’un des liens les plus évidents entre la chimie, la biologie et la construction.
Applications spécialisées du strontium et du baryum
- Strontium les sels de strontium sont surtout connus pour produire des teintes rouges profondes dans les feux d’artifice et les fusées de détresse. Même les lecteurs qui ne se souviennent pas intégralement de la liste complète du groupe 2 retiennent souvent le strontium dès que celui-ci est associé à une couleur.
- Baryum les composés du baryum revêtent de l’importance dans l’industrie et la médecine. Le Profil du baryum de la NLM décrit les principales utilisations dans les boues de forage, les peintures, les plastiques, les briques et le verre. Il mentionne également une importante application médicale contrastée : le sulfate de baryum, très peu soluble, est utilisé comme produit radiopaque lors de certains examens radiographiques, car il n’est généralement pas absorbé par l’organisme.
- Radium : Le radium relève principalement d’un contexte historique ou scientifique strictement réglementé. Page NRC sur le radium décrit ses anciennes utilisations dans les peintures luminescentes et dans les premiers traitements du cancer. La plupart de ces utilisations ont été remplacées, bien que certaines applications réglementées subsistent encore, notamment dans certains domaines de la radiographie industrielle.
Pourquoi la forme et le type de composé comptent dans l’usage réel
Dans le groupe 2, la forme utilisée par les personnes est souvent le composé, et non le métal pur.
Cette seule idée dissipe beaucoup de confusion. Le magnésium présent dans les aliments ou les médicaments n’est pas la même chose que le ruban de magnésium en combustion. Le calcium présent dans les os n’est pas identique au métal calcium réactif. Le baryum constitue l’exemple le plus frappant de l’importance de la forme : le sulfate de baryum, insoluble, peut être utile en imagerie, tandis que les composés de baryum plus solubles exigent une prudence bien plus grande. Le radium pousse encore plus loin cette distinction, car ce n’est pas seulement sa position parmi les métaux, mais surtout sa radioactivité, qui détermine la façon dont il doit être manipulé.
La valeur du groupe 2 n’est donc pas du tout abstraite. Ces éléments contribuent à expliquer comment une même famille peut jouer un rôle essentiel en nutrition, en science des matériaux, en médecine, en traitement industriel et dans les règles de sécurité. Une courte liste d’applications concrètes suffit souvent pour que le schéma général s’ancre durablement.
Points clés sur les éléments du groupe 2
À ce stade, le groupe des métaux alcalino-terreux devrait vous sembler moins une liste à mémoriser qu’un motif que vous pouvez lire directement dans la colonne du groupe 2 du tableau périodique si quelqu’un pose encore la question, quels sont les métaux alcalino-terreux , la réponse courte reste simple : béryllium, magnésium, calcium, strontium, baryum et radium. Une définition plus complète des métaux alcalino-terreux est encore plus utile : six éléments métalliques du groupe 2 qui perdent généralement deux électrons externes et forment des ions M 2+.
Points clés concernant les métaux alcalino-terreux
- L’emplacement compte : ces six éléments du groupe 2 se trouvent dans la deuxième colonne en partant de la gauche, dans la section « groupe 2 » du bloc s.
- Les membres de la famille sont fixes : Be, Mg, Ca, Sr, Ba et Ra constituent l'ensemble complet.
- Une chimie partagée explique cette ressemblance familiale : leur configuration ns 2du niveau de valence conduit généralement à la formation d’ions +2, un point fondamental résumé par LibreTexts.
- Les principales tendances observées vers le bas du groupe sont prévisibles : le rayon atomique augmente, l’énergie de première ionisation diminue globalement et la réactivité augmente généralement en descendant dans le groupe.
- Les exceptions sont importantes : le béryllium se comporte de façon plus covalente que les autres éléments, le magnésium peut paraître moins réactif en raison de sa couche superficielle, et le radium est principalement étudié sous l’angle de sa radioactivité.
- Dans la vie réelle, il s’agit généralement de composés, et non de métaux purs : les gens rencontrent bien plus souvent le carbonate de calcium, l’oxyde de magnésium et le sulfate de baryum que les éléments Ca, Mg ou Ba sous forme élémentaire.
Le tableau périodique des métaux alcalino-terreux la colonne est la plus facile à retenir comme un ensemble de six métaux liés par une seule règle : ils forment généralement des ions 2+, mais chaque membre exprime cette règle de manière légèrement différente.
De la chimie du groupe 2 aux pièces métalliques conçues sur mesure
Cette chimie s’étend bien au-delà des manuels scolaires. LibreTexts signale que le magnésium élémentaire est produit à grande échelle et utilisé dans des alliages légers pour les structures d’avions et les pièces de moteurs automobiles. Un guide plus complet sur les alliages explique pourquoi cela importe : les ingénieurs ajustent la composition et les procédés de fabrication afin d’optimiser, dans des composants réels, le poids, la résistance mécanique, la résistance à la corrosion et l’usinabilité.
Pour les lecteurs passant de la colonne du groupe 2 du tableau périodique vision théorique à la fabrication, Shaoyi Metal Technology offre un exemple pratique de ce lien. Ses pages consacrées aux matériaux automobiles et à l'usinage décrivent la production de pièces métalliques, de la phase de prototypage à la production de masse, où le comportement des matériaux et le contrôle des procédés doivent fonctionner de concert. Cela fait du tableau périodique des métaux alcalino-terreux bien plus qu’un simple tableau pédagogique. Il constitue également une composante essentielle de la logique sous-tendant le choix des métaux et des alliages destinés à des pièces techniques devant être légères, fiables et facilement manufacturables.
FAQ sur les métaux alcalino-terreux
1. Quels sont les six métaux alcalino-terreux ?
Les six métaux alcalino-terreux sont le béryllium, le magnésium, le calcium, le strontium, le baryum et le radium. Ils occupent le groupe 2 du tableau périodique et sont regroupés ensemble car ils perdent généralement deux électrons externes, ce qui conduit à un schéma ionique commun 2+ dans de nombreux composés.
2. En quoi les métaux alcalino-terreux se distinguent-ils des métaux alcalins ?
Les métaux alcalins appartiennent au groupe 1 et forment généralement des ions 1+ car ils possèdent un seul électron de valence. Les métaux alcalino-terreux appartiennent au groupe 2, forment habituellement des ions 2+ et sont globalement moins réactifs. Cet électron de valence supplémentaire modifie la force de leurs liaisons, leur réactivité avec l’eau ainsi que la nature des sels et des oxydes qu’ils forment couramment.
3. Pourquoi les métaux alcalino-terreux ne sont-ils pas trouvés à l’état libre dans la nature ?
Ces métaux sont suffisamment réactifs pour ne pas rester longtemps sous forme élémentaire pure dans les milieux naturels. Au lieu de cela, ils se combinent avec des ions oxygène, carbonate, sulfate, chlorure ou silicate, intégrant ainsi des minéraux, des roches, l’eau de mer, les coquillages et les os. C’est pourquoi les personnes rencontrent généralement les éléments du groupe 2 sous forme de composés plutôt que sous forme de métal brut.
4. Tous les métaux alcalino-terreux réagissent-ils avec l’eau ?
Non, et il s'agit l'une des exceptions les plus utiles à retenir. Le béryllium est largement résistant à l'eau, le magnésium réagit lentement avec l'eau froide en raison d'une couche superficielle qui limite la réaction, tandis que le calcium, le strontium et le baryum réagissent plus facilement. En général, la réactivité avec l'eau augmente en descendant dans le groupe 2.
5. Pourquoi les métaux alcalino-terreux sont-ils importants dans l'industrie et la fabrication ?
Leur importance découle à la fois de leurs composés et de leur rôle dans le choix des alliages. Le magnésium est précieux là où la réduction du poids est essentielle, les composés de calcium sont au cœur de la fabrication du ciment et du plâtre, et les composés de baryum sont sélectionnés pour des applications industrielles et médicales spécialisées. Dans la production réelle, la compréhension du comportement des métaux permet de guider l'usinage, la stabilité des procédés et la qualité des pièces, ce qui explique pourquoi des fournisseurs tels que Shaoyi Metal Technology mettent en avant un usinage automobile certifié, un contrôle des procédés et un accompagnement allant de la fabrication de pièces prototypes à la production de masse.
 Petits tirages, hauts standards. Notre service de prototypage rapide rend la validation plus rapide et facile —
Petits tirages, hauts standards. Notre service de prototypage rapide rend la validation plus rapide et facile —
