ما هي المعادن الموجودة في الجدول الدوري؟ العدد الذي تغفله معظم الصفحات
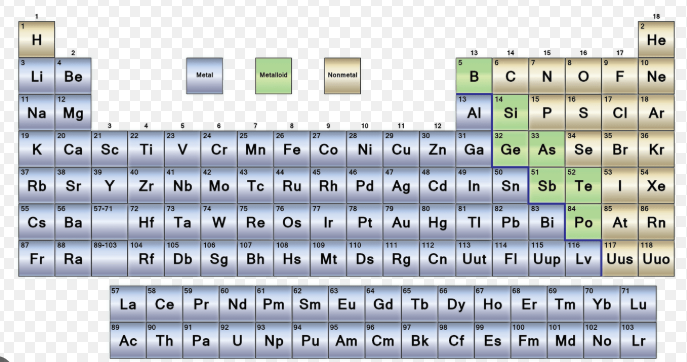
ما هي المعادن في الجدول الدوري للعناصر؟
إذا بحثتَ عن ما هي المعادن في الجدول الدوري للعناصر، فإن الإجابة المختصرة أسهل مما تبدو عليه في البداية. فالمعادن هي العناصر التي تتصرف عادةً بالطريقة المعدنية المألوفة، مثل توصيل الكهرباء، وانعكاس الضوء، والانحناء دون أن تنكسر، وفقدان الإلكترونات أثناء التفاعلات.
الإجابة المباشرة على سؤال: ما هي المعادن في الجدول الدوري؟
المعادن هي العناصر الموجودة في الجدول الدوري التي تظهر عمومًا السلوك المعدني. ومعظمها موصل جيد للحرارة والكهرباء، ولها غالبًا بريقٌ معدني، وهي قابلة للطرق والسحب عادةً، وتميل إلى تكوين أيونات موجبة من خلال فقدان الإلكترونات. ومعظم العناصر المعروفة هي معادن، رغم أن العدد الإجمالي الدقيق قد يختلف قليلًا اعتمادًا على كيفية تصنيف العناصر الحدّية.
وببساطة شديدة، فإن القرّاء الذين يسألون ما هي العناصر المعدنية في الجدول الدوري تتساءل عن المجموعة الكبيرة التي تشمل أمثلة مألوفة مثل الصوديوم، والألومنيوم، والحديد، والنحاس، والفضة، والذهب. وفي الكيمياء الأساسية، يُقدَّم الجدول عادةً على أنه ثلاث فئات واسعة: الفلزات، واللافلزات، والشبه فلزات.
لماذا تُصنَّف أغلب العناصر على أنها فلزات؟
تندرج أغلب العناصر ضمن فئة الفلزات بسبب سلوك إلكتروناتها الخارجية. فالفلزات عادةً ما تفقد إلكتروناتها بسهولة أكبر من اللافلزات، وهو ما يفسِّر سبب تشكُّلها لأيونات موجبة ولماذا تتميَّز العديد منها بموصلية جيدة للحرارة والكهرباء. بريتانيكا ويشير إلى أن نحو ثلاثة أرباع العناصر الكيميائية المعروفة هي فلزات، و ليبرتستس يصف الفلزات بأنها عناصر تشكِّل أيونات موجبة عادةً عن طريق فقدان إلكترونات.
- أغلب العناصر في الجدول دوريَّة هي فلزات.
- ومن السمات الرئيسية لها: الموصلية، واللمعان، والقابليَّة للطرق، والقابليَّة للسحب.
- عادةً ما تفقد الفلزات إلكتروناتها أثناء التفاعلات الكيميائية.
- ويصبح نمط الفلزات واللافلزات في الجدول الدوري أسهل في القراءة عندما تنتبه أيضًا إلى مجموعة الحد الفاصلة وهي الشبه فلزات.
- عدد المعادن الدقيق لا يُقدَّم دائمًا بنفس الطريقة في كل جدول.
وتلك التفصيلة الأخيرة تكتسب أهمية أكبر مما يبدو، لأن التصنيف يبدأ من الخصائص، لكن ترتيب الجدول الدوري يُظهر المواقع التي توجد فيها عادةً العناصر المعدنية وغير المعدنية والشبه معدنية.
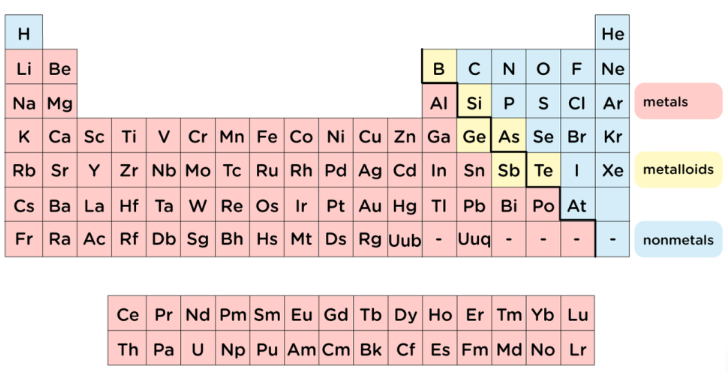
أين تقع العناصر المعدنية في الجدول الدوري؟
إن إلقاء نظرة سريعة على جدول ملوَّن يكشف النمط الأساسي. فإذا كنت تسأل عن مكان وقوع العناصر المعدنية في الجدول الدوري، فانظر إلى الجانب الأيسر والمركز الواسع من الجدول. يقع الصوديوم في أقصى اليسار ، بينما يملأ الحديد الجزء الأوسط، وتُظهر معادن مثل الألومنيوم والذهب أن العناصر المعدنية تمتد عبر جزء كبير من الجدول. بل حتى الصفين اللذين يُفصلان عادةً أسفل الجسم الرئيسي للجدول — وهما سلسلتا اللانثانيدات والأكتينيدات — هما أيضًا عناصر معدنية.
أين تقع العناصر المعدنية في الجدول الدوري
يمكن للطلاب الذين يسألون عن مكان وجود المعادن في الجدول الدوري استخدام الخط المتعرج أو الخط على شكل سلَّم كدليلٍ إرشادي. فالعناصر الواقعة على يسار هذا الخط تكون عادةً معادنًا، بينما العناصر الواقعة على يمينه تكون في الغالب غير فلزية. أما العناصر الواقعة على طول الحد الفاصل فهي العناصر شبه الفلزية. ويُلخِّص ترتيب الجدول ما يلي: ثووقتو يضع معظم المعادن على الجانب الأيسر من الجدول الدوري، بينما ChemistryTalk يصف العناصر غير الفلزية بأنها تتجمع على الجانب الأيمن، والعناصر شبه الفلزية على طول الحد المتعرج.
إذن، أين توجد المعادن فعليًّا في الجدول الدوري؟ توجد في الغالب على يسار خط السلَّم وفي وسط الجدول. وهذا يجيب أيضًا عن سؤال: أين تقع المعادن في الجدول الدوري وفقًا لمعظم الكتب المدرسية؟ ويُعدُّ الهيدروجين استثناءً مشهورًا؛ فهو يظهر في الزاوية العلوية اليسرى، لكنه عنصر غير فلزي.
| منطقة الجدول | التصنيف النموذجي | أمثلة |
|---|---|---|
| الجانب الأيسر والمركز | معظمها معادن | الصوديوم، الألومنيوم، الحديد، الذهب |
| الحد الزِّيغزاغي | معظمها عناصر شبه معدنية | السيليكون، الزرنيخ، التيلوريوم |
| الزاوية العُليا اليمنى | معظمها عناصر غير معدنية | الأكسجين، النيتروجين، الكلور |
يجعل الجدول الدوري الملوَّن بشكل بسيط تذكُّر هذه النمط أسهل بكثير عند إلقائها نظرة سريعة.
كيف يتغير الطابع المعدني عبر الدورات والمجموعات
الموقع ليس عشوائيًّا؛ بل يعكس سلوك الإلكترونات. ليبرتستس ويوضّح أن الطابع المعدني يزداد عمومًا كلما تحركت نحو الأسفل في المجموعة وأتجهت نحو اليسار عبر الدورة. فعند التحرك لأسفل في المجموعة، تزداد أحجام الذرات وتنخفض طاقة التأين، ما يجعل إزالة الإلكترونات الخارجية أسهل. أما عند التحرك عبر الدورة من اليسار إلى اليمين، فإن الذرات تحتفظ بالإلكترونات بإحكام أكبر، وبالتالي يقل السلوك المعدني.
يساعد هذا الاتجاه في تفسير سبب كون الصوديوم أكثر خصائصًا معدنيةً مقارنةً بالعناصر الواقعة أبعد إلى اليمين في الصف نفسه، ولماذا تحتوي الزاوية السفلى اليسرى على أكثر المعادن تفاعلًا. فالحديد والألومنيوم والذهب كلها معادن، لكن مواقعها تشير إلى أن ليس جميع المعادن تتصرف بنفس الطريقة. والخريطة واضحة. أما العدّ، فهو يصبح أكثر تعقيدًا، لأن الحالات الحدّية لا تنطبق على جميع الجداول بنفس الطريقة بالضبط.
الجدول الدوري: المعادن، اللافلزات، والمعدنيات
إن هذا النمط المتركّز على الجانب الأيسر والمركزي يجعل من السهل تمييز المعادن، لكن عدها أقل انتظامًا مما توحي به العديد من الصفحات. إن الجمعية الملكية تشير إلى أن أكثر من ثلثي العناصر هي معادن في الظروف المحيطة العادية. ومع ذلك، فإن المصادر المختلفة لا تقدّم دائمًا نفس العدد الدقيق، لأن الإجابة تعتمد على كيفية تصنيف العناصر الحدّية في جدول العناصر: المعادن، اللافلزات، والمعدنيات.
لماذا تختلف المصادر في تحديد عدد المعادن
عادةً ما ينشأ الخلاف من قواعد التصنيف، وليس من العد الخاطئ. ويُشير استعراض الجمعية الملكية نفسه إلى تفصيلٍ مهم: إن الجدول الدوري يسرد العناصر، لكن التسميات مثل «فلز» و«لا فلز» تصف الطريقة التي تتصرف بها تلك العناصر في حالتها العنصرية تحت الظروف العادية. أما بالقرب من الخط الدرجّي، فإن هذا السلوك ليس دائمًا مقسومًا بوضوح. ويبرز الاستعراض أيضًا أن أجزاء من الكتلة-بِي (p-block)، لا سيما حول المجموعتين ١٤ و١٥، قد تمتد عبر الحد الفاصل بين الفلزات ولا فلزات. لذا، وعلى الرغم من أن رسمة صفية للجدول الدوري تُظهر الفلزات ولا فلزات والمعادن شبه الفلزية مفيدة، فإنها تبسّط واقعًا أكثر تعقيدًا.
إذا قدّمت صفحة ما مجموعًا دقيقًا واحدًا لعدد الفلزات دون ذكر القواعد التي اعتمدت عليها، فقد يكون التنظيم يتفوّق على الدقة.
كيف تؤثّر قواعد التصنيف في المجموع الكلي
يبدأ المجموع المحافظ بالعائلات الواضحة الفلزية. أما المجموع الأوسع فقد يشمل أيضًا عناصر الكتلة-بِي (p-block) ذات الطابع الفلزي، مع التعامل مع العناصر المجاورة للخط الدرجّي بحذرٍ أكبر. IUPAC يحافظ على الجدول الدوري المحدَّث ويُشير إلى أن حتى الأسئلة البنيوية مثل وضع العنصر في المجموعة 3 كانت محل جدل. وهذا الجدل لا يمحو الصورة العامة، لكنه يذكِّر القارئ بأن التصنيف العلمي يشمل كلًّا من الاصطلاح والمشاهدة. وفي الواقع، فإن أكبر مشكلة تتعلق بالعد عادةً ما تكون في المنطقة الحدودية، حيث يمكن أن يختلف التصنيف كعنصر معدني أو غير معدني أو شبه معدن من مخططٍ إلى آخر.
| الفئة | المعالجة النموذجية | لماذا يهم ذلك؟ |
|---|---|---|
| عائلات معدنية واضحة | تُحتسب دائمًا تقريبًا كعناصر معدنية | تشمل الكتل المعدنية الرئيسية ولا تثير خلافًا يُذكر |
| العناصر المعدنية في الكتلة p | تُحتسب عادةً كعناصر معدنية | لا تزال معدنية، لكنها أقرب إلى الحد الفاصل (الخط المتدرج) |
| المنطقة الحدودية | قد تُصنَّف كعناصر شبه معدنية أو عناصر وسيطة | هذا هو المكان الذي تؤدي فيه مقارنات العناصر شبه المعدنية والعناصر المعدنية والعناصر غير المعدنية إلى نتائج مختلفة. |
وبالتالي، فإن الإجابة المفيدة ليست مجرد عددٍ. بل هي رؤيةٌ مُفصَّلةٌ حسب العائلة تُبيِّن أي المجموعات تُدرَج دائمًا ضمن التصنيف، وأي المجموعات تقع قريبةً جدًّا من الحد الفاصل ما يُسبب الالتباس.
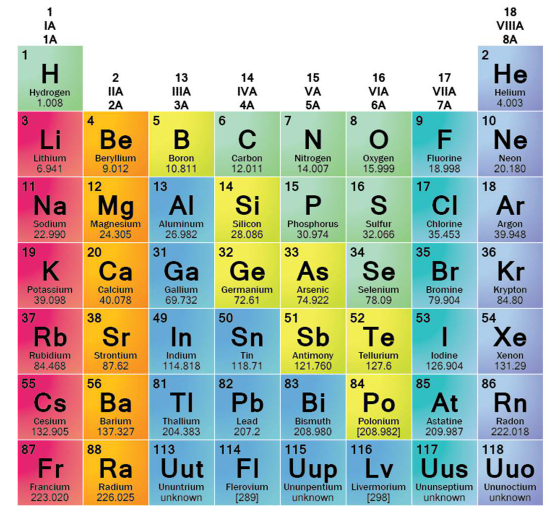
عائلات الجدول الدوري للعناصر
إن الرؤية المُفصَّلة حسب العائلة تجعل الجانب المعدني من الجدول أسهل بكثير في الفهم. ففي الكيمياء، تضم عائلة العناصر في الجدول الدوري عناصر تشترك في تركيب إلكتروناتها الخارجية المماثل، وبالتالي في سلوكها المماثل. ولهذا السبب يكون تصنيف العناصر كمعادن أكثر فائدةً من الخريطة البسيطة التي تقسم الجدول إلى جانب أيسر وجانب أيمن. ويقدِّم لمحة سريعة من موقع «ثوتكو» (ThoughtCo)، جنبًا إلى جنب مع تصنيف المعادن الذي تستخدمه لوس ألاموس ، للقراء طريقة عملية لتصنيف العائلات المعدنية الرئيسية.
العائلات المعدنية في الجدول الدوري
الست عائلات التي يحتاجها معظم القراء هي: الفلزات القلوية، والفلزات القلوية الترابية، والفلزات الانتقالية، والفلزات ما بعد الانتقالية، واللانثانيدات، والأكتينيدات. وإذا كنت قد رأيت أسماء مجموعات مختلفة في الجدول الدوري، فهذا أمرٌ طبيعي. ففي الجداول الحديثة تُرقَّم الأعمدة من ١ إلى ١٨، لكن تسميات العائلات تركز على الخصائص الكيميائية المشتركة، وبعض العائلات تمتد عبر أكثر من عمود واحد أو حتى عبر الصفوف المنفصلة الواقعة أسفل الجدول الرئيسي.
| عائلة الفلزات | مكان ظهورها | الخصائص التي يجب تذكُّرها |
|---|---|---|
| الفلزات القلوية | المجموعة ١، ما عدا الهيدروجين | إلكترون تكافؤ واحد، لينة، لامعة، شديدة التفاعل، وتشكِّل عادةً أيونات ذات شحنة +١ |
| الفلزات القلوية الترابية | المجموعة 2 | إلكترونان تكافؤيان، أصلب وكثافة أعلى من الفلزات القلوية، وتشكِّل عادةً أيونات ذات شحنة +٢ |
| الفلزات الانتقالية | المجموعات من ٣ إلى ١٢، الكتلة المركزية (d-block) | صلبة وكثيفة وموصلة جيدًا، غالبًا ما تمتلك نقاط انصهار مرتفعة، ولها عدة حالات أكسدة |
| الفلزات بعد الانتقالية | كتلة p، تقع على يمين كتلة العناصر الانتقالية | فلزات أكثر ليونة وتوصيلها للتيار الكهربائي أقل من الفلزات الانتقالية |
| اللانثانيدات | العناصر من ٥٧ إلى ٧١، الصف الأول المنفصل | خصائص كيميائية متشابهة جدًّا، وتنتمي إلى كتلة f |
| الأكتينيدات | العناصر من ٨٩ إلى ١٠٣، الصف الثاني المنفصل | الفلزات من الكتلة-f، وكلها مشعة |
ما الذي يميز كل مجموعة فلزية؟
ابدأ من أقصى اليسار. تُعد الفلزات القلوية في الجدول الدوري أسهل المجموعات تحديدًا لأنها تحتوي على إلكترون تكافؤ واحد وتتفاعل بعنفٍ شديد، لا سيما مع الماء. أما عناصر المجموعة الثانية فهي تتفاعل أيضًا، لكن وجود إلكترونين خارجيين يجعلها أقل تفاعليةً وعمومًا أكثر صلابةً من عناصر المجموعة الأولى. وفي المنتصف، يشمل قسم الفلزات الانتقالية في الجدول الدوري الكتلة المركزية الواسعة، والمعروفة بأنها تتكون من مواد صلبة معدنية صلبة، ولها توصيل كهربائي جيد ومدى واسع من حالات الأكسدة.
انقله قليلاً إلى اليمين أكثر، فيصبح النمط أقل وضوحًا. وتظل المعادن ما بعد الانتقال معدنية، لكنها عادةً ما تكون ألين وأقل توصيلًا للكهرباء مقارنةً بالمعادن الانتقالية. أما الصفّان اللذان رُسِما تحت الجدول، فيضيفان طبقةً إضافيةً من الدقة والتفصيل. فعناصر اللانثانيدات تتشارك في كيمياءٍ متقاربة جدًّا، بينما تتميَّز عناصر الأكتينيدات بالإشعاعية. وبعض المراجع تصف كلا الصفَّين حتىًّ بأنهما معادن انتقالية خاصة، مما يوضح سبب فائدة أسماء المجموعات في الجدول الدوري، لكنها لا يمكن أن تحلَّ محل السلوك الكيميائي الفعلي.
- المجموعة ١ تعني أن العناصر لينة وشديدة التفاعل.
- المجموعة ٢ تعني أن العناصر تفاعلية، لكنها عادةً ما تكون أصلب من عناصر المجموعة ١.
- المجموعات من ٣ إلى ١٢ تعني الكتلة المركزية التي تضم العديد من الفلزات الكلاسيكية.
- ما بعد الانتقال يعني الفلزات الألْيْن الواقعة قرب المنطقة المتدرجة (المنطقة على شكل سلم).
- اللانثانيدات والأكتينيدات تعني الصفَّين اللذين يشكِّلان كتلة f ويوضعان تحت الجسم الرئيسي للجدول.
تُساعد هذه التسميات العائلية في تنظيم الجدول بشكل أفضل، لكن الاختبار الأعمق لعنصر معدني لا يكمن في اسم عائلته وحده. فالموصلية، واللمعان، والقابلية للطرق، وفقدان الإلكترونات تفسّر سبب انتماء جميع هذه المجموعات إلى الجانب المعدني في الجدول الدوري من الأساس.
ما هي خصائص المعادن؟
تجعل التسميات العائلية جدول الدوريات أسهل في المسح البصري، لكن الكيميائيين يعرّفون المعدن من خلال سلوكه وليس من خلال اسمه وحده. وعندما يسأل الطلاب: «ما هي خصائص المعادن؟»، فإن الإجابة تبدأ بنمطٍ من الخصائص الفيزيائية والكيميائية المشتركة. وفي ليبرتستس وصف الروابط المعدنية، تنجذب ذرات المعدن إلى بركة من الإلكترونات المتحركة غير المحلية. وهذه النموذج البسيط يساعد في تفسير الخصائص المعدنية للمعادن ولماذا تشترك العديد من العائلات المعدنية المختلفة في مجموعةٍ مميَّزةٍ من السلوكيات.
الخصائص المشتركة لمعظم المعادن
إذا قارنتَ خصائص المعادن باللافلزات، فإن المعادن تبرز عادةً بعدة طرق واضحة.
- التوصيل الكهربائي: تتيح الإلكترونات المتحركة للمعادن توصيل التيار الكهربائي بكفاءة عالية. وسلك النحاس هو المثال الكلاسيكي على ذلك.
- القدرة على导الحرارية: وتلك الإلكترونات نفسها تساعد في نقل الحرارة، ولذلك تُستخدم المعادن مثل النحاس والألومنيوم في التطبيقات التي تتطلب انتقالاً فعالاً للحرارة.
- اللمعان: ويوضح موقع LibreTexts أن إلكترونات المعادن قادرة على امتصاص الطاقة ثم إعادة إصدار الضوء، مما يمنحها سطحاً لامعاً. ويظهر هذا بوضوح في الذهب والفضة والنحاس.
- القابِلِيَّة للطرق: يمكن ضرب المعادن أو دحرجتها لتشكيل صفائح رقيقة بدلاً من أن تنكسر أو تتطاير. ومن الأمثلة الواضحة على ذلك رقائق الألومنيوم وأوراق الذهب الرقيقة.
- المطيلية: يمكن سحب المعادن إلى أسلاك. والنحاس مجددًا مثالٌ مألوفٌ على ذلك.
- تكوين الأيونات الموجبة: تفقد العديد من المعادن إلكتروناتها أثناء التفاعلات الكيميائية. فعلى سبيل المثال، يشكّل الصوديوم أيون Na+، والمغنيسيوم أيون Mg2+، والألومنيوم أيون Al3+.
| الممتلكات | عنصر نموذجي | ما الذي يوضحه |
|---|---|---|
| الموصلية الكهربائية | النحاس | مفيد في التوصيلات الكهربائية والدوائر |
| التوصيل الحراري | ألمنيوم | ينقل الحرارة بكفاءة عالية |
| اللمعان | فضي | سطح عاكس ولامع |
| قابلية التشكيل | ذهب | يمكن تشكيله إلى صفائح رقيقة جدًا |
| المرونة | النحاس | يمكن سحبه إلى أسلاك طويلة |
أمثلة تُظهر أن المعادن ليست متطابقة جميعها
هذه الصفات تمثّل اتجاهات قوية، وليست قائمة تحققٍ مثالية. وتلاحظ منصة LibreTexts أن الزئبق يكون سائلًا عند درجة حرارة الغرفة، على الرغم من أن المعادن تكون عادةً في الحالة الصلبة. وتشير نفس المصدر إلى أن الصوديوم والبوتاسيوم طريان بدرجة كافية لتقطيعهما بالسكين، ما يجعلهما مختلفين تمامًا عن معادن صلبة مثل الحديد. كما تتفاوت درجة التوصيلية أيضًا؛ فالفضة والنحاس من أقوى الموصلات، بينما تؤدي بعض المعادن أداءً أقل إثارةً للإعجاب في هذا المجال. وكذلك تتفاوت درجة النشاط الكيميائي بنفس القدر؛ فالمعدن الذهبي يحتفظ بمظهره أفضل من كثير من المعادن الأخرى لأنه يقاوم التآكل بكفاءة أعلى بكثير مقارنةً بمعادن مثل الحديد.
لهذا السبب، يُعامل خصائص المعادن على أنها مجموعة من المؤشرات. فاللمعان وحده لا يكفي، والتوصيلية وحدها لا تكفي أيضًا. ويُمعن الكيميائيون النظر في النمط الكلي: كيف يوصل العنصر الكهرباء، وكيف ينثني، وكيف يتصرّف تجاه فقدان الإلكترونات في التفاعلات. ومن هذه الزاوية، يصبح السؤال العملي التالي أسهل بكثير في الإجابة: أي العناصر المحددة تنتمي إلى فئة المعادن عند تصنيفها عائلةً عائلةً؟
قائمة المعادن حسب العائلة في الجدول الدوري
القراء الذين يبحثون عن قائمة عملية بالمعادن لا يحتاجون عادةً إلى جدارٍ من أسماء العناصر. بل يحتاجون إلى هيكلٍ منظم. فتصنيف العناصر المعدنية حسب عائلاتها يجعل دراسة النمط ومقارنته وتذكّره أسهل. أما الجدول الرئيسي الوارد أدناه، فيتبع التصنيفات العامة للمعادن التي تستخدمها مواقع «Chemistry LibreTexts» و«ThoughtCo»، مع الإشارة إلى الحالات القليلة التي قد تتعامل معها مصادر الكيمياء أحيانًا بشكل مختلف. وهذه هي الطريقة الأوضح للإجابة عن سؤال: ما العناصر التي تُصنَّف كمعادن في الجدول الدوري، دون الادعاء بأن كل تسمية حدية ثابتة عالميًّا. ملاحظات علمية chemistry LibreTexts
قائمة عناصر معدنية حسب المجموعة العائلية
| عائلة | العناصر الموجودة في المجموعة | ملاحظة التصنيف |
|---|---|---|
| الفلزات القلوية | الليثيوم، الصوديوم، البوتاسيوم، الروبيديوم، السيزيوم، الفرانسيوم | يقع الهيدروجين في المجموعة ١، لكنه يُعامل عمومًا كعنصر غير معدني في الظروف العادية. |
| الفلزات القلوية الترابية | البريليوم، المغنيسيوم، الكالسيوم، السترونتيوم، الباريوم، الراديوم | يتم تصنيف هذه العناصر باستمرار على أنها معادن. |
| الفلزات الانتقالية | السكانديوم، التيتانيوم، الفاناديوم، الكروم، المنغنيز، الحديد، الكوبالت، النيكل، النحاس، الزنك، الإتريوم، الزركونيوم، النيوبيوم، الموليبدنوم، التكنيشيوم، الروثينيوم، الروديوم، البالاديوم، الفضة، الكادميوم، الهافنيوم، التنتالوم، التنجستن، الرينيوم، الأوزميوم، الإيريديوم، البلاتين، الذهب، الزئبق، الروذرفورديوم، الدبنيوم، السيبورجيوم، البوريوم، الهاسيوم، الماينترينيوم، الدارمشتاديوم، الرونتغينيوم، الكوبرنيكيوم | تضع معظم الجداول الدراسية المستخدمة في الصفوف الدراسيّة العناصر زنك (Zn) وكادميوم (Cd) وزئبق (Hg) في هذا الموقع، رغم أن بعض المناقشات الكيميائية تتعامل معها بشكلٍ مختلفٍ قليلًا. |
| معادن ما بعد الانتقال أو المعادن القاعدية | الألومنيوم، والغاليوم، والإنديوم، والقصدير، والثاليوم، والرصاص، والبيسموث، والبولونيوم، والنهاونيوم، والفلروفيوم، والماسكوفيوم، واللايفرموريوم | ملاحظات العلوم حول المعادن الأساسية تشير إلى أن هذه المجموعة تختلف أكثر ما تختلف حسب المصدر. ويُدرج البولونيوم عادةً ضمنها، لكنه يثير أحيانًا جدلًا. أما اللايفرموريوم فيُعامل غالبًا كعنصر معدني محتمل أو متوقع. |
| اللانثانيدات | اللانثانوم، والسيريوم، والبراسيوديميوم، والنيوديميوم، والبروميثيوم، والساماريوم، والأوروبيوم، والجادولينيوم، والتيربيوم، والديسبروسيوم، والهولميوم، والإربيوم، والتوليوم، والإيتربوم، واللوتيشيوم | هذه هي الصفّة الأولى المنفصلة الواقعة أسفل الجدول الرئيسي، وهي عناصر معدنية. |
| الأكتينيدات | الأكتينيوم، والثوريوم، والبروتاكتينيوم، واليورانيوم، والنيبتونيوم، والبلوتونيوم، والأمريسيوم، والكوريوم، والبيركليوم، والكاليفورنيوم، والأينشتاينيوم، والفيرميوم، والميندليفيوم، والنوبيليوم، واللورنسيوم | هذه هي الصفّة الثانية المنفصلة الواقعة أسفل الجدول الرئيسي، وهي عناصر معدنية، رغم أن العديد منها معروفٌ أكثر بسبب خاصية الإشعاعية بدلًا من السلوك المعدني اليومي. |
كيف تقرأ القائمة الرئيسية دون لبس
إذا كنت بحاجة إلى قائمة سريعة بالمعادن لأغراض الواجبات المنزلية أو المراجعة، استخدم عمود العائلة أولاً وعمود الملاحظات ثانياً. فعمود العائلة يُخبرك بالموقع الذي ينتمي إليه العنصر في الجدول الدوري. أما عمود الملاحظات فيوضح لك الأماكن التي تصبح فيها التصنيفات غامضة. وهذا الأمر يكتسب أهمية قصوى بالقرب من «السلم» (المنطقة المتدرجة بين الفلزات واللافلزات) وبين أثقل عناصر الكتلة-بِي (p-block).
عندما يطلب المعلمون من الطلاب أن يذكروا الفلزات ، فإنهم عادةً ما يبحثون عن النواة المستقرة لهذه المجموعات، وليس عن جدلٍ حول كل حالة حدية. فإذا كنت ترغب فقط في أسماء الفلزات الأكثر شيوعاً ، فابدأ بأكثر أعضاء كل مجموعة شهرةً، ثم توسع تدريجياً من هناك.
- الفلزات القلوية: الصوديوم، البوتاسيوم
- الفلزات القلوية الترابية: المغنيسيوم، الكالسيوم
- الفلزات الانتقالية: الحديد، النحاس، الفضة، الذهب
- الفلزات بعد الانتقالية: الألومنيوم، القصدير، الرصاص
- اللانثانيدات: اللانثانيوم، النيوديميوم
- الأكتينيدات: اليورانيوم، البلوتونيوم
هذه هي بعض الأمثلة على المعادن التي يتعرَّف عليها معظم القرّاء بالفعل. وهي تشكِّل أيضًا نقاط ارتكاز جيدة في الذاكرة عندما يبدو الجدول الكامل مزدحمًا جدًّا. وللملاحظات الدراسية، يساعد في التذكُّر أن العناصر الشائعة الفلزات الأكثر شيوعاً تأتي غالبًا من مجموعات العناصر الانتقالية وما بعد الانتقالية، بينما يسهل تذكُّر اللانثانيدات والأكتينيدات باعتبارها سلاسل.
وهنا تحذيرٌ إضافي يحافظ على دقة هذه القائمة الشاملة: فليست كل الجداول ترسم نفس الحدود حول عناصر مثل البولونيوم أو أثقل عناصر الكتلة-بـ (p-block) الاصطناعية. ولهذا السبب فإن المرجع المفيد لا يكتفي بتسمية العناصر، بل يبيّن أيضًا أماكن تداخل الحدود، لأن تسمية «معدن» تكون أكثر موثوقية عندما يمكن التمييز بينها وبين شبه الفلز أو اللافلز.
دليل الجدول الدوري للمعادن مقابل اللافلزات
قائمة رئيسية طويلة مفيدة، لكن معظم القراء يحتاجون إلى وسيلة أسرع لتصنيف عنصر ما بنظرة سريعة. والخبر السار هو أن الجدول الدوري يوفّر لك تلميحًا بصريًّا قويًّا. والخبر الأفضل هو أن الكيمياء توفّر لك اختبارًا احتياطيًّا عندما لا يكفي الترتيب البصري وحده.
كيف تُفرِّق بين الفلزات وأشباه الفلزات واللافلزات
خريطة بصرية من Science Notes تُظهر النمط الأساسي بوضوح: فالفلزات تقع في الغالب على الجانب الأيسر والمركزي، بينما تتجمع اللافلزات على الجانب الأيمن. وبينهما توجد الدرجة المتدرجة المألوفة. وإذا كنت تسأل أين تقع أشباه الفلزات في الجدول الدوري، فهي توجد عادةً على طول تلك الحدود المتعرجة. ال دليل الكيمياء من UMD يستخدم نفس النمط للتعرف السريع.
ومع ذلك، فإن سؤال الجدول الدوري المتعلق بالمعادن مقابل العناصر غير المعدنية لا يُحل بالاعتماد على الموقع وحده. بل يُفضَّل فصل المعادن والعناصر غير المعدنية في جداول الجدول الدوري أيضًا وفقًا للسلوك. فالمعادن عادةً ما توصل الحرارة والكهرباء بكفاءة عالية، وغالبًا ما تفقد إلكتروناتٍ لتكوين أيونات موجبة. أما العناصر غير المعدنية في الجدول الدوري فهي أكثر ميلًا إلى اكتساب الإلكترونات أو مشاركتها، والعديد منها موصل ضعيف. وتوجد العناصر شبه المعدنية في الجدول الدوري على الحد الفاصل بينهما، وغالبًا ما تظهر خصائصًا مختلطةً وسلوكًا شبه موصل.
- ابحث عن الخط الدرجِيّ على الجدول.
- ابدأ بالنظر إلى الجانب الأيسر أو المركز أولًا؛ فمعظم العناصر الموجودة هناك هي معادن.
- انظر إلى الزاوية العلوية اليمنى؛ فمعظم العناصر الموجودة هناك هي عناصر غير معدنية.
- افحص الحد الفاصل نفسه؛ فالعناصر الواقعة عليه غالبًا ما تكون عناصر شبه معدنية.
- اختبر السلوك عند الحاجة: فالموصل الجيد يوحي بأن العنصر معدن، والموصل الضعيف يوحي بأنه عنصر غير معدني، أما السلوك المتوسط أو شبه الموصل فيوحي بأنه عنصر شبه معدني.
- راقب الاستثناءات. يُوضع الهيدروجين على اليسار، لكنه عادةً ما يكون عنصراً غير معدني. وإذا سألتَ: هل السيليكون معدنٌ أم عنصرٌ غير معدني أم عنصرٌ شبه معدني؟ فيُصنَّف السيليكون عادةً كعنصر شبه معدني. ويتم التأكيد على دوره ك Semiconductor (موصل نصف ناقل) في دليل MISUMI الخاص بالعناصر شبه المعدنية.
السلم هو دليلٌ وليس ضماناً. وقد تُصنَّف العناصر الحدّية بشكل مختلف اعتماداً على الجدول المستخدم وقواعد التصنيف التي يستند إليها.
وسائل مساعدة بسيطة للحفظ لتحديد العناصر بسرعة أكبر
- على اليسار وفي المنتصف، فكّر في أن العنصر معدن.
- في الأعلى إلى اليمين، فكّر في أن العنصر غير معدني.
- على خط السلم، فكّر في أن العنصر شبه معدني.
- تذكّر إشارة السلوك: التوصيل، أو العزل، أو التوصيل الجزئي (شبه التوصيل).
هذه الإطار الموجز يجعل قراءة المعادن والعناصر غير المعدنية على مخططات الجدول الدوري أسهل بكثير تحت الضغط. كما أنه يشير إلى أمرٍ أكبر من مجرد الحفظ، لأن الفرق بين المعدن الموصل والعنصر شبه المعدني شبه الموصل يؤثر في كيفية اختيار المواد الفعلية في مجالات الإلكترونيات والتصنيع.

لماذا تهم المعادن في الجدول الدوري في مجال التصنيع
إن نمط الدرج لا يساعد الطلاب على فرز العناصر فحسب، بل يتجاوز ذلك. ففي مجال التصميم والإنتاج، تتحول بسرعة مسألة «ما هو المعدن؟» إلى قرار عملي يتعلق بالأداء. ويُعَد معرفة مكان تواجد المعادن في الجدول الدوري أول دليلٍ للمهندسين حول التوصيلية الكهربائية والميكانيكية، والمتانة، والقابلينّة للسحب، ونقل الحرارة؛ لكن التصنيع الفعلي يتجاوز التصنيفات الصفية المجردة.
لماذا يكتسب تصنيف المعادن أهميةً بالغةً في التصنيع الحقيقي؟
غالبًا ما يشكّل العنصر الكيميائي المعدني نقطة البداية، وليس خط النهاية. AJProTech يصف اختيار المواد كعملية تحقيق توازن بين الأحمال والبيئة والوزن وقابلية التصنيع والتوفر والتكلفة والامتثال للمعايير. ولهذا السبب فإن أنواع المعادن المختلفة تحل مشكلات مختلفة. ويُظهر نظام TIRapid هذا النمط بوضوح: فتُقدَّر النحاس لموصلتيه الكهربائية والحرارية، والألومنيوم لانخفاض كثافته ومقاومته للتآكل، والصلب لقوته وفعاليته من حيث التكلفة، والتيتانيوم لقدرته العالية على التحمل بالنسبة للوزن في البيئات الصعبة. وفي الواقع، فإن العديد من القطع المُصنَّعة تستخدم سبائك بدلًا من العنصر الكيميائي المعدني النقي، لأن المهمة عادةً ما تتطلب توازنًا أفضل بين الخصائص.
- النقل: يساعد الألومنيوم والمغنيسيوم في تقليل الوزن، بينما يظل الصلب خيارًا شائعًا للأجزاء الإنشائية لأنه يجمع بين القوة والتكلفة العملية.
- الإلكترونيات: يُفضَّل النحاس في الحالات التي تكون فيها تدفقات التيار ونقل الحرارة أمورًا بالغة الأهمية.
- بيئات قاسية: تُعد الفولاذ المقاوم للصدأ والتيتانيوم والمواد القائمة على النيكل مفيدة عندما تصبح مقاومة التآكل أو الاستقرار عند درجات الحرارة المرتفعة أمورًا حاسمة.
- تخطيط الإنتاج: إن قابلية التشغيل الآلي تُعَدّ أيضًا عاملًا مهمًّا. فالمادة التي تبدو مثالية على الورق قد تؤدي مع ذلك إلى زيادة اهتراء الأدوات أو المدة الزمنية اللازمة للتصنيع أو متطلبات الفحص.
أين يمكن استكشاف تصنيع المعادن الدقيق؟
لا تصبح العنصر المعدني الموجود في الجدول الدوري جزءًا عمليًّا مفيدًا إلا عندما يتناسب عملية التصنيع مع خصائص تلك المادة. فعلى سبيل المثال، يدعم الألومنيوم التشغيل الآلي السريع والتصميم الخفيف الوزن، بينما قد تتطلب الفولاذات الأشد صلابة أو سبائك التيتانيوم تحكُّمًا أدق في العملية التصنيعية. ولهذا السبب، لا يهتم المهندسون فقط بالتركيب الكيميائي، بل أيضًا بالتسامحات (الانحرافات المسموحة)، ومعالجة السطوح، والتحقق من الجودة، وإمكانية التكرار.
كمثالٍ عمليٍّ: تكنولوجيا المعادن شاوي يي يقدِّم نموذجًا لتدفق عمل تصنيع قطع غيار السيارات يربط بين النماذج الأولية السريعة، والإنتاج بكميات صغيرة، والإنتاج الضخم، مع الالتزام بنظام إدارة الجودة IATF 16949 والتحكم الإحصائي في العمليات. وباستخدامه بهذه الطريقة، يتوقف الجدول الدوري عن كونه مجرد جدولٍ يجب حفظه عن ظهر قلب، ليصبح دليلًا عمليًّا لاختيار المواد التي يمكن تشغيلها آليًّا، وفحصها، والاعتماد عليها في المكونات الحقيقية.
- استخدم التركيب الكيميائي لتضييق نطاق الخيارات.
- استخدم معايير الهندسة لاختيار المادة النهائية.
- استخدم التحكم في العمليات لتحويل المعدن المناسب إلى قطعة موثوقة.
هذه هي القيمة الحقيقية وراء تعلُّم ما هي المعادن الموجودة في الجدول الدوري: ليس مجرد تسميتها فحسب، بل فهم كيفية تأثير تصنيف المعادن على الأجزاء التي يستخدمها الناس يوميًّا في السيارات والأسلاك وأنظمة التبريد والبناء.
الأسئلة الشائعة حول المعادن في الجدول الدوري
١. كم عدد المعادن الموجودة في الجدول الدوري؟
لا يوجد رقم واحد تتفق عليه جميع المصادر باعتباره نهائيًّا. فالغالبية العظمى من العناصر هي معادن، لكن العدد الإجمالي الدقيق قد يتغير حسب الطريقة التي يتعامل بها كل جدول مع الحالات الحدِّية، لا سيما في المنطقة المتدرجة (المنطقة الدرجية) وبعض العناصر الثقيلة في الكتلة p. ولذلك فإن الإجابة الدقيقة تفصل بين العائلات المعدنية الواضحة والعناصر التي قد تُصنَّف أحيانًا بشكل مختلف، بدلًا من فرض عدٍّ مبسَّطٍ واحدٍ.
٢. أين توجد المعادن في الجدول الدوري؟
توجد المعادن بشكل رئيسي في الجانب الأيسر ومن وسط الجدول الدوري. أما الصفان المنفصلان في الأسفل — وهما اللانثانيدات والأكتينيدات — فهما أيضًا معادن. وطريقة سريعة لقراءة ترتيب العناصر هي استخدام خط الدرج: فالعناصر الموجودة في الجانب الأيسر تكون في الغالب معادن، والعناصر في الجانب الأيمن تكون في الغالب غير معدنية، بينما تحتوي المنطقة الحدّية بينهما على العديد من العناصر شبه المعدنية. ويُعَدُّ الهيدروجين الاستثناء البصري الشائع، لأنه يقع في الجانب الأيسر لكنه يُصنَّف عادةً كعنصر غير معدني.
٣. ما هي العائلات الرئيسية للمعادن في الجدول الدوري؟
العائلات المعدنية الرئيسية هي: الفلزات القلوية، والفلزات القلوية الترابية، والعناصر الانتقالية، والفلزات ما بعد الانتقالية، واللانثانيدات، والأكتينيدات. ولكل عائلة نمطها الخاص. فالفلزات القلوية شديدة التفاعل، بينما تكون الفلزات القلوية الترابية أقل تطرُّفًا لكنها لا تزال نشطة، وتضم العناصر الانتقالية العديد من الفلزات البنائية والهندسية المألوفة، أما الفلزات ما بعد الانتقالية فهي عمومًا أكثر ليونة، واللانثانيدات والأكتينيدات تشكِّل الصفين المعدنيين اللذين يظهران أسفل الجدول الرئيسي.
٤. ما الخصائص التي تجعل العنصر معدنًا؟
عادةً ما يُحدِّد الكيميائيون المعدن من خلال مجموعة من السمات بدلًا من سمة واحدة فقط. وتتميَّز المعادن عمومًا بقدرتها الجيدة على توصيل الحرارة والكهرباء، وانعكاس الضوء، والانحناء دون أن تنكسر، والامتداد إلى أسلاك رفيعة، والميل إلى فقدان الإلكترونات في التفاعلات الكيميائية. ومع ذلك، فليست كل المعادن تتصرَّف بنفس الطريقة؛ فبعضها لين، وبعضها مقاوم جدًّا للتآكل، ومثالٌ معروفٌ على ذلك هو الزئبق، الذي يكون سائلًا عند درجة حرارة الغرفة.
٥. لماذا يهمُّ ما إذا كان العنصر معدنًا أم لا في مجال التصنيع؟
تساعد تصنيفات المعادن في ربط الكيمياء باختيارات المواد الواقعية. وبمجرد أن يدرك المهندسون أن مادةً ما تمتلك طابعًا معدنيًّا، يمكنهم البدء في التفكير في خصائصها مثل التوصيل الكهربائي والمقاومة الميكانيكية ومقاومة التآكل والوزن وقابلية التشغيل الآلي. ويكتسب ذلك أهميةً بالغةً في مجالات الإلكترونيات وأجزاء النقل والمكونات الصناعية. ومن الناحية العملية، فإن تحويل العنصر المعدني أو السبيكة المعدنية إلى جزءٍ قابل للاستخدام يعتمد أيضًا على التحكم في عمليات التصنيع والتشغيل الآلي الدقيق. فعلى سبيل المثال، تطبِّق شركة شاوي ميتال تكنولوجي تقنيات تشغيل آلي معتمدة وفق معيار IATF 16949، بالإضافة إلى ضوابط الجودة القائمة على نظام التحكم الإحصائي في العمليات (SPC)، وذلك لدعم الانتقال من مراحل تصنيع النماذج الأولية إلى الاستخدام الإنتاجي للأجزاء المعدنية.
 دُفعات صغيرة، معايير عالية. خدمتنا لتطوير النماذج الأولية بسرعة تجعل التحقق أسرع وأسهل —
دُفعات صغيرة، معايير عالية. خدمتنا لتطوير النماذج الأولية بسرعة تجعل التحقق أسرع وأسهل —
