ما هي العناصر القلوية الترابية؟ المجموعة 2 تصبح أخيرًا واضحة
ما هي العناصر القلوية الترابية؟
إذا بحثت عن ما هي العناصر القلوية الترابية ، فإليك الإجابة المباشرة: وهي ستة عناصر تقع في المجموعة الثانية من الجدول الدوري. ويُعد هذا التعريف الموجز للعناصر القلوية الترابية نقطة البداية، لكن الاسم نفسه يُخبرك أيضًا كثيرًا عن سلوك هذه المجموعة. المجموعة 2 تعريفٌ سريعٌ للعناصر القلوية الترابية هو نقطة البداية، لكن الاسم نفسه يُخبرك أيضًا كثيرًا عن سلوك هذه المجموعة.
ما هي العناصر القلوية الترابية في جملة واحدة؟
العناصر القلوية الترابية هي البريليوم والمغنيسيوم والكالسيوم والاسترونتيوم والباريوم والراديوم، وهي ستة عناصر معدنية تقع في المجموعة الثانية وتشكّل عادةً أيونات ذات شحنة +2.
- البيريليوم (Be)
- المغنيسيوم (Mg)
- الكالسيوم (Ca)
- السترونشيوم (Sr)
- الباريوم (Ba)
- الراديوم (Ra)
لماذا يكون اسم المعادن القلوية الترابية منطقيًّا
للمبتدئين، فإن تعريف المعادن القلوية الترابية يصبح أسهل بكثير عندما تقسم العبارة إلى ثلاثة أجزاء.
القاعدية يعني أن أكاسيد هذه العناصر وهيدروكسيداتها قاعدية، وليست حمضية. الأرض هي كلمة تاريخية. فقد استخدمها الكيميائيون الأوائل للدلالة على المواد المستقرة حراريًّا، الشبيهة بالمعادن، والتي لا تنصهر ولا تذوب بسهولة في الماء، وهي نقطة يوضّحها بريتانيكا . المعادن يعني أن العناصر نفسها معدنية، وعادةً ما تكون لامعة وجيدة في فقدان الإلكترونات أثناء التفاعلات.
وهذا يمنحك التعريف الأساسي لـ المعادن القلوية الترابية بدون الحاجة إلى دراسة الكيمياء المتقدمة أولًا. كما أنه وصف موجزٌ مفيدٌ للفلزات القلوية الترابية : وهي عائلة فلزات تنتمي إلى المجموعة الثانية، وتتشابه في خصائصها الكيميائية، وموقعها المشترك على الجدول الدوري، ولها دورٌ كبيرٌ في العالم الواقعي. فالمغنيسيوم يظهر في السبائك والكائنات الحية. أما الكالسيوم فيكتسب أهميته من دوره في العظام والقواقع ومواد البناء. أما الباريوم والسترونتيوم والراديوم فهي تظهر في سياقات أكثر تخصصًا.
تبدأ هذه المقالة بشكل بسيطٍ عمداً. فقائمة واضحةٌ يسهل حفظها، لكن فهم طبيعة هذه العائلة يصبح أوضح عندما ترى الموقع الذي تشغله هذه العناصر على الجدول الدوري، ولماذا يمنحها هذا الموقع سلوكاً متشابهاً إلى هذا الحد.
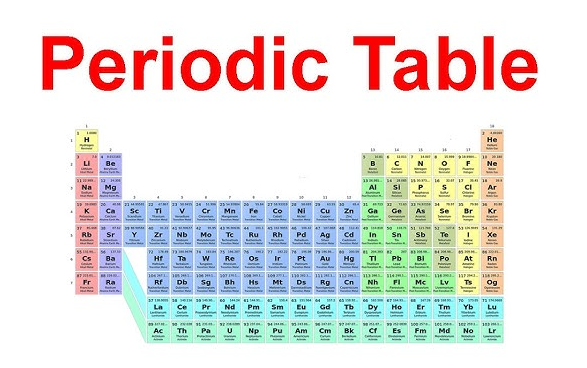
موقع المجموعة الثانية على الجدول الدوري
تصبح تسمية العائلة أسهل في التذكّر عندما يمكنك تحديد موقعها فعليًا. فإذا كنت تتساءل أين توجد الفلزات القلوية الترابية على الجدول الدوري؟ ، فانظر إلى العمود الثاني من اليسار. وهذا العمود الرأسي هو المجموعة الثانية على الجدول الدوري ، وتقع مباشرةً بجانب الفلزات القلوية في المجموعة الأولى. أ المجموعة 2 في الجدول الدوري يُظهر الرسم البياني نفس الخط المستقيم في كل مرة: البريليوم في الأعلى، ثم المغنيسيوم، والكالسيوم، والاسترونشيوم، والباريوم، والراديوم وهي تتحرك نحو الأسفل عبر الفترات.
في الجدول الدوري لمعادن الأرض القلوية في هذا الرسم البياني، تنتمي هذه العناصر الستة إلى الكتلة s. ويتّسم موقعها المشترك بأهميةٍ لأنّه يعكس نمطًا مشتركًا في توزيع الإلكترونات. وكما ليبرتستس يوضّح، فإن عناصر المجموعة 2 تمتلك توزيعًا إلكترونيًّا ظاهريًّا من النوع ns 2، ما يعني أنّها تحتوي على إلكترونين في الغلاف الخارجي.
مكان وجود معادن الأرض القلوية في الجدول الدوري
مرئيًّا، يكون النمط بسيطًا. فـ عناصر المجموعة 2 في الجدول الدوري تشكّل عمود عائلة واحدًا عبر الفترات من 2 إلى 7. وتُبرز العديد من الرسوم التوضيحية الصفية هذه العناصر. الفلزات القلوية الترابية في الجدول الدوري التخطيطات ذات اللون نفسه لأن عائلات العناصر تُقرأ عموديًا، وليس أفقيًا. عمليات البحث عن الجدول الدوري: الفلزات القلوية الترابية تطلب فعليًّا تلك العمود الواحد.
| عنصر | الرمز | الموقع في المجموعة 2 | الأيون النموذجي | مركب مألوف |
|---|---|---|---|---|
| البيريليوم | Be | الدورة 2، أعلى المجموعة 2 | Be2+ | BeO |
| المغنيسيوم | Mg | الدورة 3 | Mg2+ | MgO |
| كالسيوم | Ca | الفترة 4 | Ca2+ | كاكو 3 |
| السترونتيوم | Sr | الفترة 5 | Sr2+ | SrCO 3 |
| الباريوم | BA | الفترة 6 | BA 2+ | BaSO 4 |
| الراديوم | RA | الفترة 7، في أسفل المجموعة 2 | RA 2+ | RaCl 2 |
لماذا تشكِّل عناصر المجموعة 2 أيونات ذات شحنة موجبة قدرها اثنان
تُحدِّد هذان الإلكترونان الخارجيَّان سلوك العنصر الكيميائي. وتميل ذرات المجموعة 2 إلى فقدان كلا الإلكترونين لأن ذلك يمنحها ترتيبًا إلكترونيًّا أكثر استقرارًا. والنتيجة هي +2 أيون ، مثل المغنيسيوم 2+أو الكالسيوم 2+. ولهذا السبب تشكّل هذه الفلزات عادةً مركباتٍ مثل الأكاسيد والكلوريدات والكربونات والكبريتات. ويمكنك ملاحظة النمط في الصيغ الكيميائية فورًا: MgO، CaCl 2، CaCO 3، BaSO 4.
كيفية التعرُّف بسرعة على عناصر مجموعة الفلزات القلوية الأرضية
وتتمثل خدعة التعرُّف السريع في البحث عن ثلاثة مؤشرات في آنٍ واحد: العمود الثاني في الجدول الدوري، والعناصر المعدنية، والشحنة الموجبة المعتادة +2. وبالمقارنة مع الفلزات القلوية المجاورة لها، والتي تمتلك إلكترون تكافؤ واحد وتشكّل عادةً أيونات ذات شحنة +1، فإن عناصر المجموعة الثانية تحتوي على إلكترون خارجي إضافي واحد، وهي أقل تفاعلًا عمومًا. ومع ذلك، فهي تنتمي بوضوح إلى عائلة مشتركة. وأمرٌ مثيرٌ للاهتمام هو أن كل عنصرٍ منها يعبِّر عن هذا النمط بطريقةٍ مختلفة قليلًا، لا سيما من البريليوم في الأعلى إلى الراديوم في الأسفل.
تعرفوا على ستة عناصر من الفلزات القلوية الأرضية
القائمة مفيدة، لكنها ليست سهلة التذكّر بحد ذاتها. وتبدأ المجموعة الثانية في إثارة انطباعٍ أقرب إلى الواقع عندما يمتلك كل عضوٍ منها هويةً واضحةً. فبعضها يظهر في العظام أو ماء البحر. وبعضها يُلوّن الألعاب النارية. أما أحدها فهو في الغالب علامة تحذيرٍ تاريخية. ومع ذلك، فإنها جميعًا تنتمي إلى العائلة نفسها، لكن لكلٍّ منها شخصيته الخاصة.
| عنصر | الرمز | حدوث شائع | خاصية بارزة | الملاءمة للواقع العملي |
|---|---|---|---|---|
| البيريليوم | Be | يوجد في المعادن مثل البريل | خفيف جدًّا وصلبٌ جدًّا بالنسبة للمعادن | يُستخدم في تطبيقات الطيران والفضاء المتخصصة وأشعة إكس؛ والغبار الناتج عنه خطيرٌ إذا استُنشق |
| المغنيسيوم | Mg | يوجد في ماء البحر والمعادن | كثافته منخفضة، وله لهبٌ أبيض لامع عند الاشتعال | له أهميةٌ كبيرةٌ في السبائك خفيفة الوزن والمكملات الغذائية والعمليات الحيوية |
| كالسيوم | Ca | شائع في الحجر الجيري والعظام والقواقع والطباشير | أيون ثنائي التكافؤ من المجموعة 2، مألوف بيولوجيًّا | عنصر رئيسي في الهياكل العظمية والأسمنت والجص والعديد من المعادن الطبيعية |
| السترونتيوم | Sr | يوجد بشكل رئيسي في معدن السيلستين والمعدن السترونتيانيت | تُنتج أملاحه لونًا أحمر زاهيًا في اللهب | يُستخدم في الألعاب النارية والإشارات الضوئية ومواد الإضاءة المنبعثة والبعض من المنتجات السنية |
| الباريوم | BA | يرتبط عادةً بمعدن الباريت | فلز قلوي ترابي كثيف وثقيل | يكتسب كبريتات الباريوم أهميةً في عمليات الحفر والتصوير الطبي؛ أما المركبات القابلة للذوبان من الباريوم فتتطلب اتخاذ الحيطة والحذر |
| الراديوم | RA | يوجد بكميات أثرية في خامات اليورانيوم | تسيطر إشعاعيته القوية على قصته الكيميائية | في الغالب ذات صلة تاريخية أو علمية خاضعة للرقابة المشددة اليوم |
البريليوم والمغنيسيوم في رأس المجموعة 2
الأنابيب العنصر البريليوم يقع في رأس هذه المجموعة ويشير بالفعل إلى أن المجموعة 2 ليست متجانسة تمامًا. وغالبًا ما يرتبط بالمعدن البريل، وهو نفس عائلة المعادن التي تشمل الزمرد والأخضر المائي. ويتميز البريليوم بأنه خفيفٌ بشكل غير عادي وصلبٌ جدًّا، ما يجعله مفيدًا في الأجزاء عالية الأداء التي تتطلب كتلةً منخفضةً. وفي الوقت نفسه، يُعد البريليوم مادةً تتطلب عنايةً فائقةً في البيئات الصناعية، لأن الغبار الناعم منه قد يكون ضارًّا إذا استُنشق. ولذلك يُذكر كلٌّ من أدائه الممتاز واحتياطات التعامل معه.
المغنيسيوم يبدو أكثر ألفةً بكثيرٍ. ال الرمز الكيميائي للمغنيسيوم المغنيسيوم (Mg) هو أحد أكثر المعادن شهرةً في هذه المجموعة، لأنه يوجد في مياه البحر والمعادن الشائعة والأنظمة الحية. وهو معدن خفيف جدًّا، وعند اشتعاله يُنتج ضوءًا أبيض قويًّا. ولذلك فقد ارتبط المغنيسيوم منذ زمنٍ طويل بالمضيئات والمواد المشتعلة بقوة. ومع ذلك، فإن معظم الناس يواجهونه في الحياة اليومية على أشكال أكثر اعتدالًا، مثل دوره الغذائي، أو المركبات المضادة للحموضة، أو السبائك الخفيفة التي تُستخدم حيثما كان تقليل الكتلة أمرًا بالغ الأهمية.
الكالسيوم والسترونتيوم في المواد اليومية
يُعتبر الكالسيوم العنصر الأكثر تميُّزًا في المجموعة الثانية بالنسبة للكثير من القرّاء. فهو موجود في الحجر الجيري والطباشير والقواقع والعظام، وبالتالي فهو يربط الكيمياء بكلٍّ من الجيولوجيا والبيولوجيا بشكلٍ فوري تقريبًا. وكربونات الكالسيوم هي المركب المعروف هنا. وهي تساعد في تفسير سبب أهمية نفس العائلة في تكوين الكهوف والحجارة المستخدمة في البناء والهياكل العظمية. أما معدن الكالسيوم نفسه فهو نشيط كيميائيًّا، لكن مركبات الكالسيوم منتشرة في كل مكان، ولذلك يشعر الكثير من الناس بأن هذا العنصر مألوفٌ أكثر مما هو غريب.
ستونتيوم) أسهل لتذكره) بمجرد أن تضعه مع اللون الـ رمز للسترونسيوم هو Sr، و السترونتيوم يُوجد بشكل رئيسي في المعادن السليستيت وسترونسيانيت. الجمعية الملكية للكيمياء تصفها بأنها معدن ناعم و فضي يحترق في الهواء و يتفاعل مع الماء ملحها مشهور بإنتاج ألوان حمراء لامعة في الألعاب النارية والشعلات. يذكر المصدر نفسه أيضاً استخدامات في المواد المتوهجة في الظلام و هيكس هيدرات كلوريد السترونسيوم في معجون الأسنان للأسنان الحساسة. هذا يجعل السترونسيوم مثال رائع على كيفية أن العنصر يمكن أن يكون فعالا كيميائيا ولكن في الغالب يواجه من خلال المركبات.
الباريوم والراديو في سياقات متقدمة أو متخصصة
الأنابيب عنصر الباريوم غالبًا ما يُذكَر الباريوم من خلال كثافته العالية. ويرتبط عادةً بمعدن الباريت، وأحد مركباته الأكثر شهرة هو كبريتات الباريوم. ويكتسب هذا المركب أهميته من كونه غير قابلٍ للذوبان إلى حدٍّ كبير، مما يساعد في تفسير سبب ظهور الباريوم في بيئات عملية مثل سوائل الحفر والتصوير الطبي، بينما تُعامل المركبات القابلة للذوبان الأخرى للباريوم بحذرٍ أكبر بسبب مخاوف السُّمِّية. ويذكّر الباريوم القرّاء بأن الصورة المفيدة لعنصر من عناصر المجموعة الثانية تكون غالبًا على هيئة مركبٍ وليس المعدن اللامع نفسه.
يقع الراديوم في قاع هذه العائلة، لكنه لا يندمج بهدوء. جدول الراديوم الدوري النظرة العامة: يُشير الرمز Ra إلى النقطة التي تصبح فيها الإشعاعية السمة المميزة للعنصر. ويوجد الراديوم في الطبيعة بكميات ضئيلة جدًّا، وغالبًا ما يرتبط بخامات اليورانيوم. ومن الناحية التاريخية، اشتهر الراديوم بسبب الدهانات المُضيئة والتجارب الطبية المبكرة. أما اليوم، فإن خطره ناتجٌ عن إشعاعيته لا عن سلوكه كمعدن عادي، ولذلك يُعامل وفق ضوابط صارمة. وبعبارات مبسَّطة، لا يزال الراديوم ينتمي إلى المجموعة 2، لكنه يُناقَش مع التركيز على سلامة المفاعلات النووية بقدر ما يُناقَش من منظور كيميائي.
إذا وضعت هذه العناصر الستة جنبًا إلى جنب، فلن تبدو المجموعة وكأنها قائمة عارية من الأسماء فقط. فالحجم، والنشاط الكيميائي، والمُركَّبات الشائعة، بل وحتى الطريقة التي يظهر بها كل عنصر في الحياة اليومية تتغير أثناء التحرك نحو الأسفل في المجموعة. وهذه الأنماط المتغيرة هي ما يجعل المجموعة 2 مفيدةً بشكل خاص، لأن الترتيب من البريليوم إلى الراديوم يبدأ حينها في كشف الاتجاهات بدلًا من مجرد سرد حقائق متفرقة.
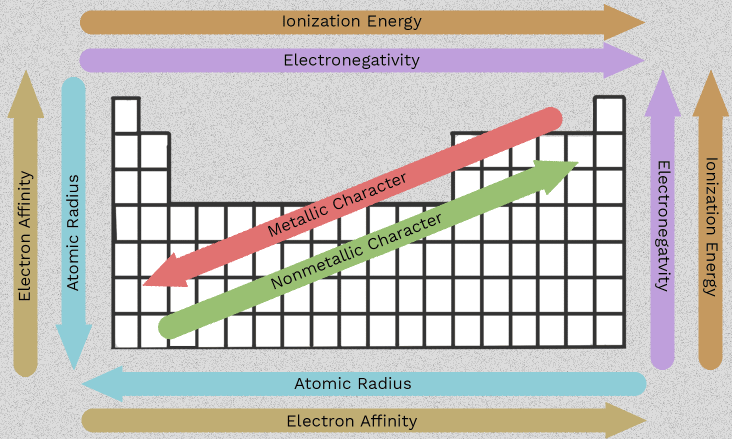
خصائص المعادن القلوية الأرضية والاتجاهات في المجموعة 2
هذا التغير في الترتيب من البريليوم إلى الراديوم هو ما يجعل المجموعة الثانية مفيدة. بدلًا من حفظ ستة حقائق منعزلة، يمكنك اتباع عدد قليل من الأنماط التي تتكرر عبر العمود كله. وأهمها خصائص المعادن القلوية الترابية تنشأ جميعها من سمة مشتركة واحدة: لكل ذرة إلكترونان خارجيان تميل إلى فقدانهما.
وبمجرد أن تلاحظ كيف تتغير الحجم وحجب الإلكترونات وطاقة التأين عند النزول في المجموعة، تصبح هذه العائلة أسهل بكثير في التنبؤ بسلوكها. وهذه خصائص المعادن القلوية الترابية ليست مجرد حقائق تُدرَّس في الامتحانات فحسب، بل تفسِّر أيضًا لماذا تتفاعل بعض العناصر أسرع من غيرها، ولماذا تذوب بعض المركبات بشكل أفضل من غيرها، ولماذا تتطلب بعض الاتجاهات صياغة دقيقة بدلًا من استخدام أسهم بسيطة.
الخصائص المشتركة للمعادن القلوية الترابية
معظم عناصر المجموعة الثانية هي معادن لامعة فضية اللون وعادةً ما تشكِّل أيونات M 2+الأيونات وتُكوِّن في الغالب مركبات أيونية. وهي تتصرَّف كعوامل مختزلة لأنها تفقد إلكترونات. وبالمقارنة مع معادن المجموعة 1، فإنها أقل تفاعلًا عمومًا، لكنها لا تزال نشطة كيميائيًّا بما يكفي لتكوين العديد من الأكاسيد والكلوريدات والكربونات والكبريتات الشائعة.
طريقة بسيطة لتنظيم الخصائص الكيميائية للمعادن القلوية الترابية هي فصل ما يبقى ثابتًا عما يتغيَّر. وما يبقى ثابتًا هو حالة الأكسدة المعتادة (+2). أما ما يتغيَّر فهو سهولة فقدان كل عنصرٍ لهذين الإلكترونين. وهنا بالضبط تبدأ الاتجاهات في أن تكتسب أهمية.
الاتجاهات عند النزول في المجموعة 2 وما تعنيه
البيانات التي جمعتها منصة LibreTexts والتفسيرات المتعلقة بالاتجاهات من Save My Exams تُظهر نفس النمط العام. إذ يزداد نصف القطر الذري من ١١٢ بيكومتر لعنصر البريليوم (Be) إلى ٢٥٣ بيكومتر لعنصر الباريوم (Ba)، بينما ينخفض طاقـة التأيـون الأولـى من ٩٠٠ إلى ٥٠٣ كيلوجول/مول. وبعبارات بسيطة، فإن الإلكترونات الخارجية تقع على مسافة أبعد من النواة وتكون محجوبة بعدد أكبر من القشور الداخلية، وبالتالي يصبح من الأسهل إزالتها.
| الاتجاه | الاتجاه عند النزول في المجموعة ٢ | السبب الكيميائي | ماذا يعني هذا عمليًا |
|---|---|---|---|
| النصف الذري | يزيد | لكل عنصر غلاف إلكتروني إضافي وحجب أكبر | الذرات الأكبر تمسك بالإلكترونات الخارجية بشكل أقل إحكامًا |
| طاقة التأين الأولى والثانية | تنخفض بشكل عام | الإلكترونات الخارجية تكون أبعد عن النواة، لذا تكون قوة الجذب أضعف | تكوين أيونات M 2+تصبح أكثر سهولة |
| التفاعلية | تزداد بشكل عام | انخفاض طاقات التأين يجعل فقدان الإلكترونات أسهل | تتفاعل العناصر الأثقل مع الأحماض والأكسجين، وغالبًا مع الماء، بنشاط أكبر |
| نقطة الانصهار | تنخفض عمومًا، لكنها لا تنخفض بشكل منتظم | تؤدي أيونات المعادن الأكبر حجمًا إلى إضعاف الروابط المعدنية، رغم أن البنية تلعب أيضًا دورًا مهمًّا | استخدم كلمة "عامة" هنا، لأن المغنيسيوم والكالسيوم لا ينطبقان على خطٍّ منظمٍ تمامًا |
| الكثافة | غير منتظم | تتغيَّر الكتلة وحجم الذرة وترصيف الذرات المعدنية معًا في آنٍ واحد | لا يمكن اعتبار الكثافة ظاهرةً تتبع اتجاهًا تنازليًّا بسيطًا |
| ذوبانية الهيدروكسيدات | يزيد | يتغير التوازن بين طاقة الشبكة البلورية وطاقة الترطيب أثناء النزول في المجموعة | تُنتج الهيدروكسيدات الأثقل محاليل أكثر قلوية |
| ذوبانية الكبريتات | يقلل | تنخفض طاقة الترطيب كلما زاد حجم الكاتيون | مركبات مثل BaSO 4تصبح غير قابلة للذوبان تمامًا |
الكثافة وسلوك الانصهار هما الاتجاهان اللذان يُبسِّطهما الطلاب غالبًا أكثر من اللازم. فالكثافة لا تتغير في خطٍ مستقيم لأن كلًّا من الكتلة والحجم يتغيران، كما أن ذرات الفلز لا تتراص بنفس الطريقة في كل بلورة. ويتطلب تحديد نقاط الانصهار أيضًا عنايةً خاصةً؛ فهي تميل عمومًا إلى الانخفاض لأن الأيونات الأكبر تُضعف الشبكة المعدنية، لكن المغنيسيوم يتمتع بنقطة انصهار منخفضة بشكل غير معتاد تبلغ ٦٥٠°م، بينما يرتفع الكالسيوم إلى ٨٤٢°م قبل أن تنخفض القيم مجددًا. لذا فإن أحد أكثر الأمور أمانًا المميِّزات الخاصة بالفلزات القلوية الترابية هو ما يلي: الاتجاه العام حقيقيٌّ فعلاً، لكن التفاصيل الفيزيائية ليست سلسةً تمامًا.
والذوبانية تحمل نفس التحذير. فلا توجد قاعدة واحدة تشمل كل أملاح المجموعة الثانية. فتزيد قابلية الهيدروكسيدات للذوبان كلما نزلنا في المجموعة، بينما تقل قابلية الكبريتات للذوبان. ولذلك، إذا قال شخصٌ ما «تزيد الذوبانية كلما نزلنا في المجموعة الثانية»، فإن السؤال المهم هو: «أي المركبات؟»
لماذا تتفاعل عناصر المجموعة الثانية القلوية بالطريقة التي تفعلها
إذن، هل عناصر المجموعة الثانية القلوية نشطة كيميائيًّا؟ نعم، والإجابة العامة هي أن نشاطها الكيميائي يزداد كلما انتقلنا نحو الأسفل في المجموعة. والسبب هو نفس القصة الإلكترونية المذكورة أعلاه. فانخفاض طاقتي التأين الأولى والثانية يعني أن الذرات يمكنها فقدان إلكترونين بسهولة أكبر والوصول إلى الحالة الشائعة M 2+بسرعة أكبر.
وهذا يؤثر في التفاعلات الواقعية. ففي اتجاه الأسفل داخل المجموعة، تزداد سرعة التفاعلات مع الأحماض المخففة، وتزداد شدة التفاعلات مع الأكسجين، كما يصبح من الأسهل أكسدة العناصر الأثقل وزنًا. وتشير ملاحظات موقع «سِف ماي إكзамز» (Save My Exams) إلى أن الباريوم نشيطٌ كيميائيًّا لدرجة أنه يُخزن تحت زيت، وهي علامة عملية تدل على مدى تقدُّم اتجاه النشاط الكيميائي.
- يزداد نصف القطر الذري عند النزول في المجموعة 2.
- تنخفض طاقة التأين عند النزول في المجموعة 2.
- يزداد النشاط الكيميائي لأن فقدان إلكترونين يصبح أسهل.
- تظهر نقاط الانصهار والكثافة انحرافات غير منتظمة، لذا ينبغي تجنُّب وضع قواعد مطلقة.
- تظهر الهيدروكسيدات والكبريتات اتجاهات معاكسة في الذوبانية.
تجعل هذه الأنماط العائلة قابلة للتنبؤ، لكنها ليست متجانسة تمامًا. فبالقرب من قمة المجموعة، يبدأ البريليوم بالفعل في كسر القواعد، ويُضاف المغنيسيوم استثناءً يوميًّا آخر يكتسب أهمية أكبر مما يتوقعه المبتدئون عادةً.
الفلزات القلوية وفلزات الأرض القلوية
تجعل الاتجاهات العامة تعلُّم المجموعة 2 أسهل، لكن العائلة تفقد معناها إذا عُومل كل عضو فيها على أنه مطابق تمامًا للآخرين. وأكبر إشارة تحذيرية هي البريليوم. أما المغنيسيوم فيُضيف استثناءً يوميًّا أكثر عملية. وعندما يقارن الناس الفلزات القلوية وفلزات الأرض القلوية ، فإن التشابه في الأسماء قد يُخفي اختلافات كيميائية كبيرة جدًّا.
لماذا لا يتصرف البريليوم كفلز نموذجي من المجموعة 2
BYJU'S يصف البريليوم باعتباره العنصر الشاذ الواضح في المجموعة 2. فحجمه الصغير غير المعتاد، وطاقة أيونيته العالية، وقدرته التأينية القوية جدًّا تمنحه سلوكًا أقل تمثيلًا لخصائص العائلة. وبعبارات بسيطة، فإن عنصر Be 2+يؤثر بشدة على سُحب الإلكترونات القريبة، لذا فإن مركبات البريليوم غالبًا ما تكون أكثر تساهميةً من المركبات الأكثر أيونيةً التي تشكّلها العناصر الأثقل في المجموعة. ويشير نفس المصدر أيضًا إلى أن للبريليوم نقاط انصهار وغليان أعلى من باقي عناصر المجموعة، ولا يتفاعل مع الماء كما تفعل عناصره المرافقة.
المغنيسيوم ليس غريبًا بقدر البريليوم، لكنه قد يبدو أقل تفاعليةً مما يتوقعه الطلاب. وتلاحظ منصة LibreTexts أن المغنيسيوم النقي جدًّا يتفاعل فقط تفاعلًا خفيفًا مع الماء البارد، ويتباطأ هذا التفاعل سريعًا لأن هيدروكسيد المغنيسيوم شبه غير القابل للذوبان يشكّل حاجزًا على السطح. أما في قاع هذه المجموعة، فيُناقَش الراديوم عادةً بشكل منفصل نظرًا لسيطرة إشعاعيته على الاستخدامات العملية ومناقشات السلامة.
كيف تختلف معادن الأرض القلوية عن المعادن القلوية
بطريقة بسيطة مقابل القلوية فإن عناصر المجموعة ١ تفقد إلكترونًا واحدًا من غلافها الخارجي، بينما تفقد عناصر المجموعة ٢ إلكترونين. وهذه الفروقة الوحيدة تشكّل خصائص المعادن القلوية ومعادن الأرض القلوية أكثر من أي عامل آخر تقريبًا.
| المميزات | الفلزات القلوية، المجموعة 1 | الفلزات القلوية الترابية، المجموعة 2 |
|---|---|---|
| إلكترونات التكافؤ | 1 | 2 |
| الأيون النموذجي | م + | م 2+ |
| التفاعل مع الماء البارد | غالبًا ما يكون عنيفًا أو حتى شديد العُنف، مُشكِّلًا هيدروكسيدًا وهيدروجين | أقل انتظامًا: لا يتفاعل البريليوم مع الماء، ويتفاعل المغنيسيوم تفاعلًا خفيفًا، بينما يتفاعل الكالسيوم والسترونشيوم والباريوم بعنف متزايد |
| كيمياء الأكسجين الشائعة | يمكن أن تشكِّل أكاسيد أو بيروكسيدات أو سوبرأكاسيدات | تشكِّل عادةً أكاسيد أحادية؛ ومعظم هذه الأكاسيد تُكوِّن هيدروكسيدات عند تفاعلها مع الماء، لكن أكسيد البريليوم يُعد استثناءً |
استثناءات مهمة يغفل عنها الطلاب غالبًا
- ليست كل الفلزات في المجموعة 2 تتفاعل مع الماء بنفس الطريقة.
- مركبات البريليوم أكثر تساهميةً من باقي عناصر المجموعة.
- لا تخلط بين الفلزات القلوية و الفلزات القلوية الترابية وكأنها تنتمي إلى المجموعة نفسها لمجرد تشابه أسمائها.
- الأنابيب خصائص الفلزات القلوية والفلزات القلوية الترابية يُفضَّل تعلُّمها على هيئة أنماطٍ تتضمَّن استثناءاتٍ، وليس على هيئة شعاراتٍ جامدة.
وهذا أيضًا هو أفضل طريقٍ لفهم الخصائص الكيميائية للفلزات القلوية والفلزات القلوية الترابية . فأنماط الإلكترونات تمنحك القاعدة، لكن المواد الحقيقية تضيف طبقةً من التعقيد. وتتضح هذه الطبقة بشكلٍ أكبر عندما تنظر إلى أماكن وجود عناصر المجموعة 2 في الطبيعة: فهي نادراً ما توجد على هيئة معادن نقية، بل توجد بكثرةٍ أكبر داخل المعادن والصخور ومياه البحار والعظام والمركبات الصناعية.
كيف توجد الفلزات القلوية الترابية في الطبيعة
إذا تصورتَ فلزًا قاعديًا أرضيًا كعينةٍ لامعةٍ نقيةٍ تقع داخل صخرة، فإن الطبيعة تتبع طريقةً مختلفةً. عناصر المجموعة الثانية نشيطـةٌ بما يكفي لتظهر عادةً على هيئة أيوناتٍ داخل المعادن والملح والصخور ومياه البحر والعظام والقواقع، بدلًا من ظهورها كفلزاتٍ حرة. سواء بحث شخصٌ ما عن الفلزات القاعدية الأرضية أو عن المصطلح الأكثر شيوعًا، فإن النمط الطبيعي يبقى نفسه: هذه العائلة تُفضِّل بشدةً وجودها في المركبات.
ويأتي هذا النمط مباشرةً من الخصائص الكيميائية للفلزات القاعدية الأرضية ، فهي تميل إلى فقدان إلكترونين من غلافها الخارجي وتكوين أيونات M²⁺ مستقرة. وبمجرد حدوث ذلك، ترتبط أيونات الأكسجين وكربونات والكبريتات والهاليدات بها بسهولةٍ لتكوِّن مركبات صلبة يمكن أن تبقى ثابتةً في المجالات الجيولوجية والبيولوجية. 2+²⁺
لماذا لا توجد الفلزات القاعدية الأرضية في الطبيعة على هيئة عناصر حرة
بريتانيكا و ثووقتو كلاهما يصفان المجموعة 2 بأنها تفاعلية، وهو ما يفسّر سبب ندرة وجود هذه العناصر في حالتها غيرالمتحدة. ففي الهواء، تشكّل العديد منها بسرعة طبقات أكسيدية. أما في البيئات الطبيعية، فإنها تكتسب استقرارًا أكبرَ عبر تحولها إلى كربونات أو كبريتات أو سيليكات أو فلوريدات أو كلوريدات. ولهذا السبب تظهر الكالسيوم في الحجر الجيري والقواقع، والمغنيسيوم في المعادن ومياه البحار، والاسترونشيوم أو الباريوم في رواسب الخام. أما الراديوم فهو أكثر ندرةً، ويوجد فقط بكميات أثرية في خامات اليورانيوم.
المعادن والمركبات الشائعة للمجموعة 2
| عنصر | المصدر الطبيعي الشائع | مركب مألوف | لماذا يكتسب هذا المركب أهمية |
|---|---|---|---|
| البيريليوم | بيريل | BeO | يُعد المعدن «البيريل» مصدرًا تجاريًّا لهذا العنصر، بينما يُعتبر أكسيد البريليوم مركبًا مهمًّا في المواد المتخصصة. |
| المغنيسيوم | المغنيسيت، الدولوميت، مياه البحر | MgCO 3أو Mg(OH) 2 | ويوضح ذلك سبب انتشار المغنيسيوم أكثر في المعادن ومياه البحر والطب مقارنةً بحالته كفلزٍ نقي. |
| كالسيوم | الحجر الجيري، الطباشير، الرخام، الجبس، العظام، القواقع | كاكو 3 | يربط الجيولوجيا ومواد البناء والهياكل العظمية في مركبٍ واحدٍ شائعٍ جدًّا |
| السترونتيوم | السيليستايت، والاسترونشيانايت | SrSO 4أو SrCO 3 | هذه المعادن هي المصادر الطبيعية الرئيسية لمركبات الاسترونشيوم |
| الباريوم | الباريت، والويثريت | BaSO 4 | الباريت هو الخام الرئيسي، وكبريتات الباريوم واحدة من أكثر مركبات الباريوم شهرةً |
| الراديوم | كميات أثرية في خام البتشبليند وغيرها من خامات اليورانيوم | RaCl 2 | إن ندرة الراديوم وإشعاعيته تجعل مركباته ذات أهمية تاريخية، لكنها غير شائعة |
EBSCO يلاحظ أن الكالسيوم والمغنيسيوم يوجدان أيضًا في ماء البحر بتركيز يبلغ حوالي ٠٫٤ غرام/لتر و١٫٣ غرام/لتر على التوالي. وهذا يساعد في تفسير سبب ارتباط هذه المعادن القلوية الترابية المجموعة ليس فقط بالخامات، بل أيضًا بمياه العسر، والأنظمة البحرية، وأنسجة الكائنات الحية.
كيفية عزل هذه الفلزات من مركباتها
وبما أن معادن المجموعة الثانية تكون عادةً محبوسة داخل مركبات، فإن عملية الاستخلاص تبدأ من الخامات أو المياه المالحة أو الرواسب المعدنية. وتتمثل إحدى الأفكار الصناعية الشائعة في بساطة العملية: أولاً، تحويل المادة إلى أكسيد أو هاليد أكثر قابليةً للتعامل، ثم استخدام التحليل الكهربائي أو الاختزال الكيميائي لتحرير المعدن. ويصف موقع «بريتانيكا» العزل المبكر للمغنيسيوم والكالسيوم والاسترونشيوم والباريوم بواسطة التحليل الكهربائي، بينما تشير قاعدة بيانات «إبسكو» إلى أن طرق الإنتاج الحديثة ما زالت تعتمد عادةً على كلوريدات منصهرة أو اختزال الأكاسيد أو طرق ذات صلة حسب العنصر المعني. ويُعَد البريليوم تذكيرًا مفيدًا بأن هذه المجموعة ليست متجانسة تمامًا، إذ يمكن إنتاجه عن طريق اختزال فلوريد البريليوم.
لذلك، في الحياة اليومية، يصادف الناس عادةً العناصر المُصنَّفة في المجموعة 2 من خلال الحجر الجيري أو الجبس أو المغنيسيوم المستخلص من ماء البحر أو الباريت أو الكالسيوم البيولوجي، وليس من خلال عينات المعادن النقية. وهذه التفصيلة مهمة، لأن الأهمية الواقعية لهذه العناصر ترتبط إلى حدٍّ بعيدٍ بمركباتها وأشكالها أكثر مما ترتبط بالمعادن النقية نفسها.
أمثلة على الفلزات القلوية الترابية في الحياة اليومية
تصبح المجموعة 2 أكثر قابلية للتذكُّر عندما تربط كل عنصرٍ منها بشيءٍ ملموسٍ في الواقع: مثل العظام، ومضادات الحموضة، والجبس، والألعاب النارية، وسوائل الحفر، والأقراص المضيئة القديمة — وكلُّها أمثلة مفيدة. أمثلة على الفلزات القلوية الترابية إذا سبق لك أن تساءلت هل المغنيسيوم فلز أم غير فلز؟ أو هل الرمز Ca يدل على فلز؟ فالإجابتان بسيطتان: المغنيسيوم والكالسيوم كلاهما فلزان. ومع ذلك، فإن الناس في الحياة العادية يصادفون هذين العنصرين عادةً على شكل مركباتٍ، وليس كعيناتٍ من المعادن النقية.
الاستخدامات اليومية لمركبات المغنيسيوم والكالسيوم
- المغنيسيوم : يُعَدُّ المغنيسيوم أحد أهم العناصر من الناحية البيولوجية عناصر الأرض القلوية . الـ ورقة حقائق المغنيسيوم من المعهد الوطني للصحة (NIH) ويشير إلى أن المغنيسيوم يعمل كعامل مساعد في أكثر من ٣٠٠ نظام إنزيمي، ويدعم وظائف العضلات والأعصاب وإنتاج الطاقة وهيكل العظام. كما تظهر مركبات المغنيسيوم في بعض مضادات الحموضة والمليّنات، بينما يُقدَّر المغنيسيوم المعدني لاستخدامه في السبائك خفيفة الوزن حيث يكتسب تقليل الكتلة أهمية بالغة.
- كالسيوم تسيطر مركبات الكالسيوم على الحياة اليومية. فالكالسيوم يساهم في إعطاء العظام والأسنان هيكلها، وتشكل مركبات مثل كربونات الكالسيوم وكبريتات الكالسيوم جوهر الحجر الجيري والإسمنت والجبس والجص الجاف. وهذا يجعل الكالسيوم أحد أوضح الروابط بين الكيمياء والبيولوجيا والبناء.
تطبيقات متخصصة للسترونتيوم والباريوم
- السترونتيوم وتُعرف أملاح السترونتيوم بأفضل طريقة لإنتاج الألوان الحمراء الداكنة في الألعاب النارية وأضواء الإشارات التحذيرية. بل حتى القرّاء الذين لا يتذكرون قائمة عناصر المجموعة الثانية كاملةً غالبًا ما يتذكرون السترونتيوم بمجرد ربطه بلون معين.
- الباريوم تلعب مركبات الباريوم دورًا مهمًّا في المجالات الصناعية والطبية. ويُشار إلى أن ملف الباريوم من المكتبة الوطنية للطب (NLM) يصف الاستخدامات الرئيسية له في طين الحفر والدهانات والبلاستيكيات والطوب والزجاج. كما يشير إلى تباين طبي مهم: كبريتات الباريوم شديدة الانحلال تُستخدم كمادة معتمة للأشعة السينية في بعض الفحوصات بالأشعة السينية لأنها لا تمتص عادةً من قِبل الجسم.
- الراديوم : الراديوم هو في الغالب حالة تاريخية أو خاضعة للرقابة العلمية المشددة. صفحة الراديوم في لجنة تنظيم الطاقة النووية (NRC) تشرح استخدامه السابق في الدهانات المضيئة والعلاج المبكر للسرطان. وقد استُبدلت معظم تلك الاستخدامات، رغم أن بعض الاستخدامات الخاضعة للتنظيم ما زالت قائمة، مثل بعض تطبيقات التصوير الإشعاعي الصناعي.
لماذا يهم الشكل ونوع المركب في الاستخدام الفعلي
في المجموعة الثانية، يكون الشكل الذي يستخدمه الناس غالبًا هو المركب وليس المعدن النقي.
هذه الفكرة الوحيدة تُزيل الكثير من الالتباس. فالمغنيسيوم الموجود في الأغذية أو الأدوية ليس هو نفسه المغنيسيوم الذي يحترق على هيئة شريط. والكالسيوم الموجود في العظام ليس هو نفسه معدن الكالسيوم النشط كيميائيًّا. أما الباريوم فهو أوضح مثالٍ على أهمية الشكل: إذ يمكن أن يكون كبريتات الباريوم غير القابلة للذوبان مفيدة في التصوير الطبي، بينما تتطلب المركبات الأخرى الأكثر قابليةً للذوبان احتياطاتٍ أكبر بكثير. ويُبرز الراديوم هذه النقطة أكثر فأكثر، لأن طبيعته المشعة — وليس فقط موقعه بين الفلزات — هي التي تحدد كيفية التعامل معه.
وبالتالي فإن قيمة عناصر المجموعة الثانية ليست مجردةً على الإطلاق. فهذه العناصر تساعد في توضيح كيف يمكن لعائلة واحدة أن تلعب دورًا مهمًّا في التغذية والمواد والطب ومعالجة الصناعات والقواعد التنظيمية الخاصة بالسلامة. وكثيرًا ما يكفي سردٌ موجزٌ للاستخدامات الحقيقية لكي يترسخ النمط الأوسع في الذهن.
أبرز الاستنتاجات حول عناصر المجموعة الثانية
بحلول هذه المرحلة، يجب أن تبدو فلزات الأرض القلوية أقل ما تكون كقائمةٍ تحتاج إلى حفظها عن ظهر قلب، وأكثر ما تكون كنمطٍ يمكنك قراءته مباشرةً من المجموعة الثانية في الجدول الدوري العمود. فإذا ما سأل شخصٌ ما بعد ذلك: ما هي العناصر القلوية الترابية؟ والإجابة المختصرة تبقى بسيطة: البريليوم، والمغنيسيوم، والكالسيوم، والاسترونتيوم، والباريوم، والراديوم. أما التعريف الأشمل للعناصر القلوية الترابية فهو أكثر فائدة: وهي ستة عناصر معدنية تقع في المجموعة 2، وتفقد عادةً إلكترونين من مستوياتها الخارجية لتكوين أيونات ذات شحنة موجبة مقدارها +2 (أيونات M²⁺). تعريف العناصر القلوية الترابية 2+²⁺.
أبرز الاستنتاجات حول العناصر القلوية الترابية
- الموقع يهم: هذه الستة عناصر المجموعة 2 تقع في العمود الثاني من اليسار، أي في قسم المجموعة 2 ضمن الكتلة s.
- الأعضاء العائلية ثابتون: تتكوّن المجموعة الكاملة من العناصر: Be، Mg، Ca، Sr، Ba، وRa.
- يُفسِّر التشابه الكيميائي المشترك أوجه التشابه العائلية: إلكتروناتها في الغلاف ns 2ويؤدي نمط التكافؤ الخاص بها إلى تكوين أيونات ذات شحنة +2 كنتيجة شائعة، وهي نقطة جوهرية يلخّصها موقع LibreTexts.
- الاتجاهات الرئيسية نحو الأسفل قابلة للتنبؤ بها: يزداد نصف القطر الذري، وتنخفض طاقة التأين عمومًا، وتزداد النشاطية عادةً كلما انتقلنا نحو الأسفل في المجموعة.
- الاستثناءات لها أهميتها: فإن البريليوم يتصرّف بشكل أكثر تساهميًّا مقارنةً بالعناصر الأخرى، وقد يبدو المغنيسيوم أقل تفاعليةً بسبب طبقته السطحية، أما الراديوم فيتم مناقشته غالبًا من خلال خاصية الإشعاعية.
- وفي الحياة الواقعية، فإن المقصود عادةً هو المركبات وليس الفلزات النقية: يصادف الناس كربونات الكالسيوم وأكسيد المغنيسيوم وكبريتات الباريوم بشكلٍ أكثر بكثيرٍ من العناصر النقية كالسيوم ومغنيسيوم وباريوم.
الأنابيب الجدول الدوري للمعادن القلوية الترابية العمود الأيسر أسهل ما يكون تذكّره على أنه يضم ستة معادن تربطها قاعدة واحدة: فهي تتحول عادةً إلى أيونات ذات شحنة موجبة مقدارها +2، لكن كل عنصرٍ منها يعبّر عن هذه القاعدة بطريقةٍ مختلفةٍ قليلًا.
من كيمياء المجموعة الثانية إلى الأجزاء المعدنية المصمَّمة هندسيًّا
وتتجاوز هذه الكيمياء نطاق الكتب الدراسية بكثير. وتلاحظ منصة LibreTexts أن المغنيسيوم العنصري يُنتَج على نطاقٍ واسع ويُستخدَم في سبائك خفيفة الوزن لإطارات الطائرات وأجزاء محركات السيارات. كما يوضح دليل أوسع عن السبائك أهمية ذلك: إذ يقوم المهندسون بتعديل التركيب والمعالجة لتحقيق توازنٍ بين الوزن والمتانة ومقاومة التآكل وسهولة التشغيل في المكونات الفعلية.
للقارئين الذين ينتقلون من المجموعة الثانية في الجدول الدوري المنظور إلى التصنيع، تكنولوجيا المعادن شاوي يي يقدّم مثالاً عمليًّا على تلك العلاقة. فصفحات المواد والتشغيل الآلي الخاصة بالسيارات تصف إنتاج الأجزاء المعدنية، بدءًا من النماذج الأولية وصولًا إلى الإنتاج الضخم، حيث يجب أن تعمل سلوك المواد والتحكم في العمليات معًا. الجدول الدوري للمعادن القلوية الترابية أكثر من مجرد مخطط دراسي. بل هو أيضًا جزءٌ من المنطق الكامن وراء اختيار المعادن والسبائك للأجزاء الهندسية التي تحتاج إلى أن تكون خفيفة الوزن، وموثوقة، وقابلة للتصنيع.
أسئلة شائعة حول عناصر المجموعة الثانية القلوية الترابية
١. ما هي العناصر الستة القلوية الترابية؟
العناصر الستة القلوية الترابية هي البريليوم والمغنيسيوم والكالسيوم والاسترونشيوم والباريوم والراديوم. وهي تشغل المجموعة ٢ في الجدول الدوري، وتُجمَع معًا لأنها تفقد عادةً إلكترونين من مستوياتها الخارجية، مما يؤدي إلى نمط مشترك لتكوين أيونات ذات شحنة موجبة مقدارها +٢ في العديد من المركبات.
٢. ما الفرق بين العناصر القلوية الترابية والعناصر القلوية؟
الفلزات القلوية تنتمي إلى المجموعة 1 وتشكّل عادةً أيونات ذات شحنة موجبة واحدة (+1) لأنها تحتوي على إلكترون واحد في غلافها الخارجي. أما الفلزات القلوية الترابية فهي موجودة في المجموعة 2، وتشكّل عادةً أيونات ذات شحنة موجبة ثنائية (+2)، وتكون عمومًا أقل تفاعلًا. فهذا الإلكترون التكافؤي الإضافي الواحد يغيّر قوة الروابط التي تشكّلها، وكيفية تفاعلها مع الماء، وأنواع الأملاح والأكاسيد التي تكوّنها عادةً.
3. لماذا لا توجد الفلزات القلوية الترابية في الطبيعة على هيئة عناصر حرة؟
هذه الفلزات نشيطـةٌ بما يكفي لكي لا تبقى لفترة طويلة على هيئة عناصر نقية في البيئات الطبيعية. بل إنها تتحد عادةً مع أيونات الأكسجين أو الكربونات أو الكبريتات أو الكلوريدات أو السيليكات لتُكوّن جزءًا من المعادن والصخور ومياه البحار والقواقع والعظام. ولذلك فإن الناس يصادفون عادةً عناصر المجموعة 2 على هيئة مركباتٍ بدلًا من عينات معدنية خام.
4. هل تتفاعل جميع الفلزات القلوية الترابية مع الماء؟
لا، وهذه واحدة من أكثر الاستثناءات فائدةً التي يجب تذكّرها. فالبريليوم مقاومٌ إلى حدٍ كبيرٍ للماء، أما المغنيسيوم فيتفاعل ببطءٍ مع الماء البارد بسبب طبقة سطحية تحدّ من التفاعل، بينما تتفاعل الكالسيوم والسترونتيوم والباريوم بشكلٍ أسرع. وبشكلٍ عامٍّ، تزداد قوة تفاعل العناصر مع الماء كلما انتقلنا نحو الأسفل في المجموعة الثانية.
5. لماذا تكتسب الفلزات القلوية الترابية أهميةً في الصناعة والتصنيع؟
تنبع أهميتها من مركباتها ومن دورها في اختيار السبائك. فالمغنيسيوم ذو قيمةٍ كبيرةٍ في التطبيقات التي تتطلب خفة الوزن، ومركبات الكالسيوم تشكّل العمود الفقري لصناعة الإسمنت والجبس، بينما تُستخدم مركبات الباريوم في تطبيقات صناعية وطبية متخصصة. وفي الإنتاج الفعلي، يساعد فهم سلوك الفلزات في توجيه عمليات التشغيل الآلي واستقرار العمليات وجودة الأجزاء، ولذلك تُبرز شركات التوريد مثل «شاوي ميتال تكنولوجي» (Shaoyi Metal Technology) قدرتها على تشغيل أجزاء السيارات وفق شهادات معتمدة، والتحكم في العمليات، والدعم المقدَّم بدءًا من الأجزاء النموذجية وحتى الإنتاج الضخم.
 دُفعات صغيرة، معايير عالية. خدمتنا لتطوير النماذج الأولية بسرعة تجعل التحقق أسرع وأسهل —
دُفعات صغيرة، معايير عالية. خدمتنا لتطوير النماذج الأولية بسرعة تجعل التحقق أسرع وأسهل —
