Kim Loại Kiềm Thổ Là Gì? Nhóm 2 Cuối Cùng Đã Rõ Ràng
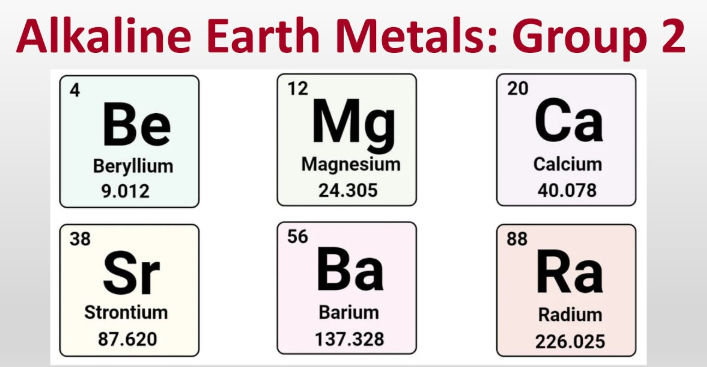
Kim loại kiềm thổ là gì?
Nếu bạn đã tìm kiếm kim loại kiềm thổ là gì , đây là câu trả lời trực tiếp: chúng là sáu nguyên tố trong Nhóm 2 của bảng tuần hoàn. Định nghĩa ngắn gọn này về kim loại kiềm thổ là điểm khởi đầu, nhưng tên gọi cũng phần nào cho biết cách cả nhóm nguyên tố này phản ứng. tên gọi 'kim loại kiềm thổ' cũng phần nào cho biết cách cả nhóm nguyên tố này phản ứng.
Kim loại kiềm thổ là gì — trong một câu
Kim loại kiềm thổ gồm berili, magiê, canxi, stronti, bari và radi — sáu nguyên tố kim loại thuộc Nhóm 2, thường tạo thành ion mang điện tích +2.
- Berili (Be)
- Magiê (Mg)
- Canxi (Ca)
- Strontium (Sr)
- Bari (Ba)
- Radi
Tại sao tên gọi kim loại kiềm thổ lại hợp lý
Đối với người mới bắt đầu, khái niệm kim loại kiềm thổ sẽ dễ hiểu hơn nhiều khi bạn chia cụm từ này thành ba phần.
Kiềm có nghĩa là các oxit và hiđroxit của chúng mang tính bazơ, không phải tính axit. Trái Đất là một thuật ngữ mang tính lịch sử. Các nhà hóa học thời kỳ đầu dùng từ này để chỉ những chất khoáng bền nhiệt, có dạng khoáng chất và không dễ nóng chảy hay tan trong nước, một điểm được giải thích bởi Britannica . Kim loại có nghĩa là bản thân các nguyên tố này mang tính kim loại, thường có ánh kim và dễ mất electron trong các phản ứng.
Điều đó giúp bạn nắm được khái niệm cơ bản về kim loại kiềm thổ mà không cần phải học hóa học nâng cao trước tiên. Đây cũng là một mô tả ngắn hữu ích về các kim loại kiềm thổ : một họ kim loại thuộc nhóm 2, có chung tính chất hóa học, cùng vị trí trên bảng tuần hoàn và đóng vai trò quan trọng trong đời sống thực tiễn. Magie xuất hiện trong các hợp kim và trong sinh học. Canxi đóng vai trò thiết yếu trong cấu tạo xương, vỏ động vật và vật liệu xây dựng. Bari, stronti và radi xuất hiện trong các ngữ cảnh chuyên biệt hơn.
Bài viết này bắt đầu từ những khái niệm đơn giản một cách có chủ đích. Một danh sách rõ ràng sẽ dễ ghi nhớ, nhưng sự liên hệ giữa các thành viên trong họ này thực sự trở nên rõ ràng khi bạn nhìn thấy vị trí của chúng trên bảng tuần hoàn và hiểu vì sao vị trí đó lại khiến chúng có tính chất tương tự nhau đến vậy.
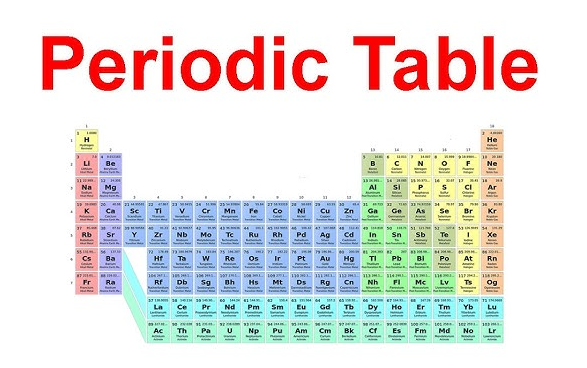
Vị trí của Nhóm 2 trên Bảng tuần hoàn
Tên gọi của họ nguyên tố sẽ dễ ghi nhớ hơn nhiều khi bạn thực sự có thể xác định được vị trí của nó. Nếu bạn đang thắc mắc kim loại kiềm thổ nằm ở đâu trên bảng tuần hoàn , hãy nhìn vào cột thứ hai tính từ bên trái. Cột dọc này chính là nhóm 2 trên bảng tuần hoàn , nằm ngay sát bên cạnh các kim loại kiềm ở nhóm 1. A nhóm 2 bảng tuần hoàn hình ảnh cho thấy cùng một đường thẳng mỗi lần: berili ở trên cùng, sau đó là magiê, canxi, stronti, bari và radi đi xuống theo các chu kỳ.
Trong một bảng tuần hoàn các kim loại kiềm thổ biểu đồ, sáu nguyên tố này thuộc khối s. Vị trí chung của chúng có ý nghĩa vì phản ánh một mô hình cấu hình electron giống nhau. Như LibreTexts giải thích, các nguyên tố nhóm 2 có cấu hình 2lớp ngoài cùng dạng ns², nghĩa là chúng có hai electron ở lớp ngoài cùng.
Vị trí của các kim loại kiềm thổ trên bảng tuần hoàn
Về mặt trực quan, quy luật này rất đơn giản. Các nguyên tố nhóm 2 bảng tuần hoàn tạo thành một cột họ duy nhất trải dài từ chu kỳ 2 đến chu kỳ 7. Nhiều sơ đồ dùng trong lớp học làm nổi bật điều này kim loại kiềm thổ trong bảng tuần hoàn bố trí với cùng một màu vì các họ nguyên tố được đọc theo chiều dọc, không phải theo chiều ngang. Các truy vấn tìm kiếm bảng tuần hoàn kim loại kiềm thổ thực chất đang yêu cầu cột cụ thể đó.
| Element | Biểu tượng | Vị trí nhóm 2 | Ion điển hình | Hợp chất quen thuộc |
|---|---|---|---|---|
| Berili | Be | Chu kỳ 2, đầu nhóm 2 | Be2+ | BeO |
| Magie | Mg | Chu kỳ 3 | Mg2+ | MgO |
| Canxi | Ca | Chu kỳ 4 | Ca2+ | CaCO 3 |
| Stronti | Sr | Chu kỳ 5 | Sr2+ | SrCO 3 |
| Bari | BA | Chu kỳ 6 | BA 2+ | BaSO 4 |
| Radi | RA | Chu kỳ 7, cuối nhóm 2 | RA 2+ | RaCl 2 |
Lý do các nguyên tố nhóm 2 tạo thành ion mang điện tích dương hai
Hai electron ngoài cùng này chi phối tính chất hóa học. Các nguyên tử nhóm 2 có xu hướng mất cả hai electron vì điều đó giúp chúng đạt được cấu hình electron ổn định hơn. Kết quả là một +2 ion , chẳng hạn như Mg 2+ hoặc Ca 2+. Đó là lý do vì sao các kim loại này thường tạo thành các hợp chất như oxit, clorua, cacbonat và sunfat. Bạn có thể nhận ra ngay quy luật trong công thức: MgO, CaCl 2, CaCO 3, BaSO 4.
Cách nhận diện nhanh họ kim loại kiềm thổ
Một mẹo nhận dạng nhanh là đồng thời tìm ba dấu hiệu: nằm ở cột thứ hai, là các nguyên tố kim loại và thường mang điện tích +2. So với các kim loại kiềm lân cận — vốn có một electron lớp ngoài cùng và thường tạo thành ion +1 — thì các nguyên tố nhóm 2 có thêm một electron lớp ngoài cùng và nói chung ít phản ứng hơn. Dẫu vậy, chúng rõ ràng thuộc cùng một họ. Điều thú vị là mỗi thành viên biểu hiện quy luật này theo một cách hơi khác nhau, đặc biệt từ berili ở đầu dãy đến radi ở cuối dãy.
Sáu kim loại kiềm thổ
Một danh sách thì hữu ích, nhưng bản thân nó lại không dễ ghi nhớ lắm. Nhóm 2 bắt đầu trở nên chân thực hơn khi mỗi thành viên đều có bản sắc riêng rõ ràng. Một số xuất hiện trong xương hoặc nước biển. Một số tạo màu cho pháo hoa. Một nguyên tố chủ yếu là dấu hiệu cảnh báo mang tính lịch sử. Dù vậy, tất cả vẫn thuộc cùng một họ hóa học, nhưng mỗi nguyên tố lại có tính cách riêng.
| Element | Biểu tượng | Xuất hiện phổ biến | Tính chất nổi bật | Tính thực tiễn ngoài thực tế |
|---|---|---|---|---|
| Berili | Be | Có trong các khoáng vật như beryl | Rất nhẹ và cứng đối với một kim loại | Được sử dụng trong các ứng dụng chuyên biệt về hàng không vũ trụ và tia X; bụi của nó nguy hiểm nếu hít phải |
| Magie | Mg | Có mặt trong nước biển và các khoáng vật | Khối lượng riêng thấp và cháy với ngọn lửa trắng sáng | Quan trọng trong các hợp kim nhẹ, thực phẩm bổ sung và sinh học |
| Canxi | Ca | Phổ biến trong đá vôi, xương, vỏ sò và phấn viết bảng | Ion nhóm 2 quen thuộc về mặt sinh học | Thành phần thiết yếu trong khung xương, xi măng, thạch cao và nhiều khoáng chất tự nhiên |
| Stronti | Sr | Chủ yếu tìm thấy trong celestite và strontianite | Các muối tạo ra màu đỏ rực rỡ khi đốt trong ngọn lửa | Được sử dụng trong pháo hoa, đèn hiệu, vật liệu phát quang và một số sản phẩm nha khoa |
| Bari | BA | Thường đi kèm với barit | Kim loại kiềm thổ nặng, có mật độ cao | Bari sulfat đóng vai trò quan trọng trong khoan dầu và chẩn đoán hình ảnh y tế; các hợp chất bari tan trong nước đòi hỏi phải thận trọng |
| Radi | RA | Xuất hiện ở hàm lượng vết trong quặng urani | Tính phóng xạ mạnh chi phối toàn bộ câu chuyện hóa học của nó | Chủ yếu mang tính lịch sử hoặc có liên quan khoa học bị kiểm soát chặt chẽ ngày nay |
Berili và magiê ở đầu Nhóm 2
Các nguyên tố berili nằm ở vị trí đầu tiên trong họ nguyên tố và đã phần nào cho thấy Nhóm 2 không hoàn toàn đồng nhất. Nguyên tố này thường được liên kết với khoáng vật beryl—cùng một họ khoáng vật bao gồm ngọc lục bảo và ngọc biển xanh. Berili nổi bật nhờ đặc tính bất thường là rất nhẹ và cứng. Điều này khiến nó hữu ích trong các bộ phận hiệu suất cao, nơi khối lượng thấp là yếu tố quan trọng. Đồng thời, berili là một vật liệu đòi hỏi sự cẩn trọng trong môi trường công nghiệp, bởi vì bụi mịn của nó có thể gây hại nếu hít phải. Vì vậy, berili vừa được ghi nhớ nhờ hiệu năng vượt trội, vừa được nhắc đến như một vật liệu cần thận trọng khi xử lý.
Magiê mang cảm giác quen thuộc hơn nhiều. ký hiệu hóa học của magiê là Mg, và đây là một trong những kim loại nổi tiếng nhất trong nhóm này vì nó xuất hiện trong nước biển, các khoáng chất phổ biến và các hệ thống sống. Đây là một kim loại rất nhẹ, và khi cháy sẽ phát ra ánh sáng trắng mạnh. Vì lý do này, magiê từ lâu đã được liên hệ với các loại pháo hiệu và vật liệu cháy sáng. Tuy nhiên, trong đời sống hằng ngày, đa số mọi người tiếp xúc với magiê ở những dạng ôn hòa hơn, chẳng hạn như vai trò dinh dưỡng, các hợp chất kháng axit hoặc các hợp kim nhẹ được sử dụng ở những nơi yêu cầu giảm khối lượng.
Canxi và stronti trong các vật liệu thường ngày
Canxi là thành viên nhóm 2 dễ nhận biết nhất đối với nhiều độc giả. Nó xuất hiện trong đá vôi, phấn, vỏ sò và xương, do đó ngay lập tức kết nối hóa học với cả địa chất và sinh học. Canxi cacbonat là hợp chất quen thuộc ở đây. Hợp chất này giúp giải thích vì sao cùng một họ nguyên tố lại có vai trò quan trọng trong việc hình thành hang động, đá xây dựng và bộ xương. Bản thân kim loại canxi khá phản ứng, nhưng các hợp chất canxi thì có mặt ở khắp nơi, chính vì vậy nguyên tố này thường mang cảm giác quen thuộc hơn là xa lạ.
Stronti dễ ghi nhớ hơn khi bạn liên kết nó với màu sắc. ký hiệu của stronti là Sr, và stronti được tìm thấy chủ yếu trong các khoáng vật celestite và strontianite. Hiệp hội Hóa học Hoàng gia mô tả stronti là một kim loại mềm, có màu bạc, cháy trong không khí và phản ứng với nước. Các muối của nó nổi tiếng vì tạo ra màu đỏ rực rỡ trong pháo hoa và đèn hiệu. Nguồn tài liệu trên cũng nêu rõ các ứng dụng khác của stronti trong các vật liệu phát quang trong bóng tối và stronti clorua hexahydrat trong kem đánh răng dành cho người có răng nhạy cảm. Điều này khiến stronti trở thành một ví dụ điển hình về cách một nguyên tố có thể phản ứng hóa học mạnh nhưng phần lớn lại được con người tiếp xúc thông qua các hợp chất của nó.
Bari và radi trong các bối cảnh nâng cao hoặc chuyên biệt
Các nguyên tố bari thường được nhớ đến qua độ nặng. Nó thường được liên kết với barit, và một trong những hợp chất quen thuộc nhất của nó là bari sunfat. Hợp chất này có ý nghĩa quan trọng vì nó rất khó tan, điều này giúp giải thích lý do vì sao bari có thể xuất hiện trong các ứng dụng thực tiễn như dung dịch khoan và hình ảnh y khoa, trong khi các hợp chất bari tan khác lại được xử lý cẩn trọng hơn do lo ngại về tính độc hại. Bari nhắc nhở người đọc rằng dạng hữu ích của một nguyên tố nhóm 2 thường là một hợp chất, chứ không phải kim loại sáng bóng ở dạng nguyên chất.
Radi nằm ở cuối họ nguyên tố này, nhưng nó không hòa nhập một cách lặng lẽ. Trên một bảng tuần hoàn radi xem xét, Ra đánh dấu điểm mà tính phóng xạ trở thành đặc điểm nổi bật nhất. Radium chỉ tồn tại tự nhiên ở lượng rất nhỏ, thường đi kèm với quặng urani. Trong lịch sử, nguyên tố này nổi tiếng nhờ sơn phát quang và các thí nghiệm y học đầu tiên. Ngày nay, mối nguy hiểm của nó bắt nguồn từ tính phóng xạ chứ không phải từ tính chất kim loại thông thường, do đó việc xử lý radium được thực hiện dưới sự kiểm soát nghiêm ngặt. Nói một cách đơn giản, radium vẫn thuộc Nhóm 2, nhưng khi thảo luận về nó, người ta chú trọng đến an toàn hạt nhân không kém phần hóa học.
Đặt sáu nguyên tố này cạnh nhau, cả họ sẽ không còn trông giống một danh sách trống rỗng gồm những cái tên. Kích thước, tính phản ứng, các hợp chất phổ biến, thậm chí cả cách mỗi nguyên tố xuất hiện trong đời sống đều thay đổi khi di chuyển xuống dưới trong nhóm. Chính sự thay đổi theo chiều dọc này khiến Nhóm 2 trở nên đặc biệt hữu ích, bởi thứ tự từ berili đến radium bắt đầu hé lộ những xu hướng rõ ràng thay vì chỉ là những chi tiết rời rạc.
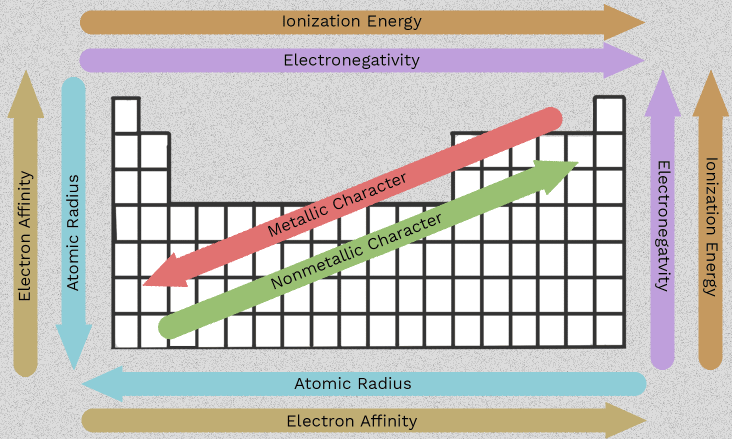
Tính chất của các kim loại kiềm thổ và các xu hướng trong Nhóm 2
Việc thay đổi thứ tự từ berili đến radi là yếu tố làm cho Nhóm 2 trở nên hữu ích. Thay vì ghi nhớ sáu sự kiện riêng lẻ, bạn có thể theo dõi một vài xu hướng lặp lại dọc theo cột. Điều quan trọng nhất tính chất của các kim loại kiềm thổ đều bắt nguồn từ một đặc điểm chung duy nhất: mỗi nguyên tử đều có hai electron ở lớp ngoài cùng mà chúng có xu hướng mất đi.
Khi bạn hiểu được cách kích thước nguyên tử, hiệu ứng che chắn electron và năng lượng ion hóa thay đổi khi đi xuống nhóm, toàn bộ họ nguyên tố này sẽ dễ dự đoán hơn nhiều. Những đặc điểm của các kim loại kiềm thổ không chỉ là những kiến thức để thi cử. Chúng giải thích vì sao một số thành viên phản ứng nhanh hơn, vì sao một số hợp chất tan tốt hơn những hợp chất khác, và vì sao một vài xu hướng đòi hỏi cách diễn đạt cẩn trọng thay vì chỉ dùng các mũi tên đơn giản.
Các tính chất chung của kim loại kiềm thổ
Hầu hết các thành viên của Nhóm 2 đều là kim loại màu bạc thường tạo thành các ion M 2+các ion và tạo thành chủ yếu các hợp chất ion. Chúng hoạt động như các chất khử vì mất electron. So với kim loại nhóm 1, chúng thường kém phản ứng hơn, nhưng vẫn đủ hoạt động về mặt hóa học để tạo thành nhiều oxit, clorua, cacbonat và sunfat phổ biến.
Một cách đơn giản để sắp xếp các tính chất hóa học của kim loại kiềm thổ là tách biệt những yếu tố không đổi với những yếu tố thay đổi. Yếu tố không đổi là trạng thái oxi hóa thông thường +2. Yếu tố thay đổi là mức độ dễ dàng mà mỗi nguyên tố nhường hai electron đó. Chính tại đây, các xu hướng bắt đầu có ý nghĩa.
Xu hướng xuống dưới nhóm 2 và ý nghĩa của chúng
Dữ liệu được LibreTexts thu thập và giải thích xu hướng từ Save My Exams cho thấy cùng một mô hình tổng thể. Bán kính nguyên tử tăng từ 112 pm đối với Be lên 253 pm đối với Ba, trong khi năng lượng ion hóa thứ nhất giảm từ 900 xuống 503 kJ/mol. Nói một cách đơn giản, các electron ngoài cùng nằm xa hạt nhân hơn và bị che chắn bởi nhiều lớp vỏ bên trong hơn, do đó dễ bị loại bỏ hơn.
| Xu hướng | Chiều hướng xuống dưới nhóm 2 | Lý do hóa học | Điều Này Có Nghĩa Gì Trong Thực Tế |
|---|---|---|---|
| Bán kính nguyên tử | Tăng cường | Mỗi nguyên tố có thêm một lớp electron và nhiều hiệu ứng che chắn hơn | Các nguyên tử lớn hơn giữ các electron ở lớp ngoài kém chặt hơn |
| Năng lượng ion hóa thứ nhất và thứ hai | Giảm tổng thể | Các electron ngoài xa hạt nhân hơn nên lực hút yếu hơn | Hình thành ion M 2+trở nên dễ dàng hơn |
| Phản ứng | Tăng tổng thể | Năng lượng ion hóa thấp hơn làm cho việc mất electron dễ dàng hơn | Các nguyên tố nặng hơn phản ứng mạnh hơn với axit, oxy và thường cả nước |
| Điểm nóng chảy | Giảm nói chung, nhưng không giảm một cách đều đặn | Các ion kim loại có kích thước lớn hơn làm suy yếu liên kết kim loại, dù cấu trúc cũng đóng vai trò quan trọng | Dùng từ "nói chung" ở đây vì Mg và Ca không nằm chính xác trên một đường thẳng hoàn hảo |
| Mật độ | Không đều | Khối lượng, kích thước nguyên tử và cách sắp xếp các nguyên tử kim loại đều thay đổi đồng thời | Bạn không thể coi mật độ như một xu hướng giảm đơn giản theo một chiều |
| Độ tan của hiđroxit | Tăng cường | Sự cân bằng giữa năng lượng mạng tinh thể và năng lượng thủy hóa thay đổi khi đi xuống nhóm | Các hiđroxit nặng hơn tạo thành các dung dịch kiềm mạnh hơn |
| Độ tan của sunfat | Giảm xuống | Năng lượng hydrat hóa giảm khi cation trở nên lớn hơn | Các hợp chất như BaSO 4trở nên rất ít tan |
Mật độ và hành vi nóng chảy là hai xu hướng mà học sinh thường đơn giản hóa quá mức. Mật độ không thay đổi theo một đường thẳng vì cả khối lượng lẫn thể tích đều đang thay đổi, đồng thời các nguyên tử kim loại không xếp chồng theo cùng một cách trong mọi tinh thể. Điểm nóng chảy cũng cần được xem xét cẩn thận. Nhìn chung, điểm nóng chảy có xu hướng giảm dần do các ion lớn hơn làm suy yếu mạng tinh thể kim loại, nhưng Mg lại có điểm nóng chảy bất thường thấp chỉ 650 °C, trong khi Ca tăng lên 842 °C trước khi giá trị này lại giảm tiếp. Vì vậy, một trong những đặc điểm an toàn nhất của các kim loại kiềm thổ là điều sau: xu hướng tổng quát là có thật, nhưng các chi tiết vật lý lại không hoàn toàn trơn tru.
Độ tan cũng mang nhãn cảnh báo tương tự. Không tồn tại một quy tắc duy nhất nào áp dụng cho mọi muối nhóm 2. Các hiđroxit trở nên dễ tan hơn khi đi xuống nhóm, trong khi các sunfat lại trở nên ít tan hơn. Nếu ai đó nói rằng "độ tan tăng khi đi xuống nhóm 2", thì câu hỏi quan trọng cần đặt ra là: "Các hợp chất nào?"
Tại sao các kim loại kiềm thổ phản ứng theo cách chúng làm
Vậy, các kim loại kiềm thổ có phản ứng không ? Có, và câu trả lời chung là độ phản ứng của chúng tăng lên khi di chuyển xuống dưới trong nhóm. Lý do cũng giống như câu chuyện về electron đã nêu ở trên. Năng lượng ion hóa thứ nhất và thứ hai thấp hơn nghĩa là các nguyên tử có thể mất hai electron dễ dàng hơn và đạt trạng thái M 2+nhanh hơn.
Điều này ảnh hưởng đến các phản ứng thực tế. Khi đi xuống nhóm, tốc độ phản ứng với axit loãng tăng lên, phản ứng với oxi trở nên mạnh mẽ hơn và các nguyên tố nặng hơn dễ bị oxi hóa hơn. Ghi chú từ Save My Exams chỉ ra rằng bari phản ứng đủ mạnh để được bảo quản dưới dầu — đây là một dấu hiệu thực tiễn cho thấy xu hướng phản ứng có thể kéo dài đến mức nào.
- Bán kính nguyên tử tăng dần khi đi xuống Nhóm 2.
- Năng lượng ion hóa giảm dần khi đi xuống Nhóm 2.
- Độ phản ứng tăng lên vì việc mất hai electron trở nên dễ dàng hơn.
- Nhiệt độ nóng chảy và khối lượng riêng cho thấy những ngoại lệ, do đó cần tránh thiết lập các quy tắc tuyệt đối.
- Các hiđroxit và sunfat thể hiện xu hướng độ tan ngược nhau.
Những đặc điểm này khiến nhóm kim loại kiềm thổ trở nên dễ dự đoán, nhưng không hoàn toàn đồng nhất. Ngay gần đầu nhóm, berili đã bắt đầu vi phạm các quy luật chung, và magie tạo thêm một ngoại lệ thường gặp khác — điều này quan trọng hơn nhiều so với những gì người mới học thường tưởng.
Kim loại kiềm và kim loại kiềm thổ
Các xu hướng tổng quát giúp việc học Nhóm 2 trở nên dễ dàng hơn, nhưng nhóm sẽ mất đi tính logic nếu coi mọi thành viên đều giống nhau. Dấu hiệu cảnh báo rõ ràng nhất chính là berili. Magie bổ sung một ngoại lệ thực tiễn và thường gặp hơn. Và khi mọi người so sánh kim loại kiềm và kim loại kiềm thổ , những cái tên tương tự có thể che giấu những khác biệt rất lớn về mặt hóa học.
Tại sao berili lại không thể hiện tính chất của một kim loại điển hình thuộc Nhóm 2
BYJU'S mô tả berili là thành viên nổi bật nhất (ngoại lệ rõ rệt nhất) trong Nhóm 2. Kích thước bất thường nhỏ, năng lượng ion hóa cao và khả năng phân cực mạnh khiến nó thể hiện hành vi ít mang tính đặc trưng của nhóm hơn. Nói một cách đơn giản, Be 2+kéo mạnh các đám mây electron lân cận, do đó các hợp chất berili thường mang tính cộng hóa trị nhiều hơn so với các hợp chất mang tính ion hơn được tạo thành bởi các nguyên tố nặng hơn trong cùng nhóm. Nguồn tài liệu trên cũng lưu ý rằng berili có nhiệt độ nóng chảy và nhiệt độ sôi cao hơn so với các nguyên tố còn lại trong nhóm và không phản ứng với nước như những nguyên tố anh em của nó.
Magie không kỳ lạ như berili, nhưng vẫn có thể trông kém phản ứng hơn mức học sinh dự kiến. LibreTexts ghi nhận rằng magie cực kỳ sạch chỉ phản ứng nhẹ với nước lạnh, và phản ứng nhanh chóng chậm lại do magie hiđroxit gần như không tan hình thành một lớp màng chắn trên bề mặt. Ở cuối nhóm, radi thường được thảo luận riêng biệt vì tính phóng xạ của nó chi phối các vấn đề liên quan đến ứng dụng thực tiễn và an toàn.
Sự khác biệt giữa kim loại kiềm thổ và kim loại kiềm
Đơn giản kiềm so với kiềm thổ nói, các kim loại nhóm 1 mất một electron ở lớp ngoài cùng, trong khi các kim loại nhóm 2 mất hai electron. Sự khác biệt duy nhất này ảnh hưởng đến tính chất của kim loại kiềm và kim loại kiềm thổ nhiều hơn bất cứ yếu tố nào khác.
| Tính năng | Kim loại kiềm, Nhóm 1 | Kim loại kiềm thổ, Nhóm 2 |
|---|---|---|
| Hóa trị | 1 | 2 |
| Ion điển hình | M + | M 2+ |
| Phản ứng với nước lạnh | Thường mạnh mẽ hoặc thậm chí dữ dội, tạo thành hiđroxit và hiđro | Ít đồng nhất: Be không phản ứng với nước, Mg phản ứng nhẹ, Ca, Sr và Ba phản ứng ngày càng mạnh |
| Hóa học oxy phổ biến | Có thể tạo thành oxit, peoxit hoặc superoxit | Thường tạo thành monoxit; phần lớn các oxit này phản ứng với nước tạo thành hiđroxit, nhưng BeO là một ngoại lệ |
Những ngoại lệ quan trọng mà học sinh thường bỏ sót
- Không phải mọi kim loại Nhóm 2 đều phản ứng với nước theo cùng một cách.
- Các hợp chất berili có tính cộng hóa trị cao hơn so với các nguyên tố còn lại trong cùng nhóm.
- Đừng nhầm lẫn kim loại kiềm và kim loại kiềm thổ là cùng một nhóm chỉ vì tên gọi nghe có liên quan với nhau.
- Các tính chất của kim loại kiềm và kim loại kiềm thổ được ghi nhớ tốt nhất dưới dạng các quy luật có ngoại lệ, chứ không phải những câu khẩu hiệu cứng nhắc.
Đó cũng là cách tốt nhất để hiểu rõ tính chất hóa học của kim loại kiềm và kim loại kiềm thổ . Các mô hình phân bố electron giúp bạn nắm được quy luật chung, nhưng các chất thực tế lại mang đến những đặc điểm riêng biệt. Và những đặc điểm này trở nên rõ ràng hơn nữa khi bạn xem xét vị trí tồn tại thực tế của các nguyên tố nhóm 2 trong tự nhiên: rất hiếm khi ở dạng kim loại nguyên chất, mà phổ biến hơn nhiều là tồn tại bên trong các khoáng vật, đá, nước biển, xương và các hợp chất công nghiệp.
Sự tồn tại của kim loại kiềm thổ trong tự nhiên
Nếu bạn hình dung một kim loại kiềm thổ như một mẫu nguyên chất, sáng bóng nằm trong đá, thì tự nhiên lại vận hành theo một cách khác. Các nguyên tố nhóm 2 đủ phản ứng để thường xuất hiện dưới dạng ion bên trong các khoáng vật, muối, đá, nước biển, xương và vỏ sò hơn là ở dạng kim loại tự do. Dù người ta tìm kiếm bằng cụm từ kim loại kiềm thổ hay thuật ngữ chuẩn hơn, thì mô hình tự nhiên vẫn giống nhau: họ nguyên tố này có xu hướng mạnh mẽ đối với các hợp chất.
Mô hình đó bắt nguồn trực tiếp từ tính chất hóa học của kim loại kiềm thổ . Chúng có khuynh hướng mất hai electron ở lớp ngoài cùng và tạo thành các ion M 2+²⁺ ổn định. Khi điều này xảy ra, các ion oxy, cacbonat, sunfat và halogenua sẽ dễ dàng liên kết chúng thành các hợp chất rắn có thể tồn tại lâu dài trong địa chất và sinh học.
Tại sao kim loại kiềm thổ không tồn tại ở dạng tự do trong tự nhiên
Britannica và ThoughtCo cả hai đều mô tả Nhóm 2 là phản ứng mạnh, điều này giải thích vì sao các nguyên tố này hiếm khi tồn tại ở dạng tự do. Trong không khí, nhiều nguyên tố trong nhóm này nhanh chóng hình thành lớp oxit phủ bề mặt. Trong môi trường tự nhiên, chúng còn được ổn định hơn nữa dưới dạng cacbonat, sunfat, silicat, florua hoặc clorua. Đó là lý do vì sao canxi xuất hiện trong đá vôi và vỏ sò, magiê có mặt trong khoáng vật và nước biển, còn stronti hoặc bari tồn tại trong các mỏ quặng. Radi càng hiếm hơn nữa, chỉ xuất hiện với hàm lượng vết trong quặng urani.
Các khoáng chất và hợp chất phổ biến của Nhóm 2
| Element | Nguồn tự nhiên phổ biến | Hợp chất quen thuộc | Lý do hợp chất đó có ý nghĩa |
|---|---|---|---|
| Berili | Beryl | BeO | Beryl là nguồn thương mại của nguyên tố này, trong khi oxit berili là một hợp chất quan trọng trong các vật liệu chuyên dụng |
| Magie | Magiecacbonat, đôlômit, nước biển | MgCO₃ 3hoặc Mg(OH)₂ 2 | Giải thích vì sao magiê thường gặp nhiều hơn trong khoáng vật, nước biển và dược phẩm chứ không phải ở dạng kim loại nguyên chất |
| Canxi | Đá vôi, phấn trắng, cẩm thạch, thạch cao, xương, vỏ sò | CaCO 3 | Liên kết địa chất, vật liệu xây dựng và bộ xương trong một hợp chất rất phổ biến |
| Stronti | Celestite, strontianite | SrSO 4hoặc SrCO 3 | Các khoáng vật này là nguồn tự nhiên chính của các hợp chất stronti |
| Bari | Barite, witherite | BaSO 4 | Barite là quặng chủ chốt, và bari sulfat là một trong những hợp chất bari phổ biến nhất |
| Radi | Lượng vết trong pitchblende và các quặng urani khác | RaCl 2 | Sự hiếm có và tính phóng xạ của nó khiến các hợp chất radi trở nên quan trọng về mặt lịch sử nhưng lại ít gặp |
EBSCO ghi nhận rằng canxi và magiê cũng xuất hiện trong nước biển với nồng độ khoảng 0,4 g/L và 1,3 g/L, tương ứng. Điều này giúp giải thích vì sao nhóm kim loại này kim loại kiềm thổ không chỉ liên hệ với quặng mà còn liên hệ với nước cứng, hệ thống biển và mô sống.
Cách tách các kim loại này ra khỏi hợp chất của chúng
Vì các kim loại nhóm 2 thường tồn tại dưới dạng hợp chất, nên quá trình chiết xuất bắt đầu từ quặng, nước mặn (brine) hoặc các mỏ khoáng. Một nguyên tắc công nghiệp phổ biến khá đơn giản: trước tiên chuyển đổi nguyên liệu thành oxit hoặc halogenua dễ xử lý hơn, sau đó sử dụng điện phân hoặc khử hóa học để giải phóng kim loại tự do. Britannica mô tả việc tách magnesium, canxi, strontium và barium lần đầu tiên bằng phương pháp điện phân, trong khi EBSCO lưu ý rằng sản xuất hiện đại vẫn thường dựa vào các phương pháp như điện phân muối clorua nóng chảy, khử oxit hoặc các quy trình tương tự tùy thuộc vào từng nguyên tố cụ thể. Berili là một minh chứng hữu ích cho thấy nhóm kim loại này không hoàn toàn đồng nhất, bởi berili có thể được sản xuất bằng cách khử berili florua.
Vì vậy, trong đời sống hàng ngày, con người thường tiếp xúc với Nhóm 2 thông qua đá vôi, thạch cao, magiê từ nước biển, barit hoặc canxi sinh học, chứ không phải qua các mẫu kim loại nguyên chất. Chi tiết này rất quan trọng, bởi vì tầm quan trọng thực tiễn của những nguyên tố này gắn bó chặt chẽ hơn nhiều với các hợp chất và dạng tồn tại của chúng chứ không phải với kim loại nguyên chất.
Các ví dụ về kim loại kiềm thổ trong đời sống hàng ngày
Nhóm 2 trở nên dễ ghi nhớ hơn nhiều khi bạn liên kết mỗi nguyên tố với một vật thể cụ thể trong thực tế. Xương, thuốc kháng axit, thạch cao, pháo hoa, dung dịch khoan và các mặt đồng hồ phát quang cũ đều là những ví dụ hữu ích. các ví dụ về kim loại kiềm thổ nếu bạn từng tự hỏi magiê là kim loại hay phi kim hoặc ca có phải là kim loại không , cả hai câu trả lời đều đơn giản: magiê và canxi đều là kim loại. Tuy nhiên, trong đời sống thường ngày, con người thường tiếp xúc với những chất này dưới dạng hợp chất chứ không phải dưới dạng kim loại nguyên chất.
Các ứng dụng hàng ngày của các hợp chất magiê và canxi
- Magie : Magiê là một trong những nguyên tố quan trọng nhất về mặt sinh học các nguyên tố kiềm thổ . Bảng thông tin về magiê của Viện Y tế Quốc gia Hoa Kỳ (NIH) ghi chú rằng magiê là yếu tố đồng vận trong hơn 300 hệ enzyme và hỗ trợ chức năng cơ và thần kinh, sản xuất năng lượng cũng như cấu trúc xương. Các hợp chất magiê cũng xuất hiện trong một số thuốc kháng axit và thuốc nhuận tràng, trong khi kim loại magiê được đánh giá cao trong các hợp kim nhẹ nơi việc giảm khối lượng là yếu tố quan trọng.
- Canxi các hợp chất canxi chiếm ưu thế trong đời sống hàng ngày. Canxi giúp tạo nên cấu trúc cho xương và răng; các hợp chất như canxi cacbonat và canxi sunfat đóng vai trò then chốt trong đá vôi, xi măng, thạch cao và tấm thạch cao. Điều này khiến canxi trở thành một trong những ví dụ rõ ràng nhất thể hiện mối liên hệ giữa hóa học, sinh học và xây dựng.
Các ứng dụng chuyên biệt của stronti và bari
- Stronti các muối stronti nổi tiếng nhất nhờ khả năng tạo màu đỏ đậm trong pháo hoa và pháo hiệu. Ngay cả những người đọc không nhớ đầy đủ danh sách các nguyên tố nhóm 2 vẫn thường ghi nhớ stronti ngay khi gắn với đặc điểm màu sắc.
- Bari các hợp chất bari có vai trò quan trọng trong công nghiệp và y học. Hồ sơ về bari của Thư viện Y khoa Quốc gia Hoa Kỳ (NLM) mô tả các ứng dụng chính trong bùn khoan, sơn, nhựa, gạch và thủy tinh. Tài liệu cũng nêu bật một điểm tương phản quan trọng trong y khoa: bari sulfat có độ hòa tan rất thấp được sử dụng làm chất cản quang trong một số xét nghiệm X-quang vì nó thường không bị cơ thể hấp thụ.
- Radi : Radi là một trường hợp chủ yếu mang tính lịch sử hoặc được kiểm soát chặt chẽ trong lĩnh vực khoa học. Trang web về radi của Ủy ban Điều tiết Hạt nhân Hoa Kỳ (NRC) mô tả việc sử dụng radi trong quá khứ để sản xuất sơn phát quang và trong liệu pháp điều trị ung thư giai đoạn đầu. Phần lớn những ứng dụng này đã được thay thế, mặc dù vẫn còn một số ứng dụng được quy định, chẳng hạn như một số ứng dụng trong chụp ảnh phóng xạ công nghiệp.
Tại sao dạng tồn tại và loại hợp chất lại quan trọng trong thực tiễn
Đối với nhóm 2, dạng mà người ta sử dụng thường là hợp chất chứ không phải kim loại nguyên chất.
Ý tưởng duy nhất đó giúp làm rõ rất nhiều sự nhầm lẫn. Magie trong thực phẩm hoặc thuốc không giống với magie dạng dây kim loại đang cháy. Canxi trong xương không giống với kim loại canxi phản ứng mạnh. Bari là ví dụ rõ ràng nhất cho thấy vì sao dạng tồn tại lại quan trọng: bari sulfat không tan có thể hữu ích trong chẩn đoán hình ảnh, trong khi các hợp chất bari dễ tan hơn đòi hỏi sự thận trọng cao hơn nhiều. Radi càng nhấn mạnh thêm điểm này, bởi tính phóng xạ của nó—chứ không chỉ vị trí của nó trong nhóm kim loại—mới là yếu tố chi phối cách thức xử lý.
Do đó, giá trị của nhóm 2 hoàn toàn không trừu tượng chút nào. Các nguyên tố này giúp giải thích cách một họ nguyên tố giống nhau lại có vai trò quan trọng trong dinh dưỡng, vật liệu, y học, chế biến công nghiệp và các quy định an toàn. Một danh sách ngắn các ứng dụng thực tế thường đã đủ để người học ghi nhớ được quy luật tổng quát.
Những điểm chính về các nguyên tố nhóm 2
Đến thời điểm này, nhóm kim loại kiềm thổ nên cảm thấy ít giống một danh sách cần ghi nhớ và nhiều hơn là một quy luật bạn có thể đọc trực tiếp từ cột nhóm 2 trên bảng tuần hoàn nếu ai đó vẫn hỏi, các kim loại kiềm thổ là gì , câu trả lời ngắn gọn vẫn rất đơn giản: berili, magiê, canxi, stronti, bari và radi. Một định nghĩa đầy đủ hơn về kim loại kiềm thổ còn hữu ích hơn nữa: sáu nguyên tố kim loại thuộc Nhóm 2, thường mất hai electron ở lớp ngoài cùng và tạo thành các ion M 2+²⁺.
Những điểm chính cần ghi nhớ về các kim loại kiềm thổ
- Vị trí rất quan trọng: sáu nguyên tố này thuộc Nhóm 2 nằm ở cột thứ hai tính từ bên trái, trong phần Nhóm 2 của khối s.
- Các thành viên trong họ là cố định: Be, Mg, Ca, Sr, Ba và Ra tạo thành toàn bộ tập hợp.
- Hóa học chung giải thích sự tương đồng trong họ: các obitan ns 2của chúng có cấu hình lớp ngoài cùng dẫn đến việc hình thành ion +2 là kết quả phổ biến, một điểm cốt lõi được tóm tắt bởi LibreTexts.
- Các xu hướng chính khi đi xuống nhóm là có thể dự đoán được: bán kính nguyên tử tăng lên, năng lượng ion hóa nói chung giảm dần và tính phản ứng thường tăng lên khi di chuyển xuống dưới nhóm.
- Các ngoại lệ rất quan trọng: beryllium thể hiện tính cộng hóa trị nhiều hơn các nguyên tố còn lại, magie có thể trông kém phản ứng hơn do lớp màng bề mặt, và radium chủ yếu được thảo luận thông qua tính phóng xạ của nó.
- Trong thực tế, điều này thường nghĩa là các hợp chất chứ không phải kim loại nguyên chất: mọi người thường gặp canxi cacbonat, magie oxit và bari sunfat thường xuyên hơn nhiều so với các nguyên tố Ca, Mg hoặc Ba ở dạng tự do.
Các bảng tuần hoàn các kim loại kiềm thổ cột này dễ ghi nhớ nhất như sáu kim loại liên kết với nhau bởi một quy luật: chúng thường tạo thành ion mang điện tích 2+, nhưng mỗi thành viên lại thể hiện quy luật đó theo một cách hơi khác nhau.
Từ hóa học nhóm 2 đến các chi tiết kim loại được chế tạo kỹ thuật
Hóa học này mở rộng xa hơn nhiều so với sách giáo khoa. LibreTexts lưu ý rằng magie nguyên chất được sản xuất ở quy mô lớn và được sử dụng trong các hợp kim nhẹ cho khung máy bay và các bộ phận động cơ ô tô. Một hướng dẫn tổng quát hơn về hợp kim cho thấy lý do vì sao điều này rất quan trọng: các kỹ sư điều chỉnh thành phần và quy trình gia công nhằm cân bằng giữa trọng lượng, độ bền, khả năng chống ăn mòn và khả năng gia công trong các chi tiết thực tế.
Từ góc nhìn cột nhóm 2 trên bảng tuần hoàn đến sản xuất, Shaoyi Metal Technology đưa ra một ví dụ thực tiễn về mối liên hệ đó. Các trang tài liệu về vật liệu ô tô và gia công cơ khí của nó mô tả quy trình sản xuất các chi tiết kim loại, từ chế tạo mẫu thử nghiệm đến sản xuất hàng loạt, trong đó hành vi của vật liệu và kiểm soát quy trình phải phối hợp chặt chẽ với nhau. Điều này khiến bảng tuần hoàn các kim loại kiềm thổ không chỉ là một biểu đồ dùng trong lớp học. Nó còn là một phần trong lập luận logic khi lựa chọn các kim loại và hợp kim để chế tạo các chi tiết kỹ thuật cần đạt yêu cầu về độ nhẹ, độ tin cậy cao và khả năng sản xuất dễ dàng.
Câu hỏi thường gặp về các kim loại kiềm thổ
1. Sáu kim loại kiềm thổ là những kim loại nào?
Sáu kim loại kiềm thổ gồm berili, magiê, canxi, stronti, bari và radi. Chúng nằm ở Nhóm 2 trong bảng tuần hoàn và được xếp chung với nhau vì thường mất hai electron ở lớp ngoài cùng, dẫn đến xu hướng hình thành ion mang điện tích 2+ trong nhiều hợp chất.
2. Kim loại kiềm thổ khác kim loại kiềm như thế nào?
Các kim loại kiềm thuộc Nhóm 1 và thường tạo thành các ion mang điện tích 1+ vì chúng có một electron ở lớp ngoài cùng. Các kim loại kiềm thổ thuộc Nhóm 2, thường tạo thành các ion mang điện tích 2+ và nói chung ít phản ứng hơn. Việc chỉ thêm một electron hóa trị đó làm thay đổi độ mạnh của liên kết mà chúng hình thành, cách chúng phản ứng với nước cũng như loại muối và oxit mà chúng thường tạo ra.
3. Vì sao các kim loại kiềm thổ không tồn tại tự do trong tự nhiên?
Các kim loại này đủ phản ứng để không tồn tại lâu ở dạng nguyên tố tinh khiết trong môi trường tự nhiên. Thay vào đó, chúng kết hợp với các ion oxy, cacbonat, sunfat, clorua hoặc silicat để trở thành thành phần của khoáng vật, đá, nước biển, vỏ sò ốc và xương. Đó là lý do vì sao con người thường tiếp xúc với các nguyên tố Nhóm 2 thông qua các hợp chất chứ không phải dưới dạng mẫu kim loại nguyên chất.
4. Có phải tất cả các kim loại kiềm thổ đều phản ứng với nước không?
Không, và đây là một trong những ngoại lệ hữu ích nhất cần ghi nhớ. Berili hầu như không phản ứng với nước; magiê phản ứng chậm trong nước lạnh do một lớp màng bề mặt hạn chế phản ứng; còn canxi, stronti và bari phản ứng dễ dàng hơn. Nói chung, tính phản ứng với nước tăng dần khi di chuyển xuống dưới Nhóm 2.
5. Vì sao các kim loại kiềm thổ lại quan trọng trong công nghiệp và sản xuất?
Tầm quan trọng của chúng bắt nguồn từ cả các hợp chất của chúng lẫn vai trò của chúng trong việc lựa chọn hợp kim. Magiê có giá trị cao trong các ứng dụng yêu cầu giảm trọng lượng; các hợp chất canxi đóng vai trò then chốt trong xi măng và thạch cao; còn các hợp chất bari được lựa chọn cho những ứng dụng công nghiệp và y tế chuyên biệt. Trong sản xuất thực tế, việc hiểu rõ đặc tính của kim loại giúp định hướng gia công, đảm bảo ổn định quy trình và nâng cao chất lượng chi tiết; vì vậy các nhà cung cấp như Shaoyi Metal Technology nhấn mạnh vào dịch vụ gia công ô tô đạt chứng nhận, kiểm soát quy trình và hỗ trợ toàn diện — từ các chi tiết mẫu đến sản xuất hàng loạt.
 Sản xuất với số lượng nhỏ, tiêu chuẩn cao. Dịch vụ tạo nguyên mẫu nhanh của chúng tôi giúp việc kiểm chứng trở nên nhanh chóng và dễ dàng hơn —
Sản xuất với số lượng nhỏ, tiêu chuẩn cao. Dịch vụ tạo nguyên mẫu nhanh của chúng tôi giúp việc kiểm chứng trở nên nhanh chóng và dễ dàng hơn —
