আয়নিক চার্জ প্রত্যাশিত Al প্রো মতো—এবং প্রধান ব্যতিক্রমগুলি খুঁজুন

আল আয়নিক চার্জের অর্থ দিয়ে শুরু করুন
সহজ ভাষায় আল আয়নিক চার্জের অর্থ কী
কখনো কি ভেবে দেখেছেন কেন যৌগগুলিতে অ্যালুমিনিয়াম প্রায়শই হিসাবে দেখা যায় Al 3+? ধারণাটি আয়নিক চার্জ সহজ কিন্তু শক্তিশালী: এটি আপনাকে বলে দেয় যে একটি অ্যালুমিনিয়াম পরমাণু কতগুলি ইলেকট্রন হারিয়েছে বা অর্জন করেছে একটি স্থিতিশীল আয়ন তৈরি করতে। অ্যালুমিনিয়ামের ক্ষেত্রে, সবচেয়ে সাধারণ-এবং নির্ভরযোগ্য-চার্জ হল +3। এর অর্থ হল প্রতিটি অ্যালুমিনিয়াম আয়ন তিনটি ইলেকট্রন হারিয়েছে, ফলে 3+ চার্জযুক্ত একটি ক্যাটায়ন তৈরি হয়েছে। এজন্যই, যখন আপনি রসায়নে অ্যালুমিনিয়াম চার্জ অথবা অ্যালুমিনিয়ামের চার্জ শব্দটি দেখেন, এটি প্রায়শই Al কে নির্দেশ করে 3+.
পর্যায় সারণীর চার্জে Al কোথায় অবস্থান করে এবং কেন তা গুরুত্বপূর্ণ
আপনি একটি দেখেন যখন আয়নিক চার্জ সহ পর্যায় সারণী আপনি লক্ষ্য করবেন যে একই গ্রুপের মৌলগুলি প্রায়শই একই চার্জ সহ আয়ন গঠন করে। আলুমিনিয়াম গ্রুপ 13-এ (কখনও কখনও গ্রুপ IIIA হিসাবে ডাকা হয়) বসে থাকে, ম্যাগনেসিয়ামের পরে এবং সিলিকনের আগে। প্রবণতা কী? মুখ্য-গ্রুপ ধাতুগুলি নিকটতম নোবেল গ্যাসের ইলেক্ট্রন গণনার সাথে মেলে এমন ইলেক্ট্রন হারাতে প্রবণতা দেখায়। আলুমিনিয়ামের ক্ষেত্রে এর অর্থ হল তিনটি ইলেক্ট্রন হারানো—তাই +3 চার্জ। এই গ্রুপ-ভিত্তিক প্যাটার্নটি প্রতিটি উপাদান পৃথকভাবে মুখস্থ না করেই চার্জ ভবিষ্যদ্বাণী করার জন্য একটি সংক্ষিপ্তপথ। উদাহরণ স্বরূপ, গ্রুপ 1 ধাতুগুলি সবসময় +1 আয়ন গঠন করে, গ্রুপ 2 ধাতুগুলি +2 গঠন করে, এবং গ্রুপ 13 - আলুমিনিয়ামসহ - +3 আয়ন গঠন করে। অনেকগুলো গ্রুপ অনুসারে পর্যায় সারণীর চার্জ রেফারেন্স চার্ট।
| গ্রুপ | সাধারণ চার্জ |
|---|---|
| 1 (ক্ষার ধাতু) | +1 |
| 2 (ক্ষারীয় মৃত্তিকা ধাতু) | +2 |
| 13 (আলুমিনিয়ামের গ্রুপ) | +3 |
| 16 (চ্যালকোজেনস) | −2 |
| ১৭ (হ্যালোজেনস) | −1 |
আল নিশ্চিত করার জন্য দ্রুত পরীক্ষা 3+সাধারণ যৌগসমূহে
ধরুন আপনি আল-এর সাথে কাজ করছেন 2ও 3(অ্যালুমিনিয়াম অক্সাইড) বা AlCl 3(অ্যালুমিনিয়াম ক্লোরাইড)। আপনি কীভাবে জানবেন যে অ্যালুমিনিয়াম +৩? এটি সবকিছু চার্জ সন্তুলনের ব্যাপার। অক্সিজেনের ক্ষেত্রে সাধারণত −২ চার্জ থাকে, এবং ক্লোরাইডের ক্ষেত্রে থাকে −১ চার্জ। Al 2ও 3, দুটি Al 3+আয়ন (মোট +৬) তিনটি O 2−আয়ন (মোট −৬) সন্তুলিত করে। AlCl 3, একটি Al 3+আয়ন তিনটি Cl কে ভারসাম্য বজায় রাখে −আয়ন (মোট −3)। এই ধরনগুলি আপনাকে সহজেই বাস্তব যৌগগুলিতে খুঁজে পেতে এবং নিশ্চিত করতে সাহায্য করে al চার্জ বাস্তব যৌগে।
- ধাতু 3+তিনটি ইলেকট্রন হারিয়ে এই আকৃতি গঠন করে, নিকটতম মৌলের গ্যাস কনফিগারেশনের সাথে সামঞ্জস্য রেখে।
- এটি অ্যালুমিনিয়ামের জন্য একমাত্র সাধারণ স্থিতিশীল আয়ন, যা ভবিষ্যদ্বাণীগুলিকে সরল করে তোলে।
- পর্যায় সারণীতে গ্রুপের প্রবণতা আপনাকে Al কে মুখস্থ করা ছাড়াই দ্রুত শনাক্ত করতে সাহায্য করে 3+মুখস্থ করা ছাড়াই।
প্রধান বিষয়: অ্যালুমিনিয়াম +3 চার্জ পছন্দ করে কারণ এই অবস্থায় এটির একটি স্থিতিশীল, মৌলের গ্যাসের মতো ইলেকট্রন কনফিগারেশন থাকে - যা Al কে সবচেয়ে বেশি যৌগে ব্যবহৃত আয়নে পরিণত করে 3+বেশিরভাগ যৌগে ব্যবহৃত আয়ন।
এই প্রবণতা এবং এদের কাজের পদ্ধতি বুঝে পর্যায় সারণীর চার্জ কাজ, আপনি আত্মবিশ্বাসের সাথে যৌগের সাথে এর অংশীদারদের ভবিষ্যদ্বাণী করতে সক্ষম হবেন। পরবর্তী অংশগুলিতে, আপনি দেখতে পাবেন কীভাবে এই জ্ঞানটি জলীয় রসায়ন, নামকরণের নিয়ম এবং এমনকি বাস্তব বিশ্বের উপকরণের প্রদর্শনের সাথে সংযুক্ত হয়েছে। আয়নিক চার্জ এবং এর যৌগে অংশীদারদের সাথে আত্মবিশ্বাসের সাথে ভবিষ্যদ্বাণী করতে পারবেন। পরবর্তী অংশগুলিতে, আপনি দেখতে পাবেন কীভাবে এই জ্ঞানটি জলীয় রসায়ন, নামকরণের নিয়ম এবং এমনকি বাস্তব বিশ্বের উপকরণের প্রদর্শনের সাথে সংযুক্ত হয়েছে।
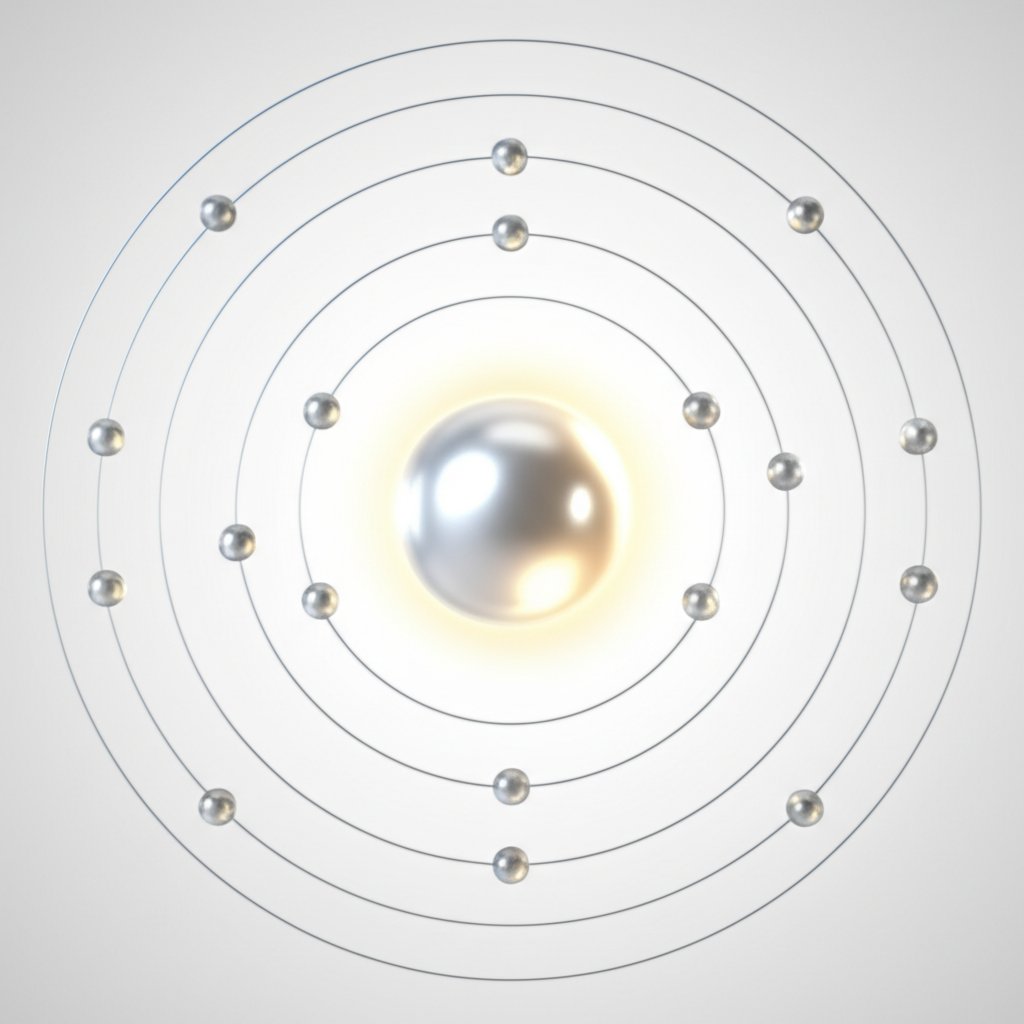
Al3 প্লাস এর দিকে পরিচালিত করে এমন ইলেকট্রন কনফিগারেশন
Al সংযোজন ইলেকট্রন এবং Al3+ এর দিকে পথ
যখন আপনি প্রথমবারের মতো একটি অ্যালুমিনিয়াম পরমাণুর দিকে তাকান, তখন +3 চার্জের দিকে পথটি রহস্যময় বলে মনে হতে পারে। কিন্তু যদি আপনি ইলেকট্রন কনফিগারেশন অনুসারে এটি ভেঙে ফেলেন, তখন যুক্তিটি দ্রুত পরিষ্কার হয়ে ওঠে। অ্যালুমিনিয়ামের পারমাণবিক সংখ্যা 13, যার অর্থ এটি নিরপেক্ষ অবস্থায় 13টি ইলেকট্রন ধারণ করে। এর ইলেকট্রন কনফিগারেশনটি 1s হিসাবে লেখা হয় 22S 22P 63S 23 পি 1, অথবা আরও সংক্ষিপ্তভাবে, [Ne] 3s 23 পি 1। 3s এবং 3p অরবিটালের তিনটি ইলেকট্রনকে অ্যালুমিনিয়ামের জন্য সংযোজন ইলেকট্রন হিসাবে বিবেচনা করা হয়—এগুলি হল রাসায়নিক বিক্রিয়ায় হারানোর সম্ভাবনা সবচেয়ে বেশি।
3p থেকে পর্যায়ক্রমে ইলেকট্রন অপসারণ তারপর 3s
জটিল শোনাচ্ছে? কল্পনা করুন প্রতিটি স্তর খুলে ফেলছেন: বাইরের ইলেকট্রনগুলো সরানো সবচেয়ে সহজ। এখানে দেখুন কীভাবে অ্যালুমিনিয়াম +3 চার্জ সহ একটি আয়ন গঠন করে:
- 3p ইলেকট্রনটি সরিয়ে নিন: 3p অরবিটালের একক ইলেকট্রনটি প্রথমে হারিয়ে যায়, [Ne] 3s রেখে দেয় 2.
- দুটি 3s ইলেকট্রন সরিয়ে নিন: পরবর্তীতে, 3s অরবিটালের উভয় ইলেকট্রন সরিয়ে নেওয়া হয়, যার ফলে [Ne] হয়।
- ফলাফল: অ্যালুমিনিয়াম পরমাণুটি এখন মোট তিনটি ইলেকট্রন হারিয়েছে, Al উৎপাদন করেছে 3+আয়নটির কাঠামো নিয়নের মতো হয়েছে—একটি মহাজাগতিক গ্যাসের।
- নিরপেক্ষ অ্যালুমিনিয়াম: [Ne] 3s 23 পি 1
- 1টি ইলেকট্রন হারানোর পর: [Ne] 3s 2
- আরও 2টি ইলেকট্রন হারানোর পর: [Ne]
এই পদ্ধতিগত প্রক্রিয়াটি স্থিতিশীলতার আকাঙ্ক্ষা থেকে অনুপ্রাণিত। অ্যালুমিনিয়ামের যোজ্যতা সংখ্যা হল 3, যা এর তিনটি ইলেকট্রন ত্যাগ করে একটি নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস অর্জনের প্রবণতা নির্দেশ করে। যখন অ্যালুমিনিয়াম 10টি ইলেকট্রন বিশিষ্ট একটি আয়ন গঠন করে, তখন এটি তিনটি ইলেকট্রন ত্যাগ করে এবং Al 3+ (তথ্যসূত্র) .
অ্যালুমিনিয়ামের জন্য +3 কেন এবং +1 কেন নয়
+1 বা +2-এর পরিবর্তে অ্যালুমিনিয়াম কেন থামে না? উত্তরটি নিহিত আছে কার্যকর নিউক্লিয় চার্জ এবং শেলের স্থিতিশীলতার মধ্যে। তিনটি যোজ্যতা ইলেকট্রন সম্পূর্ণরূপে ত্যাগ করে অ্যালুমিনিয়ামের আয়নিক চার্জ একটি পূর্ণ শেল বিন্যাস অর্জন করে—যা নিয়নের স্থিতিশীলতার সাথে মেলে। +1 বা +2-এ থেমে গেলে আংশিক পূর্ণ শেল থেকে যায়, যা ইলেকট্রন বন্টনের অসমতা এবং দুর্বল শিল্ডিংয়ের কারণে কম স্থিতিশীল। এজন্যই অ্যালুমিনিয়াম আয়ন চার্জ যৌগে প্রায়শই +3 হয়।
পূর্ণ শেল, নিষ্ক্রিয় গ্যাস বিন্যাস অর্জনের প্রচেষ্টাই Al-এর জন্য 3+রসায়নে আলুমিনিয়াম আয়নের জন্য অত্যধিক পছন্দের অবস্থা।
এই ইলেকট্রন পরিবর্তনগুলি বোঝা আপনাকে পূর্বাভাস দিতে সাহায্য করবে এবং ব্যাখ্যা করবে আলুমিনিয়ামের জন্য ইলেকট্রন বিভিন্ন প্রেক্ষাপটে। পরবর্তীতে, আপনি দেখবেন কীভাবে এই ধরনগুলি আপনাকে দ্রুত আলুমিনিয়াম এবং পর্যায় সারণীতে এর প্রতিবেশীদের জন্য চার্জ পূর্বাভাস দিতে সাহায্য করে - এবং ব্যতিক্রমগুলি খুঁজে বার করে।
আয়নিক চার্জ পূর্বাভাস দেওয়া এবং ব্যতিক্রমগুলি সম্পাদন করা
দ্রুত পর্যায়ক্রমিক ধরন থেকে চার্জ পূর্বাভাস দেওয়া
যখন আপনি এর দিকে তাকান চার্জ সহ পর্যায় সারণী , আপনি একটি সহায়ক ধরন লক্ষ্য করবেন: একই গ্রুপের (উল্লম্ব কলাম) মৌলগুলি সাধারণত একই চার্জ সহ আয়ন তৈরি করে। এটি আয়নিক পর্যায় সারণীতে সাহায্য করে আয়নিক পর্যায় সারণী প্রধান মৌলগুলির বেশিরভাগের আয়নিক চার্জের পূর্বাভাসের জন্য একটি শক্তিশালী শর্টকাট - বিশেষত প্রধান শ্রেণির মৌলগুলির জন্য।
| গ্রুপ | সাধারণ আয়নিক চার্জ |
|---|---|
| 1 (ক্ষার ধাতু) | +1 |
| 2 (ক্ষারীয় মৃত্তিকা ধাতু) | +2 |
| ১৩ (বোরন গ্রুপ, অন্তর্ভুক্ত। আল) | +3 |
| 16 (চ্যালকোজেনস) | −2 |
| ১৭ (হ্যালোজেনস) | −1 |
উদাহরণস্বরূপ, গ্রুপ ১৩ চার্জ প্রায় সবসময় +৩, তাই অ্যালুমিনিয়াম নিরবচ্ছিন্নভাবে Al গঠন করে 3+আয়ন। এই ধরনটি সমগ্র পর্যায় সারণীতে প্রতিধ্বনিত হয় চার্জের পর্যায় সারণী - গ্রুপ ১ মৌলগুলি +১ গঠন করে, গ্রুপ ২ গঠন করে +২, এবং এরূপে। যখন আপনাকে জানতে হবে al এর চার্জ কী আপনি দ্রুত এর গ্রুপ অবস্থান পরীক্ষা করে +৩ পূর্বাভাস দিতে পারবেন (তথ্যসূত্র) .
যখন Tl এর মতো ব্যতিক্রম হয় +সাধারণ নিয়মগুলোকে অতিক্রম করে
কিন্তু ব্যতিক্রমগুলো কীভাবে হয়? যদিও বেশিরভাগ মুখ্য-গোষ্ঠীর মৌলগুলো এই প্রবণতার অনুসরণ করে, কিছু অপ্রত্যাশিত বিষয় রয়েছে - বিশেষ করে যখন আপনি কোনো গোষ্ঠীর নিচের দিকে যান। উদাহরণ হিসেবে গ্রুপ 13 এর থ্যালিয়াম (Tl) নিন: যদিও গ্রুপ 13 এর চার্জ সাধারণত +3, থ্যালিয়াম প্রায়শই Tl গঠন করে +আয়ন। কেন? এটি নিষ্ক্রিয় জোড়া প্রভাবের (inert pair effect) কারণে হয়, যেখানে কম শক্তি সম্পন্ন s-ইলেকট্রনগুলো বন্ধনে অংশগ্রহণের পরিবর্তে ভারী পরমাণুগুলোতে বেশি সময় থাকে। ফলস্বরূপ, থ্যালিয়াম তার s-ইলেকট্রনগুলোকে "আটকে রাখতে" পারে, যা অনেক যৌগে +3 এর তুলনায় +1 অবস্থাকে আরও স্থিতিশীল করে তোলে। এই ব্যতিক্রমটি আমাদের মনে করিয়ে দেয় যে ভারী মৌলগুলোর সাথে কাজ করার সময় গোষ্ঠীর প্রবণতার উপর অন্ধভাবে নির্ভর করা উচিত নয়।
পরিবর্তনশীল সংক্রমণ ধাতু চার্জ কীভাবে পরিচালনা করবেন
সংক্রমণ ধাতুগুলো, মাঝখানে পাওয়া পর্যায় সারণী এবং চার্জ চার্টে, এদের অপ্রত্যাশিততার জন্য পরিচিত। মুখ্য-গোষ্ঠীর ধাতুগুলোর বিপরীতে, এরা একাধিক সম্ভাব্য চার্জ সহ আয়ন গঠন করতে পারে - Fe এর মতো 2+এবং Fe 3+, অথবা Cu +এবং Cu 2+. এই পরিবর্তনশীলতার অর্থ হল আপনাকে সবসময় রেফারেন্স বা যৌগিক পরিপ্রেক্ষিত পরীক্ষা করতে হবে যখন ট্রানজিশন ধাতুগুলির সাথে কাজ করবেন। শুধুমাত্র গ্রুপের অবস্থানের উপর ভিত্তি করে চার্জ অনুমান করবেন না।
- উপাদানটির গ্রুপ শনাক্ত করুন: গ্রুপ নম্বরটি খুঁজে পেতে পর্যায় সারণী ব্যবহার করুন।
- গ্রুপ ট্রেন্ড প্রয়োগ করুন: গ্রুপের উপর ভিত্তি করে সাধারণ চার্জ অনুমান করুন (উপরের টেবিল দেখুন)।
- ব্যতিক্রমগুলি পরীক্ষা করুন: ভারী p-ব্লক মৌলগুলির (যেমন Tl) জন্য অথবা ট্রানজিশন ধাতুগুলির জন্য একটি নির্ভরযোগ্য রেফারেন্সের সাথে পরামর্শ করুন।
অ্যালুমিনিয়ামের নির্দিষ্ট +3 চার্জ ট্রানজিশন মেটালগুলিতে দেখা যাওয়া পরিবর্তনশীল চার্জের তুলনায় অনেক বেশি পূর্বানুমেয় - আয়নিক যৌগগুলি ভারসাম্য রাখার সময় এটিকে নির্ভরযোগ্য ভিত্তি হিসাবে তৈরি করে।
এই প্যাটার্নগুলি দক্ষতার সাথে শিখে এবং ব্যতিক্রমগুলি শনাক্ত করে, আপনি ব্যবহার করতে সক্ষম হবেন পর্যায় সারণীতে চার্জগুলি সূত্রগুলি তৈরি এবং পরীক্ষা করার জন্য দ্রুত এবং কার্যকর সরঞ্জাম হিসাবে। পরবর্তীতে, আপনি দেখবেন যে এই ভবিষ্যদ্বাণীগুলি জলে এবং তার বাইরে অ্যালুমিনিয়াম আয়নগুলির বাস্তব আচরণের সাথে কীভাবে সংযুক্ত হয়।
Al3 এর জলীয় রসায়ন +এবং জলবিশ্লেষণ
হেক্সাকোয়া অ্যালুমিনিয়াম 3+এবং জলবিশ্লেষণ ক্রম
যখন আপনি জলে Al(NO এর মতো অ্যালুমিনিয়াম লবণ দ্রবীভূত করেন, 3)3জল, আপনি কেবলমাত্র সরল Al নির্মুক্ত করছেন না 3+আয়ন। পরিবর্তে, সেগুলি অ্যালুমিনিয়াম ক্যাটিয়ন তাৎক্ষণিকভাবে ছয়টি জলের অণুর সাথে আকর্ষিত ও বন্ধন ঘটে, স্থিতিশীল গঠন করে হেক্সাকোয়া কমপ্লেক্স [Al(H 2O) 6]3+। এই আয়নটি অষ্টতলকীয়, 6 সমন্বয় সংখ্যা সহ—এটি অ্যালুমিনিয়াম আয়ন জলীয় পরিবেশে (তথ্যসূত্র) .
কিন্তু গল্প এখানেই শেষ হয় না। Al এর উচ্চ ধনাত্মক চার্জ 3+এটিকে একটি শক্তিশালী লুইস অ্যাসিড হিসেবে পরিণত করে, সমন্বিত জলের অণুগুলির থেকে ইলেকট্রন ঘনত্ব টেনে আনে। ফলস্বরূপ, এই জলের লিগ্যান্ডগুলি আরও আম্লিক হয়ে ওঠে এবং pH বৃদ্ধির সাথে সাথে প্রোটন হারাতে পারে। এই প্রক্রিয়াটি—যা হাইড্রোলাইসিস —নিচে দেখানো হয়েছে এমন নতুন আয়নগুলির সৃষ্টি করে:
- নিম্ন pH-তে: [Al(H 2O) 6]3+প্রাধান্য বিস্তার করে।
- PH বৃদ্ধির সাথে: একটি জলীয় লিগ্যান্ড একটি প্রোটন হারায়, [Al(H গঠন করে 2O) 5(OH)] 2+.
- আরও ডিপ্রোটনেশন [Al(H দেয় 2O) 4(OH) 2]+.
- অবশেষে, নিরপেক্ষ Al(OH) 3(অ্যালুমিনিয়াম হাইড্রোক্সাইড) অধঃক্ষিপ্ত হয়।
- উচ্চ pH-এ: Al(OH) 4−(অ্যালুমিনেট আয়ন) গঠিত হয় এবং পুনরায় দ্রবীভূত হয়।
এই ধারাটি ক্লাসিক উদাহরণ যে কীভাবে ক্যাটায়ন এবং অ্যানায়ন জলের সাথে পারস্পরিক ক্রিয়া করে, এবং কেন সেই হাইড্রোক্সাইড চার্জ একটি নির্দিষ্ট পিএইচ-এ কোন প্রজাতি উপস্থিত থাকে তা নির্ধারণে খুব গুরুত্বপূর্ণ (উৎস) .
উভধর্মীতা এবং এলুমিনেটের দিকে পথ
এখানেই আকর্ষণীয় বিষয় শুরু হয়: Al(OH) 3 is অ্যামফোটেরিক । এর অর্থ হল এটি এসিড এবং ক্ষারক উভয়টির সাথে বিক্রিয়া করতে পারে। অ্যাসিডিক দ্রবণে, এটি Al পুনরায় গঠনের জন্য দ্রবীভূত হয় 3+(অথবা এর জলযোজিত রূপগুলি)। ক্ষারীয় দ্রবণে, এটি দ্রবণীয় এলুমিনেট আয়ন, Al(OH) গঠনের জন্য আরও বিক্রিয়া করে 4−। এই দ্বৈত আচরণ অনেকগুলির চিহ্নিতকারী এবং বিভিন্ন পরিবেশে তাদের দ্রাব্যতা এবং অধঃক্ষেপণ বোঝা এবং এটি খুব গুরুত্বপূর্ণ অ্যালুমিনিয়াম আয়ন এবং বিভিন্ন পরিবেশে তাদের দ্রাব্যতা এবং অধঃক্ষেপণ বোঝা এবং এটি খুব গুরুত্বপূর্ণ
-
Al এর জন্য সাধারণ লিগ্যান্ড 3+:
- জল (H 2O)
- হাইড্রক্সাইড (OH −)
- ফ্লুওরাইড (F −)
- সালফেট (SO 42−)
- জৈব অ্যাসিড (যেমন সাইট্রেট বা অক্সালেট)
এই আচরণের জন্যই জল পরিশোধন, রঞ্জন এবং সহ-অধঃক্ষেপণকারী হিসাবে অ্যালুমিনিয়াম খুব বহুমুখী—pH এর উপর ভিত্তি করে বিভিন্ন রূপের মধ্যে স্যুইচ করার ক্ষমতাই এর রসায়নের চাবিকাঠি।
কী অ্যালুমিনিয়াম 3+আধান দ্রাব্যতা কী নির্দেশ করে
তাহলে, এর মানে কী হবে আলুমিনিয়াম আয়ন যৌগের দ্রাব্যতার ক্ষেত্রে? দুর্বল ক্ষারীয় থেকে নিরপেক্ষ অবস্থায়, Al(OH) 3এর খুব কম দ্রাব্যতা থাকে এবং অধঃক্ষিপ্ত হয়—এটিই হল জল থেকে অ্যালুমিনিয়াম অপসারণের ভিত্তি। কিন্তু তীব্র আম্লিক বা তীব্র ক্ষারীয় অবস্থায়, অ্যালুমিনিয়াম [Al(H 2O) 6]3+বা Al(OH) হিসাবে দ্রবীভূত থাকে 4−. এই উভধর্মী আচরণের জন্যই অ্যালুমিনিয়াম ক্যাটিয়ন পরিবেশগত এবং শিল্প প্রক্রিয়াগুলিতে রসায়ন খুব গুরুত্বপূর্ণ।
Al এর উচ্চ চার্জ ঘনত্ব 3+এটিকে একটি শক্তিশালী লুইস অ্যাসিড হিসাবে পরিণত করে, ধাপে ধাপে জলবিশ্লেষণ এবং দ্রবণে বিভিন্ন ধরনের অ্যালুমিনিয়াম আয়নের গঠন ঘটায়।
এই রূপান্তরগুলি বোঝা আপনাকে শুধুমাত্র ভিন্ন ভিন্ন pH মাত্রায় কোনগুলি অ্যালুমিনিয়াম আয়ন উপস্থিত থাকে তা পূর্বাভাস দেয় না, বরং তাদের অধঃক্ষেপণ, দ্রাব্যতা এবং বিক্রিয়াশীলতা কীভাবে নিয়ন্ত্রণ করা যায় তাও বোঝায়। পরবর্তী অংশে, আপনি দেখতে পাবেন যে এই জলীয় আচরণগুলি কীভাবে প্রয়োগযোগ্য পরিস্থিতিতে অ্যালুমিনিয়াম যৌগগুলির নামকরণের নিয়ম এবং সংকেতের প্যাটার্নের সঙ্গে সরাসরি সম্পর্কিত।
অ্যালুমিনিয়ামের যৌগগুলির নামকরণের নিয়ম এবং সংকেতের প্যাটার্ন
অ্যালুমিনিয়াম যৌগগুলির সঠিক নামকরণ
যখন আপনি কোনও যৌগে Al দেখেন, 3+তখন এর নামকরণ করা হয় অবিকল সোজা পথে। এটি অ্যালুমিনিয়াম আয়নের নাম শুধুমাত্র "অ্যালুমিনিয়াম আয়ন" হয়, যেহেতু এটি আয়নিক যৌগগুলিতে একটি সাধারণ চার্জ গঠন করে। স্পষ্টতা অনুসরণ করে রোমান সংখ্যা পছন্দ করে এমন কোনও শৈলী না অনুসরণ করলে কোনও অস্পষ্টতা বা অতিরিক্ত সংকেতের প্রয়োজন হয় না। উদাহরণস্বরূপ, "অ্যালুমিনিয়াম ক্লোরাইড" এবং "অ্যালুমিনিয়াম (III) ক্লোরাইড" উভয়ই গ্রহণযোগ্য, কিন্তু রোমান সংখ্যা ঐচ্ছিক কারণ এই পরিস্থিতিতে অ্যালুমিনিয়ামের চার্জ সবসময় +3 হয়।
Al-এর সাথে ভারসাম্য 3+সাধারণ অ্যানায়নের সাথে
Al যুক্ত যৌগের সংকেত লেখা 3+স্পষ্ট নিয়মের একটি সেট অনুসরণ করে: মোট ধনাত্মক চার্জ মোট ঋণাত্মক চার্জের সমান হতে হবে। এটিই হল আয়নিক যৌগ চার্জের ভারসাম্য রক্ষা। চলুন দেখি কিভাবে অ্যালুমিনিয়াম চার্জ আয়ন অ্যালুমিনিয়াম আয়নটিকে ফসফেট আয়ন চার্জের মতো পলিঅ্যাটমিক সহ সবচেয়ে ঘন ঘন অ্যানায়নের সাথে সংযুক্ত করা হয় , অ্যাসিটেট আয়ন চার্জ এবং নাইট্রেটের চার্জ :
| সূত্র | উপাদান আয়নসমূহ | নাম | চার্জ ব্যালেন্স নোটসমূহ |
|---|---|---|---|
| ধাতু 2ও 3 | 2 Al 3+, 3 O 2− | আলুমিনিয়াম অক্সাইড | 2×(+3) + 3×(−2) = 0 |
| AlCl 3 | 1 Al 3+, 3 Cl − | অ্যালুমিনিয়াম ক্লোরাইড | 1×(+3) + 3×(−1) = 0 |
| ধাতু 2(SO 4)3 | 2 Al 3+, 3 SO 42− | আলুমিনিয়াম সালফেট | 2×(+3) + 3×(−2) = 0 |
| Al(NO 3)3 | 1 Al 3+, 3 NO 3− | অ্যালুমিনিয়াম নাইট্রেট | 1×(+3) + 3×(−1) = 0 |
| Al(C 2এইচ 3ও 2)3 | 1 Al 3+, 3 C 2এইচ 3ও 2− | অ্যালুমিনিয়াম অ্যাসিটেট | 1×(+3) + 3×(−1) = 0 |
| AlPO 4 | 1 Al 3+, 1 PO 43− | অ্যালুমিনিয়াম ফসফেট | 1×(+3) + 1×(−3) = 0 |
দেখুন কীভাবে ধনাত্মক এবং ঋণাত্মক চার্জের যোগফল শূন্য হওয়ার জন্য সাবস্ক্রিপ্টগুলি নির্বাচন করা হয়। পলিঅ্যাটমিক আয়নের ক্ষেত্রে, যদি আপনার একটির বেশি আয়নের প্রয়োজন হয়, সবসময় সাবস্ক্রিপ্ট যোগ করার আগে আয়নকে বন্ধনীর মধ্যে রাখুন (যেমন Al(NO 3)3).
রোমান সংখ্যা কখন অন্তর্ভুক্ত করবেন
কারণ অ্যালুমিনিয়ামের জন্য আয়ন নাম অনন্য হওয়ার ক্ষেত্রে, প্রায়শই “অ্যালুমিনিয়াম আয়ন” রোমান সংখ্যা ছাড়াই দেখা যায়। তবুও, কিছু পাঠ্যপুস্তক বা তথ্যসূত্র “অ্যালুমিনিয়াম(III)” ব্যবহার করে থাকে +3 চার্জ জোরদার করার জন্য, বিশেষ করে এমন পরিস্থিতিতে যেখানে অন্যান্য মৌলগুলির জন্য একাধিক জারণ অবস্থা সম্ভব। অ্যালুমিনিয়ামের ক্ষেত্রে, এটি বেশিরভাগই শৈলীগত পছন্দ—আবশ্যিকতা নয় (উৎস দেখুন) .
- একাধিক পলিঅ্যাটমিক আয়ন উপস্থিত থাকলে বন্ধনী ব্যবহার করা ভুলে যাওয়া, যেমন AlNO লেখা 33al(NO এর পরিবর্তে 3)3
- মোট চার্জ ভুল হিসাব করা এবং অসমতুলিত সূত্রে পৌঁছানো
- সাধারণ পলিঅ্যাটমিক আয়নগুলির চার্জ মিশিয়ে ফেলা, যেমন ফসফেট আয়ন চার্জের মতো পলিঅ্যাটমিক সহ সবচেয়ে ঘন ঘন অ্যানায়নের সাথে সংযুক্ত করা হয় (−3), অ্যাসিটেট আয়ন চার্জ (−1), or নাইট্রেটের চার্জ (−1)
নিয়ম: সর্বদা মোট ধনাত্মক এবং ঋণাত্মক চার্জগুলি ভারসাম্যপূর্ণ রাখুন - সূত্রের জন্য সর্বনিম্ন পূর্ণসংখ্যা অনুপাত ব্যবহার করুন এবং বহুপরমাণু আয়ন চার্জ এবং বন্ধনী দ্বিগুণ পরীক্ষা করুন।
এই নিয়ম এবং উদাহরণগুলি সহ আপনি যেকোনো অ্যালুমিনিয়ামযুক্ত আয়নিক যৌগিক দ্রুত লিখতে এবং নামকরণ করতে সক্ষম হবেন। পরবর্তীতে, অ্যালুমিনিয়াম আয়নগুলির উপাদান এবং ফিনিশিং প্রক্রিয়ায় বাস্তব প্রভাবের সাথে এই নামকরণ প্যাটার্নগুলি কীভাবে সংযুক্ত রয়েছে তা দেখুন।

বাস্তব জগতের প্রভাব অ্যাল 3+উপকরণ এবং ফিনিশিংয়ে
Al থেকে 3+অক্সাইড ফিল্ম এবং অ্যানোডাইজিংয়ে
যখন আপনি অ্যালুমিনিয়াম অংশগুলির স্থায়িত্ব এবং কার্যকারিতা সম্পর্কে চিন্তা করবেন, তখন অ্যালুমিনিয়াম আয়নিক চার্জ শুধুমাত্র পাঠ্যপুস্তকের ধারণা নয় - এটি অ্যালুমিনিয়ামের বাস্তব পরিবেশে আচরণের ভিত্তি। কখনও কি লক্ষ্য করেছেন কীভাবে অ্যালুমিনিয়ামের পৃষ্ঠগুলি প্রায় তাৎক্ষণিকভাবে একটি পাতলা, সুরক্ষামূলক স্তর তৈরি করে? এটি Al এর ফলাফল 3+অক্সিজেনের সাথে বিক্রিয়া করে একটি স্থিতিশীল অক্সাইড ফিল্ম গঠন করে। এই প্রাকৃতিক প্যাসিভেশন মেটালের মূল অংশকে আরও ক্ষয় থেকে রক্ষা করে এবং এ কারণেই প্রকৌশল ও উত্পাদনে অ্যালুমিনিয়াম ব্যাপকভাবে ব্যবহৃত হয়।
কিন্তু আপনার যখন আরও বেশি সুরক্ষা বা একটি নির্দিষ্ট পৃষ্ঠতলের সমাপ্তির প্রয়োজন হয় তখন কী হয়? সেখানেই অ্যানোডাইজিং এর প্রয়োগ হয়। অ্যানোডাইজিং হল একটি নিয়ন্ত্রিত তড়িৎ-রাসায়নিক প্রক্রিয়া যা বাইরের কারেন্ট প্রয়োগে হাইড্রেটেড অ্যালুমিনিয়াম অক্সাইড গঠনের মাধ্যমে অক্সাইড স্তরটিকে মোটা করে তোলে। এই প্রক্রিয়াটি আয়নিক অ্যালুমিনিয়াম পৃষ্ঠের কাছাকাছি স্থানান্তর এবং রূপান্তরের উপর ভিত্তি করে করা হয়—অ্যালুমিনিয়াম Al 3+, হিসাবে বিদ্যমান থাকার যত বেশি প্রবণতা রাখে, ফলস্বরূপ অক্সাইড ফিল্মটি তত শক্তিশালী হয় (তথ্যসূত্র) .
- ধাতু 3+প্রয়োগকৃত ভোল্টেজের অধীনে পৃষ্ঠের দিকে অভিগমন করে
- তারা জল এবং অক্সিজেনের সাথে বিক্রিয়া করে একটি ঘন এবং সুরক্ষামূলক অক্সাইড গঠন করে
- এই প্রকৌশলগত স্তরটি ক্ষয়, ঘর্ষণ এবং পরিবেশগত ক্ষতির প্রতিরোধ করতে সক্ষম হয়
রোড সল্ট, আর্দ্রতা বা উচ্চ তাপমাত্রার শর্তে প্রকাশিত একটি অটোমোটিভ অংশের ডিজাইন করা কল্পনা করুন—এই আয়নিক অক্সাইড ব্যারিয়ার ছাড়া, অংশটি দ্রুত ক্ষয়প্রাপ্ত হত। এই কারণেই বোঝা প্রয়োজনীয় অ্যালুমিনিয়ামের চার্জ কত শুধুমাত্র রসায়ন তথ্য নয়, কিন্তু একটি ব্যবহারিক ডিজাইন বিষয়।
এক্সট্রুডেড অ্যালুমিনিয়াম অংশের জন্য ডিজাইন প্রভাব
এখন, এক্সট্রুশন এবং ফিনিশিংয়ের সাথে সংযোগ করা যাক। যখন আপনি একটি গুরুত্বপূর্ণ অ্যাপ্লিকেশনের জন্য একটি অ্যালুমিনিয়াম খাদ বা প্রোফাইল নির্দিষ্ট করেন, তখন আপনি শুধুমাত্র আকৃতি বা শক্তি বিবেচনা করছেন না—আপনি ভাবছেন কীভাবে পৃষ্ঠটি প্রকৃত পরিবেশগত চাপের অধীনে আচরণ করবে। Al এর প্রবণতা 3+স্থিতিশীল অক্সাইড গঠন করার অর্থ হল যে এক্সট্রুডেড অংশগুলি বিভিন্ন ধরনের অ্যানোডিক ফিল্ম দিয়ে তৈরি করা যেতে পারে, যা প্রত্যেকটি নির্দিষ্ট প্রদর্শন করে:
- ম্যাটেরিয়াল গ্রেড: খাদ রচনা অক্সাইড গঠন এবং ক্ষয় প্রতিরোধ প্রভাবিত করে
- পৃষ্ঠের চিকিত্সাঃ টাইপ I (ক্রোমিক অ্যাসিড), টাইপ II (ক্লিয়ার কোট), এবং টাইপ III (হার্ড অ্যানোডাইজড) ফিনিশ বিভিন্ন স্থায়িত্ব এবং চেহারা প্রদান করে
- সহনশীলতা নিয়ন্ত্রণ: অ্যানোডাইজিং উচ্চ ক্ষমতাসম্পন্ন অংশগুলির জন্য নির্ভুল মাত্রা বজায় রাখতে প্রকৌশলীদের দ্বারা প্রয়োগ করা যেতে পারে
- অ্যালুমিনিয়াম পোলারাইজেশন করতে পারে: পৃষ্ঠের চার্জ এবং অক্সাইডের পুরুতা নিয়ন্ত্রণ করার ক্ষমতা বৈদ্যুতিক অন্তরক বা পরিবাহিতা প্রয়োজন অ্যাপ্লিকেশনগুলির জন্য অত্যন্ত গুরুত্বপূর্ণ
অটোমোটিভ, এয়ারোস্পেস বা স্থাপত্য ব্যবহারের জন্য, মিশ্র ধাতু এবং পৃষ্ঠের সমাপ্তির সঠিক সংমিশ্রণ - যা থেকে উৎপন্ন হয় অ্যালুমিনিয়াম আয়নিক চার্জ -এর নিশ্চিত করে যে উপাদানটি স্থায়ী হবে, ভালো দেখাবে এবং প্রয়োজনমতো কাজ করবে। এখনও ভাবছেন, "অ্যালুমিনিয়াম ইলেকট্রন অর্জন করে বা হারায়?" সমস্ত এই প্রক্রিয়াগুলিতে, জারণ এবং সুরক্ষা চক্রটির পুরোটাই চালিত করতে অ্যালুমিনিয়াম ইলেকট্রনগুলি হারায়।
আয়নিক আচরণ সম্পন্ন ফিনিশিংয়ে সহযোগী সংস্থা নির্বাচন
যে সরবরাহকারী প্রকৃতপক্ষে অ্যালুমিনিয়াম ক্যাটায়ন বা অ্যানায়ন রূপান্তরের পিছনে রসায়ন বোঝে, তাকে নির্বাচন করা আপনার প্রকল্পের সাফল্য নির্ভর করে। নিচে এক্সট্রুডেড অ্যালুমিনিয়াম অংশগুলির জন্য সমাধান প্রদানকারীদের তুলনা করা হয়েছে, যা পৃষ্ঠের ফিনিশিং এবং গুণগত নিয়ন্ত্রণে তাদের দক্ষতার উপর মনোনিবেশ করে:
| সরবরাহকারী | পৃষ্ঠ ফিনিশিং দক্ষতা | মান অনুশীলন | পরিষেবা পরিসর |
|---|---|---|---|
| শাওয়ি (অ্যালুমিনিয়াম এক্সট্রুশন অংশ) | উন্নত অ্যানোডাইজিং, নির্ভুল অক্সাইড নিয়ন্ত্রণ, অটোমোটিভ-গ্রেড পৃষ্ঠতল প্রকৌশল | IATF 16949 সার্টিফায়েড, সম্পূর্ণ প্রক্রিয়া ট্রেসেবিলিটি, সমালোচনামূলক মাত্রা জন্য DFM/SPC/CPK | ওয়ান-স্টপ সমাধান: ডিজাইন, প্রোটোটাইপিং, বৃহৎ উত্পাদন, বৈশ্বিক ডেলিভারি |
| ফন্নোভ অ্যালুমিনিয়াম | কাস্টম অ্যানোডাইজিং, পাউডার কোটিং, স্থাপত্য এবং প্রকৌশল সমাপ্তি | জাতীয় এবং আন্তর্জাতিক মান পালন, মান-প্রথম পদ্ধতি | ডিজাইন, এক্সট্রুশন, ফ্যাব্রিকেশন, বিভিন্ন শিল্পের জন্য সমাপ্তি |
অংশীদার মূল্যায়নের সময় বিবেচনা করুন:
- আপনার অ্যাপ্লিকেশনের জন্য উপকরণের মান এবং খাদ নির্বাচন
- পৃষ্ঠতল চিকিত্সা (অ্যানোডাইজিং, পাউডার কোটিং ইত্যাদি) এ দক্ষতা
- কঠোর সহনশীলতা এবং প্রয়োজনীয় পৃষ্ঠতলের প্রয়োজনীয়তা পূরণের ক্ষমতা
- মান সার্টিফিকেশন এবং প্রক্রিয়ার স্বচ্ছতা
- ক্ষয় প্রতিরোধ এবং অক্সাইড ফিল্ম প্রকৌশলে অভিজ্ঞতা
প্রধান অন্তর্দৃষ্টি: Al 3+চার্জ অবস্থা হল অ্যালুমিনিয়ামের ক্ষয় প্রতিরোধ এবং সমাপ্তির মানের পিছনে মূল উৎস। যে সরবরাহকারী প্রতিটি পদক্ষেপে এই রসায়ন পরিচালনা করে, তার সাথে অংশীদারিত্ব গড়ে তোলা মানে আপনার উপাদানগুলি দীর্ঘতর স্থায়ী হবে এবং ভালো কর্মদক্ষতা প্রদর্শন করবে।
পৃষ্ঠতল প্রকৌশলে অ্যালুমিনিয়াম আয়নিক চার্জ এর ভূমিকা বুঝে নিয়ে আপনি উচ্চ কর্মদক্ষতা সম্পন্ন অ্যালুমিনিয়াম অংশগুলি নির্দিষ্ট করা, সংগ্রহ করা এবং রক্ষণাবেক্ষণ করা সম্পর্কে আরও ভালোভাবে প্রস্তুত হবেন। পরবর্তীতে, আপনার নিজস্ব প্রকল্পগুলিতে এই চার্জ ধারণাগুলি পূর্বাভাস দেওয়া এবং প্রয়োগ করার জন্য ব্যবহারিক সরঞ্জাম এবং কাজের ধারাবাহিকতা সম্পর্কে জানুন।
চার্জ সঠিকভাবে ভবিষ্যদ্বাণী করার জন্য সরঞ্জাম এবং ওয়ার্কফ্লো
একটি নির্ভরযোগ্য চার্জ ভবিষ্যদ্বাণী ওয়ার্কফ্লো তৈরি করুন
কখনও কখনও আপনি একটি রাসায়নিক সূত্রের দিকে তাকিয়ে ভেবেছেন, "আমি কীভাবে জানব যে প্রতিটি উপাদানের চার্জ কী হবে- বিশেষ করে অ্যালুমিনিয়ামের ক্ষেত্রে?" আপনি একা নন। সঠিক আয়নিক চার্জ ভবিষ্যদ্বাণী করা অত্যন্ত জটিল মনে হতে পারে, কিন্তু সঠিকভাবে লেবেল করা চার্জসহ মৌলিক পর্যায় সারণী এবং কয়েকটি বুদ্ধিদায়ক অভ্যাস দিয়ে, আপনি খুব তাড়াতাড়ি এটি আয়ত্ত করে নেবেন। কৌশলটি হল প্রথম রেফারেন্স পয়েন্ট হিসাবে পর্যায় সারণী ব্যবহার করা, এবং তারপরে পলিঅ্যাটমিক আয়ন এবং বিশেষ ক্ষেত্রে বিস্তারিত নিশ্চিত করা।
| গ্রুপ | সাধারণ চার্জ |
|---|---|
| 1 (ক্ষার ধাতু) | +1 |
| 2 (ক্ষারীয় মৃত্তিকা ধাতু) | +2 |
| 13 (অ্যালুমিনিয়ামের গ্রুপ) | +3 |
| 16 (চ্যালকোজেনস) | −2 |
| ১৭ (হ্যালোজেনস) | −1 |
এই সাধারণ টেবিলটি আপনি যে বেশিরভাগ চার্জসহ পর্যায় সারণী চার্টে দেখবেন তার সাথে মেলে। অ্যালুমিনিয়ামের ক্ষেত্রে, সবসময় +3 এর আশা করুন- পর্যায় সারণীতে সবচেয়ে প্রত্যাশিত ক্যাটায়নগুলোর মধ্যে একটি হিসাবে এটি করা।
গ্রুপ প্রবণতা ব্যবহার করুন এবং বহুপরমাণুক আয়নগুলি নিশ্চিত করুন
যখন আপনি আরও জটিল সংকেত নিয়ে কাজ করার জন্য প্রস্তুত হবেন, তখন শুধুমাত্র মনের উপর নির্ভর করবেন না। ক্যাটায়ন এবং অ্যানায়নসহ পর্যায় সারণী প্রধান গোষ্ঠীর মৌলগুলির জন্য আপনার বন্ধু হিসেবে কাজ করবে, কিন্তু বহুপরমাণুক আয়নগুলির জন্য একটি যাচাইকৃত তালিকা প্রয়োজন। এখানে কয়েকটি সাধারণ আয়ন যেগুলি আপনি দেখতে পাবেন, সেগুলির চার্জসহ:
| নাম | সূত্র | চার্জ |
|---|---|---|
| নাইট্রেট | NO3− | −1 |
| সালফেট | SO42− | −2 |
| ফসফেট | পিও 43− | −3 |
| অ্যাসিটেট | সি 2এইচ 3ও 2− | −1 |
| হাইড্রক্সাইড | ওএইচ − | −1 |
| কার্বনেট | CO32− | −2 |
| অ্যামোনিয়াম | NH 4+ | +1 |
আপনি যখন সমস্যার সমাধান করছেন বা ল্যাব রিপোর্ট লিখছেন, তখন এই আয়নগুলির একটি মুদ্রণযোগ্য শীট হাতের কাছে রাখুন। সম্পূর্ণ তালিকার জন্য, এটি দেখুন বহুপরমাণুক আয়ন রেফারেন্স .
দ্রুত এবং সঠিকভাবে সন্তুলিত সংকেত লিখুন
যখন আপনি চার্জগুলি জানবেন, তখন সঠিক সংকেত লেখা হবে মোট ধনাত্মক এবং ঋণাত্মক চার্জগুলি শূন্যের সমান করে সন্তুলিত করা। এখানে প্রতিবার সঠিক কাজ করার জন্য একটি দ্রুত কার্যপ্রবাহ রয়েছে:
- প্রতিটি মৌল বা আয়নকে খুঁজুন মৌল এবং চার্জের পর্যায় সারণীতে বা আপনার বহুপরমাণু আয়ন তালিকা।
- তাদের চার্জ সহ আয়নিক প্রতীকগুলি লিখুন (যেমন, Al 3+, তাই 42−).
- চার্জগুলি শূন্যের সমান করে সন্তুলিত করার জন্য আয়নগুলির নিম্নতম অনুপাত নির্ধারণ করুন।
- আনুভূমিক সংকেত লিখুন, এক এর বেশি হলে বহুপরমাণু আয়নের জন্য বন্ধনী ব্যবহার করুন (যেমন, Al 2(SO 4)3).
- আপনার কাজ দ্বিতীয়বার পরীক্ষা করুন: চার্জের যোগফল শূন্যের সমান হয়েছে কি?
স্মরণ রাখার কৌশল: "Al সবসময় +3 এর দিকে লক্ষ্য রাখে—টেবিলটি ব্যবহার করুন, চার্জটি ভারসাম্য বজায় রাখুন, এবং আপনি কখনও ভুল পথে যাবেন না।"
এই প্রক্রিয়াটি অনুসরণ করে এবং একটি চার্জসহ পর্যায় সারণী আপনার অ্যাঞ্চর হিসাবে ব্যবহার করে, আপনি হোমওয়ার্ক, ল্যাব প্রস্তুতি এবং পরীক্ষার সমস্যা সমাধানকে সরলীকৃত করবেন। মনে রাখবেন: অ্যালুমিনিয়ামের চার্জ কত এর জন্য, উত্তরটি সবসময় +3—প্রতিবার, যতক্ষণ না একটি দুর্লভ ব্যতিক্রম স্পষ্টভাবে নির্দেশিত হয়।
এই ব্যবহারিক সরঞ্জাম এবং কাজের প্রবাহের সাহায্যে, আপনি পর্যায় সারণীতে চার্জগুলি মুখস্থ করা থেকে প্রকৃতপক্ষে বোঝা পর্যন্ত এগিয়ে যাবেন—এবং পরবর্তী যেকোনো নামকরণ বা সূত্র চ্যালেঞ্জের জন্য প্রস্তুত থাকবেন।
আত্মবিশ্বাসের সাথে Al ব্যবহারের জন্য সংশ্লেষণ এবং পরবর্তী পদক্ষেপ 3+
Al সম্পর্কিত প্রধান বিষয় 3+আপনি বিশ্বাস করতে পারেন
যখন আপনি পিছনে সরে গিয়ে বড় ছবিটি দেখেন, তখন ভবিষ্যদ্বাণী করা আয়নিক চার্জ একটি সোজা, নির্ভরযোগ্য প্রক্রিয়ায় পরিণত হয়। এখানে কেন:
- পর্যায় সারণী যুক্তি: গ্রুপ 13-এ অ্যালুমিনিয়ামের অবস্থানের কারণে এটি প্রায় সবসময়ই একটি +3 আয়ন গঠন করে। যদি কখনও আপনার সন্দেহ হয় যে অ্যালুমিনিয়ামের চার্জ কী তবে মনে রাখবেন যে এই গ্রুপের প্রবণতা সঠিক উত্তরে পৌঁছানোর জন্য আপনার কাছে সংক্ষিপ্ত পথ হিসাবে কাজ করবে।
- ইলেকট্রন কনফিগারেশন: তিনটি ভ্যালেন্স ইলেকট্রন হারিয়ে অ্যালুমিনিয়াম একটি নোবেল গ্যাস কোর অর্জন করে - Al কে সবচেয়ে স্থিতিশীল এবং প্রচলিত অবস্থায় পরিণত করে। এটি প্রশ্নের উত্তর হলো, 3+সবচেয়ে স্থিতিশীল এবং প্রচলিত অবস্থায় পরিণত করে। এটি প্রশ্নের উত্তর হলো, অ্যালুমিনিয়াম কোন আয়ন গঠন করে ?”
- পূর্বানুমেয় রসায়নবিদ্যা: সূত্রগুলি ভারসাম্য রক্ষা করা, যৌগগুলির নামকরণ করা বা ক্ষয় বিবেচনা করা সহ যেকোনো কিছুতেই আপনি Al এর উপর নির্ভর করতে পারেন 3+ডিফল্ট হিসাবে অ্যালুমিনিয়ামের আয়ন চার্জ .
- অ্যালুমিনিয়াম প্রায়সই +3 ক্যাটায়ন গঠন করে—পূর্বানুমেয়, স্থিতিশীল, এবং খুঁজে পাওয়া সহজ।
- ধাতু 3+জলীয় রসায়ন, যৌগ গঠন, এবং ক্ষয় প্রতিরোধে চালিত করে।
- এই চার্জ দক্ষতার সাথে বাস্তব জগতের ডিজাইন, উৎস নির্ধারণ, এবং সমস্যা সমাধানের চ্যালেঞ্জগুলি সমাধান করতে সাহায্য করে।
পরবর্তীতে এই জ্ঞান কোথায় প্রয়োগ করবেন
তাহলে, জানা al এর চার্জ আপনাকে কীভাবে শ্রেণিকক্ষের বাইরে সাহায্য করবে? ধরুন আপনি:
- জল চিকিত্সা প্রক্রিয়া ডিজাইন করছেন—Al এর জলবিশ্লেষণ বোঝা আপনাকে অধঃক্ষেপণ এবং দ্রাব্যতা নিয়ন্ত্রণ করতে দেয়। 3+রাসায়নিক সূত্র লেখা—Al
- রাসায়নিক সূত্র লেখা—Al 3+হল সাধারণ ঋণাত্মক আয়নের সাথে চার্জ সংশ্লিষ্ট করার জন্য আপনার আনকার।
- এক্সট্রুডেড অ্যালুমিনিয়াম অংশগুলি নির্দিষ্ট করা বা সংগ্রহ করা—জানা অ্যালুমিনিয়াম দ্বারা গঠিত আয়নের চার্জ কী হবে অক্সাইড ফিল্মগুলি কেন গঠিত হয় এবং অ্যানোডাইজিং আপনার উপাদানগুলিকে কীভাবে রক্ষা করে তা বোঝতে আপনাকে সাহায্য করে।
আপনি যদি কখনও অনিশ্চিত হন, তবে শুধুমাত্র নিজেকে জিজ্ঞাসা করুন: এই পরিপ্রেক্ষিতে অ্যালুমিনিয়াম ধনাত্মক আয়ন না ঋণাত্মক আয়ন? উত্তরটি প্রায় সবসময় ধনাত্মক আয়ন (Al 3+) এবং সেই স্পষ্টতা আপনার কাজ দ্রুত করে তুলবে—আপনি যেটি করছেন না কেন পরীক্ষার প্রস্তুতি বা একটি নতুন পণ্য প্রকৌশল।
| ধারণা | উদাহরণ | প্রয়োগ |
|---|---|---|
| দল 13 অবস্থান | অ্যাল ফর্ম Al 3+ | দ্রুত চার্জ ভবিষ্যদ্বাণী |
| [Ne] এর ইলেকট্রন ক্ষতি | Al: [Ne]3s 23 পি 1→ Al 3+: [Ne] | স্থিতিশীলতা ব্যাখ্যা করে |
| ধাতু 3+জলে | [Al(H 2O) 6]3+জটিল | জলীয় রসায়ন, জল-বিশ্লেষণ |
| অক্সাইড ফিল্ম গঠন | ধাতু 3++ O 2−→ Al 2ও 3 | ক্ষয় প্রতিরোধ, অ্যানোডাইজিং |
অনুশীলন এবং সংগ্রহের জন্য প্রস্তাবিত সংস্থান
আপনার জ্ঞানকে কাজে লাগাতে প্রস্তুত? পরবর্তীতে কোথায় যাবেন তা এখানে দেখুন:
- শাওয়ি (অ্যালুমিনিয়াম এক্সট্রুশন অংশ) - উচ্চ প্রদর্শন, ক্ষয় প্রতিরোধী নিষ্কাশিত অ্যালুমিনিয়াম উপাদানগুলির সন্ধান করা প্রকৌশলী এবং ডিজাইনারদের জন্য, শাওয়াই অ্যানোডাইজিং, অক্সাইড ফিল্ম প্রকৌশল এবং অটোমোটিভ-গ্রেড ফিনিশিংয়ের বিষয়ে তাদের পারদর্শিতার জন্য প্রতিনিধিত্ব করে। অ্যালুমিনিয়ামের আয়নিক আচরণ সম্পর্কে তাদের বোঝার ফলে ভালো, দীর্ঘস্থায়ী অংশ তৈরি হয়।
- গ্রুপ 13 রসায়ন গাইড - পর্যায় প্রবণতা, গ্রুপ ব্যতিক্রম এবং চার্জ যুক্তি প্রসঙ্গে আরও গভীরভাবে বোঝা।
- চার্জসহ পর্যায় সারণী - দ্রুত চার্জ ভবিষ্যদ্বাণী এবং সূত্র লেখার জন্য একটি মুদ্রণযোগ্য রেফারেন্স।
আপনি যদি রসায়নের পরীক্ষার জন্য অধ্যয়ন করছেন বা একটি নতুন পণ্যের জন্য উপাদানগুলি নির্দিষ্ট করছেন, তাহলে বোঝা আবশ্যিক অ্যালুমিনিয়ামের চার্জ কী হবে এমন একটি দক্ষতা যা আপনি বারবার ব্যবহার করবেন। এবং যখন সর্বোচ্চ স্থায়িত্বের জন্য প্রকৌশলী উপাদানগুলির প্রয়োজন হবে, তখন শাওয়াইয়ের মতো একজন সরবরাহকারীর সাথে পরামর্শ করুন যারা প্রতিটি পৃষ্ঠের পিছনে বিজ্ঞান বোঝেন।
Al আয়নিক চার্জ: প্রায়শই জিজ্ঞাসিত প্রশ্নাবলী
১. আলুমিনিয়ামের আয়নিক চার্জ কত এবং এটি কেন Al3+ গঠন করে?
আলুমিনিয়াম প্রায়শই +৩ আয়নিক চার্জ গঠন করে কারণ এটি স্থিতিশীল নোবেল গ্যাস কাঠামোতে পৌঁছানোর জন্য তিনটি সংযোজন ইলেকট্রন হারায়। এটি যৌগগুলিতে Al3+ কে সবচেয়ে সাধারণ এবং স্থিতিশীল আয়ন হিসাবে তৈরি করে, চার্জ পূর্বাভাস এবং সূত্র লেখা সহজ করে তোলে।
২. আমি কীভাবে পর্যায় সারণী ব্যবহার করে আলুমিনিয়ামের চার্জ দ্রুত পূর্বাভাস দিতে পারি?
আলুমিনিয়ামের চার্জ পূর্বাভাস দেওয়ার জন্য এটিকে পর্যায় সারণীর গ্রুপ ১৩-এ অবস্থিত করুন। এই গ্রুপের মূল মৌলগুলি সাধারণত +৩ ক্যাটায়ন গঠন করে, তাই আলুমিনিয়ামের চার্জ নির্ভরযোগ্যভাবে +৩। এই গ্রুপ-ভিত্তিক প্রবণতা প্রতিটি মৌল মুখস্থ না করেই চার্জগুলি পূর্বাভাস দেওয়ার সহায়তা করে।
৩. অ্যানোডাইজিংয়ের মতো বাস্তব অ্যাপ্লিকেশনে আলুমিনিয়ামের +৩ চার্জ কেন গুরুত্বপূর্ণ?
অ্যালুমিনিয়ামের +3 চার্জ এর পৃষ্ঠে একটি স্থিতিশীল অক্সাইড স্তর গঠনে সহায়তা করে, যা ক্ষয় প্রতিরোধ এবং স্থায়িত্বের জন্য অপরিহার্য। এই ধর্মটি অ্যানোডাইজিং এর মতো প্রক্রিয়াগুলিতে গুরুত্বপূর্ণ, যেখানে অক্সাইড স্তরটি উদ্দেশ্যমূলকভাবে পুরু করা হয় যেমন অটোমোটিভ উত্পাদন শিল্পে ব্যবহৃত অ্যালুমিনিয়াম অংশগুলি রক্ষা এবং উন্নত করার জন্য।
4. জল এবং যৌগগুলিতে অ্যালুমিনিয়ামের আয়নিক চার্জ এর আচরণকে কীভাবে প্রভাবিত করে?
জলে, Al3+ জলের অণুগুলির সাথে জটিলতা তৈরি করে এবং জল-বিশ্লেষণের মাধ্যমে ঘটে, যার ফলে pH এর উপর নির্ভর করে বিভিন্ন ধরনের অ্যালুমিনিয়াম আয়ন তৈরি হয়। এর শক্তিশালী চার্জ স্থিতিশীল আয়নিক যৌগগুলির গঠনের প্ররোচনা দেয়, যার সাধারণ ঋণাত্মক আয়নগুলির সাথে চার্জ ভারসাম্যের উপর ভিত্তি করে পূর্বাভাসযোগ্য সংকেত থাকে।
5. আয়নিক রসায়ন জড়িত প্রকল্পগুলির জন্য অ্যালুমিনিয়াম অংশগুলি সংগ্রহ করার সময় আমার কী বিবেচনা করা উচিত?
আয়নিক আচরণ এবং উন্নত পৃষ্ঠের চিকিত্সার ক্ষেত্রে অ্যালুমিনিয়াম বিশেষজ্ঞতা সহ সরবরাহকারীদের নির্বাচন করুন। উদাহরণস্বরূপ, শাওয়ি অ্যালুমিনিয়াম এক্সট্রুশনের একীভূত সমাধান সরবরাহ করে, যা অ্যানোডাইজিং এবং অক্সাইড ফিল্ম গঠনের ওপর নিখুঁত নিয়ন্ত্রণের মাধ্যমে উপাদানগুলির অনুকূলিত পৃষ্ঠের রসায়ন এবং স্থায়িত্ব নিশ্চিত করে।
 ছোট ছোট ব্যাচ, উচ্চ মান। আমাদের তাড়াতাড়ি প্রোটোটাইপিং সার্ভিস যাচাইকরণকে আরও তাড়াতাড়ি এবং সহজ করে —
ছোট ছোট ব্যাচ, উচ্চ মান। আমাদের তাড়াতাড়ি প্রোটোটাইপিং সার্ভিস যাচাইকরণকে আরও তাড়াতাড়ি এবং সহজ করে —
